亚麻醉剂量艾司氯胺酮用于胸腔镜肺叶切除术镇痛效果的观察
2023-01-17冯兆胜武亚芸梁士权王建刚郭志佳
冯兆胜,武亚芸,梁士权,王建刚,朱 健,郭志佳
0 引言
胸腔镜手术目前广泛应用于胸外科,该术式与开胸手术相比,减少了对患者的伤害性刺激,但仍有78%的患者术后存在中重度疼痛[1],其术后疼痛是一种合并神经病理性疼痛(Neuropathic pain,NP)成分的混合性疼痛,常表现为触觉异常痛和痛觉过敏[2]。在疼痛管理中,神经病理性疼痛受到了医生的关注。在此背景下,越来越多的新型麻醉药及神经阻滞剂应用于胸外科手术[3]。
艾司氯胺酮作为N-甲基-D-天门冬氨酸(N-methyl-D-aspartate,NMDA)受体拮抗剂,可通过多途径缓解神经病理性疼痛,减弱中枢敏化、阿片耐受和痛觉敏感的发生,从而减轻急性疼痛,并可能有预防慢性疼痛的作用[4]。Vadivelu等[5]的研究表明,艾司氯胺酮在低浓度时镇痛效果明显,高浓度时麻醉效果明显。在术中即使低剂量的艾司氯胺酮也可以起到提高痛阈的作用,为亚麻醉剂量艾司氯胺酮应用于急性疼痛的管理提供了理论基础。本研究旨在探讨亚麻醉剂量艾司氯胺酮对胸腔镜肺叶切除手术术后急慢性疼痛的影响,为临床用药提供参考。
1 资料与方法
1.1 一般资料 选择2021年10月至2022年3月山西医科大学第一医院择期全麻下经胸腔镜肺叶切除手术者100例,入选标准:①年龄35~70岁;②体重指数18.0~28.0 kg/m2;③美国麻醉医师协会分级Ⅱ级或Ⅲ级;④同意参加临床试验观察并能配合按期随访者。排除标准:①有全身麻醉禁忌证,有麻醉药物过敏史者;②有血压或颅内压升高严重风险者;③未经治疗或者治疗不足的甲亢患者;④24 h内使用过麻醉性镇痛药或者5 d内使用过麻醉药;⑤有慢性疼痛史或有长期服用镇静镇痛药物史;⑥有长期饮酒成瘾史;⑦抑郁症患者或其他精神功能障碍患者。剔除标准:①术中改变手术方式(胸腔镜改为开胸手术者);②手术过程中出现休克、心律失常等情况;③术后出现严重并发症者。脱落标准:不愿接受术后回访患者,失访患者。按照随机数字表法将患者随机分为2组:瑞芬太尼复合艾司氯胺酮组(试验组)和单纯瑞芬太尼组(对照组)。本研究经山西医科大学第一医院伦理委员会批准〔[2021]伦审字(K089)号〕,入组患者或家属签署知情同意书。
1.2 麻醉方法 两组患者入室后均持续监测心电图(ECG)、脉博、血氧饱和度(SpO2)、平均动脉压(MAP)、呼气末CO2分压(PETCO2)和脑电双频指数(BIS),开放静脉通路,所有患者均实施静脉全身麻醉。提前给予0.5 mg盐酸戊乙奎醚注射液和20 mg泼尼松。充分预充氧,依次静脉注射舒芬太尼0.3~0.5 μg/kg,依托咪酯0.2~0.5 mg/kg,顺式阿曲库铵0.2 mg/kg进行诱导。达到理想插管条件后,可视喉镜下经口气管插管置入双腔支气管导管,男性选择F37,女性选择 F35,纤维支气管镜定位准确后妥善固定导管,连接麻醉机实施机械通气。术中调整呼吸参数,维持PETCO2为35~45 mmHg。术中微量泵泵入丙泊酚注射液和瑞芬太尼注射液,监测患者生命体征,调节药量使BIS值在40~60,间断给予适量肌松药推注。试验组患者在切皮前额外静脉滴注艾司氯胺酮 0.25 mg/kg,术中持续泵注剂量为 0.15 mg/(kg·h),手术结束前30 min停药。对照组给予等量生理盐水泵注。手术结束前给予托烷司琼5 mg预防呕吐。待患者苏醒,自主呼吸恢复,吸除口咽腔分泌物后,拔除气管导管,必要时使用阿托品和新斯的明拮抗肌松。手术结束后随之连接静脉自控镇痛泵(Patient-controlled intravenous analgesia,PCIA)(舒芬太尼150 μg加托烷司琼5 mg稀释到100 ml生理盐水中),背景剂量为2 ml/h,时间锁定15 min,单次按压量1 ml。术后两组患者均进入麻醉后恢复室,待患者Steward苏醒评分4分以上后送其安返病房,并告知患者镇痛泵的使用方法。
1.3 观察指标 ① 24 h内PCIA中舒芬太尼累计用量、首次按压镇痛泵的时间、24 h内实际按压次数和有效按压次数。②患者术后 4 h(T0)、8 h(T1)、12 h(T2)、24 h(T3)、48 h (T4)5个时间点的疼痛情况。所有入组患者均使用视觉模拟评分(Visual analogue scale,VAS)评估静息和活动时的术后疼痛程度 (无痛为0分,剧痛为10分)。在观察期,VAS≥3分时,患者自行按压镇痛泵1次。镇痛效果不佳(按压镇痛泵无效,且VAS≥5分)时,由医生静脉注射哌替啶,并记录追加次数。③术后1 d、1个月、3个月时,电话随访患者利兹神经病理性症状和体征疼痛评分 (Leeds assessment of neuropathic symptoms and sign,LANSS)(7个问题,包括对感觉描述和感觉的异常检查)。④记录患者头晕、恶心、呕吐、幻觉等不良反应的发生情况。⑤记录患者的满意度,分3个等级(满意、可接受、不满意),包括对镇痛的满意度和总体评价(镇痛效果、不良反应和性价比3项指标形成总体评价)。
1.4 统计学分析 采用SPSS 25.0软件进行数据分析。计数资料采用例数(百分比)进行描述,组间比较采用卡方检验或Fisher精确检验。符合正态分布的计量资料采用均数±标准差进行描述,采用t检验进行组间比较;否则采用中位数(四分位数间距)进行统计描述,采用非参数检验进行组间比较。重复测量资料的比较使用重复测量方差分析。P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者一般情况比较 两组患者的一般情况、手术时间和麻醉时间比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者一般情况比较
2.2 两组患者术后不同时间点疼痛评分的比较 不同时间和不同组别对静息VAS评分的影响存在交互作用(F=19.760,P<0.001),即在两组患者中,不同时间点对患者的静息疼痛评分的影响差异有统计学意义。通过交互作用的两两比较后,关于时间的简单效应显示,时间点的不同对试验组静息VAS评分的影响差异有统计学意义(F=108.876,P<0.001),见图1A的虚线部分,在术后12 h(T2)时患者疼痛评分达到最高,而在此之后,疼痛评分随着时间推移逐渐下降。时间点的不同对对照组静息VAS评分的影响差异有统计学意义(F=106.403,P<0.001)。其疼痛评分变化趋势见图1A实线部分。关于组别的简单效应显示,在T0、T1和T2时,试验组的静息VAS评分相比对照组下降,差异有统计学意义(P<0.05);T3与T4时,试验组和对照组的静息VAS评分差异无统计学意义(P>0.05),见表2。
不同时间和不同组别对活动VAS评分的影响存在交互作用(F=46.218,P<0.001),通过交互作用的两两比较后,关于时间的简单效应显示,时间点的不同对试验组活动VAS评分的影响差异有统计学意义(F=169.648,P<0.001),见图1B的虚线部分,在术后12 h(T2)时,患者疼痛评分达到最高,而在此之后,疼痛评分随着时间推移逐渐下降;时间点的不同对对照组活动VAS评分的影响差异有统计学意义(F=97.781,P<0.001)。其疼痛评分变化趋势见图1B实线部分。关于组别的简单效应显示,在T0、T1和T2时,试验组的活动VAS评分相比对照组下降,差异有统计学意义(P<0.05);T3与T4时,试验组和对照组的活动VAS评分差异无统计学意义(P>0.05),见表2。
LANSS的组内因素(不同时间)和组间因素(不同组别)交互作用不显著(F=2.481,P=0.089)。时间的主效应显著(F=181.941,P<0.001),组别的主效应显著(F=263.148,P<0.001)。从图1C中可以观察到,随着时间的推移,LANSS逐渐下降,且试验组的评分明显低于对照组(P<0.05)。

图1 两组患者静息VAS评分、活动VAS评分及LANSS评分比较
2.3 两组患者术后急性疼痛情况 试验组24 h内PCIA的舒芬太尼累计用量低于对照组(P<0.05)。试验组首次按压镇痛泵的时间晚于对照组(P<0.05)。试验组有效按压次数少于对照组(P<0.05),有效按压次数较实际按压次数少,是因为患者在疼痛时连续按压镇痛泵,未超出镇痛泵的锁定时间。见表3。

表2 两组患者疼痛评分比较
2.4 两组患者术后不良反应及满意度的比较 两组患者恶心、呕吐、幻觉、头晕的发生率较低,差异无统计学意义(P>0.05),且两组患者不良反应总发生率差异也无统计学意义(P>0.05)。见表4。试验组术后患者麻醉满意度和总体评价高于对照组(P<0.05),见表5。
3 讨论
胸腔镜术后切口的组织损伤、肌肉与肋间神经的病理损伤、术中瑞芬太尼大剂量或长时间的输注诱发痛觉过敏现象,与手术引起的疼痛有协同作用[6],可诱发机体外周敏化和中枢敏化,产生急性疼痛,并继发神经病理性疼痛。艾司氯胺酮对术后阿片类药物的保留效应已经在胸部、腹部、骨科手术中报道[7-8],本研究术中泵入亚麻醉剂量艾司氯胺酮,观察其对术后疼痛和预防神经病理性疼痛的影响。
研究表明,与对照组相比,围术期给予低剂量艾司氯胺酮后,患者的疼痛评分、术后镇痛药物总消耗量显著降低,其在胸腔镜手术中的应用是目前研究的热点[9]。本研究中试验组首次按压镇痛泵的时间较晚,且试验组在术后4 h、8 h、12 h的VAS评分低于对照组,分析原因如下:当伤害感受信号达到一定阈值时,NMDA受体活性会对μ-阿片受体(Mu-opioid receptor,MOR)的信号传导能力产生负面影响,因此,拮抗NMDA受体有助于阿片镇痛[2]。提早阻断NMDA受体,起到了预防性镇痛的作用,使得镇痛时间明显延长[10]。艾司氯胺酮通过延缓胞外信号,调节激酶脱敏,防止中枢敏化[11-13];同时通过减轻外周机械刺激疼痛,防止中枢致敏的发展。这种作用与单次剂量或短期输注氯胺酮后的长期镇痛作用相关。此外,一氧化氮是造成组织损伤和炎症反应的重要因子,炎性疼痛会引起疼痛的正反馈效应。艾司氯胺酮可通过抑制一氧化氮合酶减少一氧化氮的产生,抑制炎症性疼痛[14],缓解患者急性期疼痛程度。在本研究中,试验组术后疼痛程度明显减轻,有效按压镇痛泵的次数减少;24 h内PCIA中舒芬太尼累计用量低于对照组,与报道一致。

表3 两组患者术后急性疼痛情况比较
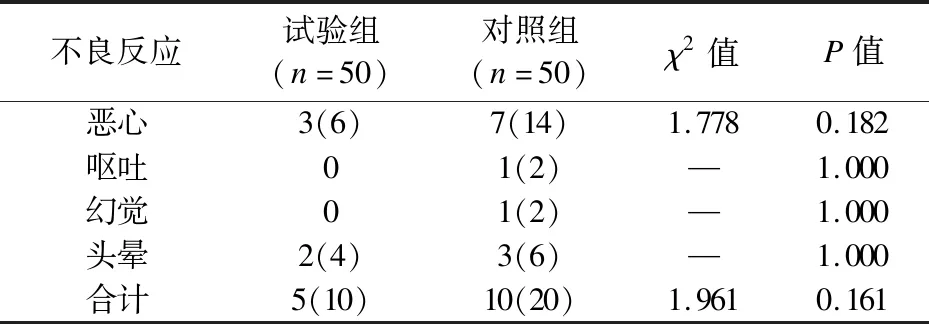
表4 两组患者术后不良反应的比较[例(%)]
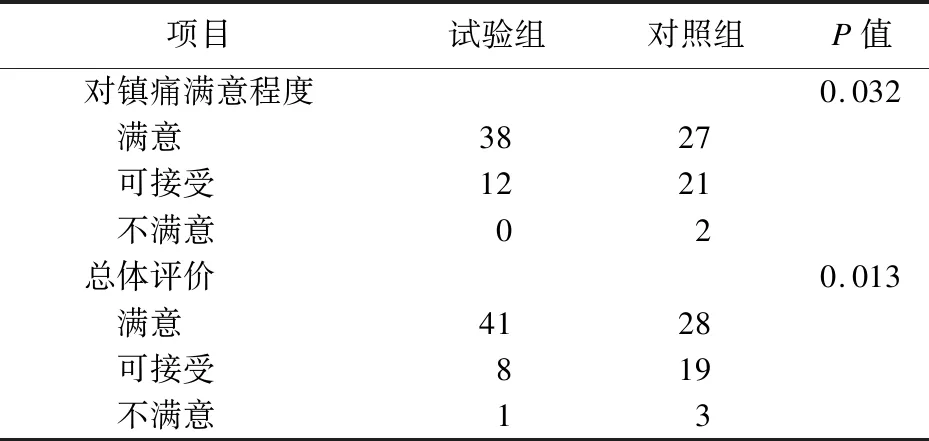
表5 两组患者术后满意度和总体评价的比较(例)
疼痛评估是疼痛管理的关键组成部分,一项关于胸科手术术后疼痛评估的分析提出,除了观察患者的疼痛强度外,应从多维度、使用多种工具评估患者的疼痛需求[15]。LANSS评分量表由Bennett于2001年设计,主要应用于筛查及诊断神经病理性疼痛,也用于神经病理性疼痛治疗后的疗效评估[16]。本研究中试验组在术后1 d、1个月、3个月的LANSS评分明显低于对照组,说明艾司氯胺酮能减轻神经病理性疼痛。分析原因如下:MOR引起的NMDA受体持续激活是神经病理性疼痛的原因之一[2],如果增加阿片类药物的剂量,往往超过了其对抗伤害性疼痛的剂量,且缓解程度有限,而通过阻断NMDA受体的功能,能对神经病理性疼痛起到很好的缓解作用。炎性介质引起的痛阈异常可引起神经病理性疼痛,艾司氯胺酮具有一定的抗炎作用,可预防急性疼痛转变为慢性疼痛。艾司氯胺酮通过阻断谷氨酸盐与NMDA受体的结合,阻断钙离子通道,减少钙离子进入细胞,进而减少细胞凋亡和神经损伤。此外,艾司氯胺酮直接或间接降低脊髓神经胶质细胞P2X7受体的表达,能部分缓解神经病理性疼痛[17]。术中静脉泵注艾司氯胺酮在预防神经病理性疼痛中有一定价值,与之前的研究一致[18]。在不良反应事件的比较中,两组患者不良反应无明显差异。在患者的镇痛满意度和总体评价的比较中,试验组患者总体评价高于对照组,且其对镇痛满意度较高,考虑与患者伤口区域疼痛敏感下降、疼痛程度减轻有关;艾司氯胺酮的情绪改善、抗焦虑、抗抑郁等特点可能也发挥着作用[19]。
本研究存在一定局限性:观察数量有限,其可靠性仍需多中心、大样本的随机试验进一步论证;疼痛是主观感觉,存在个体差异。在今后的研究中,艾司氯胺酮在特定人群中使用及其最佳使用方案仍是探索的方向。在国外研究中,术中使用氯胺酮后,试验组术后第1秒用力呼气容积的改善更快[20],其在胸科手术中对呼吸功能的影响也是下一步研究的重点。
综上所述,术中持续泵注亚麻醉剂量艾司氯胺酮可以减轻胸腔镜肺叶切除术术后患者的急性疼痛,减少术后阿片类药物的使用量,且不增加患者的不良反应,其对缓解神经病理性疼痛有一定意义。
