碳钢表面电化学沉积氧化锌层的腐蚀防护性能研究
2023-01-17张椿英赵浩峰陈鸿飞何孔杰周衍浩陈家星
张椿英, 赵浩峰,2, 陈鸿飞, 何孔杰, 周衍浩, 陈家星
(1.安徽信息工程学院 机械工程学院, 安徽 芜湖, 241000;2.南京信息工程大学 材料学院, 江苏 南京, 210044)
0 引言
金属防腐研究是材料工作者的重要任务之一.世界上每年金属腐蚀量达到使用量的20%以上,有些国家造成的腐蚀使得国民经济损失量达到2%~4%.有研究表明,金属腐蚀后的承受载荷会大幅降低,例如在受力情况下,若钢被腐蚀达到1%,其强度会下降10%~15%,当两面都被腐蚀各自达到5%,钢就会报废[1-3].电化学沉积法是形成耐腐蚀薄膜的一种重要方法,也广泛应用于制备金属化合物半导体薄膜、高温超导氧化物薄膜.这种方法的优点是沉积层密度高和孔隙率低.材料的结晶组织结构由电化学参数决定,通过对电压、电解液等因素的调整可以控制沉积膜的厚度、晶粒直径和孔隙率等.另外电沉积可以在较低温度和压力下操作,避免高温高压反应对能源的浪费[4-5].张振岳[6]通过电沉积的方法制备了硅烷膜,在其基础上利用Hummers法制备了氧化石墨烯,并用电沉积的方法在不锈钢表面沉积,得到的薄膜对基体有很好的保护作用.沈广霞等人[7]采用溶胶凝胶法制备了TiO2-V2O5纳米复合膜并对其进行了紫外光照射下的腐蚀性能的研究.韩燕[8]为了改善铝合金材料的耐腐蚀性能,研究了纳米氧化锌掺杂聚氨酯涂料中,制备纳米氧化锌复合涂层.但是氧化锌电化学沉积层对钢基体的腐蚀保护研究并不多.本文拟就打底层氧化锌电化学沉积参数对钢的腐蚀防护的电化学行为影响进行研究.
1 实验方法和条件
试验用钢为20钢.氧化锌沉积采用三电极装置,即铂碳电极作为对电极,甘汞电极作为参比电极,工作电极是钢片,电极之间的距离是参比电极和工作电极距离0.6 cm,参比电极和对电极之间的距离是1.4 cm.基片为是市售普通钢片.电解液为六水合硝酸锌溶液.在试验前,将金相试样抛光,再用丙酮、乙醇清洗三遍以上,最后用去离子水冲洗干净.沉积电压为-1 V,电解液浓度为0.005 mol/L及 0.010 mol/L,沉积时间为5 min、20 min及35 min,沉积温度40 ℃、60 ℃及80 ℃ .实验过程中的温度控制是依靠恒温水浴锅.塔菲尔曲线采用CHI660和CS310H两种电化学工作站制取及校验.在测试之前要先用AB胶对样品进行封胶,使之露出的面积为1×1 cm2,用去离子水配置质量分数为3%的氯化钠溶液.把试样置于工作电极,静置30 min,同时进行开路电位(OCPT)测试,若曲线不平稳需要继续静置(变动在10mV以内即算作稳定),待曲线相对稳定时,开始交流阻抗谱(EIS)测试,使得开路电位作为其测阻抗的初始电位.
2 实验结果及讨论
图1及图2为电沉积参数不同,得到的塔菲尔曲线.曲线图中右侧为阴极反应,图中左侧为阳极反应,曲线交汇点所对应的E和I分别是腐蚀电位和腐蚀电流密度.从图中可以看出,在阴极的塔菲尔斜率Bc比较大,阳极的塔菲尔斜率Ba比较小,说明在阴极时反应比较快.另外,可以根据腐蚀电流密度来判断整体反应腐蚀的快慢,腐蚀电流密度越大,则腐蚀越快.腐蚀电位越大,说明能发生此腐蚀反应的难度越大.
从图1的塔菲尔曲线可以看得出,当条件为:沉积时间5 min、沉积温度为40 ℃,电解液浓度为0.005 mol/L时的腐蚀电位为-0.85 V,而电解液浓度为0.010 mol/L时的腐蚀电位为-0.55 V.说明电解液浓度低,在制备氧化锌薄膜时生成的氧化锌膜是最薄的,所以它在试样中是不耐腐蚀的.腐蚀电位低的样品其表面处于不稳定的体系,容易被腐蚀.当电解液浓度提高,氧化锌薄膜增长速度加快,氧化锌薄膜稳定而变厚,耐腐蚀能力提高.此外,从塔菲尔曲线可以看出,电解液浓度为0.005 mol/L时的钝化区很长,所以会被很快就击穿,进行基体的自我保护作用.因此,电解液浓度为0.005 mol/L时的表面膜的保护作用较差.说明在沉积时间5 min、沉积温度为40 ℃时,电解液浓度高些(0.010 mol/L)有好的防护作用.
图2的塔菲尔曲线可以看出,电解液浓度为 0.005 mol/L时的在20 min及60 ℃的腐蚀电位达-0.66 V,而电解液浓度为 0.010 mol/L时的腐蚀电位达-0.63 V.说明在温度提高和时间增加后,电解液浓度的影响作用并不大.由图2(a)和图1(a)的塔菲尔曲线比较可以看出,在低浓度(0.005 mol/L)条件下,当条件为沉积时间20 min、沉积温度为60 ℃时的腐蚀电位比沉积时间5 min、沉积温度40 ℃的高.说明温度提高和时间增加对于沉积是有益的,有助于厚实膜的形成.由图2(b)和图1(b)的塔菲尔曲线比较可以看出,在高浓度(0.010 mol/L)条件下,条件为沉积时间20 min、沉积温度为60 ℃的腐蚀电位反而比沉积时间5 min、沉积温度为40 ℃要低一些.说明,当浓度提高后,提高温度和增加时间,反而因为沉积速度过快,造成氧化锌膜的疏松.所以在电解液浓度为 0.010 mol/L时提高温度和增加时间反而会耐蚀能力.

(a)电解液浓度 0.005 mol/L (b)电解液浓度 0.010 mol/L
由实验表明,沉积时间为20 min及35 min、沉积温度为60 ℃以及沉积时间为20 min及35 min、沉积温度为80 ℃的塔菲尔曲线几乎相同.说明沉积时间35 min和沉积温度为80 ℃对沉积几乎没有改善作用.
由图3(a)腐蚀电位(Q)与沉积时间(t)和沉积温度(T)的关系曲线可以看出,低浓度0.005 mol/L时,增加沉积时间和提高沉积温度时,腐蚀电位会提高,有利于腐蚀电位提高.但是,由图3(b)腐蚀电位与沉积时间和沉积温度的关系曲线可以看出,高浓度0.010 mol/L时,腐蚀电位反而降低.其原因是,随着温度的提高,离子运动加剧,所生成的氧化锌膜变得疏松,表面有孔,即使表面沉积氧化钛,也无法弥补这种疏松,所以耐腐蚀性没有得到有效增强.图3(b)中,实验温度为60 ℃时,即使增加沉积时间,腐蚀电位变化并不大.说明,虽然氧化锌膜在厚度,但是由于沉积组织疏松,防腐蚀作用也不再增加.由图3也可以看出,电解液的浓度变化对沉积有影响.
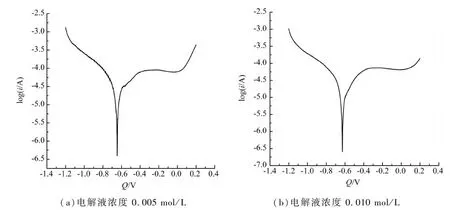
图2 塔菲尔曲线
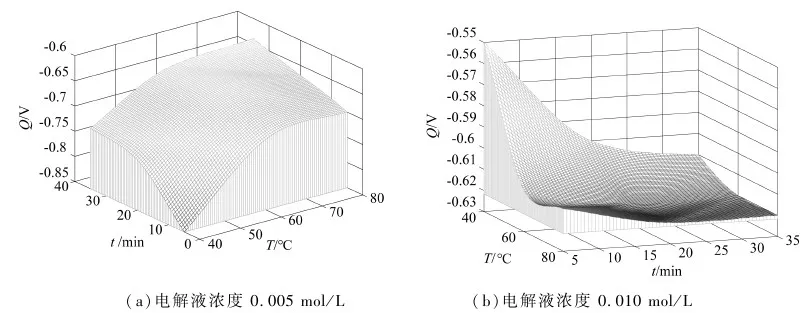
图3 腐蚀电位与沉积参数的关系
图4是试样的交流阻抗谱.可以看出,沉积时间5 min、沉积温度为40 ℃、电解液浓度高些(0.010 mol/L)时的曲率半径大,阻抗圆弧大,导电效果差,缓蚀性好.这和前面腐蚀电位分析的结论是一致的,沉积层的厚度致密性提高,造成导电性变差.说明,合适的工艺参数,有助于得到致密的氧化锌膜,利于改善缓蚀性.
图5为试样的XRD图谱,分析得到,通过沉积形成了ZnO涂层.图6为电解液浓度 0.010 mol/L的涂层的表面状态.图6(a)为沉积时间为5 min、沉积温度为40 ℃的试样,表面膜组织均匀而致密,表面空洞缺陷很少.图6(b)为沉积时间为20 min、沉积温度为60 ℃的试样的表面.可以看出,当温度和时间提高后,表面膜变得粗糙,表面有空洞缺陷.
3 结论
本文通过电沉积法,对钢基体表面氧化锌沉积层的耐腐蚀性做了研究.采用通过电化学中心测定出各种沉积状态的塔菲尔曲线和阻抗图谱.通过塔菲尔曲线得到的腐蚀电位及阻抗谱的变化规律,研究了打底层氧化锌电沉积参数对钢表面氧化锌沉积层的耐腐蚀性的影响.研究结果表明,电解液浓度为0.010 mol/L、沉积时间为5 min、温度为40 ℃的试样的腐蚀电位高,阻抗大,表面钝化区缩小,因此耐腐蚀性最好.电解液浓度、沉积时间及温度都会对腐蚀电位和阻抗谱有影响.电解液浓度提高后,温度过度提高、时间过度增加会离子运动加剧,所生成的氧化锌膜变得疏松,耐腐蚀性反而变坏.
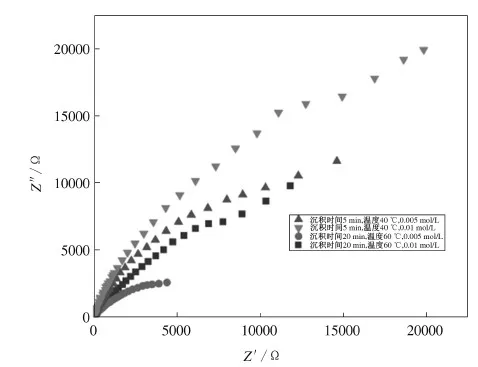
图4 不同沉积条件下的阻抗谱
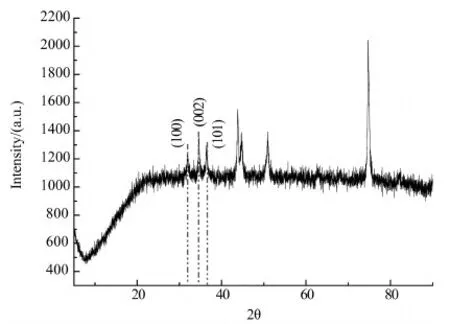
图5 ZnO膜的XRD图

图6 涂层形貌
[1] 张舒研,高洋洋,张志彬,等.高熵非晶合金耐腐蚀性能研究进展[J].材料工程,2021,49(1):44-54.
[2] 戴明杰,刘静,黄峰,等. 基于正交方法研究阴极保护电位波动下X100管线钢的点蚀行为[J].中国腐蚀与防护学报, 2020, 40(5):425-431.
[3] 薛宗岳. 氧化锌-石墨烯复合材料的制备及光响应研究[M]. 天津:天津大学出版社, 2011.
[4] 张娇娇,王鹤峰,邢学刚,等.电沉积Cu对纳米结构Ti-16Zr合金腐蚀性能的影响[J].功能材料,2018,49(10):10053-10058.
[5] 冯辉霞, 雷姣姣, 陈丽. 电化学沉积石墨烯/DLC复合薄膜的腐蚀性能研究[J].当代化工,2015, 44(8): 1729-1236.
[6] 张振岳. 不锈钢表面硅烷/氧化石墨烯膜层制备及其腐蚀性能研究[D].青岛:中国海洋大学,2015.
[7] 高博文,王美涵,闫茂成.2024铝合金表面PEDOT涂层的电化学制备及耐腐蚀性能[J].金属学报,2020,56(11):1541-1550.
[8] 韩燕, 郝迷花. 纳米 ZnO 复合涂层的制备及其对铝合金的防腐性能研究[J]. 西安石油大学学报(自然科学版),2011,26(6):79-82.
