电解锰阳极渣吸附硫酸锰溶液中钼的行为研究
2023-01-13贺跃李明东杨攀王松王海峰王家伟
贺跃, 李明东, 杨攀, 王松, 王海峰, 王家伟*
(1.贵州大学材料与冶金学院,贵阳 550025;2.贵州省冶金工程与过程节能重点实验室,贵阳 550025)
0 引 言
随着电池产业的不断发展,电池的性能要求不断提高,作为锰系电池最重要、最基础的锰源材料硫酸锰的纯度问题也不断被重视[1]。硫酸锰溶液中重金属离子(尤其是钼离子)对锰系材料电池的比容量、充放电性能及高温储存性能影响较大,因此硫酸锰溶液中重金属离子的深度净化,一直是锰行业研究的热点和重点[2-4]。目前关于硫酸锰溶液中重金属离子的除杂工艺较为复杂,主要有硫化物沉淀法、蒸发结晶法、离子交换法及溶剂萃取法等,这些方法除硫酸锰溶液中钼存在着工序复杂、效果不佳外,还存在成本及能耗高等缺点[5-8]。本文所用硫酸锰溶液经锰矿浸出而来,溶液中重金属离子种类多,相互干扰严重,要达到高效除钼的目的,需寻找一种新的方法。
而有着简单经济环保特点的吸附法逐渐被广泛使用,近年来,二氧化锰由于较高的比表面积和丰富的羟基结构在水体中吸附重金属离子取得了很好的效果,但是对于硫酸锰溶液体系中重金属的吸附研究较少[9-12]。夏文堂等采用化学二氧化锰和电解二氧化锰吸附硫酸锰溶液中钼取得了一定效果,吸附后的硫酸锰溶液中残余钼浓度低于0.015 mg/L,满足生产高纯硫酸锰要求[13-14]。本课题组前期采用新生二氧化锰和电解锰阳极渣对吸附硫酸锰溶液中钼的工艺条件、动力学和热力学等进行了探讨,但需进一步研究二氧化锰吸附硫酸锰溶液中钼的行为机理[15-16]。
本文对电解锰阳极渣吸附硫酸锰溶液中钼进行正交试验分析,结合Visual Minteq软件模拟硫酸锰溶液中Mn和Mo的离子形态随pH的变化关系,比较了不同pH下阳极渣的表面络合模拟数据与试验数据,阐明电解锰阳极渣吸附钼的行为和机理,为生产符合要求的电池级锰系正极材料提供理论依据及技术支持,同时妥善处理了电解锰阳极渣,减少了锰资源浪费和环境污染[17-18]。
1 实 验
1.1 试验原料
试验所需的吸附剂取自贵州铜仁某锰生产企业制备的纯净电解锰阳极渣,含钼的硫酸锰待吸附溶液取自贵州铜仁某电解锰企业的锰矿浸出液,成分由ICP分析得到,如表1所列。
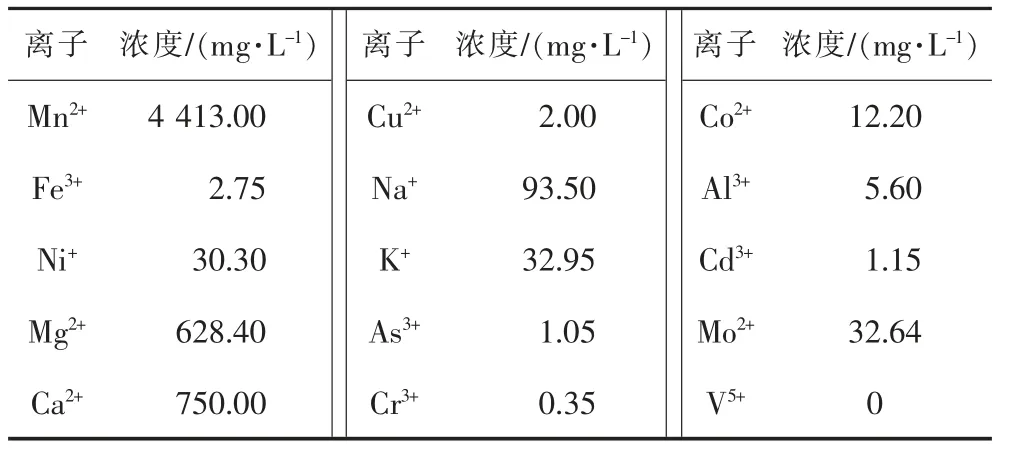
表1 锰矿浸出液成分Table 1 Composition of manganese ore leaching solution
1.2 仪器设备
实验主要仪器如表2所列。

表2 实验仪器Table 2 Equipments for the experiment
1.3 表 征
采用荷兰帕纳科有限公司的X’Pert PRO MPD衍射分析仪进行物相鉴定,采用日本日立公司的SU8020扫描电镜进行微观结构分析,FT-IR分析在美国尼高力公司生产的NICOLET IS 10红外光谱仪上采集,成分分析由安捷伦科技公司的Agilent-8800型ICP-MS质谱仪检测得出,Zeta电势用美国赛默飞公司生产的Zetasizer Nano ZS90型号激光粒度仪测定。
1.4 吸附实验
取500 mL含钼32.64 mg/L的硫酸锰溶液,用稀氨水和稀硫酸调节溶液至一定pH值,加入一定量的电解锰阳极渣,在80℃的水浴锅中不断搅拌,反应一段时间后快速将溶液过滤、洗涤、定容。采用ICP-MS测定溶液中残余钼浓度,电解锰阳极渣对钼吸附率Q采用如下公式计算:
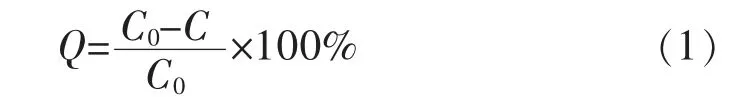
式(1)中:Q为吸附率;C0为初始浓度;C为吸附后浓度。
2 结果与讨论
2.1 电解锰阳极渣的表征
对电解锰阳极渣进行XRD分析,如图1所示。可以看出电解锰阳极渣成分较为复杂,主要以MnO2为主,掺杂着少量MnOOH、PbO和(NH4)3Fe(SO4)3。可见,MnO2在2θ=12.8°、28.7°、37.6°和65.7°出现明显的特征峰,与标准卡片(JCPDS-44-0141)吻合度较高,属于典型的α-MnO2,该结构的MnO2中存在较多的隧道和空穴,有利于吸附更多的钼离子。
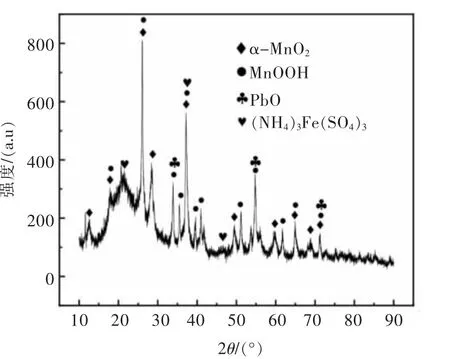
图1 电解锰阳极渣的XRD图谱Fig.1 XRD pattern of electrolytic manganese anode slag
电解锰阳极渣表面形貌和成分如图2所示,从SEM图可以明显发现电解锰阳极渣由不规则的纳米棒状相互交错团聚而成,有丰富的孔隙结构,这将提供更多的吸附位点,从而为吸附钼离子提供了条件。从EDS图可以进一步说明电解锰阳极渣表面主要有Mn和O两种元素组成,并存在着部分Pb元素。
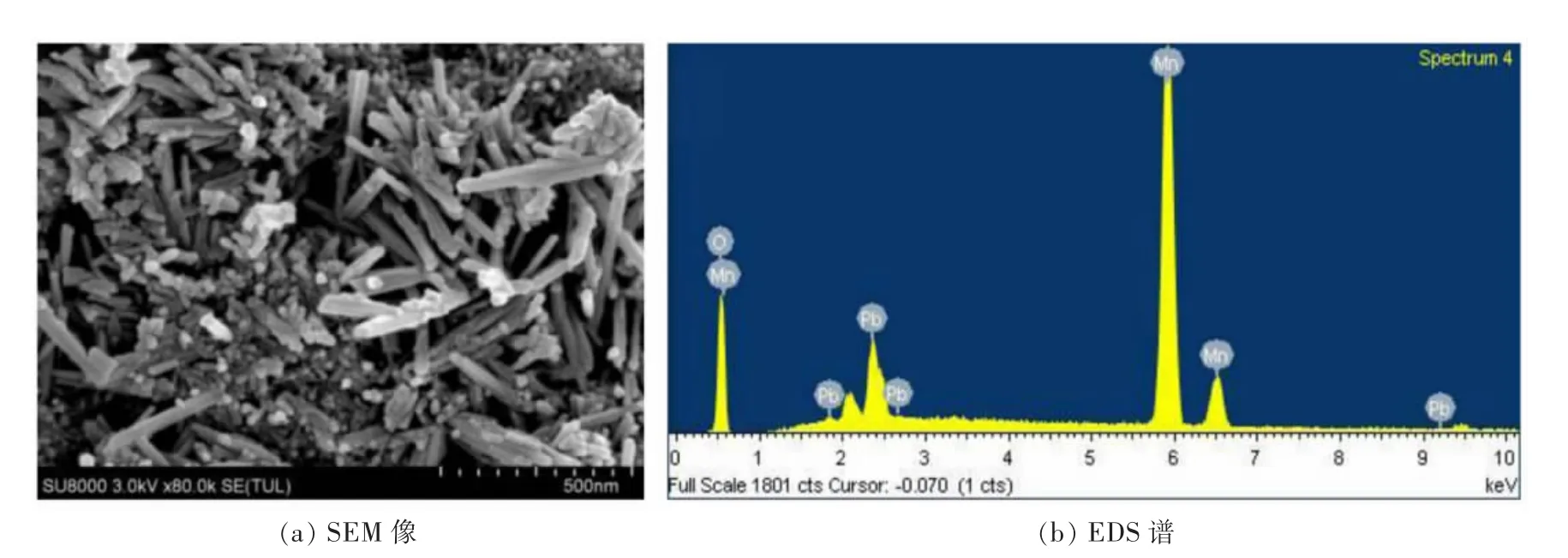
图2 电解锰阳极渣的SEM像和EDS谱Fig.2 SEM nd EDSimagesa of electrolytic manganese anode slag
采用FT-IR分析了电解锰阳极渣的红外光谱特征,如图3所示。电解锰阳极渣在3 407.21 cm-1处为表面羟基伸缩振动峰,在1 621.88 cm-1、1 147.62 cm-1和1084.48cm-1处为表面羟基弯曲振动峰,在594.96 cm-1、514.21 cm-1表示为Mn-O晶格振动特征峰,其他峰属于阳极渣中Pb、Fe等杂质的振动峰。电解锰阳极渣表面存在丰富的表面羟基,能与钼离子发生表面络合反应,使大量钼离子被吸附在其表面。
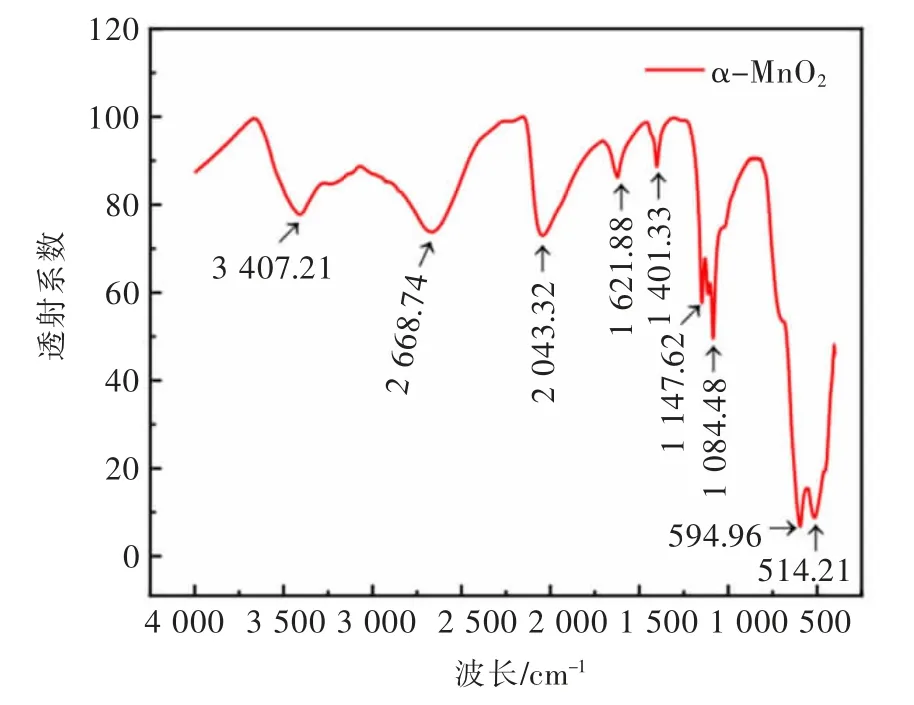
图3 电解锰阳极渣的FT-IR谱Fig.3 FT-IR of electrolytic manganese anode slag
图4所示为电解锰阳极渣的表面Zeta电势图,从图4中可以看出随着pH的升高,表面Zeta电势下降,通过计算可以得到电解锰阳极渣的等电点(IEP)为3.6。当溶液pH值高于3.6,电解锰阳极渣表面带负电;当溶液pH低于3.6,电解锰阳极渣表面带正电,能与带负电的钼氧阴离子基团发生吸附反应。
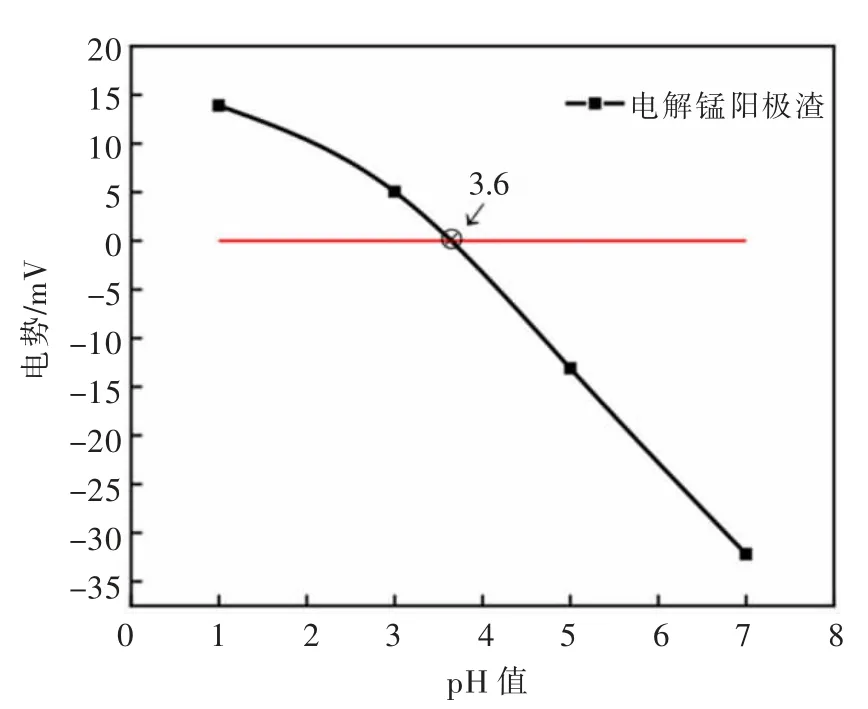
图4 电解锰阳极渣的表面Zeta电势Fig.4 Surface zeta potential diagram of electrolytic manganese anode slag
2.2 阳极渣吸附钼的正交试验分析
结合本课题组前期实验结果[15-16],以硫酸锰溶液pH值、二氧化锰添加量、反应时间进行正交试验。选用L9(34)正交试验表前3列安排试验方案,因素水平选择见表3。
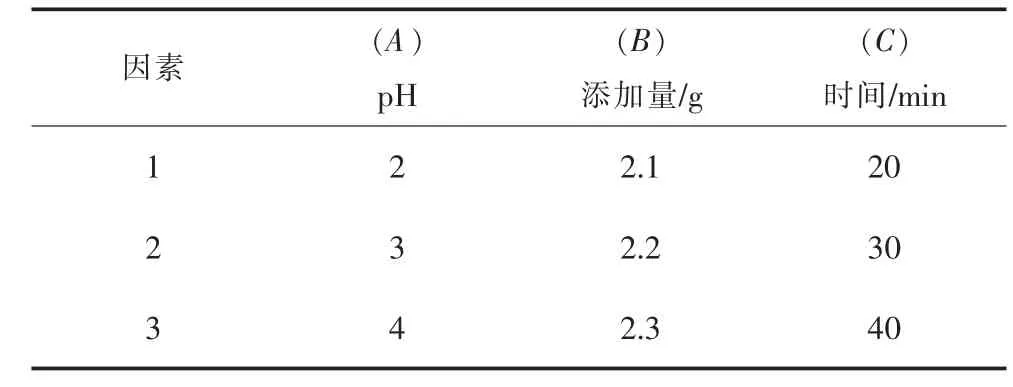
表3 试验因素水平表Table 3 Factor and level table of experiment
正交试验结果见表4。
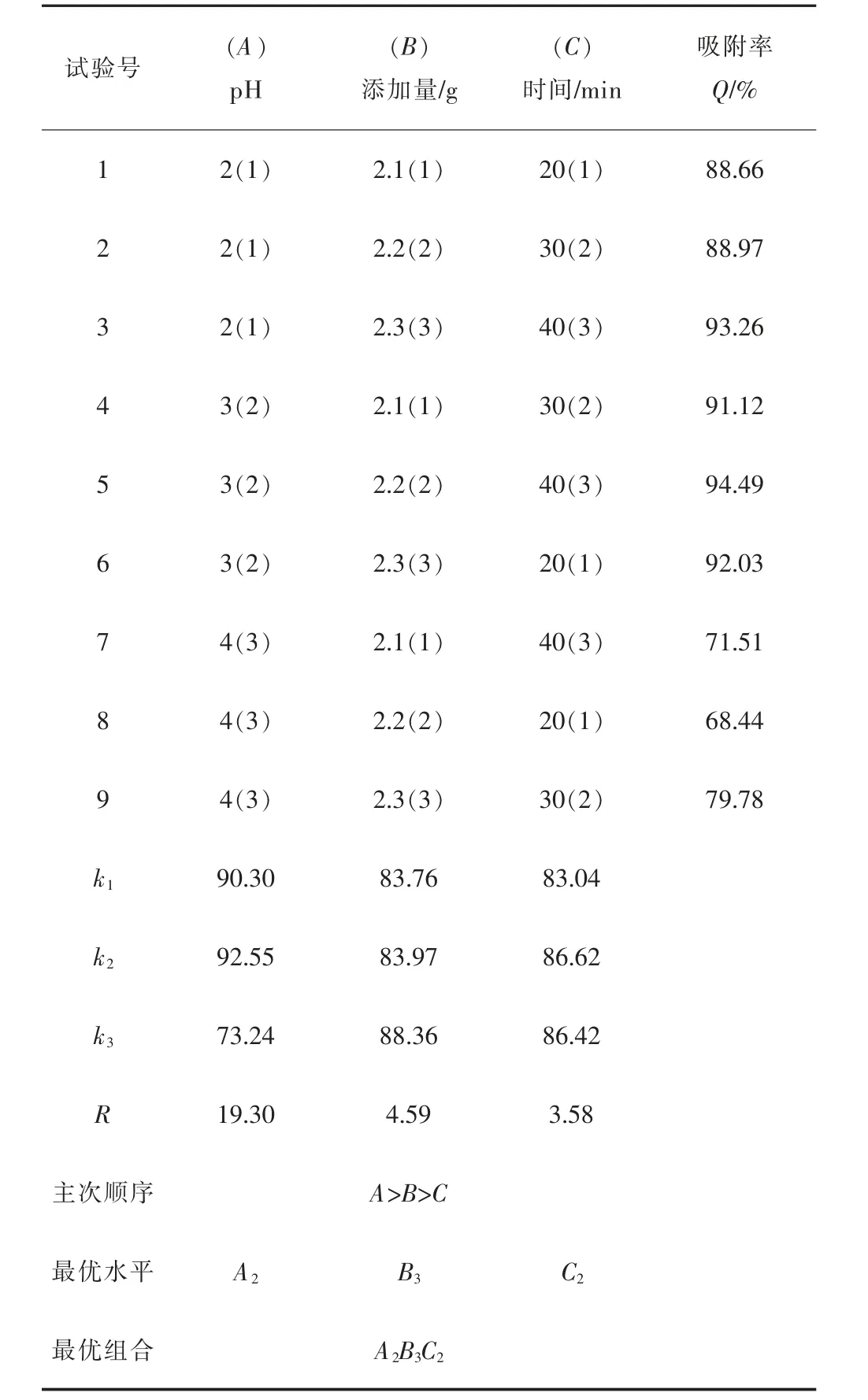
表4 正交试验结果Table 4 The result of orthogonal test
正交试验可通过对比极差来描述因素对指标影响的主次,该列因子水平变化反应对钼吸附率的影响大小。由表4可知,极差由强到弱顺序为RA>RB>RC,即各因素对电解锰阳极渣除钼影响的主次顺序为:硫酸锰溶液pH值>二氧化锰添加量>反应时间,反应较适宜的工艺条件为A2B3C2。极差分析未考虑误差的影响,为降低试验误差,进一步确定实验可靠性,继续进行方差分析,方差分析结果见表5。
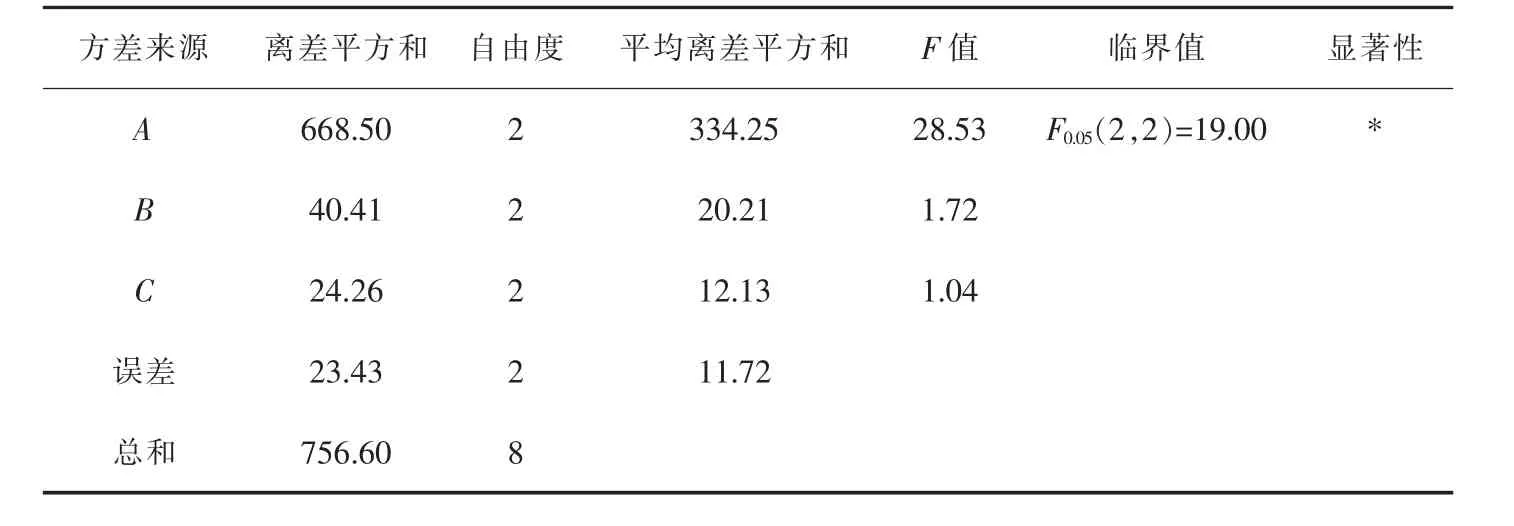
表5 方差分析Table 5 Analysis of variance
由表5可知,A因素对钼去除率影响显著,B因素对钼去除率影响不显著,C因素对钼去除率无显著影响,与极差分析结果一致,各因素对电解锰阳极渣去除硫酸锰溶液中钼影响的显著性顺序为:硫酸锰溶液pH值>二氧化锰添加量>反应时间。因此可以看出硫酸锰溶液pH值对电解锰阳极渣的吸附性能有显著的影响,深入研究硫酸锰溶液pH值如何影响钼离子吸附有望揭示其吸附机理。
2.3 不同p H下硫酸锰溶液中Mn和Mo的离子形态
Visual Minteq软件是基于溶液体系各组分的水解、配位、沉淀化学平衡原理来模拟溶液体系化学平衡以及利用表面络合模型进行吸附模拟的软件,在环境化学领域已经得到广泛应用[19-20]。利用Visual Minteq软件模拟硫酸锰溶液中Mn和Mo的离子形态随pH的变化关系,如图5所示。
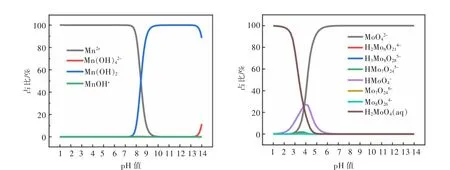
图5 不同p H下硫酸锰溶液中Mn和Mo的离子形态Fig.5 The ion forms of Mn and Mo in manganese sulfate solution at different p H values
根据图5可以发现,Mn在酸性条件下以Mn2+的形态存在,溶液pH值高于7.5时开始出现Mn(OH)2沉淀,pH较高时出现MnOH+,因此为了减少Mn损失,吸附反应最好控制pH值在8以下进行。而Mo在硫酸锰溶液中的形态较为丰富,主要以MoO42-、HMoO4-和H2MoO4(aq)形态以及微量的其他形态存在。Mo在溶液中通常形成阴离子基团,能更好地与阳离子基团或表面带正电的物质结合在一起。而电解锰阳极渣在pH值低于3.6时,表面带正电,能吸引带负电的钼氧阴离子基团,同时由于电解锰阳极渣表面带有大量羟基,能与钼离子基团发生表面络合反应,从而大大提高吸附效果。当硫酸锰溶液的pH值调整为低于3.6之后,引入的H+,对其直接加氨水就能调节。一般硫酸锰溶液处理后进一步电解会需要一定的氨根,所以加入少量的氨水基本不增加成本。
2.4 不同p H下阳极渣的吸附模拟数据与试验数据比较
不同pH下阳极渣的吸附模拟和吸附试验都在同一条件下进行,Mn离子浓度为4.413 g/L,Mo离子浓度为32.64 mg/L,温度为80℃,阳极渣添加量为2 g,时间为30 min,pH值为:1、2、3、4、5、6、7、8。吸附模拟采用漫反射层模型(DLM),这是最简单的模型,其中考虑了羟基的化学反应和静电反应对表面络合的贡献。D ZOMBAK等在其极具影响力的书籍表面络合建模[21]中使用了该模型,自那时以来,DLM一直是应用最广泛的表面络合模型(SCM)。模型参数如表6所列,电解锰阳极渣吸附位点参照张海鹏所测量的α-MnO2数据[22]。比表面积由美国麦克公司的ASAP 2460物理吸附仪测量所得,其他参数采用Visual Minteq软件系统自带数据。吸附模拟数据与试验数据对比情况如图6所示。

表6 模型参数Table 6 Model parameter
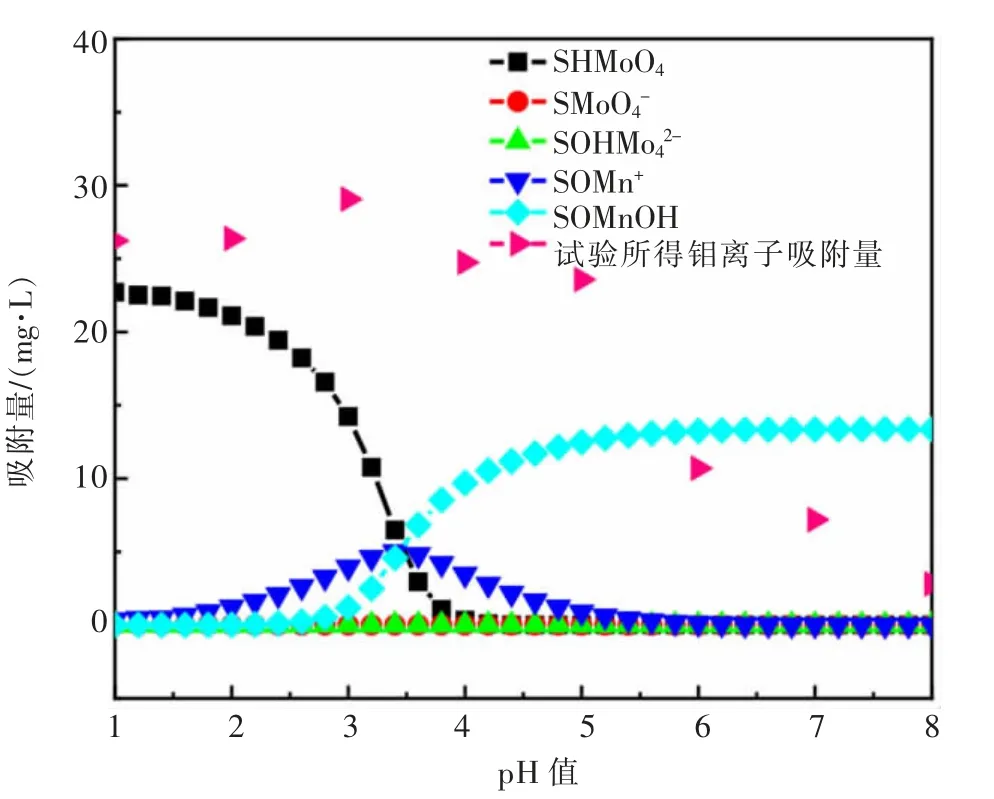
图6 不同p H值下阳极渣的吸附模拟数据与试验数据比较Fig.6 Comparison of adsorption simulation data and experimental data of anode slag at different p H
根据图6吸附模拟结果可以看出钼离子主要被电解锰阳极渣表面羟基(≡SOH)以≡SHMoO4络合形态吸附在其表面,随着pH值的升高,表面羟基位点被锰离子以≡SOMn+和≡SOMnOH络合形态占据,钼离子的吸附量逐渐减少,当pH值达到4时,表面羟基位点被锰离子完全占据[23]。该表面络合模型模拟结果仅针对阳极渣表面羟基对钼离子的络合作用,因此对钼离子的吸附量低于实际试验结果。从试验所得钼离子吸附量来看,钼离子的吸附量随pH值的升高呈先增加后减少趋势,pH值为3时,钼离子受阳极渣表面羟基络合、表面电荷吸引以及缺陷孔隙等共同作用,吸附效果较优。结合图5,当pH值低于3时,钼离子以不带电的H2MoO4(aq)形态存在,钼离子吸附效果主要受羟基络合作用影响。当pH值高于阳极渣等电点3.6时,阳极渣表面带负电,表面羟基位点被锰离子占据,钼离子仅通过进入阳极渣缺陷孔隙的方式被吸附,吸附效果大大减弱。
3 结 论
1)对电解锰阳极渣进行XRD、SEM、EDS、FTIR和Zeta表征发现该阳极渣主要成分为α-MnO2,形貌为孔隙丰富的棒状结构,存在着较多的表面羟基,等电点(IEP)为3.6。
2)通过正交试验分析发现反应条件对电解锰阳极渣除钼影响的主次顺序为:硫酸锰溶液pH值>二氧化锰添加量>反应时间。
3)模拟了硫酸锰溶液中Mn和Mo的离子形态随pH的变化关系,通过吸附模拟和吸附试验对比证明了钼离子被吸附是受阳极渣表面羟基络合、表面电荷吸引以及缺陷孔隙等共同作用。
