乳腺癌化疗相关心脏毒性预防及管理的最佳证据总结
2023-01-11马珠月程芳张柳柳邾萍陆宁宁姚珊珊史妍妍
马珠月 程芳, 张柳柳 邾萍 陆宁宁 姚珊珊 史妍妍
(1.南京医科大学 护理学院,江苏 南京211000;2.江苏省肿瘤医院 江苏省肿瘤防治研究所南京医科大学附属肿瘤医院,江苏 南京 210018)
世界卫生组织国际癌症研究机构(international agency for research on cancer,IARC)发布的最新癌症负担数据显示,乳腺癌已成为全球第1大癌,2020年确诊的乳腺癌患者高达226万例[1]。随着诊疗水平的提高,乳腺癌患者5年生存率已达90%,治疗前景可观[2]。现有的治疗方式主要包括化疗、放疗、靶向及内分泌治疗等,其中化疗是主要的治疗手段[3]。值得注意的是,化疗进程中蒽环类等化疗药物的广泛使用,虽有效提高了患者的生存率,但不可避免地带来一系列心律失常、心力衰竭等可逆或不可逆性的心脏毒性反应,此类药物作用于患者的心肌或心电传导系统,可发生在化疗任何一个阶段[4-5]。研究[6]显示,心脏毒性成为乳腺癌化疗患者自我报告最常见反应之一,且随访期间2年累积发生率达20.2%。心脏毒性的出现不仅导致治疗中断或延迟,还给患者的远期预后带来严重影响,成为非癌症性死亡的主要原因[7-8]。因此,心血管疾病等继发性后遗症对癌症幸存者尤为关键,积极预防和管理乳腺癌化疗相关心脏毒性具有重要意义。目前,国内外指南及共识对心脏毒性的知识内容庞大,临床医护人员在学习过程中不易理解,需对证据进行高度精炼和聚焦,以利于传播及应用。基于此,本研究对国内外心脏毒性相关证据进行系统检索,全面汇总出预防及管理的最佳证据,并对其进行严格的质量评价,旨在对乳腺癌化疗患者心脏毒性的预防与管理提供借鉴。
1 资料与方法
1.1问题确立 基于“如何预防及管理乳腺癌化疗相关心脏毒性”的临床问题,按照PIPOST模式将临床问题转化为循证问题[9]。证据应用目标人群(P,population):乳腺癌化疗患者;干预方法(I,intervention):包括心脏毒性风险评估与管理的干预措施等;证据应用专业人员(P,professional):临床医护人员或乳腺癌照顾者;结局(O,outcome):包括乳腺癌化疗患者心脏毒性发生率及风险因素;证据应用场所(S,setting):临床医疗机构或家庭;证据类型(T,type of evidence):包括临床决策、指南、专家共识及系统评价等。
1.2文献检索 按照“6S”证据模型[10]从上至下分别检索Up to Date、Cochrane Library、British Medical Journal、加拿大安大略注册护士协会网站(Registered nurses association of ontario,RNAO)、苏格兰院际指南网(Scottish intercollegiate guidelines network,SIGN)、美国临床肿瘤协会(American society of clinical oncology,ASCO)、美国国立指南网(National guideline clearinghouse,NGC)、中国医脉通指南网、PubMed、Embase、中国知网、万方数据库。中文检索词为:“乳腺癌/乳腺肿瘤/乳癌/乳房癌”“化疗/化学疗法”“心脏毒性”“预防/管理/防治/教育”。英文检索词为:“breast cancer/breast tumor/breast neoplasm*”“chemotherapy”“cardiotoxicit*/cardiac toxicit*”“prevention/management/educat*/care”。检索时限为建库至2022年1月31日。
1.3文献筛选 纳入标准:研究对象为乳腺癌化疗患者;涉及乳腺癌化疗相关心脏毒性的研究;研究类型为临床实践指南、系统评价/Meta分析、证据总结、专家共识等;语种为中文或英文。排除标准:无法获取全文;重复发表或内容不全;简要版本或指南解读类文献及文献质量评价未通过的证据。
1.4证据的质量评价、分级与汇总 根据原始文献类型进行相应的质量评价,对纳入的指南采用临床实践指南研究与评价系统(Appraisal of guidelines for research and evaluation instrument,AGREE II)(2009版)进行质量评价[11]。该量表共6个部分,23个条目,附加2个总体评价条目。指南的推荐等级分为3级:A级为6个领域得分均≥60%,可直接推荐;B级为得分≥30%的领域数≥3个,但有得分<60%的领域;C级为得分<30%的领域数≥3个。对纳入的专家共识类文献质量评价使用澳大利亚JBI循证卫生保健中心(2016版)评价工具[12]。该评价工具包括6个条目,各条目的评价标准为“是、否、不清楚、不适用”。对纳入的系统评价采用系统综述评价工具(Assessment of multiple systematic,Review,AMSTAR)[13]进行评价,该评价工具包括11个条目,各条目的评价标准为“是、否、不清楚、不适用”。证据汇总的原则:(1)将表达内容相似或互补的证据合并为一个证据体。(2)表达内容矛盾者,遵循高质量证据优先、最新发表优先的原则。本研究采用澳大利亚“JBI循证卫生保健中心证据分级及推荐级别(2014版)”进行预分级[14],根据研究和设计的严谨性将证据等级划分为5级(Level 1~5),其中Level 1级别最高,Level 5级别最低。再由2位研究者根据JBI的FAME结果指导,据可行性、适宜性、临床意义、有效性,并结合循证护理小组的推荐强度分级原则,将证据评为A级(强推荐)和B级(弱推荐)。整个证据的质量评价及汇总分级过程邀请7名研究人员参与,均具备循证医学或护理背景,当2名研究者对纳入的所有文献进行独立地分级和评价过程中出现不一致的结果时,统一由研究小组商讨决定。
2 结果
2.1文献检索结果 共检索到1 517篇文献。2位研究者依据文献纳入及排除标准独立阅读标题和摘要,排除明显不符合标准的文献后,对可能符合的文献阅读全文,最终筛选出11篇文献[15-25],包括4篇指南[15-18],3篇专家共识[19-21],4篇系统评价[22-25],文献筛选流程图,见图1。纳入文献的一般特征,见表1。

图1 文献筛选流程图
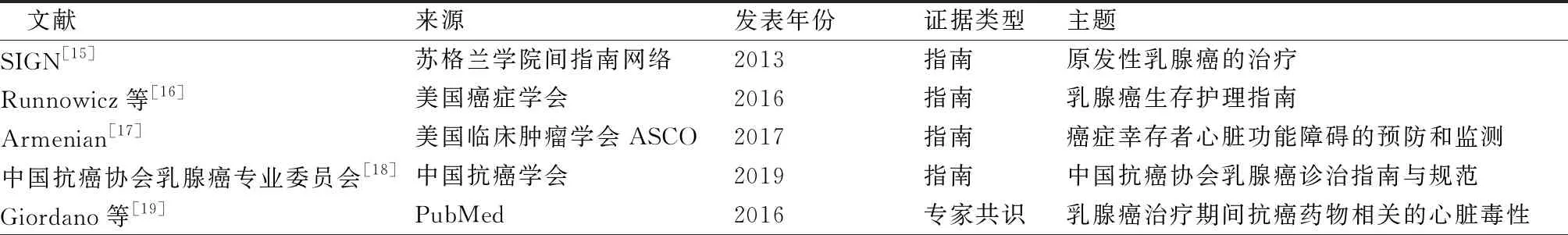
表1 纳入文献的一般特征(n=11)

续表1 纳入文献的一般特征(n=11)
2.2文献质量评价结果
2.2.1指南 共纳入4篇指南[15-18],质量评价结果,见表2。

表2 纳入指南的质量评价(n=4)
2.2.2专家共识 共纳入3篇专家共识[19-21],质量评价结果,见表3。

表3 纳入文献专家共识的质量评价(n=3)
2.2.3系统评价 共纳入4篇系统评价[22-25],质量评价结果,见表4。

表4 纳入文献的系统评价的质量评价(n=4)
2.3证据描述及汇总 本研究将最纳入的11篇文献[15-25]中表述相同的证据进行合并,经严格遴选和整理后,汇总为风险评估、早期表现识别、监测方式选择、预防治疗策略、风险管理、健康教育6个方面形成28条最佳证据,其中有16条强推荐(57.14%)和12条弱推荐(42.86%),见表5。

表5 乳腺癌化疗相关心脏毒性的预防及管理最佳证据总结
3 讨论
3.1证据总结的实践意义 乳腺癌化疗相关心脏毒性为接受化疗的乳腺癌患者较常见的不良反应,且伴随后续治疗方案可能对心脏有进一步的损害,使得心脏问题逐渐突出,影响患者的长期生存质量[26]。因此,在乳腺癌患者化疗期间,医护人员应重视心脏不良反应,预防与管理化疗药物造成的心脏毒性。现临床工作中,部分医护人员对心脏毒性的危险因素和防治措施认知不全,无法识别高危患者、判断心脏相关参数,从而准确地进行全面的健康教育[27]。本研究证据总结了风险评估、早期表现识别、监测方式选择、预防治疗策略、风险管理及健康教育6个方面,内容比较全面,尤其对心脏毒性的监测方式描述详细,对心脏毒性的预防及管理具有一定的参考价值。
3.2心脏毒性的风险评估与早期监测 化疗前应做好病史收集[23],确认患者是否存在高龄、吸烟、肥胖、高血压、糖尿病、高血脂症及化疗、放疗、靶向治疗等心脏毒性的高危因素。欧洲肿瘤内科学会(ESMO)将心脏毒性定义为LVEF下降10%~53%[17]。但LVEF降低一般发生在心脏毒性晚期,对亚临床心脏损伤不敏感[21]。证据指出,斑点追踪超声心动图可检测GLS,较基线下降超过15%时需警惕,为最佳心肌应变参数,推荐用来早期监测心脏毒性[24]。由于超声检测技术存在较大差异[18],可联合生物标志物如肌钙蛋白(cTnT/I)、利钠肽(BNP)等,首先监测血清,再依据是否高危行影像学检查,既节约医疗资源又减轻经济负担。目前监测的最佳频率尚未明晰,应由医生结合患者的病情来判断,cTnI在每次化疗周期前及末次化疗周期后12个月进行监测,BNP在基线及末次化疗周期监测[18],LVEF在每次化疗周期前或至少3个月监测1次,研究显示,联合检测的敏感性和特异性高于单独监测[28],因此,还需进一步探索心脏毒性相关参数指导预防心脏毒性的意义,临床工作中,医护人员可结合临床实际进行决策。
3.3心脏毒性的预防与治疗 目前,化疗所致心脏毒性的保护策略包括药物预防和运动预防。证据指出,蒽环类药物为常用化疗药物,且与累积剂量有关,为不可逆性心脏损害[16]。因此,首选心脏毒性较低的多柔比星脂质体以限制心肌暴露[17-18];其次,需严格控制药物累积剂量,对于蒽环类药物而言,控制在350~400 g/m2[20],但研究[29]显示累积剂量仅为50 g/m2时,对心室收缩和舒张功能已产生障碍,即开始应用时就可能出现了心脏器质性损害[29]。此外,可通过降低峰浓度达到持续性缓解药物心脏毒性[20-21]。目前,心脏保护剂包括β受体阻滞剂、血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体阻滞剂(ARE)等均被证实了能短期降低心脏毒性发生[15,18,21]。关于运动,选择有氧运动提高机体抗氧化能力,增加体内抗氧化物的活性与数量,一定程度减轻了心脏毒性[25]。
3.4心脏毒性的风险管理与健康教育 心脏毒性的早期诊断与治疗需要多学科团队共同协作,充分利用多学科、多模态手段对肿瘤治疗相关心血管功能和结构改变进行追踪,多学科管理有力地保证了癌症治疗的最佳性和延续性[17-18]。George等[30]构建的接受蒽环类化疗药的转移性乳腺癌患者心脏毒性预测模型有助于筛选出患者是否为心脏毒性高危人群,量化了风险概率值,能有效指导医疗人员根据患者的危险因素分层,安全合理用药,发挥化疗药物疗效的同时有效控制心脏毒性事件。因此,建立我国乳腺癌化疗患者心脏毒性预测模型有益于指导医护更好地预防管理患者。除了应用心脏毒性风险评估工具及定期的筛查,在患者的治疗间歇期和康复期,有效的健康教育仍是患者早期风险预警的重要依托[16,25],医护人员应加强沟通交流能力,减少宣教的群体异质性,强调不健康的生活方式对心脏毒性风险的危害性及严重性,增加患者的防范意识;应制定合理的出院计划,指导患者及家属如何识别心脏相关不良反应,及时汇报医生,以便控制心脏不良事件发生。
3.5对未来研究的展望 研究者通过此次系统检索,发现目前对于乳腺癌化疗相关心脏毒性的预防和管理内容已比较全面,监测方式多样性,但目前监测选择还比较单一,各医疗机构对证据推荐中的策略执行报告欠缺。因此,应充分开展循证实践,促进最佳证据向临床转化,在后续的研究中,增加医护人员对乳腺癌化疗相关心脏毒性的预防及管理知识,组建管理梯队,形成基于循证的管理策略与流程,对患者进行持续动态的风险评估及预防管理,完善临床护理工作。
4 小结
本研究通过规范的证据汇总方法,总结了乳腺癌化疗相关心脏毒性预防和管理的最佳证据,为临床医护提供了参考。围绕着风险评估、早期表现识别、监测方式选择、预防治疗策略、风险管理和健康教育展开,但纳入英文文献较多,与我国国情、医疗条件及患者特征均存在一定差异,因此医护人员在证据转化在应用过程中应当充分结合临床实际,合理选择,以提高证据应用的科学性和实用性。
