人TEFM基因shRNA真核表达载体的构建及其干扰效果鉴定
2023-01-07刘如爱飞再镱王播勇
刘如爱,飞再镱,李 彬,杨 玺,王播勇,余 敏,熊 伟
(1.大理大学 基础医学院,云南 大理 671000;2.云南省高校临床生物化学检验重点实验室,云南 大理 671000;3.云南大学 生命科学学院,云南 昆明 650091)
0 引言
人线粒体转录延伸因子(mitochondrial transcription elongation factor,TEFM)是核基因编码的蛋白质,也是调控线粒体基因复制和转录转换的重要因子[1].线粒体DNA(mitochondrial DNA,mtDNA)的转录终止发生于复制起始位点附近的G-四联体区域,而TEFM对这一过程有抑制作用.同时,TEFM与线粒体RNA聚合酶(mitochondrial RNA polymerase,mtRNAP)和新生转录本的相互作用阻止了复制引物的产生,并增强转录延伸的过程,充当mtDNA复制和转录之间的分子开关[2].通过邻近标记分析、亲和纯化和质谱分析,已鉴定出大量可能与TEFM存在相互作用的RNA加工相关的蛋白质,提示转录延伸并非TEFM的唯一功能,线粒体RNA的加工也受TEFM的调控[2].此外,线粒体耗氧试验结果显示,TEFM基因敲除后细胞的线粒体耗氧量降低,呼吸链复合物蛋白亚基的表达受到抑制,严重影响了氧化磷酸化(oxidative phosphorylation,OXPHOS)的活性,表明TEFM对于线粒体正常功能的维持至关重要[2].目前,有研究发现TEFM基因在脑胶质瘤组织和细胞中过表达,其基因表达水平与脑胶质瘤患者的多个临床病理参数具有显著相关性[3].笔者设计并构建了4个靶向人TEFM基因的短发夹(short hairpin RNA,shRNA)干扰表达载体,并通过转染构建稳定转染的脑胶质瘤U87细胞,检测其对TEFM基因的干扰效率,为深入发掘TEFM在脑胶质瘤中的生物学功能和作用机制奠定实验基础.
1 材料与方法
1.1 实验材料
1.1.1 菌种、载体和细胞
实验中所用的正常人脑星形胶质细胞HA1800和人脑胶质瘤T98G、U251、U87细胞株均购置于中国科学院上海细胞库,TreliefTM5α感受态菌株购自北京擎科生物科技有限公司昆明分公司,shRNA真核表达载体psi-U6由云南大学生物化学与分子生物学实验室提供(图1),DNA寡聚核苷酸片段由上海生工生物工程股份有限公司合成.
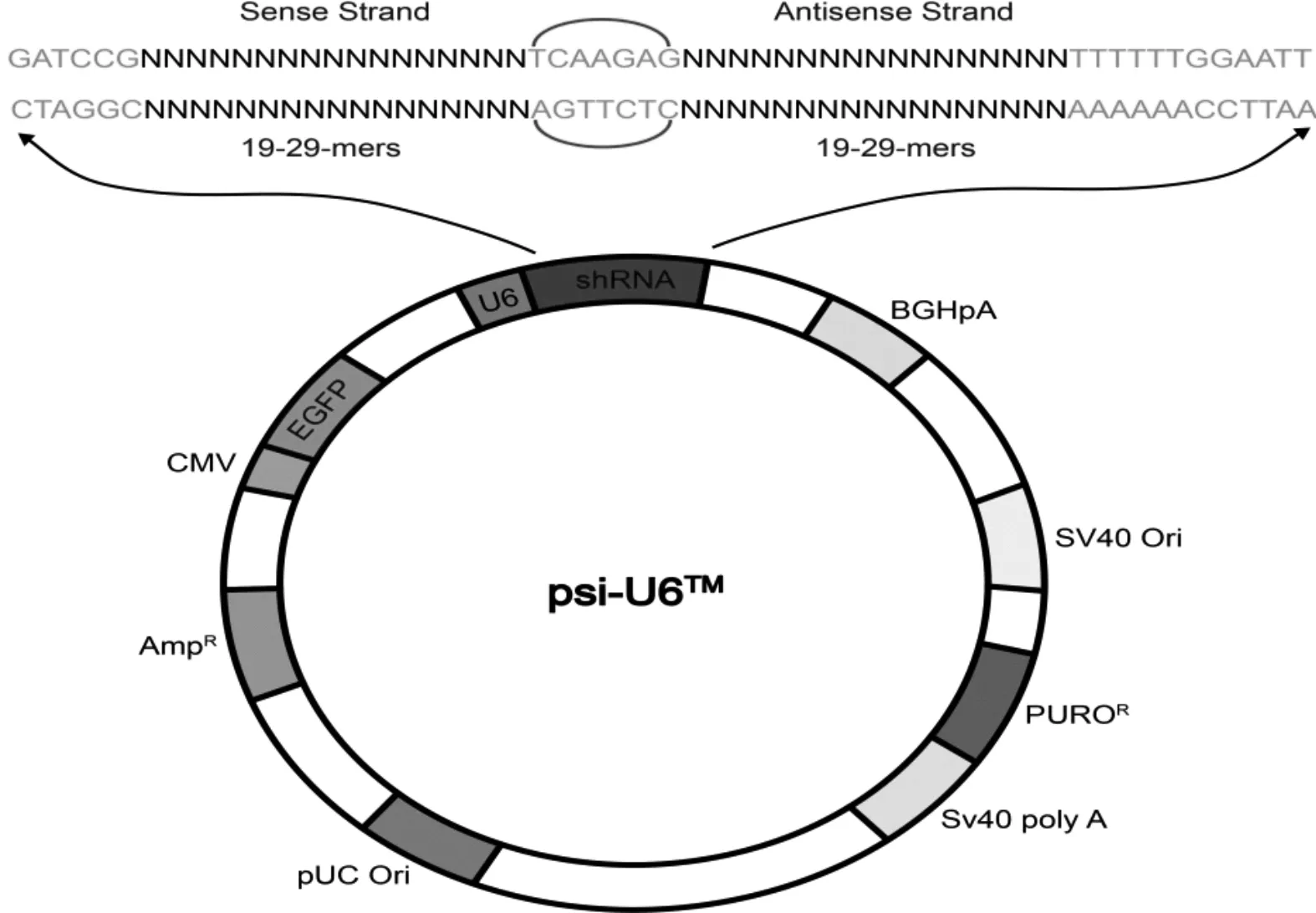
图1 psi-U6 shRNA真核表达载体示意图
1.1.2 实验试剂
DMEM高糖液体培养基、Opti-MEM液体培养基购自Hyclone公司,特级胎牛血清来自Gibco公司;逆转录试剂盒、T4 DNA连接酶、SYBR premix Ex Taq购自Abclonal公司;0.25%胰蛋白酶、青-链霉素、RIPA(强)细胞裂解液、BCA蛋白浓度定量试剂盒、LipofectamineTM6000转染试剂购自Beyotime公司;100×青霉素/链霉素购自Solarbio公司;PVDF膜来自Cytiva公司;HQ高纯度质粒DNA提取试剂盒来自Tiangen公司、TRIzol试剂购自biosharp公司;兔抗人TEFM多克隆抗体购自Abcam公司;鼠抗人GAPDH单克隆抗体、辣根过氧化物酶标记山羊抗兔抗体来自Servicebio公司;酵母提取物、DEPC水、蛋白胨及其他生化试剂购自Solarbio公司;DNA测序由北京擎科生物工程公司完成.
1.2 实验方法
1.2.1 TEFM基因shRNA靶向寡核苷酸的设计和制备
根据GenBank数据库提供的TEFM基因的核苷酸序列(基因号GI:79736),结合TEFM mRNA的核苷酸序列(NM_024683.3)及Tuschl设计原则[4-5],利用Ambion公司(http://www.ambion.com/techlib/misc/siRNA_finder.html)在线设计了4个shRNA干扰序列片段(表1).将候选的序列片段通过美国生物技术信息中心(NCBI)进行Blastn同源性比对分析,未发现包含该基因的其他基因,说明4个靶点特异性较高,根据psi-U6真核表达载体的要求,设计的每条序列两端均包含EcoRⅠ和BamHⅠ酶切位点.
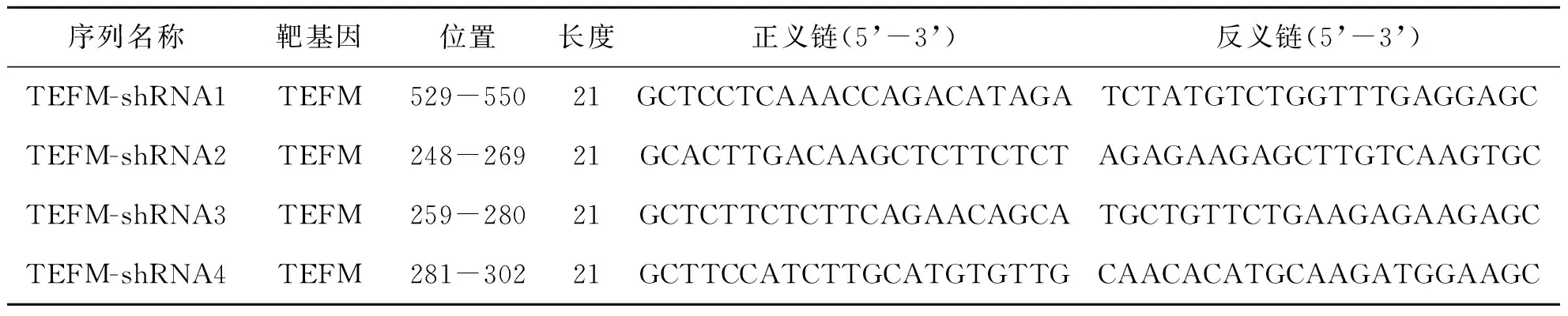
表1 靶向人TEFM基因的4条shRNA序列信息
1.2.2 靶向TEFM基因的shRNA表达载体构建与鉴定
psi-U6质粒载体进行EcoRⅠ和BamHⅠ双酶切,1.5%琼脂糖凝胶电泳后,切胶回收目的载体;将合成的寡聚核苷酸互补链分别用10 mmol/L Tris-HCl pH8.0、50 mmol/L NaCl、1 mmol/L EDTA退火缓冲液溶解,然后置于沸水浴中,进行单链退火反应,待水温缓慢降低至室温形成带有黏端的双链DNA.将不同的退火产物用T4 DNA连接酶分别连接入psi-U6真核表达载体中,构建4个TEFM-shRNA重组真核表达载体,吸取出酶连接产物加入到20 μL TreliefTM5α感受态菌株中进行热激转化,挑选氨苄青霉素(Amp)抗性单克隆,每个平板分别挑选4个克隆进行PCR鉴定.PCR鉴定正向引物(F):5’-CCGACAACCACTACCTGA-3’,反向引物(R):5’-CTCTACAAATGTGGTATGGC-3’;DNA测序正向引物(F):5’-ATGCTTACCGTAACTTGAAAG-3’,反向引物(R):5’-CTCTACAAATGTGGTATGGC-3’.保留菌种并送测序,使用BioEdit软件将测序结果与设计序列进行比对,比对结果完全符合的质粒即为目的质粒.将成功构建的4个重组干扰质粒分别命名为:TEFM-shRNA-1、TEFM-shRNA-2、TEFM-shRNA-3、TEFM-shRNA-4.
1.2.3 U87细胞培养与细胞转染
人脑胶质瘤U87细胞用含10%胎牛血清的DMEM完全培养基于37 ℃和5%CO2条件下培养.将细胞按 1×106个细胞/孔接种于6孔板内,设置为以下6组:空白对照组(未转染)、阴性对照组(转染psi-U6空载体, NC组)、TEFM-shRNA-1组、TEFM-shRNA-2组、TEFM-shRNA-3组、TEFM-shRNA-4组,每组设置3个重复.待细胞达到80%~90%的生长密度时,使用LipofectamineTM6000 Reagent 对细胞进行转染[6].
1.2.4 荧光显微镜观察转染效率
由于质粒携带绿色荧光蛋白基因(enhanced green fluorescent protein,EGFP),转染48 h后在荧光显微镜下观察细胞转染效率,488 nm光线波长激发下观察荧光反应,可观察到成功转染的细胞内由于表达EGFP而发出明亮的绿色荧光; 未转染的细胞中则未见任何荧光反应.细胞转染率=(阳性细胞数/计数细胞总数)×100%[7].
1.2.5 嘌呤霉素筛选shRNA敲低TEFM基因的稳定转染U87细胞
嘌呤霉素敏感的最优浓度筛选:将U87细胞通过培养基稀释到l 000个细胞/mL,接种至24孔板内,每孔1 mL;接种后第2天在100 μg/mL~1 mg/mL的嘌呤霉素浓度范围内进行筛选;每隔3 d~5 d换1次培养液,保持嘌呤霉素浓度不变;选择在10 d~14 d内使细胞全部死亡的嘌呤霉素最低浓度来进行下一步的试验筛选.重组shRNA真核表达载体转染细胞和稳定细胞系的筛选:将各组不同质粒转染后的U87细胞培养48 h后,待细胞密度达到60%~80%汇合,换用含嘌呤霉素最优浓度的培养基,每隔3 d~5 d换用新鲜的含有最适浓度的嘌呤霉素的培养基至抗性细胞长满,抽提RNA鉴定目的基因存在,传代及冻存细胞株,用于后续实验.
1.2.6 qRT-PCR检测TEFM基因mRNA表达水平
分别培养TEFM shRNA稳定转染的U87细胞、NC组及空白对照组的细胞,待各组细胞密度达到80%~90%时,弃去原培养液,用预冷的1×PBS洗漂3次,按Trizol说明书操作提取总RNA.据TEFM基因和β-actin基因(内参基因)序列设计qPCR反应的引物(表2).使用逆转录试剂盒逆转录形成cDNA,按照qPCR master mix试剂说明书配制成20 μL的qPCR反应体系,采用95 ℃ 2 min(预变性),95 ℃ 10 s、55 ℃ 30 s、72 ℃ 30 s(40个循环),72 ℃ 1 min进行PCR反应.根据qRT-PCR结果中Ct值分析mRNA的表达量F,F=2-△△Ct,△△Ct=(待测样品的目的基因的Ct平均值-待测样本的内参基因的Ct平均值)-(对照样品的目的基因的Ct平均值-对照样本的内参基因的Ct平均值).根据不同样本的表达量计算干扰效率=(NC组表达量-干扰组表达量)/NC组表达量.实验重复3次.
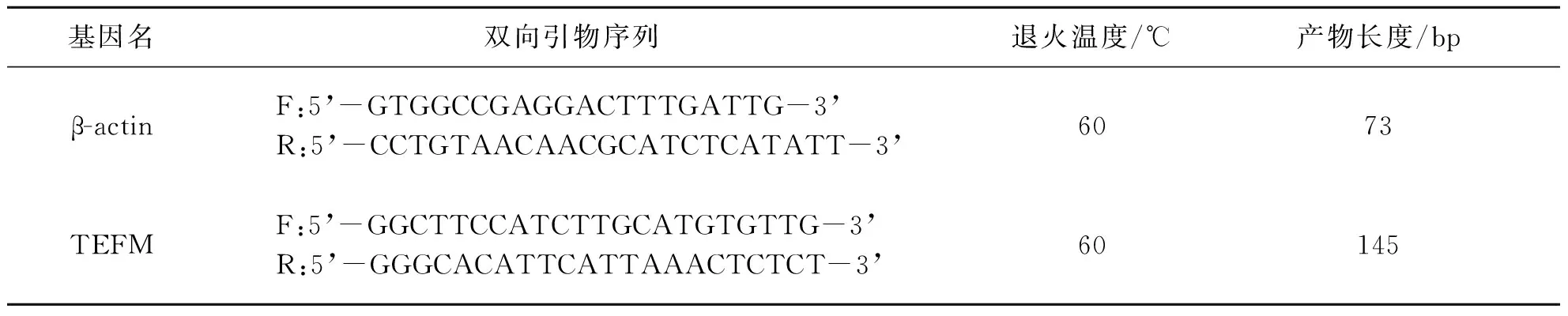
表2 RT-PCR引物列表
1.2.7 Western blotting检测TEFM蛋白表达水平
分别培养稳定转染的U87细胞、NC组及空白对照组细胞.采用RIPA 裂解液(分别加入EDTA和蛋白酶抑制剂混匀,与RIPA体积比均为1100)提取各组细胞的总蛋白质,通过BCA浓度测定试剂盒进行蛋白质浓度测定,加入上样缓冲液煮沸变性蛋白后,上样进行SDS-聚丙烯酰胺凝胶电泳(SDS-polyacrylamide gel electrophoresis,SDS-PAGE).将甲醇PVDF膜极性面紧密贴敷于胶上,转膜2 h,取出的PVDF膜封闭于0.5%脱脂牛奶中2 h,用PBST润洗膜5 min,重复3次,将PVDF膜根据所需蛋白所在条带位置进行切割,分别孵育于不同的一抗中过夜,而后取出膜,洗膜 5 min,重复3次,再根据目的蛋白抗体的种属来源情况,将其孵育于不同的二抗中2 h,取出洗膜5 min,重复3次,加上发光液后在化学发光仪上发光显影进行图像采集.使用Gel-Pro analyzer软件分析蛋白质条带的灰度值(蛋白相对表达量=条带灰度测定值/相应内参条带的灰度测定值).实验重复3次保证重复性.
1.2.8 统计学分析
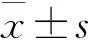
2 结果
2.1 TEFM蛋白在正常人脑胶质细胞和胶质瘤细胞中的表达差异
通过Western blotting检测3株人脑胶质瘤细胞和1株正常人星形胶质细胞(HA1800)中TEFM蛋白的表达水平,结果显示,TEFM蛋白在脑胶质瘤细胞株T98G、U251和U87 中表达水平均显著高于正常细胞株HA1800,其中以U87细胞内TEFM蛋白表达水平最高(图2).因此,笔者选取U87细胞构建稳定敲低TEFM基因的细胞株进行后续的研究.
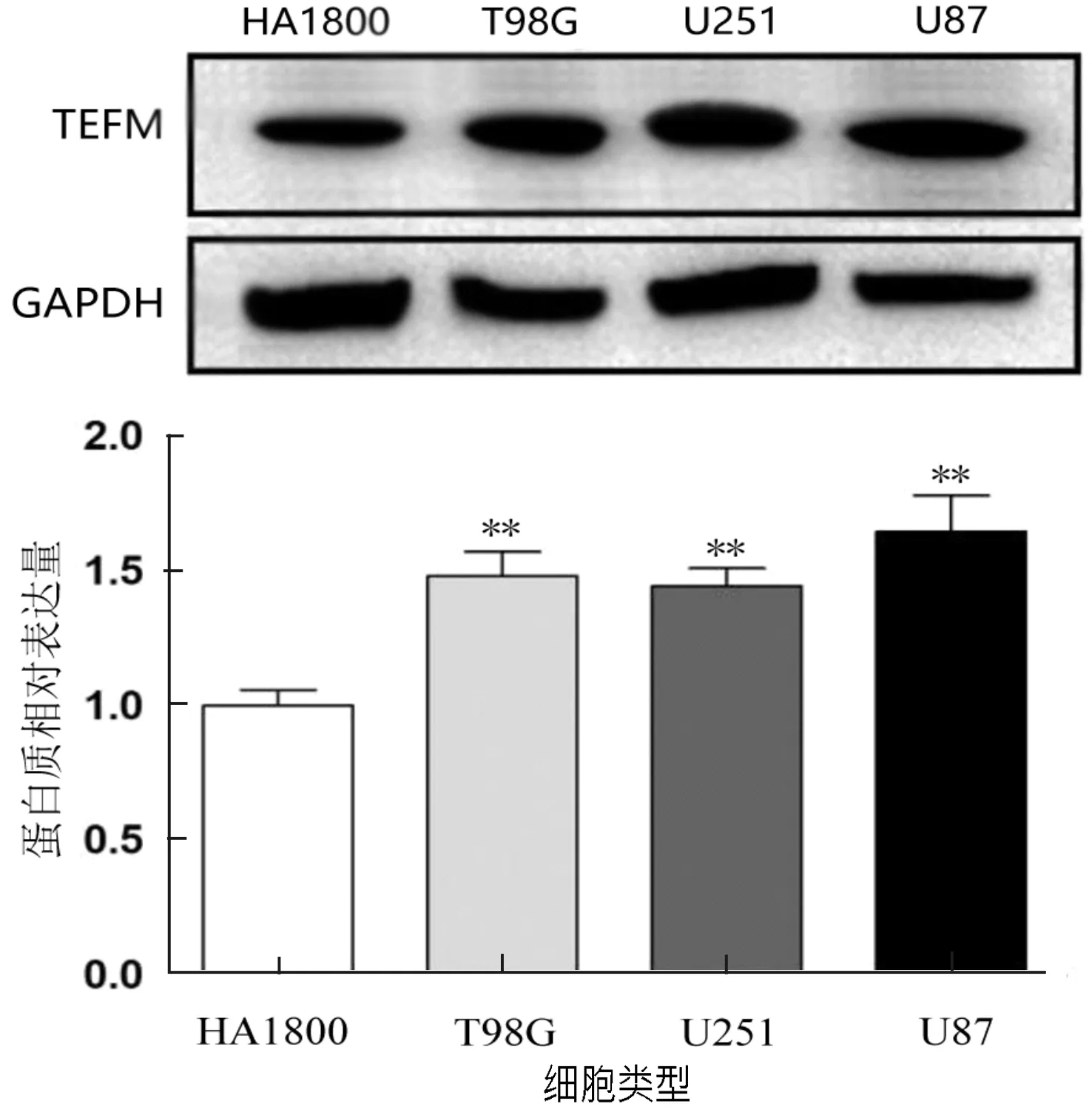
图2 TEFM蛋白在正常人星形胶质细胞和人脑胶质瘤细胞中的表达差异
2.2 靶向TEFM基因的shRNA真核表达载体的构建与鉴定
将合成的4条shRNA序列退火成双链后,与经EcoRⅠ和BamHⅠ双酶切的psi-U6载体DNA连接并转化大肠杆菌感受态细胞,分别挑取单克隆进行PCR鉴定和DNA测序.PCR鉴定结果提示,PCR扩增产物的大小均与预期的片段大小一致,说明目的片段已插入序列之中(图3(a)).经DNA测序鉴定证实,合成的双链与psi-U6真核表达载体连接成功,插入片段的测序结果与设计的序列完全一致,未发现有插入、缺失及突变(图3(b)).
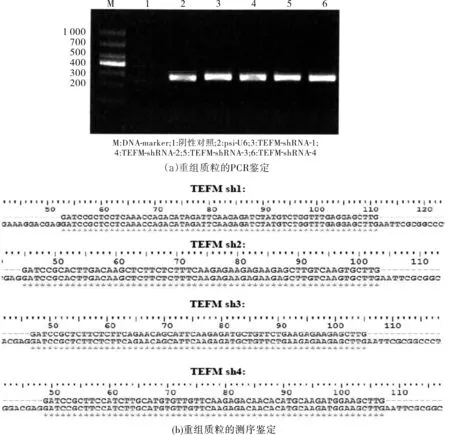
图3 TEFM-shRNA质粒的 PCR鉴定与测序鉴定
2.3 不同shRNA真核表达载体对TEFM基因mRNA表达的抑制效率
以未经转染的U87细胞为空白对照,qRT-PCR检测分别稳定转染4个TEFM-shRNA真核表达载体和psi-U6(NC组)的U87细胞内人TEFM基因mRNA的表达情况.扩增曲线与熔解曲线均良好.qRT-PCR结果显示,扩增曲线呈S型,有明显的4个时期,且复孔的CT值几乎一致(图4).与空白对照组相比,阴性对照组没有影响TEFM基因mRNA的表达水平,4个shRNA真核表达载体均能够不同程度地降低U87细胞内TEFM基因mRNA的表达,且组间差异显著(P<0.01),mRNA表达量的抑制率分别为63.6%、65.2%、76.5%和78.8%,以上结果提示,shRNA-TEFM-3、shRNA-TEFM-4质粒的抑制效果最佳(图5).
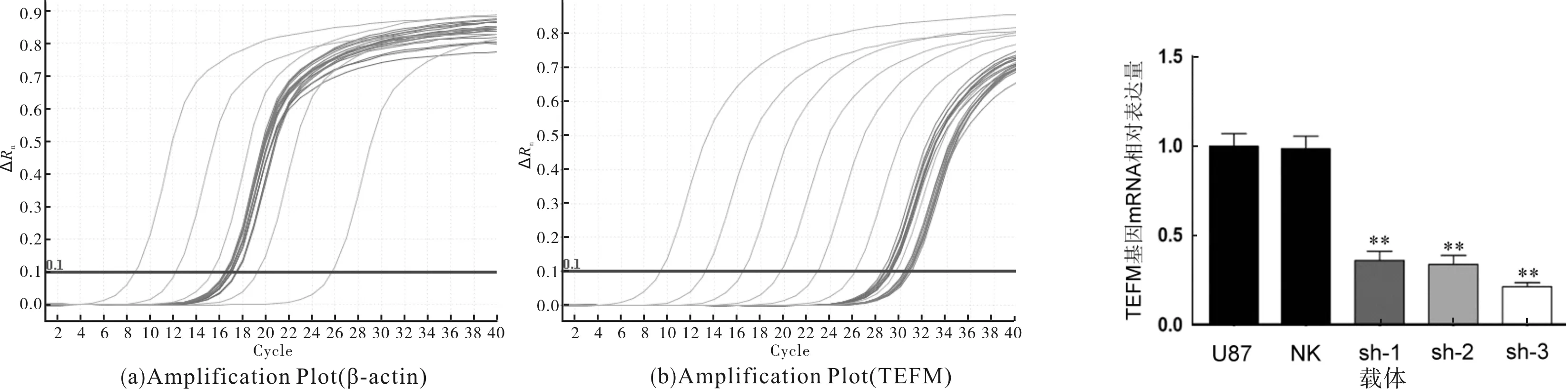
图4 PCR扩增曲线 图5 TEFM基因mRNA的相对表达量
2.4 不同shRNA真核表达载体对TEFM蛋白表达的抑制效率
以未转染的U87细胞为空白对照组,通过Western blotting检测各组细胞内人TEFM蛋白的表达情况.结果显示,各组内参蛋白GAPDH的表达未受影响,NC组U87细胞内TEFM蛋白的表达未见显著差异(P>0.05).与空白对照组相比,稳定转染4个shRNA真核表达载体后的抑制效果极其显著(P<0.01),蛋白质表达量的抑制率分别为51.2%、53.2%、69.5%和74.8%.其中,shRNA-TEFM-3、shRNA-TEFM-4重组真核表达载体对U87细胞内TEFM蛋白表达的抑制最有效(图6).
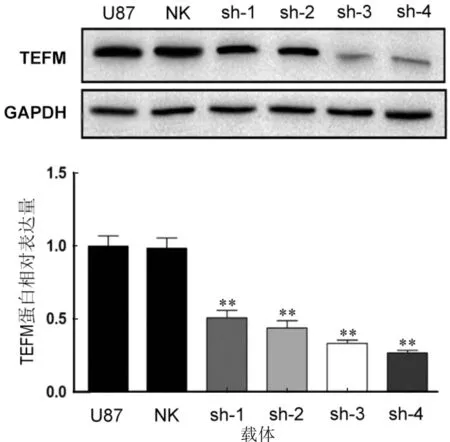
图6 shRNA干扰载体转染U87细胞后TEFM蛋白的相对表达量
3 讨论
线粒体在调节细胞能量代谢、生物合成和细胞凋亡中起着关键作用,是真核细胞中的重要细胞器.线粒体功能障碍与众多人类疾病(如癌症、神经退行性疾病、糖尿病和心脏病)密切相关.研究发现,TEFM是参与线粒体转录延伸和复制的重要调控因子[8].但目前,关于TEFM的报道多为体内和体外的功能研究,其在恶性肿瘤发生发展中的作用报道较少.有研究通过敲除TEFM发现心脏中线粒体蛋白质组发生了重大变化,且TEFM对胚胎的存活至关重要[2].通过对转录过程的广泛研究,确定了TEFM可与POLRMT相互作用以完成接近基因组长度的转录.研究人员通过进行带有POLRMT截短型突变体的pull-down实验,结果显示在强力霉素诱导型启动子控制下的瞬时表达TEFM的HEK细胞中,只有诱导表达TEFM基因时才能检测到带Myc标签的POLRMT,因此TEFM能与POLRMT的催化区域相互作用,极大地促进了mtDNA转录延伸过程的进行[6].此外,有研究通过提取TEFM表达受抑制的人骨肉瘤HOS细胞中的线粒体转录物,并对其转录产生的mRNA和rRNA水平进行定量,结果提示TEFM RNAi细胞的线粒体长转录本显著减少[7],由此推断TEFM能促进长转录本的形成.近年,随着线粒体调控机制和人类线粒体遗传病的研究日渐深入,发现TEFM基因的异常表达或缺失可能导致脑胶质瘤[3]、肝细胞性肝癌[9]和胰腺癌[10]等恶性肿瘤的发生,且TEFM高表达预示着以上各种恶性肿瘤患者的预后不良[4].最近有研究表明,TEFM通过激活ROS/ERK信号参与了HCC中的致癌过程,而TEFM 敲低则抑制了体内HCC的发展和转移[11].但目前仍然缺乏TEFM在脑胶质瘤中作用的分子机制等相关性报道.通过之前的研究,笔者发现,TEFM在脑胶质瘤癌组织中的表达高于癌旁组织,其可能成为胶质瘤的预后标志物和潜在的基因治疗靶点[3].鉴于此,笔者通过稳定转染shRNA下调脑胶质瘤细胞中TEFM的表达,并检测脑胶质瘤细胞中TEFM基因的表达变化.
RNA干扰(RNA interference,RNAi)通过双链RNA (double-stranded RNA,dsRNA)降解mRNA 来抑制特定基因的表达[12].RNAi技术广泛用于基因功能研究、基因表达调控机制等研究领域,通过探索目标基因敲低状况下细胞发生的变化,从而探究目的基因在细胞生长中的功能[13].该技术可使特定细胞中的目标基因在mRNA水平上实现降解,从而导致基因表达被沉默,相当于短时间内“敲除”了目标基因[14].通过特定方式将shRNA转染哺乳动物细胞并沉默靶基因已经成为恶性肿瘤等疾病研究领域常用的科学方法,也是一种非常有前景的临床治疗手段[15].相较于翻译技术、核酶技术等基因沉默技术,RNAi具有高稳定性、高特异性、可传播性等特点[16].
shRNA在细胞质内被核酸酶(Dicer)切割成siRNAs,发挥对靶基因的抑制作用.shRNA化学稳定性更高,又可在体外大量合成,易于筛选有效序列[17].许多研究已经表明,shRNA表达载体与其他形式的RNAi相比具有更加强烈的抑制同源基因表达的作用.笔者首先通过Western blotting检测3株人脑胶质瘤细胞和1株正常人星形胶质细胞(HA1800)中TEFM蛋白的表达水平,结果显示,TEFM蛋白在3种脑胶质瘤细胞株中表达水平均显著高于HA1800细胞,其中以U87细胞内TEFM蛋白表达水平最高.因此,笔者选取U87细胞构建稳定敲低TEFM基因的细胞株进行后续的研究.接着,以TEFM基因为靶基因,根据RNA干扰的Tuschl设计原则,体外合成了编码shRNA的4条DNA序列.RNAi体外实验中构建其干扰载体是其中非常重要的环节,因此合适载体的选择也至关重要.笔者所用的psi-U6是一个可在真核细胞中表达的shRNA质粒载体,并且携带有EGFP标记,可观察和计算细胞的转染效率[18].将合成的DNA序列插入到psi-U6质粒载体中构建了靶向于TEFM基因的shRNA干扰表达载体,其转录产物可以在细胞内形成shRNA,随后被加工形成siRNA从而降解靶基因mRNA,达到阻断靶基因表达的作用.然后,将4个重组质粒TEFM-shRNA-1~TEFM-shRNA-4以脂质体介导的转染导入U87胶质瘤细胞,通过嘌呤霉素筛选稳定转染株.分别以内参基因表达为对照,使用qRT-PCR和Western blotting方法检测各组细胞中TEFM基因和蛋白质表达水平的变化.结果发现,在4条特异性shRNA序列中,以TEFM-shRNA-3和TEFM-shRNA-4的干扰效果最好,因此可以作为靶向TEFM基因的shRNA优先选择的序列.以上结果表明,笔者已经成功构建了靶向人TEFM基因的shRNA真核表达质粒载体和稳定转染的U87胶质瘤细胞,且该shRNA表达载体能有效抑制U87细胞中TEFM基因的表达,但还需更深入的药物试验和动物体内试验来确证TEFM对靶向RNAi治疗肿瘤的有效性.在后续深入研究中,可通过敲低或过表达TEFM基因,研究其对脑胶质瘤细胞线粒体氧化磷酸化功能和其恶性生物学行为等方面的影响,为进一步阐明TEFM在脑胶质瘤发生发展中的分子生物学机制奠定基础.
4 结论
笔者成功构建了TEFM基因shRNA真核表达载体,转染人脑胶质瘤U87细胞并成功筛选出TEFM基因稳定沉默的细胞株,对TEFM基因mRNA表达和蛋白质的表达均具有显著的抑制效率.本研究为进一步探索TEFM基因在脑胶质瘤中的生物学功能和作用机制奠定了实验基础.
