ROS激活P53调控线粒体凋亡途径在α-鹅膏毒肽中毒肝损害中作用的研究进展
2023-01-07赖福平胡杰陆元兰杨登会詹江珊吴瑾王庭刚谢智慧
赖福平,胡杰,陆元兰,杨登会,詹江珊,吴瑾,王庭刚,谢智慧
(遵义医科大学附属医院1.急诊科,2.重症医学科,3.高压氧科,贵州 遵义 563003)
鹅膏毒肽类毒素是由7~8个氨基酸组成的环肽化合物,根据结构差异可分为鹅膏毒肽(amatoxin)、鬼笔毒肽(phallotixin)和毒伞肽(virotixin)3类,其中最主要的致死毒素是鹅膏毒肽[1]。鹅膏毒肽属于联吡啶N-二氧化物,其大环多肽结构类似致死性极大的敌草快,根据侧链取代基团不同可分为多种类型,目前国内外研究类型主要集中在α-鹅膏毒肽(α-amanitin,α-AMA)、β-鹅膏毒肽(β-amanitin,β-AMA)、γ-鹅膏毒肽(γ-amanitin,γ-AMA),但目前对鹅膏毒肽中毒机制研究不足,由于鹅膏毒肽在多个属蘑菇均有出现,且不仅只有1种毒素存在,因此这些毒素相互交集作用给临床诊断及诊疗带来困难[2]。α-AMA作为鹅膏毒肽中含量多、毒性强、致死剂量低(半数致死量0.05~0.1 mg·kg-1)且最为常见类型,其由8个氨基酸残基构成双环八肽,分子量约900 g·mol-1[3-4]。根据α-AMA的毒代动力学表现,肝脏是最主要的受累靶器官,主要引起肝代谢异常、肝细胞损害、肝脏合成功能受损、凝血功能障碍等,而持续性肝损害可进展至多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS)、肠系膜血栓形成等,甚至威胁生命[5-6]。线粒体作为动态的双膜结构,通过产生三磷酸腺苷(adenosine triphosphate,ATP)为细胞活动提供所需能量,而当接受线粒体凋亡途径上游信号时线粒体内凋亡因子释放至胞质中引起细胞凋亡。当机体发生α-AMA中毒可使肝细胞内活性氧(reactive oxygen species,ROS)产量增多打破细胞内环境氧化还原平衡,并作为凋亡上游信号分子促进P53过度表达和磷酸化,以非转录依赖方式向线粒体易位介导线粒体凋亡途径发生[7]。可见ROS激活P53调控线粒体凋亡途径在致肝细胞凋亡中发挥重要作用。作者就ROS激活P53调控线粒体凋亡途径与α-AMA中毒肝损害的关系作一综述,期望对α-AMA中毒肝损害有一新的认识,为α-AMA中毒肝损害诊治甚至预后评估提供理论依据。
1 α-AMA抑制RNAPⅡ活性与调控线粒体凋亡途径致肝损害的研究进展
α-AMA由肝细胞转运多肽1B3转运蛋白(organic anion transporting polypeptide 1B3, OATP1B3)以Km值(3.7±0.6)mm和钠离子-牛磺胆汁酸钠共转运蛋白(sodium taurocholate cotransporting polypeptide, NTCP)转运至胞内,与RNA聚合酶Ⅱ(RNA polymerase Ⅱ, RNAPⅡ)的桥螺旋(bridge helix)和触发环(trigger loop)之间以非共价结合形成较强极性作用的氢键,降低RNAP Ⅱ活性使mRNA转录水平降低导致蛋白质合成受阻,最终导致细胞死亡[8-10]。然而在研究中发现,一种化学性质类似于α-AMA的抗生素可释放RNAPⅡ,在预防α-AMA中毒动物模型的肝损害和增加存活率方面并未有明显上升趋势[11]。近几年研究发现,在α-AMA环境下的小鼠肝细胞内出现不同程度的形态变化,和功能失调的线粒体膜通透性转化孔呈不可逆开放状态,破坏线粒体内膜完整性引起离子平衡紊乱和线粒体内细胞色素C(Cytochrome C, CytC)等凋亡因子释放至胞质中,抑凋亡蛋白Bcl-2和促进促凋亡蛋白Bax表达使Bax/Bcl-2比值上升,进而诱导含半胱氨酸的天冬氨酸蛋白水解酶(cysteinyl aspartate specific proteinase,Caspase)家族激活,诱导细胞凋亡[7,12]。因此,线粒体作为内分泌细胞器,不仅是为发生氧化应激作用直接提供所需要的能量和信号的细胞器,还是ROS激活P53调控线粒体凋亡途径发生引起α-AMA中毒肝细胞发生凋亡的主要机制之一。
2 ROS诱导P53激活线粒体凋亡途径与α-AMA中毒肝细胞异常凋亡的相关性
2.1 α-AMA促进肝细胞内ROS产量增加
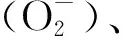
α-AMA引起肝细胞内高ROS环境下对细胞成分造成不利修饰,通过氧化修饰对生物分子如DNA、蛋白质和脂质造成损伤,而受损分子可使ROS产量进一步增加,形成恶性循环[19]。进一步引起氧化应激、脂质过氧化反应、线粒体结构受损,进而促进Bax表达和抑制Bcl-2表达使Bax/Bcl-2值上调、Caspase-9和Caspase-3激活,α-AMA使ROS产量增多可以向P53基因提供激活信号,使P53表达增多和发生磷酸化向线粒体内易位,诱导线粒体凋亡途径发生[7,20-22]。
2.2 α-AMA促进ROS产生进而诱导P53表达并磷酸化向线粒体内易位
P53作为核转录因子主要存在于细胞核和细胞质中,与DNA分子发生特异结合,通过磷酸化修饰发挥活性,同时也是细胞中具有关键调节功能的多功能转录因子,在维持基因组完整性方面占有举足轻重的地位。P53在肝细胞内表达水平较低且半衰期短,其降解过程主要与泛素蛋白连接酶鼠双微粒体2(murine double minute 2,MDM2)作为E3泛素连接酶(E3 ubiquitin ligases)相互作用降低活性,并通过泛素蛋白酶体途径和26S蛋白酶体降解,使P53维持在低水平状态[23-25]。而有文献报道,α-AMA中毒可使P53作为重要应激传感器调控线粒体凋亡途径引起肝细胞凋亡[16,26-27]。相关研究发现,α-AMA抑制CAT活性使胞内产生大量的H2O2,而经人类细胞对H2O2进行降解的微阵列分析得知,H2O2的48个高度应答基因与P53近1/3靶点相吻合,并且ROS和P53之间也存在交叉信号通路,可使α-AMA中毒诱导P53基因表达增加,也使P53蛋白多个位点发生磷酸化修饰激活活性[28-29]。另有研究发现,由于α-AMA中毒可抑制RNAPⅡ表达水平,引起非复制依赖性方式诱导P53丝氨酸-15位点发生磷酸化和P53积聚,并且由于α-AMA中毒导致胞内呈氧化应激状态,引起MDM2减弱对P53泛素化能力,进而减少P53降解、半衰期延长、稳定性和活性显著提高[30-31]。

2.3 α-AMA诱导ROS产生进而激活P53调控线粒体凋亡途径发生
线粒体凋亡途径是通过激活细胞内部途径引起凋亡的主要调节通路,以激活Caspase-9蛋白为主,α-AMA中毒肝细胞凋亡正是通过激活线粒体凋亡途径导致。ROS不仅作为α-AMA中毒诱导肝细胞线粒体凋亡的上游信号分子,同时也诱导P53调控Bcl-2家族基因和Bax基因表达触发线粒体凋亡途径发生。因此,P53在α-AMA中毒诱导线粒体凋亡途径的发生中起到极其重要作用。Chen等[7]研究也加以验证,α-AMA环境中的L-02细胞内Caspase-9和Caspase-3活性增加,但Caspase-8活性并未发生变化。众所周知,促凋亡蛋白Bax是调控细胞凋亡的关键启动因子,由于Bax基因第1个内含子中的启动子是P53依赖性转录激活反应元件,当磷酸化P53与该内含子反应元件相互作用时可促进内源性Bax的mRNA翻译,使Bax蛋白含量增加[39]。与此同时,P53通过调控衔接蛋白凋亡相关斑点样蛋白(apoptosis-associated speck-like protein, ASC)表达增加,与Bax相互作用定位于线粒体内膜上发生寡聚化,线粒体P53下调线粒体膜上抗凋亡蛋白Bcl-2表达水平,使Bax/Bcl-2值增加而引起线粒体孔隙形成,使线粒体膜通透性增加、膜电位降低、Cyt C等促凋亡因子释放至胞质[25,40]。在胞质内,P53反应元件直接上调凋亡酶激活因子(apoptotic protease activating factor-1, Apaf-1)表达水平并与Cyt C形成凋亡复合体,进一步诱导Caspase-9活化并激活效应Caspase-3,启动Caspase级联反应触发线粒体凋亡途径,最终导致肝细胞快速凋亡[41-43]。
3 α-AMA中毒肝损害的治疗展望
α-AMA中毒诱导肝细胞快速凋亡引起肝损害已成为最致命也是最难治疗环节。然而,目前对α-AMA中毒导致肝损害具体机制尚未完全清楚,因此还未有对含鹅膏毒肽类物质中毒的治疗国际共识和特异性解毒剂。ROS作为诱导人肝细胞线粒体凋亡的上游介质和启动因子之一,可调控P53表达及磷酸化激活活性,通过mPTP向线粒体易位触发线粒体凋亡途径引起肝细胞凋亡。因此,减弱细胞内氧化应激发生是最有效的治疗选择。近期研究发现,海洋蠕虫海沙躅(marine worm arenicola marina,M101)体内提取的胞外血红蛋白由198条多肽链组成,总质量为3 682 kDa,在饱和状态下可携带156个O2,具有显著O2结合能力和抗氧化特性[44]。相关实验证明,α-AMA以不同剂量与人肝脏祖细胞(HepaRG)共同孵化时,α-AMA浓度与ROS生产量成正比关系,并显著降低HepaRG细胞活力,当加入M101时线粒体ROS生成量显著降低、活性增强,抑制线粒体氧化应激发生并发生逆转效果,从而降低线粒体功能障碍发生,进而引起P53表达及磷酸化修饰减少,并且凋亡细胞相关蛋白酶、Cyt C、Caspase家族都出现可逆性作用,使人肝癌细胞(HepaRG)死亡率下降,甚至恢复活性[45]。因此M101可能会成为α-AMA中毒的有效解毒剂,但还需大量研究加以证实。对α-AMA毒性机制研究对于开发更加有特异性解毒剂至关重要。
4 结 语
综上所述,α-AMA中毒可影响多种细胞生命代谢过程,在肝细胞内可引起大量ROS产生进而导致氧化应激发生、P53与磷酸化P53表达增加并向线粒体发生易位引起线粒体通透性发生改变造成功能障碍,还可引起Bax/Bcl-2值增加使Cyt C释放至胞质中激活Caspase级联反应,激活线粒体凋亡途径造成肝细胞快速凋亡。进一步阐述了α-AMA中毒调控肝细胞凋亡的潜在机制,也验证ROS可能作为α-AMA诱导肝细胞凋亡早期上游信号分子,在诱导P53对线粒体凋亡途径调控肝细胞凋亡机制中起到关键调控作用,使α-AMA、P53、ROS、线粒体凋亡途径和肝细胞凋亡产生关联。因此,临床上发生急性α-AMA中毒时,减少ROS产生进而抑制P53过度表达和磷酸化将会是减少α-AMA中毒肝损害的工作重点,也是我们努力的方向,期望进一步明确α-AMA中毒肝损害的机制,为含α-AMA蘑菇中毒患者提供更加有效治疗方案、寻求特异性解毒剂提供合理的理论依据。
声明:所有作者均不存在利益冲突。
