淋巴结(皮)瓣治疗淋巴水肿的应用进展
2022-12-30张琳李莉李良昌秦向征于春波丁自海
张琳,李莉,李良昌,秦向征*,于春波,丁自海
1.延边大学医学院解剖学教研室,吉林 延吉 133002;2.东莞市中西医结合医院手足外科,广东 东莞 523000;3.南方医科大学微创外科解剖学研究所,广州 510515
继发性淋巴水肿是一种慢性进行性淋巴运输系统紊乱的疾病,主要原因是由于组织液的产生和回流之间存在不平衡,进而引起组织间隙中富含蛋白质的液体积聚,组织间隙胶体渗透压增加,进行性形成脂肪沉积及炎症反应。当前认为水肿、纤维化、脂肪沉积是导致淋巴水肿的原因,但其形成机制仍末完全明确[1,2]。继发性淋巴水肿的主要病因为感染性和医源性引起的导致正常淋巴管中断或阻塞的疾病。感染性淋巴水肿常见于丝虫病,医源性淋巴水肿多见于肿瘤的术后或放、化疗之后。对于淋巴水肿目前还缺少有效的治疗方法,现在主要的两大治疗方案是保守术治疗和手术治疗。在保守治疗方法中,较为认同并得到实践支持的方案是联合物理疗法(combined physical therapy,CPT)也称之为完全减充血疗法,并被认为是临床标准治疗方式,主要是改善肢体的物理特征和减轻症状,减少疾病进展且可降低并发症[3]。但CPT 并不是治愈疾病的方法,其涉及的人工因素较多,需要定期进行治疗,加之专业治疗人员短缺,进而使得患者的依从率不高。手术治疗的方法可分为两大类[4],一类是快速去除患者由于淋巴水肿引起的脂肪组织增生,改善患肢外观症状的吸脂术和切除术,但存在着再次加重淋巴水肿、瘢痕疙瘩、感染、溃疡、蜂窝炎等风险,也非治愈疾病的好方法。手术治疗的另一类方法为淋巴回流生理重建法,包括吻合淋巴管与淋巴管、淋巴管与静脉,微血管与淋巴结转移等术式使患者的临床症状得到显著改善。但是,由于淋巴管壁薄、吻合的静脉多要求管径为1 mm 以下静脉压力小的皮下静脉,技术难度高,在临床应用上推广较慢。当前临床较为认可的手术治疗方案为淋巴结(皮)瓣的移植,淋巴结(皮)瓣是指含有一定数量正常淋巴结的组织瓣,组织瓣内淋巴结的固有动脉均来源于血管蒂,可携带皮肤亦可不携带皮肤,目前临床医生对于是否携带皮肤还没有达成共识,当前临床上以携带皮肤的淋巴结皮瓣居多。其治疗淋巴水肿的优越性表现在:不需要吻合淋巴管,在技术上降低了难度;可以在无法找到适合的淋巴管且需要进行淋巴管与静脉吻合的晚期淋巴水肿患者中进行[5]。近年来淋巴结(皮)瓣移植术在临床中得到了快速的应用并取得了显著的疗效[6],被视为是一种很有前途的治疗淋巴水肿的手术方法[7-10]。国内学者研究应用淋巴结(皮)瓣治疗肿瘤术后淋巴水肿,取得了满意效果[11,12]。本文重点对淋巴结(皮)瓣移植治疗继发性淋巴水肿的生理机制、供区部位及受区部位选择、潜在的风险进行综述。
1 淋巴结(皮)瓣移植治疗淋巴水肿的生理机制
随着显微外科技术的飞速发展,目前认为应用淋巴结(皮)瓣移植治疗淋巴水肿是符合淋巴回流生理机制的外科手术,是当前提倡治疗该疾病的外科方法,研究认为淋巴回流的生理机制有两种,即淋巴管芯理论和淋巴泵理论:
1.1 淋巴管芯理论机制
外科医生利用淋巴的管芯理论机制通过使用丝线、筋膜条、网膜或皮瓣来治疗淋巴水肿。淋巴结(皮)瓣治疗淋巴水肿时,瓣内的淋巴结被认为是天然的淋巴收集器,其可作为淋巴管芯来桥接阻塞区域。若要使移植的淋巴结起到有效的毛细作用,要满足两个要求,首先,皮瓣必须桥接阻塞区,起毛细用的淋巴管要作用于受区部位的近端和远端;其次,移植的淋巴结(皮)瓣内的淋巴管与受区的淋巴管之间形成自发的吻合,从而有效地排出肢体的过多的淋巴负荷。有研究证据显示,转移的淋巴结可能是内源性血管内皮生长因子(vascular endothelial growth factor,VEGF)的来源,转移后促进淋巴结(皮)瓣及受区的淋巴管生成,尽管相关研究显示移植的淋巴结已整合到受区的淋巴管中,但是这一理论缺乏坚实的科学证据,淋巴管的连接方式还有待于进一步查证。
1.2 淋巴泵理论机制
移植至患侧的淋巴结(皮)瓣由皮瓣的血管蒂进行营养,高压动脉的流入和低压静脉的流出之间存在着陡峭的压力梯度,可以将液体从组织间隙抽吸到未受损的淋巴结中。因此,将瓣内的淋巴结视为抽吸淋巴的“泵”,皮瓣内的淋巴管与受区的淋巴管之间形成自发的吻合,吸收的组织液通过淋巴结固有静脉分流,经皮瓣内的静脉将其转移到受区静脉而进入体循环中。已有研究表明,50%~66%的淋巴可被吸收至移植的淋巴结内并被成功转入体循环。Cheng 等[13]研究发现将吲哚青绿注射到淋巴结皮瓣的边缘后,它很快的就可以在供体静脉中显示出来,随后在受区静脉中也显示了出来。因此,认为吲哚青绿可被移植皮瓣内的淋巴结吸收,并通过固有淋巴静脉分流进入供体皮瓣内的静脉。但Tourani 等[14]认为这不具备结论性,原因是吲哚青绿被供体皮瓣内的毛细血管吸收也可能产生同样的结果。此外,淋巴进入淋巴结的方式并不是很清楚。Aschen 等[15]在转基因小鼠急性淋巴水肿模型的实验中发现受区淋巴大量渗入移植的淋巴结内,受区和供体淋巴管之间出现自发吻合现象,如果这些结果能在慢性淋巴水肿模型中重现,将可进一步支持淋巴“泵”的理论。
2 淋巴结(皮)瓣供、受区的选择
2.1 供区的选择
淋巴结(皮)瓣的供区通常为:腹股沟区、胸外侧区、锁骨上区、颏下区。①腹股沟浅淋巴结(皮)瓣[16],是治疗上肢淋巴水肿选择率最高的一种淋巴结瓣,淋巴结多选择位于旋髂浅动脉和腹壁浅动脉的交界处,位于腹股沟韧带的上方的淋巴结,血管蒂多选择旋髂浅动脉。设计时应避免损伤引流下肢的前哨淋巴结,否则会引起医源性下肢淋巴水肿。此外,在进行乳房重建同时治疗上肢淋巴水肿的手术中,则选用腹壁下动脉穿支为蒂获取腹股沟淋巴结,若腹壁下动脉没有充分营养淋巴结,则需要额外吻合旋髂浅动脉和腹壁浅动脉以确保淋巴结固有血管的完整性(图1)。②胸外侧淋巴结(皮)瓣[17],通常以胸外侧动脉或胸背动脉为蒂,在所有供区中胸外侧淋巴结(皮)瓣并发症发生率较高,主要是浆膜瘤、淋巴囊肿和供区淋巴水肿。上肢淋巴水肿患者不切取同侧胸外侧淋巴结,因为它们往往在乳腺癌腋窝淋巴结清扫过程中被切除。③锁骨上淋巴结(皮)瓣[18],淋巴结位于锁骨、胸锁乳突肌和颈内静脉形成的三角形边界内,血管蒂以颈横动脉进行设计,右侧颈横动脉的平均直径略大于左侧,切取此处淋巴结瓣时建议不切取患肢同侧的淋巴结,在左侧设计锁骨上淋巴结(皮)瓣时应避免损伤胸导管,否则会导致乳糜漏。④颏下淋巴结(皮)瓣[19],淋巴结位于颏下三角内,平均为3 个淋巴结[20],以颏下动脉为血管蒂,切取时通常会携带二腹肌前腹,因颏下动脉走行与下颌下腺的关系比较密切,所以切取时难度相对较大,此外面神经的下颌缘支平下颌骨下缘走行于面动脉的浅面,因此切取淋巴结瓣时应对其加以识别和保护。⑤胃网膜淋巴结(皮)瓣,通常与腹壁下动脉穿支皮瓣联合应用,在乳房重建同时治疗上肢水肿取得了较好的效果[21]。
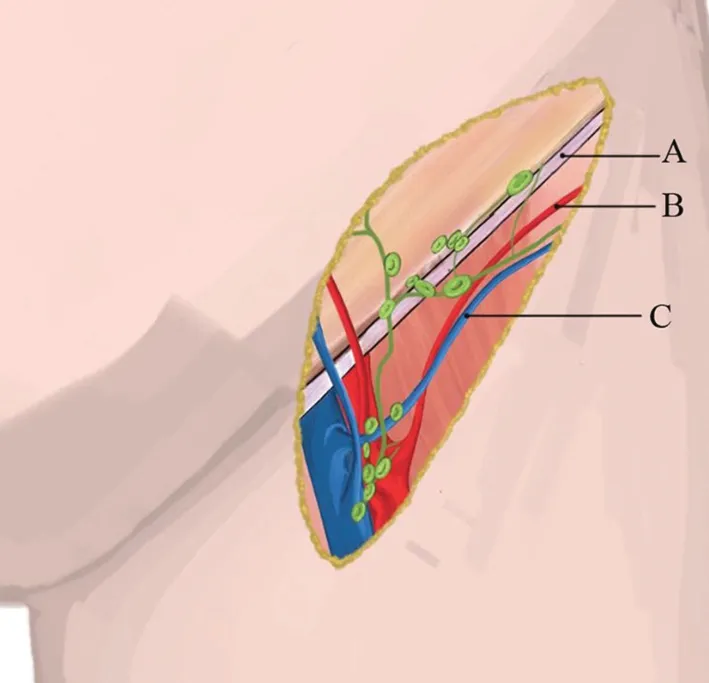
图1 腹股沟浅淋巴结皮瓣的设计A. 腹股沟韧带B.旋髂浅动脉C.旋髂浅静脉Fig.1 Design of superficial inguinal lymph node flapA, inguinal ligament; B, superficial circumflex iliac artery; C, superficial circumflex iliac vein
2.2 切取淋巴结(皮)瓣的注意事项
淋巴结(皮)瓣的外科手术移植程序与穿支皮瓣切取和移植非常相似,选择淋巴结(皮)瓣的供区通常要考虑以下因素:①供区能够提供一定数量的健康淋巴结,只有具备一定数量的健康淋巴结才能够起到“泵”的作用,进而将患处的组织液转入到体循环,淋巴结的数量越多治疗淋巴水肿的效率越高[22]。②血管蒂的长度,要足够长,并且组织瓣内的淋巴结固有血管均来源于血管蒂。③切取的淋巴结(皮)瓣,不能引起其所在区域的淋巴水肿。④要考虑供区的隐蔽性与美观性。
2.3 淋巴结(皮)瓣受区选择
总体来看,当前临床应用在受区的选择上主要有两种方式。①第一种,移植于淋巴水肿患侧肢体的近端区域。上肢淋巴水肿的患者选择腋窝或锁骨上区作为受区,下肢淋巴水肿的患者则选择腹股沟区。但是这种受区存在着一定的潜在问题,主要是由于长期慢性的淋巴水肿导致的瘢痕和纤维化较重,血管化淋巴瓣移植空间及受区血管的寻找会受到一定的影响。受区血管可以选择胸外侧血管、胸背血管或胸背血管的分支,受区供体血管还会存在可能再次受到放、化疗辐射的影响遭到损伤,移位于近端区域淋巴结(皮)瓣内的淋巴结同样也存在着上述的潜在问题。②第二种,将淋巴结(皮)瓣移植于肢体的中、远端(上肢选择肘部、腕部,下肢选择在腘窝、踝部)。这些受区位于肢体远端,血管没有受到手术及放射损伤。上肢远端的受区血管在腕部可选择“鼻咽壶”处的桡动脉,受区静脉选择头静脉的属支(图2)。下肢膝关节周围的受区血管可选择膝内侧动脉分支和隐静脉属支。在足踝处,胫前动脉或足背动脉的分支常被选为受区动脉,受区静脉常选择胫前静脉属支或足背静脉网。将淋巴结(皮)瓣移植于肢体的远端认为能更好的起到“淋巴泵”的作用。随着病变肢体组织液的不断吸收,皮下间质压力逐渐降低,由于重力的影响组织间隙内组织液会向下移动,更易形成“汇水效应”,更多的淋巴进入移植的淋巴结,使治疗淋巴水肿的效果更加明显,将淋巴结(皮)瓣移植于肢体远端会导致外观出现轮廓臃肿的现象。关于受区选择患侧肢体的远端还是近端,有统计显示两者之间的结果没有显著性差异。

图2 腕部受区 A.拇长伸肌 B.头静脉 C.桡动脉 D.拇短伸肌Fig.2 The wrist was selected as the recipient siteA, extensor pollicis longus; B,vena capitis; C, radial artery;D, extensor pollicis brevis
3 淋巴结(皮)瓣治疗淋巴水肿存在的风险及应对技术
3.1 存在的风险
淋巴结(皮)瓣移植治疗淋巴水肿能够明显改善患者临床症状,因此在临床治疗中越来越受欢迎,这项治疗方案在理念上具有创新性,并且应用了显微外科和微创手术技术,具有一定的突破性。这项外科治疗方案的主要风险是应用淋巴结(皮)瓣治疗淋巴水肿的同时,可能会引起供区部位的淋巴水肿,是当前外科医生和患者所共同关注的问题。Vignes 等[23]统计并报道了淋巴瓣移植后并发症的发病情况,包括供区肢体中的持续性淋巴水肿、丸鞘膜积液和持续的供体部位疼痛。供区部位发生淋巴水肿是最为常见的并发症,即使是由经验丰富的显微外科医师在显微镜下按正常解剖分离操作,也存在供区肢体淋巴水肿的风险。
3.2 淋巴结(皮)瓣切取的安全性技术
Thompson[24]为区分收集上肢和乳房淋巴的淋巴结,以降低乳腺癌腋窝淋巴结清扫术后医源性上肢淋巴水肿的风险,在乳晕皮下注射锝硫胶体,在同侧上肢(手臂)皮内注射蓝色染料,收集上肢淋巴的前哨淋巴结可被锚记为蓝色,腋窝淋巴结清扫术时,可以避免切除蓝色标记的上肢淋巴结,临床上将这种方法称之为(双向)逆向淋巴示踪法。Dayan 等[25]将这一方法应用到了淋巴结(皮)瓣的获取上,应用的试剂为锝硫胶体和吲哚菁绿,应用(双向)逆向淋巴示踪法切取腹股沟区、腋窝及锁骨上淋巴结(皮)瓣,降低了供区淋巴水肿的风险。锝硫胶体和吲哚菁绿注入的部位决于淋巴结所在的供区位置,术中使用Y 探针和近红外成像,识别引流的淋巴结,可以在术中及时改变淋巴结瓣的切取范围,而不是单纯以解剖标志、标线作为切取指导。如切取腹股沟区的淋巴结瓣时,可在术前约1 h,在供区同侧足部第1、2 趾蹼区注射0.2 ml 锝硫胶体(0.2mCi/0.2ml),在下腹部于脐和腹股沟韧带之间选取4 个区域,将吲哚菁绿0.1ml 皮内注射。多普勒超声确认旋髂浅动脉和腹壁浅动脉的走行,采用Y 探针定位引流下肢的前哨淋巴结,近红外成像观察收集下腹部淋巴结。应用这一方法,在切取淋巴结(皮)瓣时可以很好的避免切取下肢引流的淋巴结,从而降低了供区下肢淋巴水肿的风险。此外,影像学检查可用于术前规划,确定淋巴结最丰富的供体部位。
4 展望
继发性淋巴水肿物理治疗通常会出现耐受,自体淋巴(皮)瓣移植治疗淋巴水肿则不会出现,因此被认为是当前最佳的治疗方法。移植的淋巴结可以释放VEGF 刺激淋巴管生成,还可以充当海绵或排水泵的作用,吸收水肿肢体中的淋巴,改善水肿肢体外观和功能。此外,移植的淋巴结还可参与免疫功能,从而降低患肢罹患蜂窝织炎的风险。当前临床应用及所取得的数据,还不能完全支持淋巴结(皮)瓣转移治疗淋巴水肿的功能机制。利用淋巴水肿动物模型探讨病理机制,是一种较好的研究方法。但是使用动物模型来发现治疗淋巴水肿的正确方法及淋巴回流的生理机制仍然是一个挑战,需要对慢性淋巴水肿模型进行更多的基础研究。淋巴结(皮)瓣移植由一些外科医师首先尝试,迄今为止临床上应用淋巴结(皮)瓣转移治疗慢性淋巴水肿的初步结果是有希望的。虽然当前这种方法不能完全治愈淋巴水肿,但现已被大家逐渐接受。这种技术有一定难度,需要复杂的手术操作和显微外科技术。支持该方法作为治疗慢性淋巴水肿标准疗法的证据仍然很低,需要长期的进一步研究。再者就是需要进一步的解剖学研究来探索潜在的新供区部位,以减少并发症的发生。