嗪吡嘧磺隆在土壤中的吸附特性及其吸附过程模型的建立
2022-12-27方丽萍苑学霞梁京芸杜红霞
方丽萍, 苑学霞, 梁京芸, 官 帅, 杜红霞
(山东省农业科学院 农业质量标准与检测技术研究所/山东省食品质量与安全检测技术重点实验室,济南 250100)
除草剂作为农田杂草防除工具,因其高效、省时、适合机械化操作等特点,成为世界上占比最大的农药类型[1]。在中国,除草剂的种类和用量在持续增加[2],部分地区农田化学除草面积已占总种植面积的 90%以上[3],使用除草剂已成为控制杂草、保证作物产量不可或缺的手段。嗪吡嘧磺隆 (metazosulfuron) 是由日产化学株式会社开发的一种的磺酰脲类内吸性除草剂,2013 年在日本登记,随后在韩国和中国上市。该药通过抑制亮氨酸、缬氨酸、异亮氨酸的生物合成使细胞分裂受阻,从而达到抑制杂草生长的目的[4]。对稗草、野荸荠、水莎草、苘麻、反枝苋和马唐等具有较好的防除效果,且对传统磺酰脲类除草剂产生抗性的杂草 (萤蔺、鸭舌草、雨久花和野慈姑等) 亦有较高的活性[5-6]。
土壤是一种具有巨大吸附表面的多介质体系,是除草剂及其代谢物的重要归宿场所之一。除部分除草剂被目标杂草吸收外,仍有相当一部分除草剂进入土壤,成为有机污染物,随后发生复杂的物理及化学反应[7]。除草剂在土壤中的吸附和解吸特性是评价其潜在环境风险的重要内容。除草剂在土壤中的归趋受其在土壤中的吸附、解吸等行为的调控,这不仅影响除草剂在土壤系统中固、液、气三相的分布,也会影响其迁移、降解、转化、滞留、生物吸收利用和微生物降解等多个过程[8-9],进而影响其在土壤环境中的残留 (特别是结合残留) 及对后茬作物的负面作用。因此,研究除草剂在土壤环境中的吸附解吸行为,对全面评价除草剂在环境中的归趋和潜在危害至关重要。
磺酰脲类除草剂为弱酸性化合物,具有低挥发性、慢光解性和较强淋溶性等特点,在土壤中多以离子形式存在,具有较高的迁移率[10],其在土壤中的吸附解吸过程比较复杂,不仅取决于药物本身的性质,如水溶性、正辛醇-水的分配系数等,还取决于土壤的理化性质,如阳离子交换容量、有机质含量等,以及环境条件,如温度、pH等[11-12]。由于土壤性质的复杂性和不同地区的气候条件,不同土壤对磺酰脲类除草剂的吸附-解吸行为也不同[13-14]。郭敏等[15]研究了3 种磺酰脲类除草剂 (氟胺磺隆、氯吡嘧磺隆和磺酰磺隆) 在 5 种不同种类土壤中的吸附特性,发现吸附主要以物理吸附为主,吸附常数随土壤pH 值增大而减小。Caceres-Jensen 等[16]采用不同的模型研究了烟嘧磺隆在10 种土壤中的吸附/解吸动力学和溶质迁移机制。另外,有研究表明,添加生物炭,通过改变疏水性分配作用、孔隙填充、氢键、p/π-π 电子供体-受体作用、静电作用等可增加土壤对烟嘧磺隆的吸附[17]。但到目前为止,对于嗪吡嘧磺隆在土壤中的吸附特性及过程模型缺乏系统研究。
本文以磺酰脲类除草剂嗪吡嘧磺隆为对象,研究其在不同土壤中的吸附特性以及影响因素,利用BP 人工神经网络建立嗪吡嘧磺隆的吸附过程模型,为明确嗪吡嘧磺隆在土壤介质中的环境行为及可能存在的环境风险提供科学依据。
1 材料与方法
1.1 材料
1.1.1 试剂与仪器 99.1%嗪吡嘧磺隆 (metazosulfuron) (北京曼哈格生物科技有限公司);高岭土、高锰酸钾均为分析纯 (国药集团化学试剂有限公司);腐殖酸 (上海阿拉丁生化科技股份有限公司);甲醇、乙腈均为色谱级 (美国Thermo Fisher)。生物炭:稻壳于600 ℃马弗炉中烧制4 h。
高效液相色谱-质谱联用仪 (HPLC-MS/MS):Agilent 1290-6460 (美国Agilent)。
1.1.2 供试土壤 试验所用土壤分别采自海南、辽宁、广西、甘肃、重庆、黑龙江、陕西、山东8 个省份。土壤类型分别为砖红壤、棕壤、赤红壤、灰棕漠土、紫色土、白浆土、褐土、潮土。所有供试土壤均采自0~20 cm 土层,经自然风干后研磨过0.6 mm 筛备用。理化性质见表1。
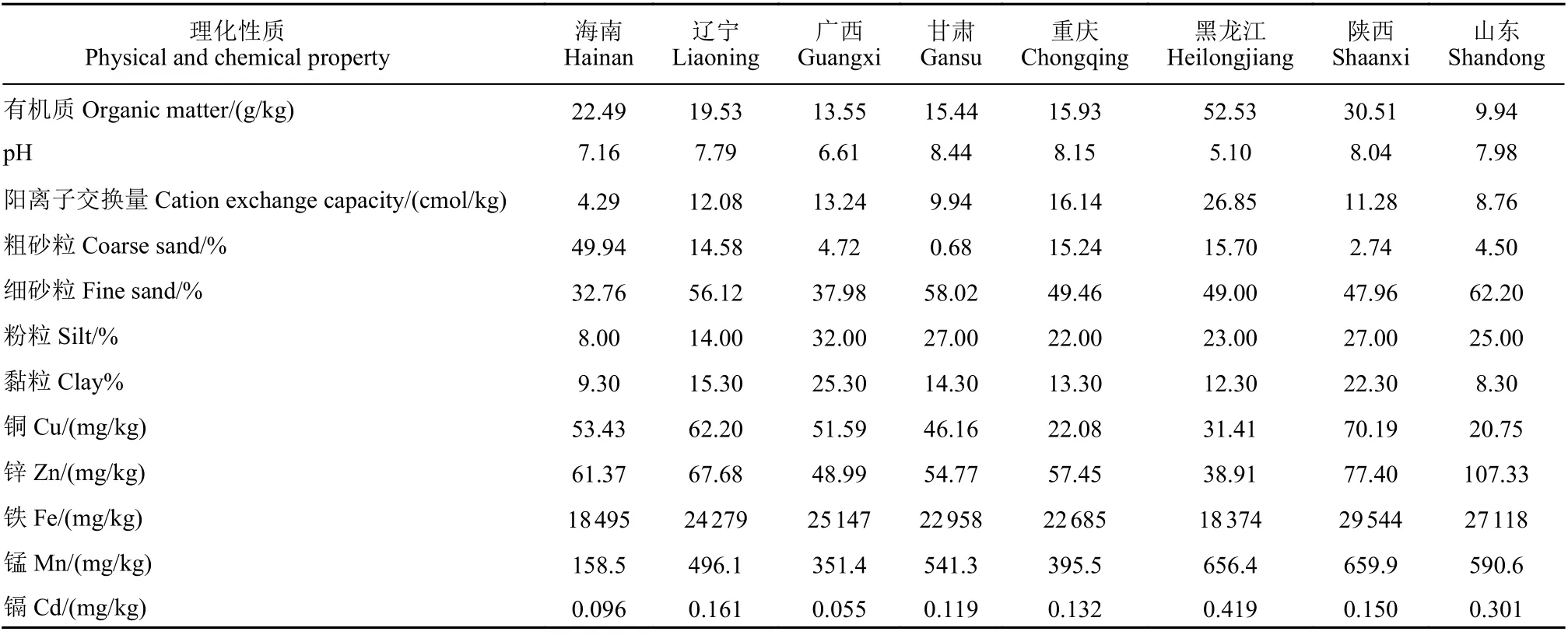
表1 供试土壤的理化性质Table 1 Physical and chemical properties of 8 selected soils
1.2 嗪吡嘧磺隆在土壤中的吸附-解吸特征
嗪吡嘧磺隆在土壤中的吸附-解吸试验采用批量平衡法[18]。
1.2.1 等温吸附试验 称取5 g (精确至0.01 g) 土壤,置于50 mL 聚乙烯离心管中,分别加入25 mL不同质量浓度 (0.1、0.2、0.5、1、2 和5 mg/L) 嗪吡嘧磺隆溶液 (含有0.01 mol/L CaCl2溶液以增强离子强度),加盖密封,于25 ℃、200 r/min 条件下振荡24 h 后,于6 000 r/min 下离心5 min;取上清液,采用 HPLC-MS/MS 测定其中嗪吡嘧磺隆的含量。根据吸附前后溶液的浓度变化值,按公式 (1) 计算土壤对嗪吡嘧磺隆的吸附量。每个处理3 次重复,同时设空白对照。
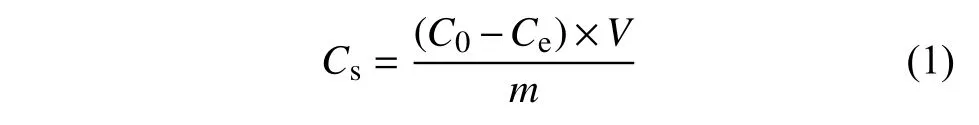
式中,V为溶液体积,mL;m为土壤质量,g;Cs为土壤对嗪吡嘧磺隆的吸附量,mg/kg;Ce为吸附平衡时水相中药液的浓度,mg/L;C0为初始质量浓度 (吸附前水相中的药液浓度),mg/L。
1.2.2 等温解吸试验 将上述等温吸附试验吸取上清液后,加入25 mL 0.01 mol/L 的CaCl2溶液作为解吸剂,混匀,于25 ℃、200 r/min 条件下振荡24 h 后,于6 000 r/min 下离心5 min;取上清液过0.22 μm 滤膜,采用HPLC-MS/MS 测定上清液中嗪吡嘧磺隆的含量,按公式 (1) 并计算解吸量。上述解吸试验步骤连续重复4 次。
1.2.3 土壤对嗪吡嘧磺隆的吸附特性分析 采用线性模型和Freundlich 模型分析土壤对嗪吡嘧磺隆的吸附,计算公式如式 (2) 和 (3) 所示。

式中:K(mL/g) 和Kf分别为两种模型的吸附和解吸附常数 (吸附为Kf-ads;解吸附为Kf-des);1/n为吸附经验常数。
每次解吸后土壤吸附嗪吡嘧磺隆由公式 (4) 求得,滞后系数 (H) 由公式 (5) 求得。
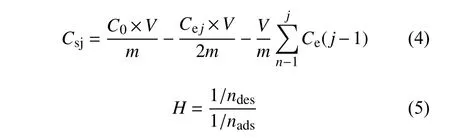
式中:j= 1~5;Csj为第j次解吸后土壤吸附嗪吡嘧磺隆质量,mg/kg;Cej为第j次解吸后上清液中药液质量浓度,mg/L;m为土壤质量;1/nads和1/ndes分别为吸附经验常数和解吸经验常数。
采用SPSS 23.0 分析供试土壤的理化性质与吸附常数 (Kf) 的相关性。
1.3 嗪吡嘧磺隆在土壤中的吸附与土壤单因素的相关性试验
称取5.0 g 土壤于50 mL 离心管,加入30 mL 5 mg/L 嗪吡嘧磺隆标准溶液,单因素试验设计见表2。在25 ℃避光条件下,于160 r/min、恒温下振摇24 h。吸附平衡后测定嗪吡嘧磺隆含量。每个处理3 次重复。
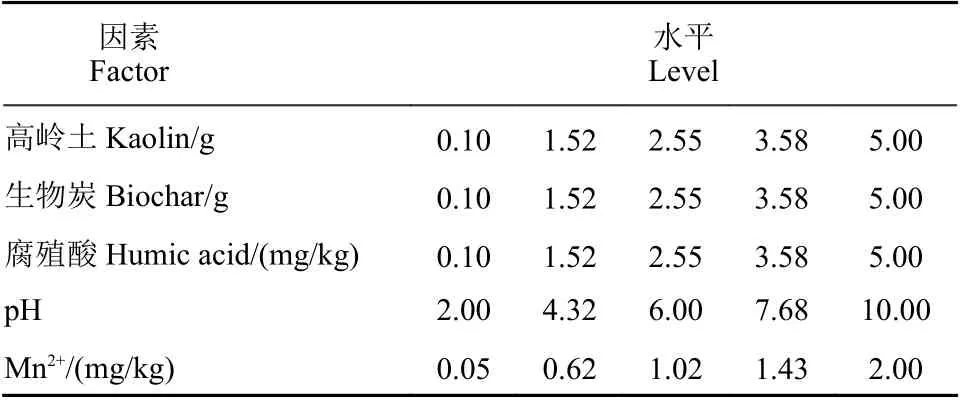
表2 嗪吡嘧磺隆在土壤中吸附行为的单因素试验设计Table 2 Design of single-factor experiment of metazosulfuron adsorption behavior in soils
采用SPSS 23.0 单因素方差分析判断单因素试验中高岭土、稻壳生物炭、腐殖酸、pH、Mn2+对吸附常数 (Kf) 的影响。
1.4 土壤中嗪吡嘧磺隆的吸附过程模型建立
1.4.1 嗪吡嘧磺隆在土壤中吸附的复合试验 通过中心复合试验 (Central Composite Design,CCD),考察高岭土、稻壳生物炭、腐殖酸、pH 和Mn2+等5 个因素对嗪吡嘧磺隆在土壤中吸附行为的复合影响。CCD 在响应面分析软件Design Expert 8.0.6 中进行,各因素取值范围和大小见表3。吸附平衡后测定嗪吡嘧磺隆的含量,按公式 (1) 计算其吸附量。
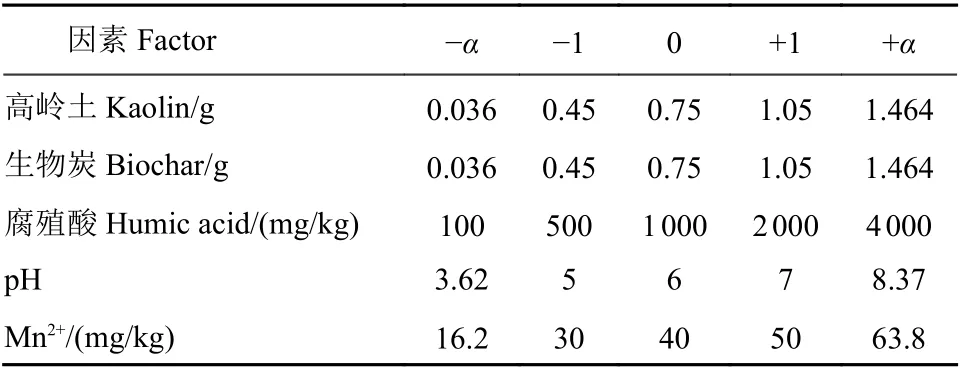
表3 中心复合试验设计Table 3 Design of central composite experiment
1.4.2 BP 神经网络模型的建立 采用Matlab 2019a BP 神经网络模型,进行实测数据和预测数据的拟合和验证,检验模型的可靠性。BP 神经网络模型的拟合方法参考胡宇玉等的方法[19]。其拓扑结构包括输入层、中间层和输出层,其中中间层神经元节点数对模型的精度影响较大。根据最佳中间层神经元节点数选择公式 (6)、 (7) 和 (8)。
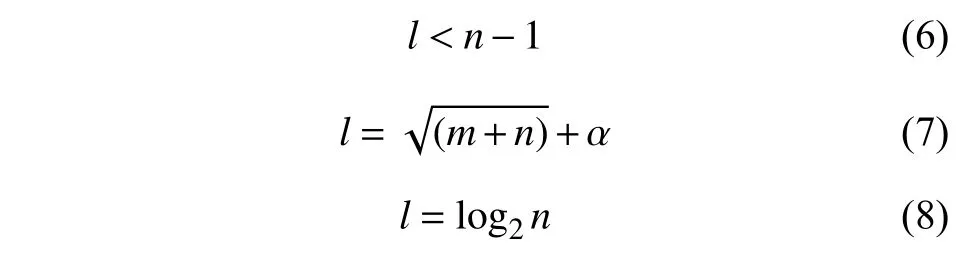
式中,n为输入层神经元节点数;l为中间层神经元节点数;m为输出层神经元节点数;α为0~10 之间常数。
选取39 组试验数据作为拟合数据,以高岭土含量、生物炭含量、腐殖酸浓度、pH 和Mn2+浓度作为输入变量,以土壤对嗪吡嘧磺隆的吸附量作为输出变量,建立BP 神经网络模型。选取11 组试验数据作为验证数据。50 组数据详情见附表S1。模型可靠性通过拟合值与实测值的相关系数来衡量。
1.5 嗪吡嘧磺隆检测方法
1.5.1 净化 吸取1.2、1.3 和1.4 节中离心后的上清液,加入100 mg PSA 和100 mg C18,于4 000 r/min 下离心5 min,取1 mL 上清液与1 mL 水混合均匀,过0.22 μm 水相滤膜,待测。
1.5.2 仪器测定条件
色谱条件:Agilent ZORBAX Eclipse Plus C18色谱柱 (100 mm × 2.1 mm , 1.8 μm);柱温35 ℃;进样体积5.0 μL;流动相A 相为含体积分数为0.1% 的甲酸溶液、B 相为甲醇,梯度洗脱程序为:0~2 min,10%B;>2~3 min,95%B;>3~5 min,10%B。流速0.3 mL/min。
质谱条件:电喷雾离子源正离子扫描模式(ESI+);毛细管电压4.0 KV;锥孔电压35 V;多反应监测 (MRM);干燥气流速8.0 L/min;离子源温度350 ℃;定量离子对 (m/z) 476/156;定性离子对 (m/z) 476/181.9;去簇电压20 V;碰撞电压15 V。
1.5.3 添加回收试验 向空白上清液中分别添加0.01、0.1 和1 mg/kg 3 个水平的嗪吡嘧磺隆,每个水平重复5 次。添加回收率为88%~108%,变异系数4.7%~6.3%,符合农药残留分析要求。
2 结果与讨论
2.1 嗪吡嘧磺隆在土壤中的吸附-解吸特征
由图1 可见,嗪吡嘧磺隆与土壤溶液接触4 h内,溶液中嗪吡嘧磺隆的浓度快速降低,表明此阶段是土壤对溶液中嗪吡嘧磺隆的快速吸附阶段。随后的4~24 h 内,溶液中嗪吡嘧磺隆的浓度基本保持不变,表明此阶段土壤对嗪吡嘧磺隆吸附过程逐渐达到平衡。
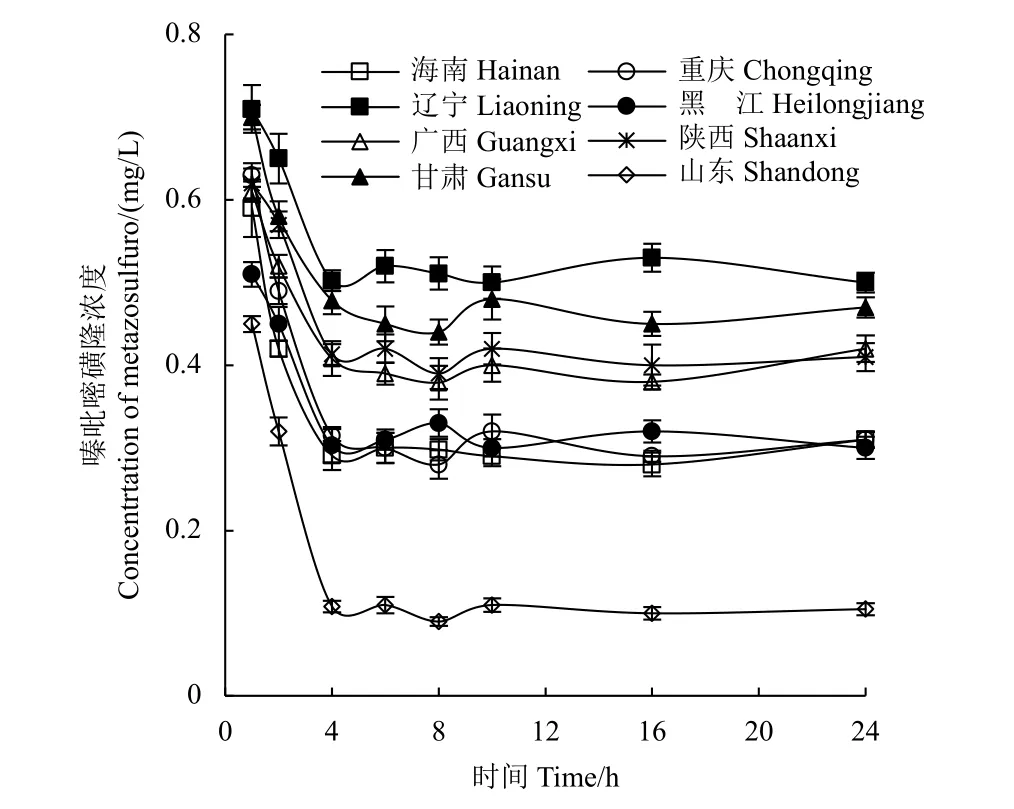
图1 嗪吡嘧磺隆在8 种土壤中的吸附动力学 (25 ℃)Fig.1 Adsorption kinetics of metazosulfuron in the soil-water compartment at 25 ℃
嗪吡嘧磺隆在8 种土壤中的吸附线性模型和Freundlich 模型见表4。吸附常数K或Kf表示土壤吸附能力的强弱[7]。吸附常数越大,土壤对农药的吸附能力越强,农药在土壤中的移动性就越弱。由表4 可见,吸附线性模型的K值在0.281~3.515之间。8 种土壤的吸附能力强弱顺序为:黑龙江 >辽宁 > 海南 > 重庆 > 广西 > 甘肃 > 山东 > 陕西;Freundlich 模型吸附常数Kf-ads在0.435~2.572 之间。8 种土壤吸附能力强弱顺序为:黑龙江 > 海南 > 辽宁 > 重庆 > 广西 > 陕西 > 山东 > 甘肃。两种模型结果都表明黑龙江白浆土对嗪吡嘧磺隆的吸附能力最强,且大大高于其他土壤。海南砖红壤、辽宁棕壤土、重庆紫色土对嗪吡嘧磺隆的吸附能力也均强于其他土壤。在广西赤红壤、陕西褐土、山东潮土、甘肃灰棕漠土中嗪吡嘧磺隆的吸附能力相对较弱。根据Kf-ads< 5 时表示土壤对农药的吸附能力弱[18],则本试验中8 种土壤对嗪吡嘧磺隆的吸附能力均为弱,表明嗪吡嘧磺隆在土壤中发生迁移快。两个模型的相关系数 (r) 值接近,线性模型的r值在0.937 5~0.991 5 之间,Freundlich 模型的r值在0.958 4~0.997 3 之间。大部分Freundlich 模型的r值略高。另外,黑龙江土壤的线性模型中C0的值为负值不合理。因此,嗪吡嘧磺隆在土壤中的等温吸附用Freundlich 模型来描述更为合理。
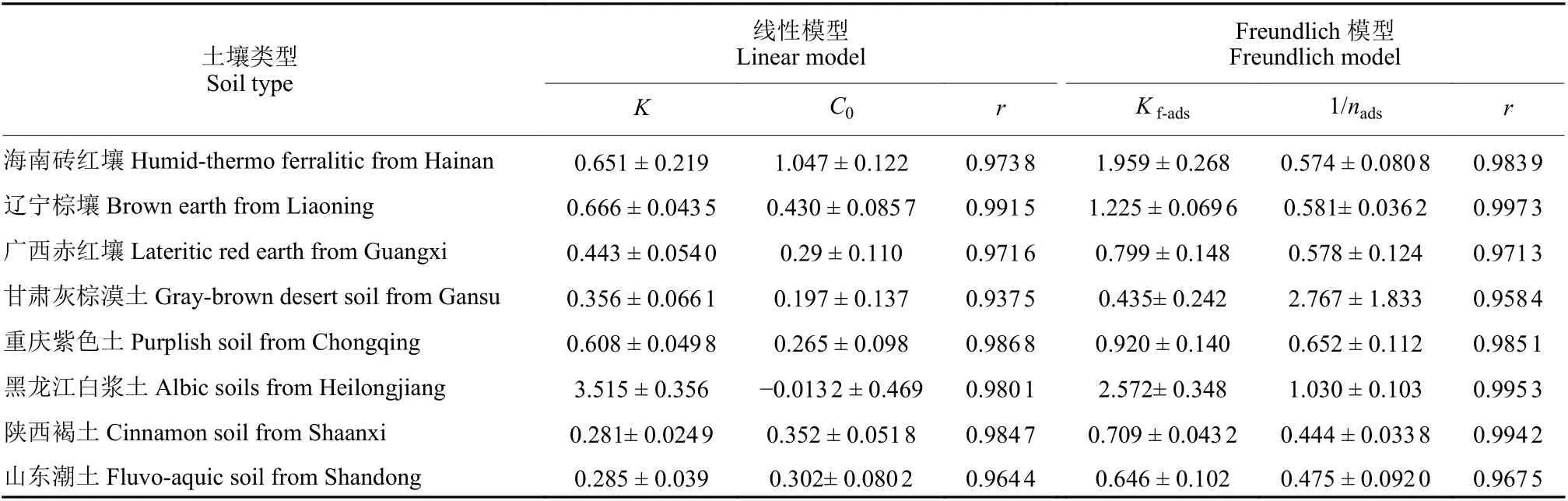
表4 嗪吡嘧磺隆在土壤中的吸附线性模型和Freundlich 模型Table 4 Linear and Freundlich models of metazosulfuron adsorption in soils
在Freundlich 模型中,1/nads与吸附过程中的表面不均一性、能量的大小和多样性有关。本研究中,在甘肃灰棕漠土中1/nads> 1,吸附等温线属于S 型等温线,表明嗪吡嘧磺隆在较低浓度时与土壤的亲和力较低,而随着浓度的增加两者之间亲和力也增强[7],其吸附过程为协同吸附,与吸附剂层内较强的分子间吸引力、溶质在吸附剂中的渗透以及农药本身的作用有关[16]。在海南砖红壤、辽宁棕壤土、广西赤红壤、重庆紫色土、陕西褐土和山东潮土中1/nads< 1,吸附等温线属于L 型等温线,表明嗪吡嘧磺隆在较低浓度时与土壤有较强的亲和力,而随着浓度增加亲和力降低[20]。其吸附过程表现为随着浓度的增加,相对吸附首先发生在高能吸附位点,然后是低能吸附位点,边际吸附能随表面浓度的增加而降低[16]。黑龙江白浆土中1/nads的值接近于1,表明其对嗪吡嘧磺隆的吸附介于以上两种情况之间。
农药在被土壤吸附后,其解吸特性是其在土壤中进行迁移和滞留的决定性因素。滞后性越强,则农药在土壤中的解吸释放越难,反之亦然。这一过程通过滞后系数 (H) 表征,H表示农药在土壤解吸过程中的迟滞程度。当H< 1 表示存在正迟滞现象,农药不易从土壤中解吸出来;当H> 1,表示发生了负迟滞现象,农药容易从土壤中解吸出来;当H= 1,表示不存在迟滞解吸现象[21]。由表5 知,Freundlich 模型对嗪吡嘧磺隆在土壤中的解吸等温线拟合性较好 (r值在0.929 5~0.999 2 之间)。除广西赤红壤外,其他7 种类型土壤中嗪吡嘧磺隆的H均小于1,表明嗪吡嘧磺隆在7 种供试土壤中的解吸过程存在滞后现象。嗪吡嘧磺隆被土壤吸附后,不易被解吸释放出来,将导致嗪吡嘧磺隆在土壤中长期残留,并在土壤基质的吸附位点累积,再缓慢释放到土壤中而造成污染。因此,嗪吡嘧磺隆在土壤中的滞后性存在潜在环境风险。
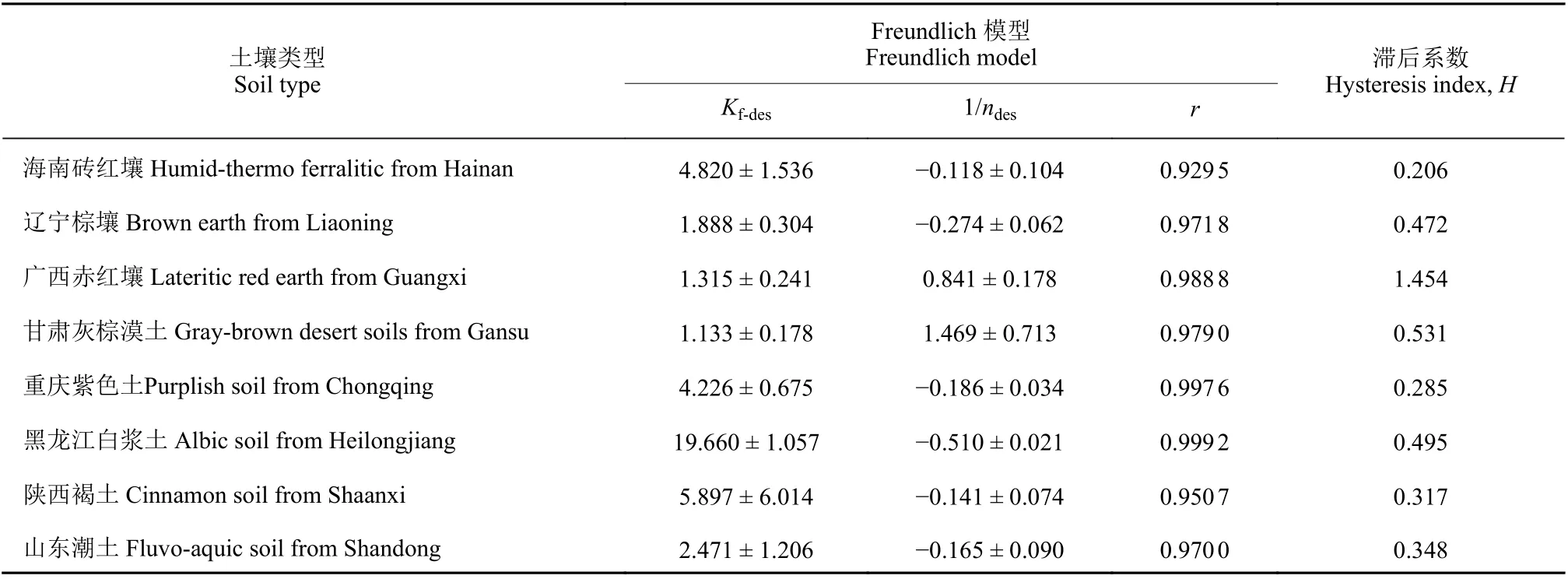
表5 嗪吡嘧磺隆在土壤中的解吸模型及滞后系数Table 5 Freundlich models of metazosulfuron desorption and hysteresis index in soils
有研究[22]认为,出现解吸迟滞现象源于土壤有机质和黏粒等成分对除草剂的吸附作用,除草剂因被吸附在土壤黏粒的层间而不易被释放到土壤中。而本研究发现,黏粒与Kf-ads、Kf-des的相关性不显著 (表6)。这可能是因为相对于黏粒,除草剂的自身理化性质及土壤的其他属性对其吸附解吸的影响更大[12]。有机质与嗪吡嘧磺隆在土壤中Kf-ads、Kf-des呈显著正相关 (表6),这可能是因为土壤中有机质因含有羧基、酚羟基、羰基、乙醇羟基和甲基等与吸附活性相关的官能团,与嗪吡嘧磺隆生成氢键、共价键、配位键、范德华力、电荷偶极-偶极键等化学键而形成吸附力[15]。另外,pH 值与Kf-ads、Kf-des呈显著负相关 (表6),表明土壤pH 显著影响嗪吡嘧磺隆在土壤中吸附和解吸,这与已有的其他磺酰脲类除草剂的研究结果一致[15]。Tang 等研究[23]也发现,土壤有机质的含量和农药的化学特征是导致土壤吸附能力差异的重要因素。单嘧磺隆在土壤中的吸附随pH 值的增加而降低。单嘧磺隆在土壤中也存在解吸迟滞现象,且受有机质含量影响。
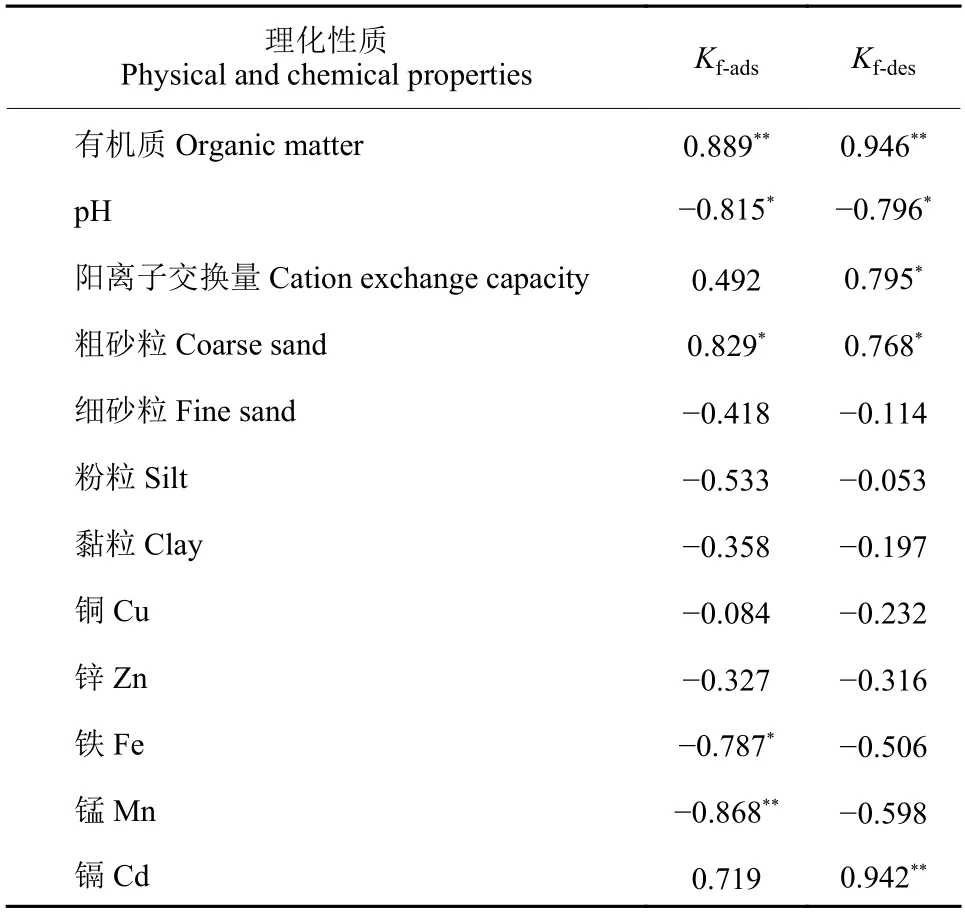
表6 土壤的理化性质与吸附-解吸常数 (Kf) 的相关性Table 6 Correlation between the physical and chemical properties of soils with Kf
2.2 土壤单因素对嗪吡嘧磺隆在土壤中吸附行为的影响
结果 (表7) 表明:腐殖酸对嗪吡嘧磺隆在土壤中吸附行为的影响极显著 (P< 0.01),pH 值和Mn2+的影响显著 (P< 0.05),而高岭土和稻壳生物炭的影响不显著 (P> 0.05)。

表7 五种因素对嗪吡嘧磺隆在土壤中吸附行为的影响Table 7 Effects of 5 factors on metazosulfuron adsorption behavior in soils
高岭土对嗪吡嘧磺隆在土壤中的吸附影响不显著 (P> 0.05),与表6 中黏粒的结果吻合。这可能是因为高岭土是一种1 : 1 型间层黏土矿物[19],其对嗪吡嘧磺隆在土壤中吸附的影响与土壤中黏粘的作用相似。稻壳生物炭含量增加土壤对农药的吸附已有报道[24],其吸附机制包括疏水分配、π-π 电子供体-受体相互作用、氢键和孔填充等,但稻壳生物炭对土壤吸附固定农药的能力的影响与其前驱物来源、结构和性能、碳化程度、后续处理、土壤性质、农药性质等密切有关[19,24]。由表7 知,稻壳生物炭对嗪吡嘧磺隆在土壤中吸附影响不显著 (P> 0.05)。本研究中所用生物炭是以稻壳为原料在600 ℃烧制4 h 而成,而灰分 (特别是在高温热解的生物炭中产生的灰分) 被证实在吸附过程中起负作用[25]。可能是本研究中使用的稻壳生物炭未做进一步改性处理所致。研究表明,同一条件制成的稻壳生物炭在电镜下表面孔隙分布较差,其比表面积、孔容和孔径相对较小[19]。腐殖酸是一类具有复杂结构、呈胶体状态的天然高分子有机物,占土壤有机质的70%~80%[26]。由表7 知,腐殖酸对嗪吡嘧磺隆在土壤中吸附的影响极显著 (P< 0.01),这与表6 中的结果相一致。腐殖酸的添加通过增加有效吸附位点而促进了土壤对农药的吸附[7,26]。结合表6 和表7,pH 显著影响嗪吡嘧磺隆在土壤中吸附 (P< 0.05),且呈负相关。嗪吡嘧磺隆是一种弱酸性除草剂 (pKa3.4)[5],与其他具有弱酸基团的磺酰脲类除草剂一样,嗪吡嘧磺隆以阴离子形式存在于土壤中。随着土壤中pH 值增加,嗪吡嘧磺隆电离的阴离子增加,与土壤胶体之间的斥力也随之增加而导致吸附减少。Mn2+显著影响嗪吡嘧磺隆在土壤中吸附 (P<0.05),且呈负相关。这可能是因为Mn2+和嗪吡嘧磺隆都与土壤的表面吸附有关,二者属于吸附位点的离子交换竞争关系。
2.3 土壤中嗪吡嘧磺隆的吸附过程模型建立
BP 人工神经网络 (ANN) 在处理没有先验函数结构且高度非线性的过程具有突出的能力,多个研究将BP 神经网络模型应用于化学吸附过程模拟,均取得了较好的预测功能和模拟效果[27-29]。本研究中嗪吡嘧磺隆设置39 组数据作为拟合数据,对BP 神经网络模型进行训练。神经网络训练有5 个输入节点,8 个隐形神经元节点,1 个输出节点。经过迭代后趋于稳定,显示良好的收敛效果(图2)。拟合和验证试验发现,神经网络模型拟合程度和精度较高,r= 0.982 6 (图3、图4)。进一步利用不同组数据进行训练,神经网络模型拟合均取得了较好的拟合结果。因此,BP 神经网络模型虽然无法产生相应的模型公式,但可以将复杂的吸附过程简单化,直接聚焦于影响因素对嗪吡嘧磺隆在土壤中吸附行为的复合影响。在本研究所涉及的影响因素和浓度范围内,BP 人工神经网络模型较好地预测了土壤中中嗪吡嘧磺隆的吸附行为。
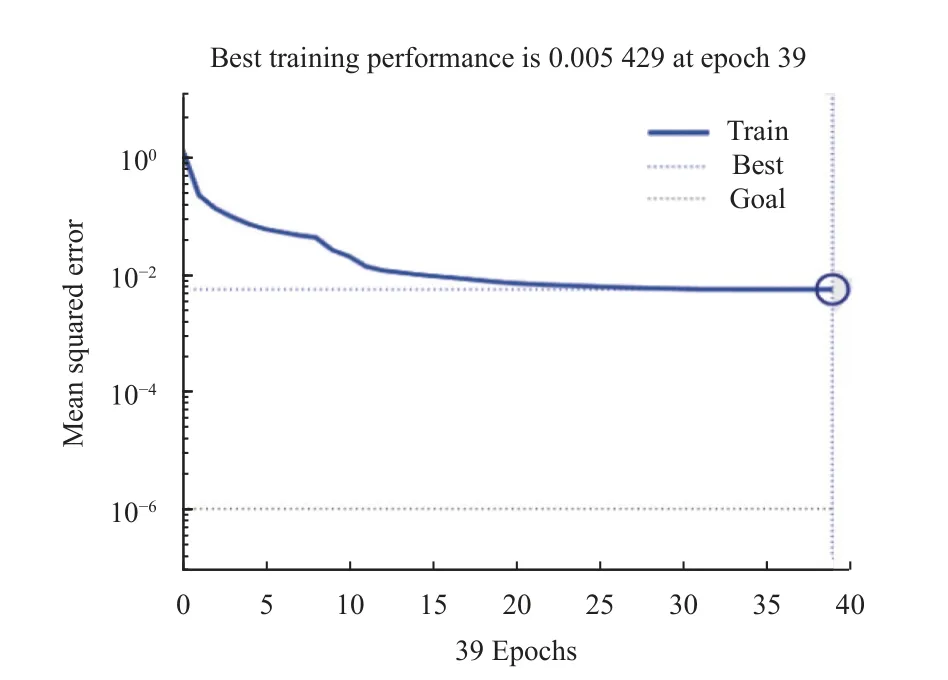
图2 BP 神经网络模型训练迭代过程误差收敛曲线Fig.2 Error convergence curve during the iteration training of neural network model
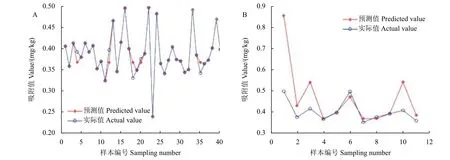
图3 BP 神经网络模型训练样本 (A) 和测试样本 (B) 预测值与实际值对比Fig.3 Comparison between the output of BP neural network model (A) and the measured value (B)during training and verifying process
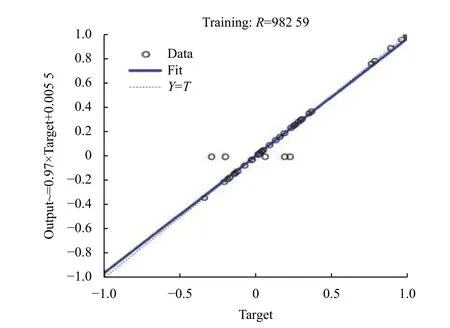
图4 BP 神经网络模型可靠性验证Fig.4 Verification of BP neural network model
3 结论
1) 嗪吡嘧磺隆与土壤溶液接触4 h 内为快速吸附阶段。Freundlich 模型可较好地拟合嗪吡嘧磺隆在土壤中的等温吸附。
2) 8 种土壤对嗪吡嘧磺隆的吸附能力为弱。除广西赤红壤外,其他7 种类型土壤中嗪吡嘧磺的解吸过程存在滞后现象。
3) 嗪吡嘧磺隆在土壤中吸附行为受腐殖酸的影响极显著,受pH 值和Mn2+的影响显著,受高岭土和稻壳生物炭的影响不显著。
4) 在本研究所涉及的影响因素和浓度范围内,BP 人工神经网络模型较好地预测了土壤中嗪吡嘧磺隆的吸附行为。
5) 本研究为评价嗪吡嘧磺隆及磺酰脲类除草剂的环境行为及环境安全性提供了科学依据,可进一步指导其合理使用及农业生态环境保护。
