MALDI-TOF MS技术直接鉴定无菌体液病原菌的效果评价*
2022-12-26张鞠玲鲍春梅贾天野陈素明庞君丽李伯安
张鞠玲,康 琳,鲍春梅,王 欢,贾天野 ,陈素明,庞君丽,李伯安△
1.解放军总医院第五医学中心检验科,北京 100039;2.军事科学院军事医学研究院微生物流行病研究所,病原微生物生物安全国家重点实验室,北京 100071
脓毒症是机体对感染反应失调进而引发器官功能障碍、危及生命的疾病[1]。脓毒症发生率高,全球每年有超过1 900万严重脓毒症病例,美国每年有75万脓毒症患者,造成超过 21万人死亡,是危重患者死亡的主要原因[2]。在临床 ICU,血液感染所致脓毒症的发生率可达到95%,病死率约为26%;腹腔感染所致脓毒症的发生率可达到 40%,病死率约为 36%[3-4]。及时识别病原菌并使用适当的抗菌药物治疗可显著降低脓毒症病死率[5-6]。基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS)是近年来关注度较高的鉴定技术,通过采集待检标本中的生物标志物蛋白,得到目标生物的蛋白指纹质谱图,与数据库中标准质谱图进行比对,从而鉴定细菌、真菌及分枝杆菌等,该方法具有快速、准确、高通量、重复性好、灵敏度高等优点[7-8]。本研究将血液和腹水阳性培养瓶中的病原菌富集后,应用MALDI-TOF MS进行直接鉴定,与传统培养法比较菌种鉴定结果的准确性,探讨此方法在脓毒症诊断中的应用价值。
1 资料与方法
1.1标本来源 连续收集2021年6-10月解放军总医院第五医学中心检验科血液、腹水培养报警阳性的标本共418份(包括需氧瓶和厌氧瓶)。其中血培养阳性标本220份,腹水培养阳性标本198份;单菌株感染培养瓶410份,混合感染培养瓶8份。单菌株感染中革兰阴性菌244 株,革兰阳性菌149 株,真菌17株。对于同一患者不同部位感染的普通和厌氧培养瓶也同时纳入本研究中。
1.2仪器与试剂 血平皿(英国Oxoid公司)、中国蓝平皿(Oxoid公司,英国)、沙保弱平皿(英国Oxoid公司)、1.5 mL离心管(美国Axygen公司)、α-氢基-4-羟基肉桂酸即HCCA(德国Bruker公司)、无水乙醇、乙腈及甲酸(美国Fisher Scientific公司),溶血剂(迈瑞南京生物技术有限公司)。基质辅助激光解吸电离飞行时间质谱仪Microflex LT(德国Bruker公司),VITEK-2全自动微生物鉴定及药敏分析仪(法国梅里埃生物股份有限公司),电热恒温培养箱(上海一恒科技有限公司),高速离心机(美国Thermo公司),BACT/ALERT 3D 240全自动血液培养仪(法国梅里埃生物股份有限公司)。
1.3方法
1.3.1MALDI-TOF MS检测
1.3.1.1标本的前处理 (1)含有血细胞阳性瓶的前处理:用5 mL无菌注射器从血阳性培养瓶中吸取2 mL液体至空白管中,15 000 r/min离心3 min,吸取200 μL上清液于EP管中,加入100 μL溶血剂振荡混匀30 s,将混合物12 000 r/min离心3 min吸去上清液,再加入700 μL蒸馏水振荡混匀30 s,将混合物12 000 r/min离心3 min吸去上清液备用。(2)不含血细胞阳性瓶的前处理:从培养瓶中吸取500 μL带菌液体于EP管中,将混合物12 000 r/min离心3 min吸去上清液,加入700 μL蒸馏水振荡混匀30 s,将混合物12 000 r/min离心3 min吸去上清液。(3)菌液富集:向留有沉淀的EP管中加入300 μL蒸馏水和900 μL无水乙醇振荡混匀30 s,将混合物12 000 r/min离心3 min吸去上清液,加入50 μL 70%甲酸,再加入50 μL乙腈,振荡混匀30 s,12 000 r/min离心2 min,得到上清液待用。
1.3.1.2MALDI-TOF MS鉴定 取1 μL上清液点在MALDI靶板上,干燥后表面加入1 μL基质,再次室温干燥后将靶板放入质谱仪中进行蛋白质指纹图谱的采集。使用MALDI Biotyper 3.0软件进行数据分析和比对得出鉴定结果。每株菌点2个靶点进行平行检测,取最高评分计入数据统计。
1.3.1.3MALDI-TOF MS 结果判读 MALDI-TOF MS系统鉴定分值>2.0为菌株鉴定结果到种水平可信;分值在1.7~2.0为菌株鉴定结果到属水平可信,重新检测或补充实验帮助鉴定;分值<1.7结果不可信。
1.3.2病原菌培养与生化鉴定 血培养仪阳性瓶报警后,经涂片、革兰染色、镜检、转种血平皿、中国蓝平皿或厌氧平板,培养24~48 h,挑取纯菌落,选取合适的鉴定卡用VITEK-2鉴定并记录结果。VITEK-2鉴定结果同MALDI-TOF MS直接鉴定结果不同的菌株,送生工生物工程(上海)股份有限公司进行PCR测序。
1.3.3质量控制 基质辅助激光解吸电离飞行时间质谱仪Microflex LT和VITEK-2全自动微生物鉴定及药敏分析仪均使用大肠埃希菌ATCC25922、金黄色葡萄球菌ATCC25923、白色念珠菌ATCC14053和肺炎链球菌ATCC49619作为质控菌株,菌株购自美国模式培养物集存库。
1.4统计学处理 采用SPSS25.0软件进行数据处理,计数资料以频数或百分率表示,比较采用χ2检验和Fisher检验。比较MALDI-TOF MS与VITEK-2菌株鉴定的准确率。准确率=准确鉴定菌株数/菌株总数×100%。以P<0.05为差异有统计学意义。
2 结 果
2.1MALDI-TOF MS单一病原菌的直接鉴定 410份单菌株感染所致的阳性标本中,MALDI-TOF MS 直接鉴定准确率为98.54%(404/410),VITEK-2鉴定的准确率为98.54%(404/410),两者比较差异无统计学意义(χ2=0.085,P>0.05)。革兰阴性菌MALDI-TOF MS 直接鉴定的准确率为99.59%(243/244),VITEK-2鉴定的准确率为98.77%(241/244),两者比较差异无统计学意义(χ2=0.252,P>0.05)。革兰阳性球菌MALDI-TOF MS鉴定的准确率为97.32%(145/149),VITEK-2鉴定的准确率为99.33%(148/149),两者比较差异无统计学意义(χ2=0.814,P>0.05)。17株真菌MALDI-TOF MS 直接鉴定的准确率为94.12%(16/17),VITEK-2鉴定的准确率为88.24%(15/17),两者比较差异无统计学意义(P=0.5)。见表1。MALDI-TOF MS和VITEK-2鉴定结果不同的单菌株共12株,经分子生物学方法确认,MALDI-TOF MS鉴定准确6株,准确率为50.00%(6/12)。见表2。
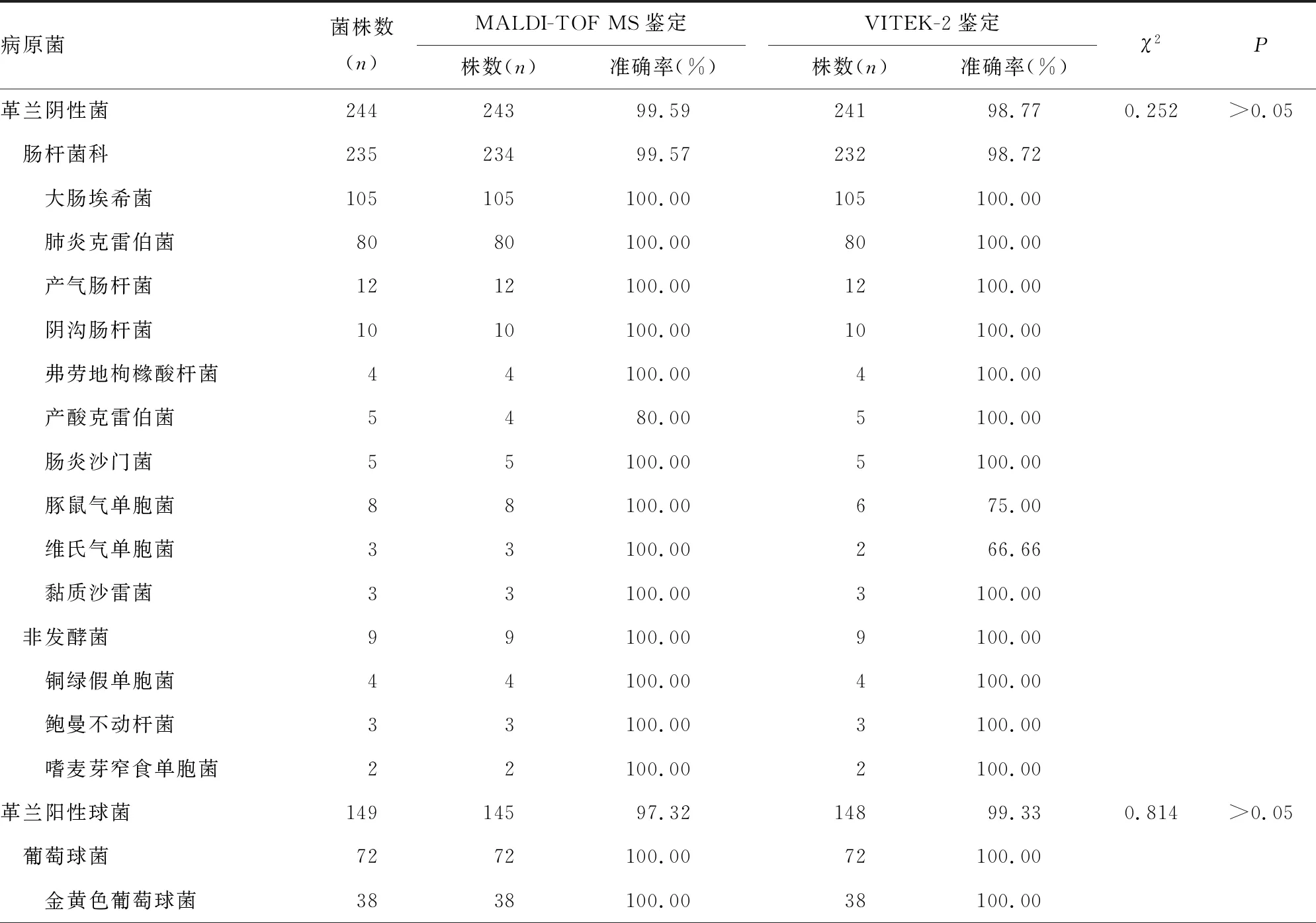
表1 单菌株感染MALDI-TOF MS和VITEK-2鉴定结果
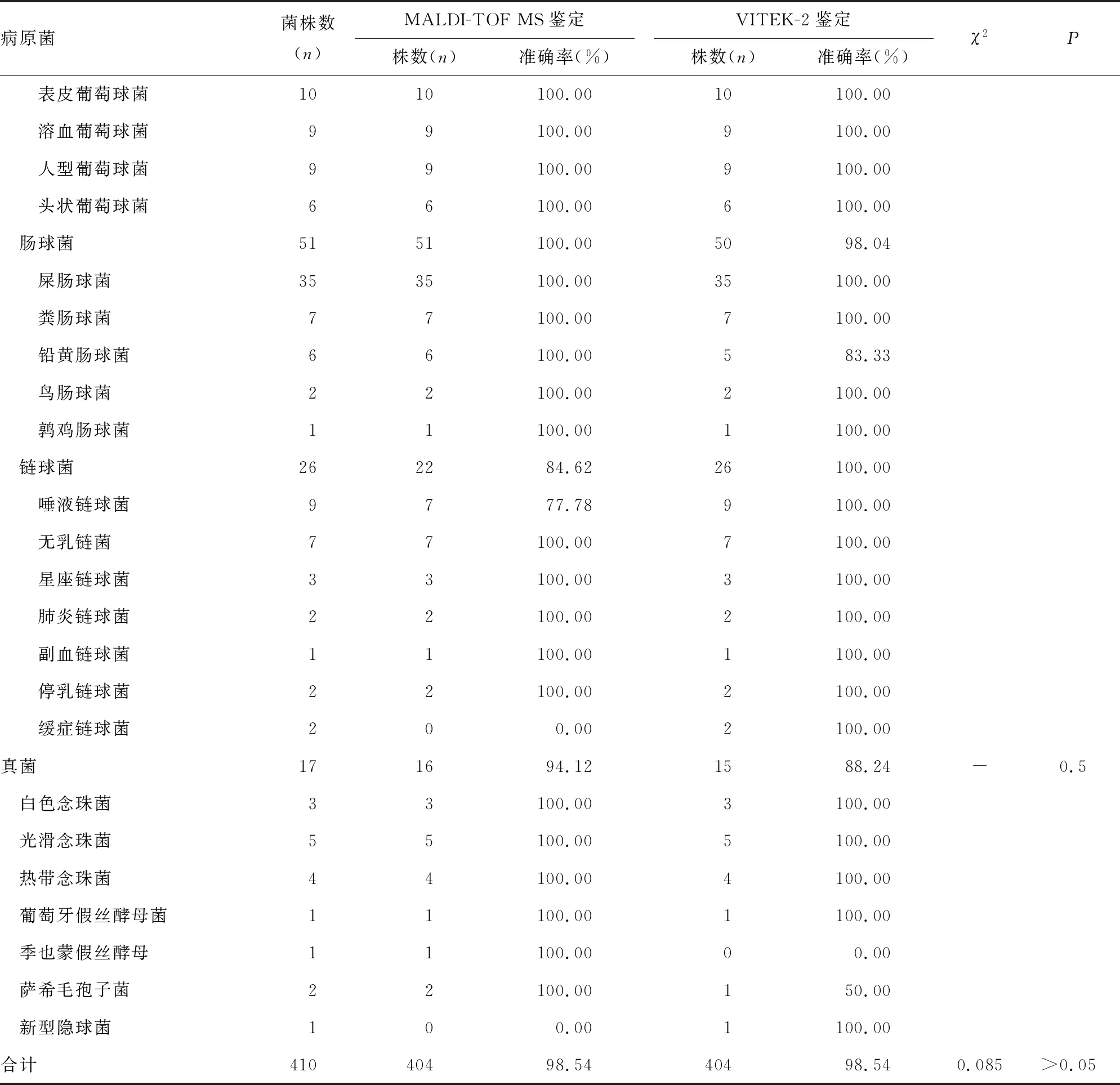
续表1 单菌株感染MALDI-TOF MS和VITEK-2鉴定结果
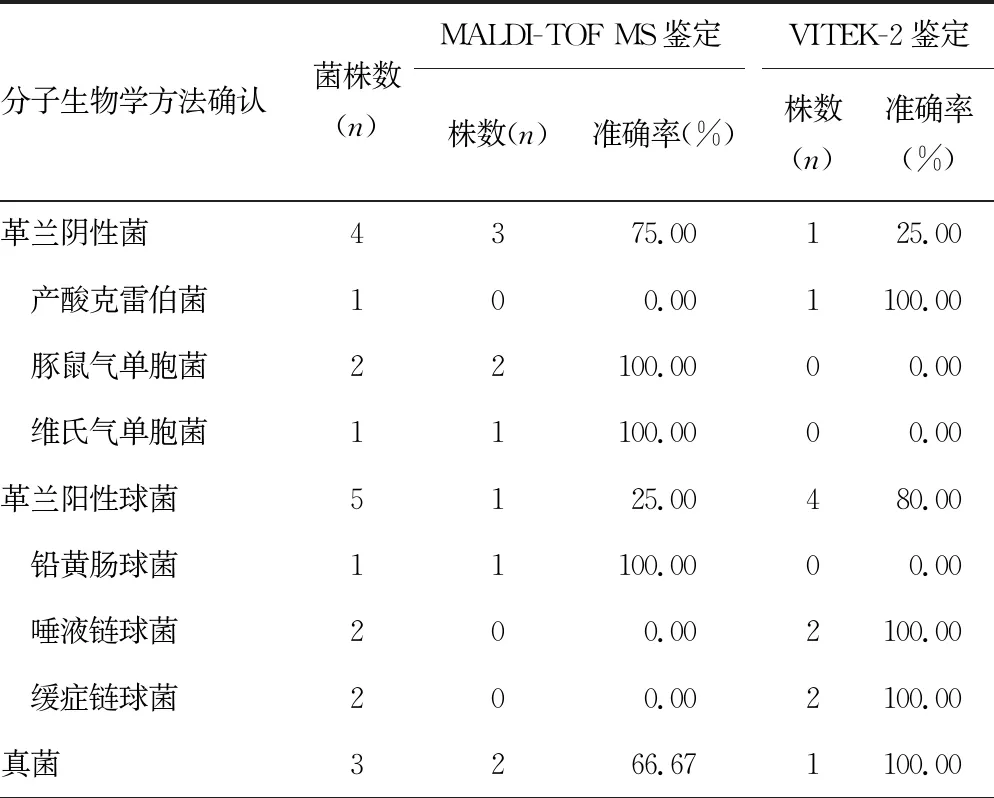
表2 两种方法鉴定结果不同的单菌株分子生物学方法鉴定情况分析
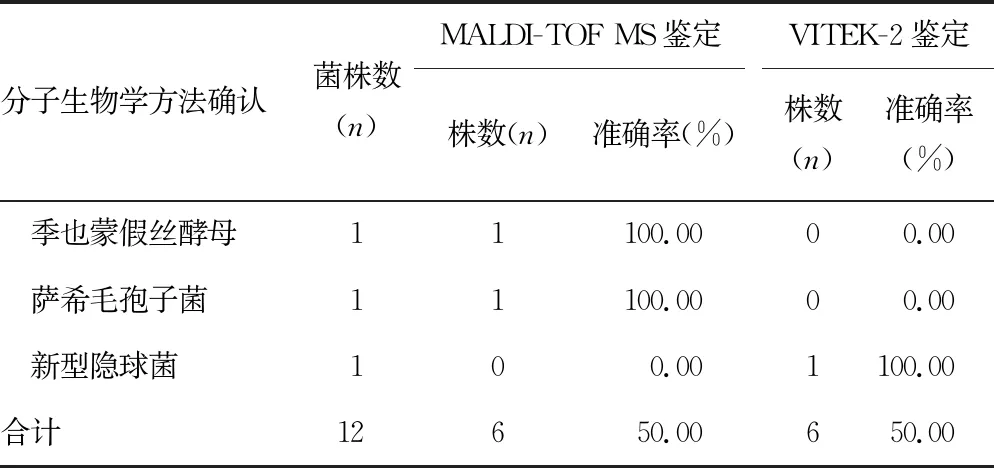
续表2 两种方法鉴定结果不同的单菌株分子生物学方法鉴定情况分析
2.2MALDI-TOF MS直接鉴定分值分布 MALDI-TOF MS直接鉴定,410株单菌株鉴定分值>1.7即鉴定至属水平占93.17%(382/410),分值>2.0即鉴定至种水平占82.68%(339/410)。其中革兰阴性菌中属、种水平鉴定率分别为97.54%(238/244)、89.34%(218/244),革兰阳性球菌中属、种水平鉴定率分别为87.92%(131/149)、74.50%(111/149),真菌中属、种水平鉴定率分别为76.47%(13/17)、58.82%(10/17)。革兰阴性菌中鉴定分值<1.7的共6株,其中5株结果正确(肠炎沙门菌1株、嗜麦芽窄食单胞菌2株、黏质沙雷菌2株),1株产酸克雷伯菌鉴定不正确。革兰阳性球菌中鉴定分值<1.7的共18株,其中14株结果正确(头状葡萄球菌2株、肺炎链球菌2株、副血链球菌1株、唾液链球菌4株、星座链球菌3株、停乳链球菌2株),4株未鉴定出结果(唾液链球菌2株、缓症链球菌2株)。真菌中鉴定分值<1.7的共4株,其中2株萨希毛孢子菌、1株葡萄牙假丝酵母菌鉴定分值<1.7,但结果正确,而1株新型隐球菌MALDI-TOF MS未鉴定出结果。复合菌株中属、种水平鉴定率分别为75.00%(6/8)、25.00%(2/8),2株复合菌鉴定分值<1.7,但是结果正确。见表3。
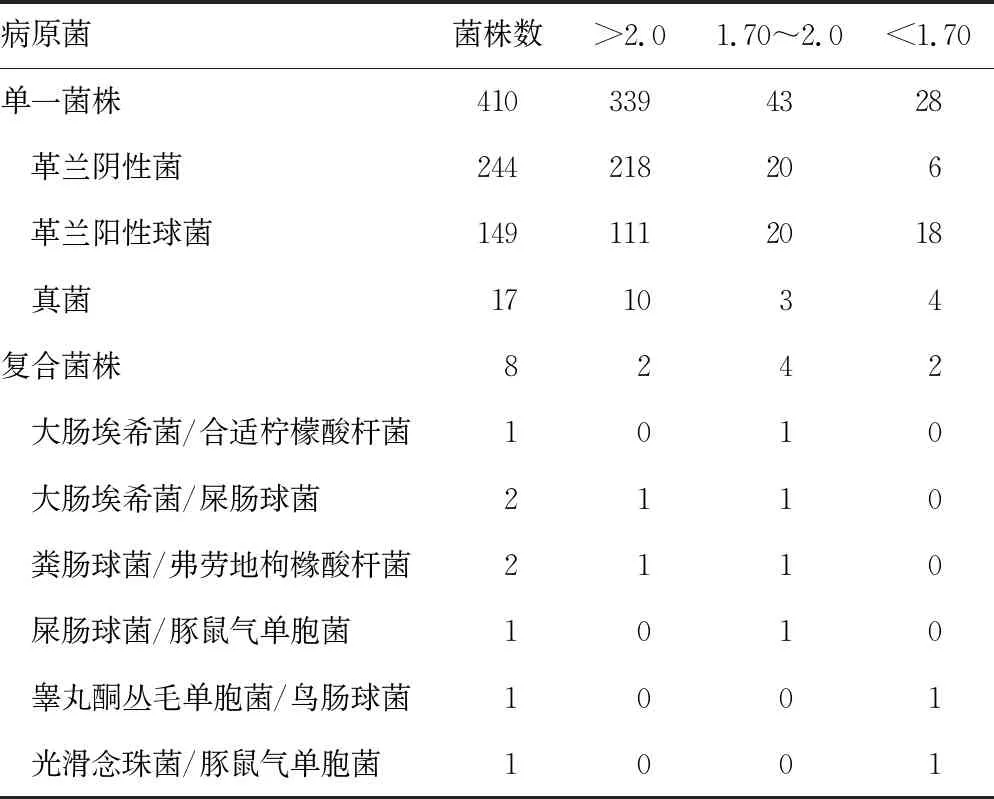
表3 418份阳性标本MALDI-TOF MS直接鉴定分值分布(n)
2.3时间比较 MALDI-TOF MS从阳性培养瓶报警、卸载、提取菌液到鉴定出结果需要30 min,VITEK-2从阳性培养瓶报警、卸载、标本接种、培养、挑取纯菌落上机到鉴定出结果需要24~48 h,分子生物学方法经测序鉴定需要 24~48 h。
3 讨 论
脓毒症发病机制复杂,涉及全身多个系统,发病率和病死率居高不下。病程早期难以察觉,常缺乏指向性的临床表现,容易被误诊成局部病灶感染,进而发展成脓毒性休克,识别致病菌并合理选用抗菌药物是脓毒症个体化诊断和精准治疗的关键[9-10]。MALDI-TOF MS在微生物病原菌的快速鉴定中发挥着越来越重要的作用[11-12],目前已报道的MALDI-TOF MS直接鉴定的标本种类包括血、脑脊液、尿等[13-14],鲜见直接鉴定腹水标本的相关报道。本研究中,腹水和血液培养阳性标本预处理后经MALDI-TOF MS直接鉴定准确度高,可为快速诊断由腹水和血液感染所致的脓毒症带来极大的便利。
利用质谱技术直接分析临床标本,其前处理方法至关重要。本研究通过裂解破坏宿主细胞,再经离心收集菌体进行鉴定,溶血剂尝试选择实验室血常规仪器配套试剂,无需其他试剂及耗材,与传统生化VITEK-2鉴定方法相比,鉴定符合率高,与王林等[15]研究结果相同。Bruker Sepsistyper试剂盒对革兰阴性菌和革兰阳性球菌的鉴定率接近但略低于LIN方法[16-17],但试剂盒成本高且部分试剂采购受限,目前不适合在临床实验室广泛推广。本研究显示,MALDI-TOF MS直接鉴定革兰阴性菌属、种的准确率最高,其次是革兰阳性球菌、真菌,与张浩然等[18]报道相同。本研究中,1株产酸克雷伯菌鉴定不准确,这可能与表层黏液影响有效菌体蛋白的获取有关。链球菌鉴定分值普遍较低,这可能与链球菌生长缓慢,细菌富集量相对较少,细胞壁较厚增加其抗溶解性有关,同时溶解后的血细胞成分也对结果产生了干扰[19]。新型隐球菌未鉴定出结果,可能与隐球菌细胞壁过厚不易破坏,且离心获得菌量不足导致未获得足够的菌体蛋白谱峰,无法完成质谱分析有关。MALDI-TOF MS可将两种菌分开鉴定,本研究中复合菌属鉴定率达75.00%,与侯伟伟等[20]报道基本一致。通过对现有鉴定方法用时比较,发现VITEK-2鉴定单菌株需24~48 h,MALDI-TOF MS对单菌株鉴定耗时约 30 min且可多菌株同时检测,用时最短、操作简便,实验室人员经过培训可独立完成,人为误差较小。
综上所述,本研究利用MALDI-TOF MS对血和腹水培养瓶标本进行快速直接鉴定,与传统菌落培养鉴定方法相比较,鉴定准确度高、快速、高效、成本低廉且实用性强,可为脓毒症病原菌的鉴定提供有效、可行的实验室检测手段,适合在临床微生物实验室中进行推广。
