金属基3D打印支架的构建与功能化研究进展*
2022-12-20蔡兴博董艳王斌张必欢张悦陆声徐永清
蔡兴博 董艳 王斌 张必欢 张悦 陆声 徐永清*
1 金属基3D打印支架概述
骨是一种复杂的不均匀多孔生物组织,起到支撑器官、肌肉和其他身体组织的关键作用。骨组织的孔隙率和纤维方向是由其具体的生物功能决定的。此外,骨的不同成分(骨小梁或皮质)在个体年龄、性别、解剖位置间的差异性,增大了生物制造的难度[1]。功能化支架可以增强、恢复或替换丢失/缺陷的受损组织微环境中的完整细胞功能。因此,机械刺激、良好的生物降解率和骨诱导的营养支持成为优化植入物设计的3 个关键因素[2]。近年来,3D打印技术可制造出适合骨整合的复杂几何形状及微结构,是具备优良应用前景的医疗器械制造技术[3]。
传统制造属于减材制造,受模具限制,难以达到精细化制造,如骨小梁结构。相对于传统制造,3D打印技术具有如下优点:①属于增材制造,通过文件导向实体,无须实体开模与制造工厂生产线,就能实现任何设计,大大提高了制造效率;②更加精细化的制造,可打印出血管、骨小梁、肝脏、心脏等器官;③个性化制造,解决个体差异问题,如手术导板、口腔烤瓷牙、骨肿瘤术后或严重创伤后的肢体重建;④将传统制造业的生产力密集转变成脑力密集,打印文件具有行业统一标准,构建文件时更加集思广益;⑤形象立体,帮助医生更全面客观地了解病情。
与非金属支架相比,金属基3D打印支架具有较高的强度、良好的韧性、性能稳定、可靠性高、延展性好、较强的抗疲劳弯曲、优异的加工性、可制成复杂结构等其他医用材料不可替代的性能。相对于常规制造金属支架,金属基3D打印支架具有如下优点:①个性化定制,形态上任意设计,能达到骨缺损的精准匹配,结构与材料属性更接近人体骨组织;②具有骨整合效果,加速金属—骨界面与宿主骨整合的速度[4]。但也有如下缺点:①金属支架的表面修饰工艺相对较少,功能化的手段不丰富;②金属支架加工成本高,加工周期较长,制造时容错率较低。
2 金属基3D打印支架的构建和功能化方法
金属基3D打印支架可以通过改变自身的拓扑结构和表面修饰,获得不同的功能。改变自身的拓扑结构,主要通过改变支架材料成分、设置不同的打印参数、改变晶胞结构来实现;在获得理想的拓扑结构之后,可以对支架进行表面修饰(浸泡技术、微弧氧化、纳米材料修饰等)进一步获得不同功能。
2.1 改变支架的拓扑结构
支架材料成分及打印参数是决定其机械性能和生物功能的关键。Lei等[5]通过设置不同的3D打印参数,如3D印刷激光功率、扫描间隔和切片厚度层,控制多孔钛合金(Ti-6Al-4V)支架的微观拓扑结构,发现支架的定制化可以调控细胞行为和生物学特性。金属基3D打印支架构建方法不仅可以通过改变打印参数来控制支架内部结构,还可以通过金属与陶瓷粉末的混合来实现。Yi 等[6]将直径约为25 μm的羟基磷灰石(hydroxyapatite,HA)粉末和直径为15 ~53 μm 的Ti-6Al-4V 粉末混合调制,制备Ti-6Al-4V/HA 复合多孔支架,证明通过不同材料的混合可以实现精确控制支架的机械性能和生物功能。该研究团队还发现电化学沉积时间的长短会影响3D 打印Ti-6Al-4V 支架表面羟基磷灰石涂层的形态和黏附MC3T3-E1 细胞的功能。设置不同的打印参数和掺入非金属粉末是控制金属支架理化特性的基础方式。
晶胞是构成3D打印金属支架的最基本的几何单元,改变晶胞结构的形状、孔隙率和孔径可以使支架达到不同的力学强度与作用。支架的孔隙率和孔径对细胞增殖、分化、细胞外基质(extracellular matrix,ECM)分泌和新生组织形成起重要作用,均匀的孔隙有利于细胞渗透、骨形成和血管生成[7]。Yang 等[8]设计了仿钻-60°、仿钻-90°、仿钻-120°、正四面体和正六面体5种不同的钛合金支架形状,每种结构形状都含3种孔径(400 μm、600 μm和800 μm);发现当孔径增大时,每种结构的强度都会降低。研究发现,在3D打印中,单元配置和参数对三周期最小表面单元的机械和渗透性能有重大影响[9]。也有学者通过仿生学制造了模拟小梁结构的钛合金单元细胞,通过改变细胞的支撑尺寸和缩放细胞整体,获得了5 种不同孔径和孔隙率的模拟小梁结构的单元细胞,发现结构孔隙率越大,刚度越小,承载能力越差[10]。因此,需要在统筹兼顾金属支架的孔隙形态和大小的基础上,寻找最优化的支架晶胞结构,使其达到既能保证力学强度,又能促进成骨的效果。复杂拓扑结构的特点可以被用作人体植入物或组织工程的支架。这些多孔结构可以为细胞的附着和增殖提供大量的空间。3D打印晶胞结构目前主要包括正六面体、球体、模拟骨小梁三维体、钻石体、陀螺体,具有150 ~500 μm多孔的金属支架都特别有利于骨长入[11]。目前尚无最优化的特定孔隙率与晶胞结构,也是多孔金属支架领域仍在探索的问题。
2.2 对支架进行表面修饰
在确定理想的拓扑结构之后,可以通过浸泡技术、微弧氧化、纳米材料修饰等对支架进行表面修饰,以获得更好的生物相容性与诱导成骨特性。
浸泡技术是将支架浸入在具有生物活性化合物液体中,使支架表面获得生物活性化合物涂层。Tsai 等[12]使用简单的浸泡技术将硅酸镁钙(Mg-CS)和壳聚糖(CH)化合物附着到Ti-6Al-4V支架上,即Mg-CS/CH涂层的Ti-6Al-4V支架;实验表现出该涂层可以创造一种有利的、诱导性的微环境,且在兔子临界尺寸骨缺损模型上得到验证。浸泡技术具有成本低、容易制备等优点,但是载药量有限,载药后药物缓释时长有限,如前期释放快、浓度高,后期释放缓慢、浓度低。
微弧氧化(micro arc oxidation,MAO)也称为阳极火花沉积或等离子体电解氧化,是通过在支架表面形成生物活性的TiO2层来提高网状结构的生物活性的技术[13]。Zhang 等[14]在MAO 多孔Ti-6Al-4V 支架中加载万古霉素,该支架显示出较高的负载能力和持续的万古霉素释放动力学,证明了这种MAO多孔Ti-6Al-4V支架可以用于治疗复杂的骨感染。微弧氧化技术不仅可用于提高钛的骨整合性,还可以对镁、银、铜、钙、锌、硅、磷等材料进行表面涂层与修饰。虽然微弧氧化技术具有稳定性好、成本低、无毒、制备简单等优点,但是微弧氧化瞬间放电特性难以控制,给不同结构和大小的孔隙修饰带来巨大挑战[15]。
纳米材料修饰是指用物理、化学方法改变支架纳米微粒表面的结构和状态,实现人们对纳米微粒表面的控制。部分研究表明,将金属支架进行纳米材料修饰,可以获得更好的生物相容性与诱导成骨特性。纳米级咪唑啉分子筛骨架-8 (nano porous zeolitic imidazolate framework,nanoZIF-8)是金属有机骨架的一个亚类,Zhong 等[16]通过挤压3D 打印技术将nanoZIF-8 加入到由聚己内酯和二水磷酸二钙组成的复合支架中;体外研究表明,与未掺入nanoZIF-8的支架相比,该支架与骨髓间充质干细胞具有更好的生物相容性,显著上调成骨相关基因和蛋白的表达,促进细胞外基质矿化。也有团队发现,通过多巴胺辅助将纳米银封装在钛合金支架表面,能够使金属钛合金支架获得抗菌能力[17]。纳米材料修饰具有更好的稳定性,容易获得单分子层表面修饰,在极大保留原本纳米材料结构特征的同时,实现其支架表面的功能化,获得微纳尺度上不同的功能界面。但是,由于纳米颗粒的形貌、尺寸较难控制,生物体或生物分子的介入使得产物回收和纯化的难度较大,大规模制造纳米颗粒的均一性较难得到保证[18]。
3 金属基3D打印支架的功能
通过上述改变拓扑结构和表面修饰后,金属支架可被赋予抗菌、载药与药物控释、诱导成骨、骨缺损重建等生物功能,在骨组织工程领域已经得到广泛应用。
3.1 抗菌
3D打印支架装置添加长期稳定缓释的生物活性金属离子,如银离子、铜离子[19]、锂离子[20]、锶离子和镁离子等可以自然地阻碍微生物的生长和细菌生物膜的植入物附着,从而不需要使用专门的抗感染药物,且金属离子在支架降解过程中缓慢释放,可以发挥促进软骨细胞增殖或血管生成等作用。Qing等[21]用激光熔融法制备了高孔不锈钢元件,并采用原位水热结晶法制备了银掺杂沸石涂层,该支架对大肠杆菌和金黄色葡萄球菌有抑制作用。Jia等[17]通过物理交联丝纤维蛋白多层膜封装纳米银,在钛合金支架上构建了原位水热生长的微/纳米结构钛酸盐层,即多层丝蛋白/纳米银生物功能化涂层/钛合金支架;该银固定支架不仅减少了细菌在表面的黏附,还能有效地杀死游离细菌,并且抗菌性能够保持6周。不仅银离子具有抗菌作用,金刚石修饰的支架也具有一定的抗菌性能。Rifai等[22]通过在选择性激光熔化钛上覆盖纳米金刚石涂层,培养3 d后明显抑制金黄色葡萄球菌的定植。除了负载金属离子,将多孔金属支架负载抗菌药物同样能够达到抗菌作用。目前,金属支架抗菌的效果主要是通过将另一种抗菌物质(银、抗菌药物等)在支架表面或内部进行交联,达到抗菌目的,如何达到良好的交联,同时又能保证长效抗菌,是亟待攻克的重点与难点。
3.2 载药与药物控释
金属基3D打印支架的多孔结构可负载一定量的药物,针对不同的疾病,可装载相应的药物进行治疗,如慢性骨髓炎、骨肿瘤、骨质疏松等[23]。支架能够搭载药物首先需要具有高比表面积和大孔容的特点。而介孔材料的结构特征是有序的大孔体系,孔径大小在2 ~50 nm 之间,非常适合进行载药;包括沸石、碳分子筛、多孔金属氧化物、有机和无机多孔杂化和柱状材料、硅包合物和包合物水合物[24]。此外,药物-3D打印金属基支架装置组合系统(应用金属药物装载等方式对3D打印装置进行表面修饰)可以在不影响支架机械性能的情况下装载抗生素,如多西环素、万古霉素,在骨科多种疾病中发挥抗感染、诱导成骨的双重生物作用[25]。对于慢性骨髓炎,也有研究团队将万古霉素负载至MAO 的3D 打印多孔Ti-6Al-4V 支架上,通过高效液相色谱证实,该支架具有高负载能力和持久的万古霉素释放动力学,且可抑制兔的耐甲氧西林金黄色葡萄球菌骨感染[14]。在临床骨肉瘤的治疗中,术后肿瘤的复发和化疗耐药性提出了开发局部功能化支架的迫切需求:选择性地杀死残留肿瘤细胞,同时为有效填补肿瘤切除引起的骨缺损提供支架[26]。Dang等[27]通过将支架浸泡在不同浓度的氮化钛(titanium nitride,TiN)和阿霉素(doxorubicin,DOX)溶液中,在支架表面连续包覆TiN微粒子和DOX;经过局部控释化疗,在体内外均取得了良好的治疗效果。对于骨质疏松症,骨重建不平衡是导致种植体植入失败的主要原因,针对此机理,Kwon等[28]开发了2,5-二羟基苯甲酸乙酯(E-2,5-DHB)结合的钛植入物,使用聚乳酸-乙醇酸(polylactic glycolic acid,PLGA)涂层进行E-2,5-DHB的局部递送,发现E-2,5-DHB 的释放导致了骨吸收的减少和植入物周围骨形成的增加。载药微球是药物与支架的中间载体,如何提高支架的载药量及控制药物的精准释放是亟待解决的问题。
3.3 诱导成骨
众所周知,若想让支架促进成骨,则需要在支架周围营造特定的微环境,金属3D打印支架经过表面涂层、掺入镁粉、负载蛋白、细胞与生物活性物质均可达成该目标。矿化胶原蛋白(mineralized collagen,MC)基质具有与天然骨组织相似的成分和微观结构,MC 基质还可诱导骨再生和刺激血管新生,可通过缓慢的替代过程被降解。Ma等[29]将3D 打印的多孔钛合金(porous titanium,PT)支架浸泡在含有胶原和羟基磷灰石(HA)前体的矿化液中,在支架上形成仿生MC 基质,是一种兼具类骨机械性能和骨诱导能力的新支架(MC/PT);该团队发现,MC/PT 支架可以促进骨髓间充质干细胞(bone mesenchymal stem cells,BMSCs)向成骨细胞分化;并在兔桡骨缺损模型中,MC/PT支架显著改善“骨—植入物”一体化,通过诱导血管生成和成骨,成功修复骨缺损,该支架可用于精确修复不规则的大型承重骨缺损。也有团队设计了一种独特的可注射生物活性水凝胶,由海藻酸盐、明胶和纳米晶羟基磷灰石组成,能够渗透到多孔结构的Ti-6Al-4V支架中,通过细胞活性检测、细胞黏附和细胞骨架蛋白表达及碱性磷酸酶检测,验证了Ti-6Al-4V 支架/水凝胶系统具有细胞相容性与诱导成骨能力[30]。
镁(Mg)是天然骨的重要组成部分,具有良好的骨诱导活性和生物活性。有研究表明,镁在体外和体内抑制破骨细胞早期分化并抑制骨吸收[31]。Lai等[32]对传统的多孔钛合金支架添加镁粉,发现该支架具有更好的成骨和血管生成能力,且植入后进行0 ~12周的生物安全性评估发现该支架未引起血清Mg 离子浓度增加。也有研究团队利用聚多巴胺的表面黏附能力,将Mg掺杂到3D打印钽金属支架的表面;通过大鼠股骨髁骨缺损模型观察,该支架可显著促进血管化骨形成和骨结合[33]。除了镁离子,功能化支架通过释放银离子、锂离子、锶离子和镁离子等,也能发挥刺激刺激软骨、软骨细胞增殖或血管生成等作用。
金属基支架表面负载蛋白与生物活性物质,也是促进支架周围成骨的方法。骨形态发生蛋白(bone morphogenetic protein,BMP)属于转化生长因子-β 家族,具有良好的骨诱导性,被认为有可能促进骨的生成[34]。Zhang 等[35]先将重组人骨形态发生蛋白加载到Ti-6Al-4V支架的空腔中,成功地改善了Ti-6Al-4V支架的骨整合能力,实现了羊颈椎缺损模型中种植体术后更早、更稳定的固定。研究表明,在多孔Ti-6Al-4V支架上负载雪旺细胞衍生的外泌体,可以促进BMSCs的迁移、增殖和分化[36]。相关蛋白与生物活性物质能够创造有利于成骨的微环境,但是活性物质的筛选具有探索性,其意义大于金属支架本身。
3.4 骨缺损重建
3D打印技术因个性设计、快速成型等特点,可以克服患者的骨缺损不规则情况和局部解剖形态变异等问题,定制个性化的骨缺损模型,实现精准治疗。金属支架材料目前主要应用在肿瘤切除术后重建,包括骨盆、骶骨、脊柱、肩关节周围、四肢长骨骨干及踝关节、肘关节、腕关节周围的骨肿瘤切除重建;其中在骶骨、脊柱、骨盆的肿瘤切除术后的骨缺损重建中应用相对成熟[4]。吴家昌等[37]通过Mimics软件三维重建肿瘤及周围解剖关系,个体化设计腰椎和颈椎的金属人工椎体,分别对2 例患者完成颈椎和腰椎椎体重建,术后长期随访显示人工椎体与周围椎体匹配良好,颈腰椎活动度好。也有研究团队设计了3D打印的钛合金人工椎体对脊柱肿瘤(T11-L1)切除术后进行重建,多孔钛合金人工椎体的孔和网的直径分别为800 μm和550 μm,平均孔隙率为50%~80%,患者随访2年,恢复良好,无肿瘤复发,无并发症[38]。其次,在复杂的关节翻修案例中金属支架也得以应用,如打印制造个体化的髋臼假体、髋臼垫块、髋臼缺损加强环及感染后的临时间隔器等。许康永等[39]应用个体化3D打印钛合金臼杯重建重度骨缺损髋臼旋转中心,术后肢体长度和髋关节功能均有显著改善,术后6个月随访X线片示3D臼杯固定可靠,有较好的骨长入。雷鹏飞等[40]应用3D打印多孔金属髋臼双动头重建系统治疗17例严重髋臼结构性骨缺损患者,术后1个月Harris 髋关节评分显著改善,随访显示髋臼组件在影像学上均稳定、无移位。
4 金属支架体内降解与生物安全性
金属支架经过修饰后在体内是否会降解、降解率如何以及生物安全性都是不可忽视的问题。传统不可降解金属材料主要为钴铬合金、钛合金、钽金属等,其优点是物理化学性能稳定,但是无法做到完全生物整合;可降解金属支架可以在体内进行生物整合,降解过程中释放的金属离子还具有诱导成骨的作用,但目前还处在实验研究阶段,主要包括镁基(Mg)可降解金属、锌基(Zn)可降解金属、铁基(Fe)可降解金属[41]。镁合金作为一种新型可降解金属材料,是目前的研究热点。值得一提的是,纯镁支架在降解过程中会产生较多的气体,不易被组织全部吸收,因此产生更少量气体的多孔镁合金支架,是目前应用最广泛的可降解金属支架。多孔镁合金支架植入兔的股骨缺损处后36周后显示出缓慢的降解和良好的骨结合,孔隙中观察到良好的血管化与适度的细胞反应[42]。类似研究表明,多孔镁支架植入兔子体内后0 ~12周,镁支架早期降解为镁离子,随后逐渐被钙、磷等无机成分所取代,经过生物安全评估,发现镁支架没有引起血清镁离子浓度的增加,兔的免疫反应、肝脏和肾脏功能参数都处于正常水平[43]。研究表明,将植入锌合金内固定板钉于新西兰兔皮下,6 个月后白细胞计数、红细胞计数、谷丙转氨酶、谷草转氨酶、总蛋白、白蛋白、尿素氮、肌酐、血锌、血镁、血钙、血铜指标与术前比较,差异无统计学意义;肝脏、肾脏、脾脏的锌离子含量也未发现异常[44]。
5 总结与展望
虽然3D打印金属支架的基础研究是近期的研究热点,创新成果也层出不穷,但是与成果转化与临床应用还有一定的距离。目前3D打印金属支架的临床适用范围:①骨肿瘤切除术后重建,包括骨盆、骶骨、脊柱、肩关节周围、四肢长骨骨干及踝关节、肘关节、腕关节周围的骨肿瘤切除重建;其中在骶骨、脊柱、骨盆的肿瘤切除术后的骨缺损重建中应用相对成熟。②个性化定制关节假体初次置换与假体翻修,如打印制造个体化的髋臼假体、髋臼垫块、髋臼缺损加强环及感染后的临时间隔器。③各种原因导致的创伤及感染性骨缺损重建。
通过基础实验的验证与临床探索,可见将金属3D打印支架功能化具有如下优势:①匹配度高,同时具备抗菌功能,降低感染风险;②治疗骨缺损时能更快诱导成骨,避免取自体骨造成二次损伤;③支架本身具有药物缓释功能,可抗骨质疏松、预防骨肿瘤切除术后复发和治疗慢性骨髓炎,提高治疗效率;④支架植入体内后,前期可提供稳定支撑,中后期在体内缓慢吸收,大大缩短治疗周期,降低治疗成本。同时也存在如下局限性:①金属弹性模量低,容易发生应力屏蔽,造成假体周围骨折或骨质吸收;②材料多孔结构容易使细菌定植,造成疾病传播和感染[45];③3D打印机目前的分辨率低,与骨组织纳米级的超微结构差距甚远,仍需提高打印设备的分辨率来匹配人体骨组织;④人体骨组织由蛋白质、钙等多种物质组成,其力学性能适应人体需求,而传统3D打印多孔支架通常局限于单一材料,支架性能与骨修复需求不吻合;⑤特定形态的骨缺损定制3D打印支架的制作周期长、时效性低下。目前,金属3D打印支架的拓扑结构如何优化,支架表面如何进一步改性,其生物安全性问题,以及如何提高体内降解效率都是亟待解决的问题。
综上所述,目前金属基3D打印支架功能化已经在基础研究中获得一定成果(见表1),但尚未广泛应用于临床;将金属支架与生物材料或生物活性物质相交联,发挥各个材料与成分的优势,开发出具有多种功能的生物活性支架;并且在承重条件下达到支架多功能化、生物相容性、成骨诱导性和生物力学完整性之间的平衡,是未来的研究方向。
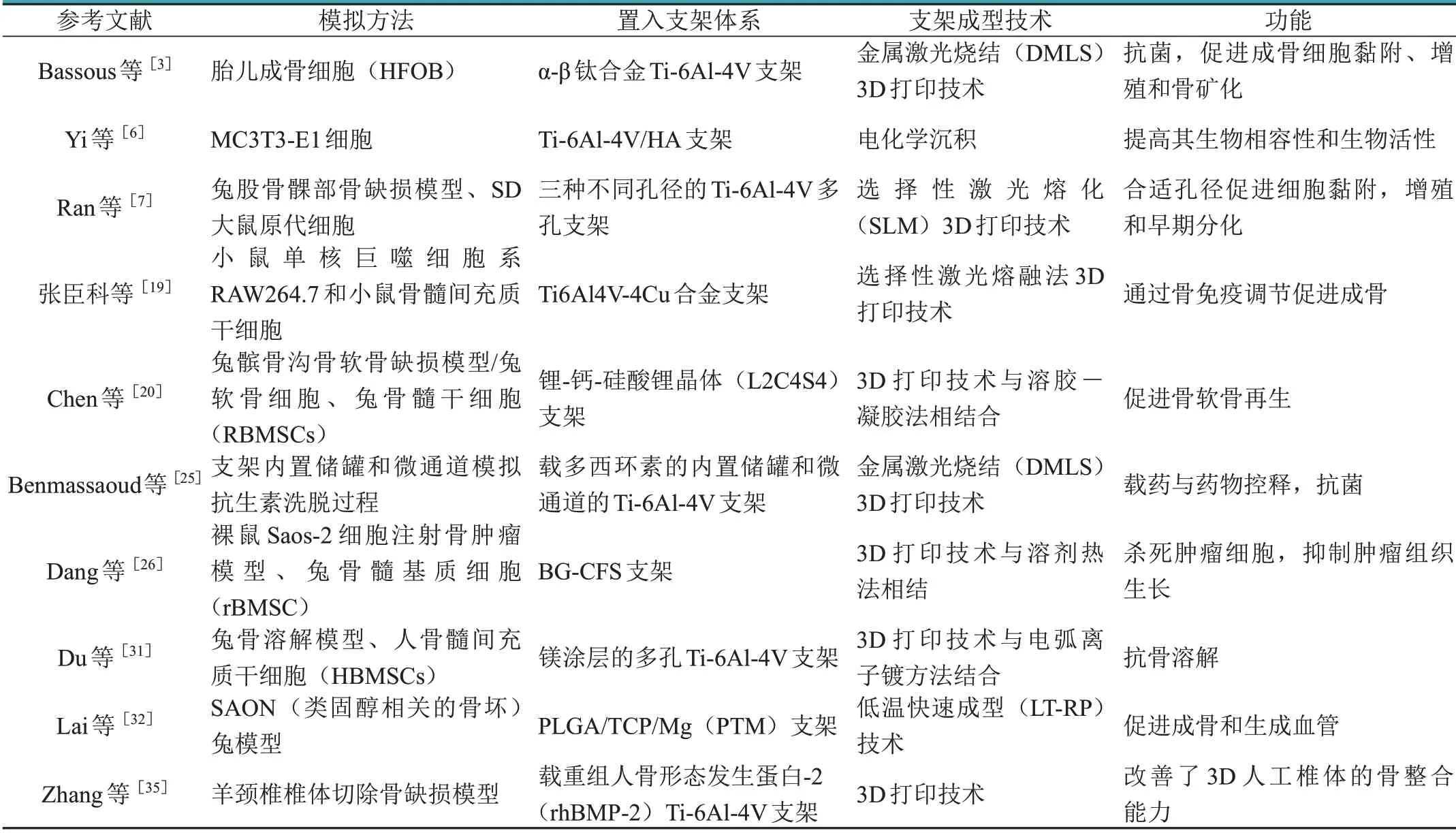
表1 金属基3D打印植入体系的基础研究
