前列腺结节T2信号强度比联合PI-RADS评分在移行带前列腺癌中的诊断价值
2022-12-20马婷
马 婷
(遂宁市中心医院放射影像科 四川 遂宁 629000)
前列腺癌(prostatic carcinoma,PCa)是老年男性常见的生殖泌尿系统恶性肿瘤;随着年龄增加,其发病率可达90.0%,严重危害老年男性的生活健康[1]。当前列腺癌灶未突破前列腺包膜时,患者5年生存率可达100.0%;而当前列腺晚期转移后,5年生存率只有不到30.0%,且患者生活质量急剧下降。因此,前列腺癌的早期诊断及干预是治疗的关键点。近年来,随着医学影像技术的快速发展,高场强磁共振(magnetic resonance imaging,MRI)的新技术层出不穷,后期技术平台不断优化,为前列腺半定量及多模态研究提供了广阔的平台。目前,临床上常应用PI-RADS评分系统对其进行诊断及鉴别诊断[2]。在前列腺外周带中,由于其外周带背景T2高信号,恶性结节多呈T2低信号且弥散受限,其诊断相对容易。但在前列腺移行带中,由于前列腺移行带增生结节性质的不同,且局部前列腺炎症及纤维增生相互混杂。在PI-RADS评分,关键的T2WI序列上,结节T2信号表现差异较大,对其定性诊断仍然存在一定的困难。近年来,许多研究均就上述问题进行了一系列的探索及总结,但是在移行带恶性结节的判定上仍然存在一定的盲区[3]。因此,有必要进一步探索、改良PI-RADS评分系统,以期进一步提高前列腺癌的早期诊断效率。
1 资料与方法
1.1 一般资料
选取2020年1月—2022年6月于遂宁市中心医院经病理证实的前列腺移行带恶性结节患者40例(A组)及前列腺移行带增生结节组30例(B组)。A组平均年龄(60.5±5.8)岁,血清前列腺特异性抗原(prostatespecific antigen,PSA)(7.7±2.3)ng/mL;B组平均年龄(62.6±11.9)岁,血清PSA(6.2±1.9)ng/mL。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
纳入标准:①患者前列腺MRI检查后,于住院期间行前列腺病理检查(包括穿刺病理及手术病理),证实为前列腺癌;②癌灶位于移行带,且后期穿刺病理或手术病理证实癌灶未突破前列腺包膜;③患者前列腺癌首次诊断,无前列腺、膀胱及尿道相关手术史;④患者知情并签署知情同意书。排除标准:①癌灶跨区分布;② 患者存在放疗及化疗病史;③患者处于急、慢性前列腺炎治疗期间;④ 存在臀肌萎缩患者;⑤临床资料不完整者。
1.2 方法
MRI检查:所有患者均于前列腺穿刺或手术前行MRI检查,MRI检查前保持膀胱适度充盈。检查设备GE 3.0T核磁共振检查仪,腹部专用通道,18通道;MRI主要序列参数分别为:FSE-T2WI序列(TR 3 800 ms,TE 100 ms,ETL 25,层厚4 mm,层距0.5 mm,矩阵 256×256,FOV=24 cm×24 cm);DWI序列(b值分别为0 s/mm2、1 000 s/mm2,TR 4 000 ms,TE 150 ms,层厚3 mm,无间距扫描,矩阵256×192,FOV=24 cm×24 cm)。
前列腺结节穿刺方法:所有患者于穿刺前3天进行肠道准备,穿刺前常规清洁肠道,术前复习穿刺点MRI图像及经直肠超声图像,定位后,应用18G自动穿刺活检枪穿刺,每个穿刺点3针左右,共穿刺8~12针。
前列腺移行带结节的判读由2名晋升主治医师3年以上男性泌尿生殖系统诊断医师单独进行,测量时采取双盲法(患者、影像诊断医师对前列腺移行带性质均不知情);若对结节性质判读意见不一致,协商后决定。前列腺结节T2信号强度比(SIRT2)的测量方法:前列腺移行带结节T2信号强度/同层面臀肌T2信号强度。前列腺结节T2信号强度比(SIRT2)测量时应避开明显坏死、出血及囊变灶,选取待观察结节相对信号均匀区域。
1.3 观察指标
以穿刺病理或手术病理为金标准,分析前列腺移行带结节SIRT2值及前列腺结节T2信号强度比(SIRT2)联合PI-RADS评分诊断前列腺恶性结节的正确率。前列腺移行带结节PI-RADS评分方法和标准[4],见表1。PIRADS评分≥4分判断为恶性;SIRT2值≤1.45为恶性结节。SIRT2联合PI-RADS评分主要应用于PI-RADS评分3、4分的评价,在PI-RADS评价基础上进行SIRT2评分,若SIRT2值≤1.45,则PI-RADS评分增加1分;余PIRADS得分不做联合评价。
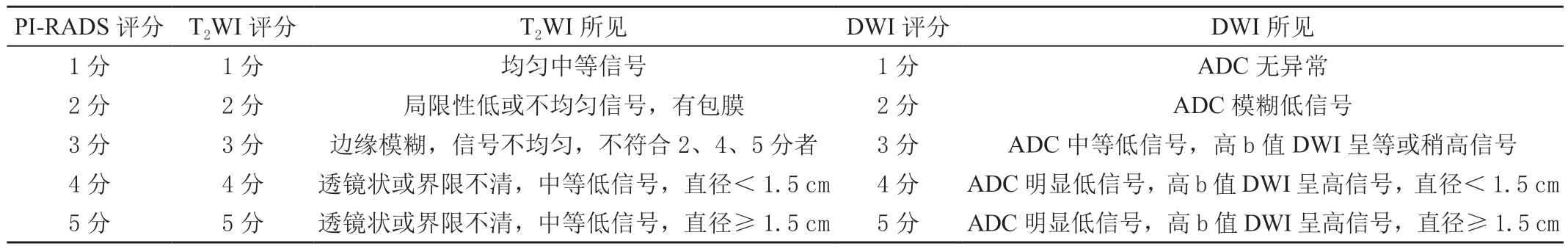
表1 前列腺移行带结节PI-RADS评分方法和标准
1.4 统计学方法
采用SPSS 25.0统计软件分析数据,符合正态分布的计量资料以均数±标准差()表示,采用t检验;计数资料以频数(n)、百分率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。应用受试者操作特征(receiver operating characteristic,ROC)曲线计算诊断效能;曲线下面积(area under curve,AUC)在0.5~0.7之间为诊断价值较低,0.7~0.9表示诊断价值中等,>0.9表示诊断价值较高。
2 结果
2.1 不同组别中前列腺结节T2信号强度比(SIRT2)对比结果
前列腺移行带恶性结节组(A组)SIRT2为(1.337±0.250),低于增生结节组(B组),差异有统计学意义(P<0.05),见表2。
表2 前列腺移行带恶性结节与增生结节组T2信号强度比对比()

表2 前列腺移行带恶性结节与增生结节组T2信号强度比对比()
组别 例数 SIRT2 A组 40 1.337±0.250 B组 30 1.638±0.336 t 0.206 P 0.0319
2.2 SIRT2联合PI-RADS评分诊断前列腺移行带恶性结节正确率比较
前列腺结节T2信号强度比(SIRT2)联合PI-RADS评分诊断前列腺移行带恶性结节正确率为81.4%(57/70),略高于常规PI-RADS评分的77.1%(54/70),但两者诊断正确率差异无统计学意义(χ2=0.425,P>0.05),见表3。
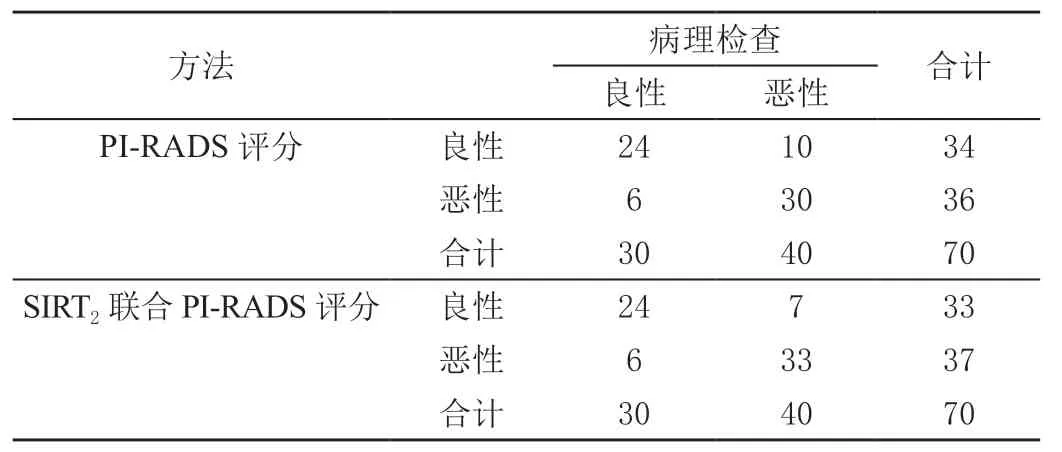
表3 两种方法诊断前列腺移行带恶性结节结果 单位:例
2.3 SIRT2联合PI-RADS评分及常规PI-RADS评分在诊断移行带恶性结节中的效能比较
前列腺结节T2信号强度比(SIRT2)联合PI-RADS评分、常规PI-RADS评分在诊断移行带恶性结节的ROC曲线下面积分别为:0.841,0.734,其中前列腺结节T2信号强度比(SIRT2)联合PI-RADS评分的诊断灵敏度及特异度分别为82.5%、80.0%,见表4及图1。

图1 SIRT2联合PI-RADS评分及常规PI-RADS评分在诊断移行带恶性结节中的效能

表4 SIRT2联合PI-RADS评分及常规PI-RADS评分在诊断移行带恶性结节中的效能
3 讨论
前列腺移行带增生结节与恶变结节对比仍然是临床关注的难点及焦点。长期以来,临床及影像诊断常用PIRADS评分作为前列腺癌的主要诊断方法。在前列腺癌外周带,前列腺结节在T2WI序列上形态、大小常常作为其分级的主要标准。实际应用中,由于该标准的临床应用需要影像判读医师一定的阅片经验,才能较为准确的判断[4]。另外,由于前列腺外周带结节的复杂性(增生结节性质的不同、前列腺炎症及纤维增生瘢痕),常规PI-RADS评分对其诊断仍然存在一定的盲区[5]。因此,有必要进一步探讨新技术、新方法,以进一步提高前列腺癌移行带恶变结节的诊断效率。
前列腺结节T2信号强度比(SIRT2)主要受前列腺结节内水分子含量多少影响。一般来说,前列腺移行带腺体增生结节及局部慢性炎症常常含有较为丰富的水分子;因此,其SIRT2值相对较高[6]。而前列腺移行带恶变结节,由于肿瘤细胞单细胞克隆,细胞排列密实,肿瘤细胞内细胞核增大,浆比相对明显增高。因此水分子含量相对减少,其SIRT2值将降低[7]。本实验结果也证实了上述观点。通过将前列腺移行带结节SIRT2进行定量,可以在一定程度上鉴别腺体增生结节及恶变结节。
本组前列腺结节T2信号强度比(SIRT2)联合PIRADS评分、常规PI-RADS评分在诊断移行带恶性结节的ROC曲线下面积分别为:0.871,0.730。常规PIRADS评分及新方法诊断正确率均略低于文献报道[8-9]。其可能的原因是:①所有病例均为早期前列腺癌患者,癌灶均未突破前列腺包膜。本组前列腺癌灶相对较小,癌灶直径<1.0 cm 38例,约占总数的54.3%(38/70)。病灶较小,其诊断难度相对增加。②由于本组病例直径较小,其影像学特点也较难以确定。常规PI-RADS移行带T2WI值评分,癌结节的评分为3分者约44例,4分者21例,两者约占总数的92.9%(65/70)。③部分前列腺增生结节为纤维增生结节,其T2信号强度比(SIRT2)相对较低,影响后续结果判读。
本研究不足之处:①理论上,前列腺移行带纤维增生结节及局限性纤维疤痕,由于组织内拥有较少的水分子,其SIRT2值应该是降低的[10]。本组病例穿刺病理及手术病理并没有将上述病理结节进一步分型、分析。但是本研究是立足于常规PI-RADS评分系统进行的,在现有基础上进行的补充相应指标以进一步鉴别诊断。研究结果提示,SIRT2联合PI-RADS评分能进一步提高前列腺移行带恶变结节的诊断率。②前列腺结节T2信号强度比(SIRT2)值还受臀肌T2值的影响。一般来说,正常人肌肉信号强度相对恒定。但我们注意到,老年人,特别是缺乏体育锻炼的老年人,其肌肉存在不同程度的萎缩。因此,寻找更加稳定,更具有可比性的参照物,是下一步研究的重点。
综上所述,前列腺结节T2信号强度比(SIRT2)联合PI-RADS评分相对于常规PI-RADS评分能进一步鉴别诊断移行带恶变结节,具有一定临床应用价值。临床实际工作中,仍然需要结合临床实验室检查、DWI信号特点及动态增强扫描曲线综合考虑,避免漏诊及误诊。
