化学发光免疫法对肿瘤生物标志物的检验效果分析
2022-12-12张杏羡
张杏羡
(天津华兴医院检验科,天津 300270)
恶性肿瘤(malignant cancer)是当前世界范围内重点关注的公共卫生问题,其早期阶段可通过手术达到一定治愈效果,是病情转归的关键节点。但肿瘤起病较为隐匿,早期诊断相对困难,易导致病情延误,进而影响患者的预后生存。肿瘤标志物(tumor marker,TM)作为肿瘤发生及增殖过程中的常见产物,在正常细胞中含量极低,可用于肿瘤疾病的早期筛查,对恶性肿瘤的检出及鉴别具有重要意义[1]。目前,甲胎蛋白(α-fetoprotein,AFP)、癌胚抗原(carcinoembryonic antigen,CEA)、糖链抗原-199(carbohydrateantigen 199,CA-199)、糖链抗原-153(carbohydrateantigen 153,CA-153)、糖链抗原-125(carbohydrateantigen 125,CA-125)等均为临床常用的肿瘤标志物[2],其检测方式也较为丰富,现以化学发光免疫法(chemiluminescent immunoassay,CLIA)最为常用,该方式不仅快速、灵敏、特异,且无放射性危害,普及面及接受度均较为理想[3,4]。在此,本研究结合2021 年1 月-12 月我院经病理学检验确诊的50 例恶性肿瘤患者与50 例健康者,观察化学发光免疫法对肿瘤生物标志物的检验效果,现报道如下。
1 资料与方法
1.1 一般资料 选择天津华兴医院2021 年1 月-12 月经病理学检验确诊的50 例恶性肿瘤患者为观察组,其中男29 例,女21 例;年龄34~65 岁,平均年龄(45.38±4.67)岁,肠癌15 例、肝癌15 例、乳腺癌11 例、卵巢癌9 例。纳入标准:①组织病理学检查明确,资料完整;②原发性恶性肿瘤者;③意识清醒,配合度好。排除标准:①合并重症心脑血管疾病者;②病历资料不全者;③采样配合度差者。另收集50例同期体检健康者为对照组,男26 例,女24 例;年龄34~67 岁,平均年龄(45.42±4.78)岁。纳入标准:①体检资料完整,无恶性疾病;②意识清醒,配合度好。排除标准:①体检结果不明确者;②配合度差者。两组性别、年龄比较,差异无统计学意义(P>0.05),有可比性。本研究所有受检者均知情且自愿参与,并签署知情同意书。
1.2 方法
1.2.1 血清肿瘤标志物检测 于清晨采集受检者空腹静脉血5 ml,离心操作(3000 r/min,15 min)后,取上层血清备用。采用全自动化学发光免疫分析仪(罗氏cobas 8000)及原装配套试剂,检测血清样本中的肿瘤生物标志物含量,包括CEA、AFP、CA-199、CA-125 与CA-153,所有操作均严格遵照说明书进行。
1.2.2 结果判断 检验值参考:CEA<5 ng/ml,AFP:<20 ng/ml,CA-199:<27 U/ml,CA-125:<35 U/ml,CA-153:<25 U/ml,超出该范围判定为阳性。
1.3 观察指标 ①比较两组肿瘤生物标志物的检测水平;②比较两组肿瘤生物标志物的阳性检出率;③分析肿瘤生物标志物在不同肿瘤中的阳性检出率,包括肠癌、肝癌、乳腺癌、卵巢癌。
1.4 统计学方法 采用SPSS 21.0 统计学软件进行数据处理,计量资料以()表示,组间比较行t检验,计数资料以[n(%)]表示,组间比较行χ2检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 两组肿瘤生物标志物水平比较 观察组CEA、AFP、CA-199、CA-125、CA-153 水平均超过正常值范围,且高于对照组,差异有统计学意义(P<0.05),对照组肿瘤生物标志物水平则处于正常值范围,见表1。
表1 两组肿瘤生物标志物水平比较()

表1 两组肿瘤生物标志物水平比较()
2.2 两组肿瘤生物标志物阳性检出率比较 观察组CEA、AFP、CA-199、CA-125、CA-153 的阳性检出率高于对照组,差异有统计学意义(P<0.05),见表2。
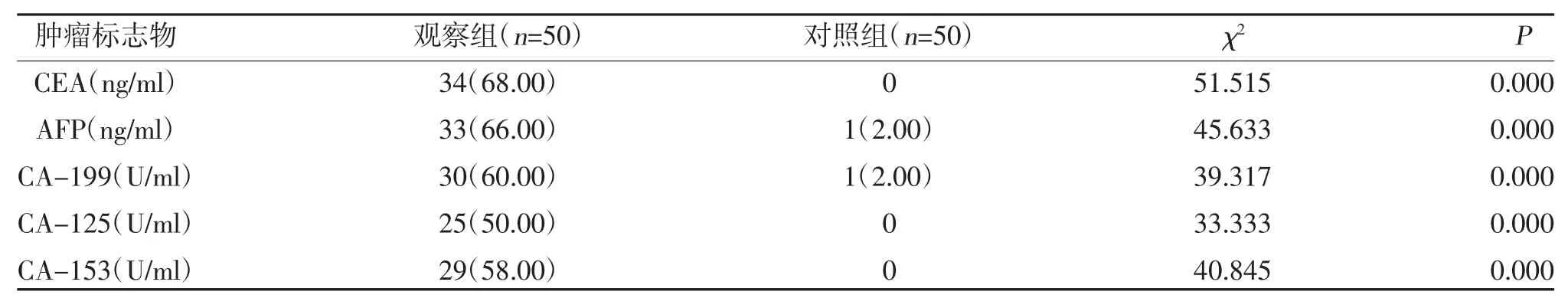
表2 两组肿瘤生物标志物阳性检出率比较[n(%)]
2.3 肿瘤生物标志物在不同肿瘤疾病中的阳性检出率分析 CEA、AFP、CA-199、CA-125、CA-153 在不同恶性肿瘤疾病中均有检出,其中CEA 在肠癌中的阳性检出率最高,AFP 在肝癌中的阳性检出率最高,CA-153 在乳腺癌中的阳性检出率最高,CA-125 在卵巢癌中的阳性检出率最高,其阳性检出率均为100.00%,见表3。
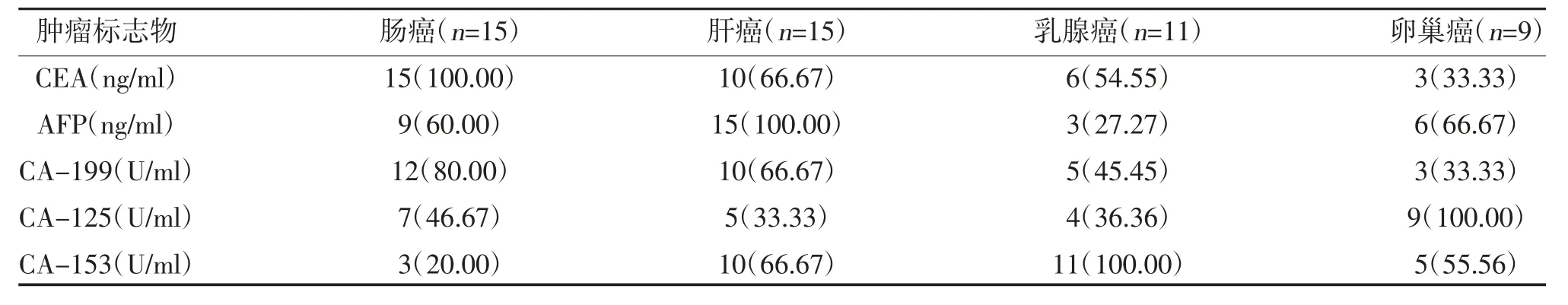
表3 肿瘤生物标志物在不同肿瘤疾病中的阳性检出率[n(%)]
3 讨论
肿瘤生物标志物是机体在恶性肿瘤发生、发展过程中产生的特异性物质,其标本易于获取,且检测操作便捷,有利于病情的动态监测,在肿瘤早期诊断中具有重要价值[5]。CEA、AFP、CA-199、CA-125、CA-153 等均为常规肿瘤标志物[6],其中CEA 属于非器官特异性肿瘤相关抗原,是在癌、胚胎组织内存在的高分子糖蛋白,在胃肠道恶性肿瘤、乳腺癌及肺癌等疾病中均有不同程度的升高表现[7,8];AFP 是在胚胎时期由肝细胞与卵黄囊合成的糖蛋白,多用于原发性肝癌、肝硬化等疾病的早期筛查与监测中;CA-199 是一种高分子唾液Lewisx-a 物质,其升高多见于胃癌、胆囊癌、胰腺癌、等消化道肿瘤中,可作为消化道癌症的辅助诊断指标[9];CA-125 与CA-153则分别是卵巢癌与乳腺癌的特异性标志物[10],其升高可用于此类肿瘤的诊断与筛查。现阶段,化学发光免疫法是检测肿瘤生物标志物的常用手段之一,该方式可利用化学发光物质经催化氧化形成的激发态中间体为检测基础,当中间体重新归于稳定基态水平时,可发射光子,通过发光信号测量仪可测定其产生的光量子数量,由此获取目标物质的真实含量[11,12]。化学发光免疫法的敏感度及特异度均较高,具有快速、精确、重复性高等应用优势,且不存在放射性及同位素污染等问题,且试剂价格成本低,有利于在基层医疗机构的普及[13]。
本研究结果显示,观察组CEA、AFP、CA-199、CA-125、CA-153 水平均超过正常值范围,且高于对照组(P<0.05),这与成晨[14]研究结果一致,提示化学发光免疫法对肿瘤患者及健康者之间的肿瘤标志物水平均具有积极的检测价值,其鉴别诊断作用显著。同时,观察组CEA、AFP、CA-199、CA-125、CA-153的阳性检出率高于对照组(P<0.05),可见化学发光免疫法对以上肿瘤标志物具有较高的阳性检出作用,可用于肿瘤疾病的早期筛查,与既往研究相符[15]。此外,研究认为[16,17],肿瘤细胞的生物学特性具有一定的多态性与复杂性,同一种肿瘤可包含一种或多种标志物,而不同肿瘤或同肿瘤不同组织间亦可存在不同的肿瘤标志物。而本次结果中,CEA、AFP、CA-199、CA-125、CA-153 在不同恶性肿瘤疾病中均有检出,这与上述理论相符。其中,CEA 在肠癌中的阳性检出率最高,AFP 在肝癌中的阳性检出率最高,CA-153 在乳腺癌中的阳性检出率最高,CA-125在卵巢癌中的阳性检出率最高,其阳性检出率均为100.00%,与范艳佳等[18]研究相吻合,提示化学发光免疫法对以上肿瘤疾病的特异性标志物具有显著的检出价值。
综上所述,化学发光免疫法对肿瘤生物标志物具有较高的检出作用,其鉴别检验效果理想,可为临床肿瘤疾病的筛查、诊断、病情监测提供可靠的参考依据。
