双标线性校正法用于川黄芩的多成分定性分析
2022-12-09周洪旭孟大利侯立新
张 毅,周洪旭,孟大利,侯立新*
(1. 重庆市食品药品检验检测研究院,重庆 400000;2. 沈阳药科大学 中药学院,辽宁 沈阳 110016)
中药的质量控制对中药的安全性和有效性具有重要意义。标准物质是中药定性和定量分析的重要依据。随着中药质量控制的发展,对标准物质的需求越来越大,而中药对照品由于其提取分离困难、成本高昂、不稳定等诸多因素,极大地影响了中药质量标准的建立和发展[1]。因此,建立中药标准物质替代测定法是解决以上问题的有效途径之一。目前已开发的标准物质替代测定法包括校正因子法[2]、一测多评法(quantitative analysis of multicomponents by single marker,QAMS)[3-4]、替代对照品法[5]、双标线性校正法(linear calibration using two reference substances,LCTRS)[6-10]等。双标线性校正法是用两个对照品进行色谱峰定位,显著提高了定位的准确度和色谱柱的适用性。
川黄芩为唇形科植物滇黄芩Scutellaria amoena C. H. Wright、连翘叶黄芩Scutellaria hypericifolia Levl.或韧黄芩展毛变种Scutellaria tenax W. W.Smith Var. patentipilosa (Hand. Mazz.) C. Y. Wu的干燥根。性味苦寒,具有清热燥湿、泻火解毒、止血、安胎等功效[11]。现代植物化学研究发现,川黄芩中主要成分为黄酮及黄酮苷类化合物、二氢黄酮及二氢黄酮醇类化合物、木质素、酚苷、醇苷类化合物等[12-13]。已报道黄酮类成分主要包括黄芩苷、汉黄芩苷、千层纸素A、汉黄芩素、黄芩素等。黄芩苷为川黄芩主要化学成分,现代药理学研究发现黄芩苷具有抗氧化及清除自由基[14]、抗病毒[15-16]、抗肿瘤[17]、对中枢神经系统的保护[18]、保肝[19]、调节脂代谢[20]等药理作用。
川黄芩现有质量标准(2015年版四川省中药饮片炮制规范)中还未有定性鉴别内容,因此本研究采用双标线性校正法对川黄芩中5个成分进行定性鉴别,填补了川黄芩质量标准研究的空白。与相对保留时间法比较,双标线性校正法的预测精度更高,适用的色谱柱范围更广,明显优于相对保留时间法。双标线性校正法的建立可为后续川黄芩的质量标准研究提供参考和依据。
1 仪器与材料
1.1 仪器
Agilent 1260 Infinity II高效液相色谱仪(安捷伦科技有限公司);Agilent 1260 Infinity高效液相色谱仪(安捷伦科技有限公司);Waters e2695-2998 PAD高效液相色谱仪(沃特世科技有限公司),3台仪器依次称为LC1~LC3。KQ-500DB型数控超声波清洗器(昆山市超声仪器有限公司);DP-02无油真空泵(天津市富城达科技有限公司);ME204T/02万分之一天平(梅特勒-托利多公司);Mill-Q Synergy型超纯水仪器(默克密理博公司);HWS-26型恒温水浴锅(上海精密仪器有限公司)。色谱柱(250 mm×4.6 mm,5 μm)信息见表1。

表1 色谱柱信息
1.2 药品与试剂
黄芩苷对照品(批号:110715-201720,含量:93.5 %,中国食品药品检定研究院);黄芩素对照品(批号:111595-200905,含量:98.5 %,中国食品药品检定研究院);汉黄芩苷(批号:111595-200905,含量:98.5 %,中国食品药品检定研究院);千层纸素A-7-O-β-D-葡萄糖醛酸苷(批号:F306-PS011092,含量:98.0 %,成都普思生物科技股份有限公司);乙腈(色谱纯,安徽时联特种溶剂股份有限公司);甲醇(色谱纯,安徽时联特种溶剂股份有限公司);去离子水为经Millipore超纯水制备系统自制;三氟乙酸(分析纯,Sigma-Aldrich);甲醇(分析纯,重庆川东化工集团有限公司)。3批川黄芩药材采集于四川、云南等地,经重庆市食品药品检验检测研究院中药室张毅副研究员鉴定为唇形科植物滇黄芩Scutellaria amoena C.H. Wright的干燥根。取干燥根适量,烘干至恒重,粉碎过筛,备用。
1.3 软件
数字化标准物质大数据平台(DRS Origin软件)V1.0(中国食品药品检定研究院)。
2 方法
2.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂;流动相:以甲醇为流动相A,以0.1 %三氟乙酸溶液为流动相B,进行梯度洗脱(0~20 min,37 %A→39 %A;20~35 min,39 %A→45 %A;35~42 min,45 %A;42~50 min,45 %A→58 %A;50~58 min,58 %A;58~68 min,58 %A→80 %A;68~68.1 min,80 %A→90 %A;68.1~70 min,90 %A);检测波长:280 nm;流速:1.0 ml/min;进样量:10 μl;柱温:30 ℃。
2.2 溶液的制备
2.2.1 混合对照品溶液的制备 取黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素对照品适量,精密称定,置于100 ml量瓶中,加甲醇制成黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素含量分别为106.2,117.5,25.2,49.7 μg/ml的混合对照品溶液。
2.2.2 供试品溶液的制备 取本品,干燥粉碎,过4号筛,称取粉末约0.3 g,精密称定,加70 %乙醇40 ml,加热回流3 h,放冷,滤过,滤液置100 ml量瓶中,用少量70 %乙醇分次洗涤容器和残渣,洗液滤入同一量瓶中,加70 %乙醇至刻度,摇匀。精密量取5 ml,置10 ml量瓶中,加甲醇至刻度摇匀,过滤即得。
2.3 方法学考察
2.3.1 精密度试验 精密吸取2.2.1项下混合对照品溶液10 μl,连续进样6针,对4个对照品色谱峰的保留时间和峰面积进行统计,结果表明各对照品的保留时间和峰面积积分值的RSD均小于2.0 %,表明仪器精密度良好。
2.3.2 重复性试验 取样品,按2.2.2项下方法平行制备6份供试品溶液,精密吸取10 μl,注入液相色谱仪,测定。对4个成分色谱峰的保留时间和相对含量进行统计,试验结果表明各成分的保留时间和含量的RSD均小于2.0 %,表明重复性良好。
2.3.3 稳定性试验 取样品,按2.2.2项下方法制备供试品溶液。精密吸取供试品溶液10 μl,注入液相色谱仪,测定。对4个成分色谱峰的保留时间和峰面积进行统计,共考察24 h,以观察供试品溶液在检测过程中待测成分的稳定性。结果表明各成分的保留时间和含量的RSD均小于2.0 %,表明待测成分稳定性良好。
2.4 色谱柱耐用性试验
分别在20根色谱柱上进行耐用性考察,其中在Col 10上出现缺峰现象(缺少黄芩苷峰前的未知峰),其余19根色谱柱上各成分分离度良好,异常结果见图1。
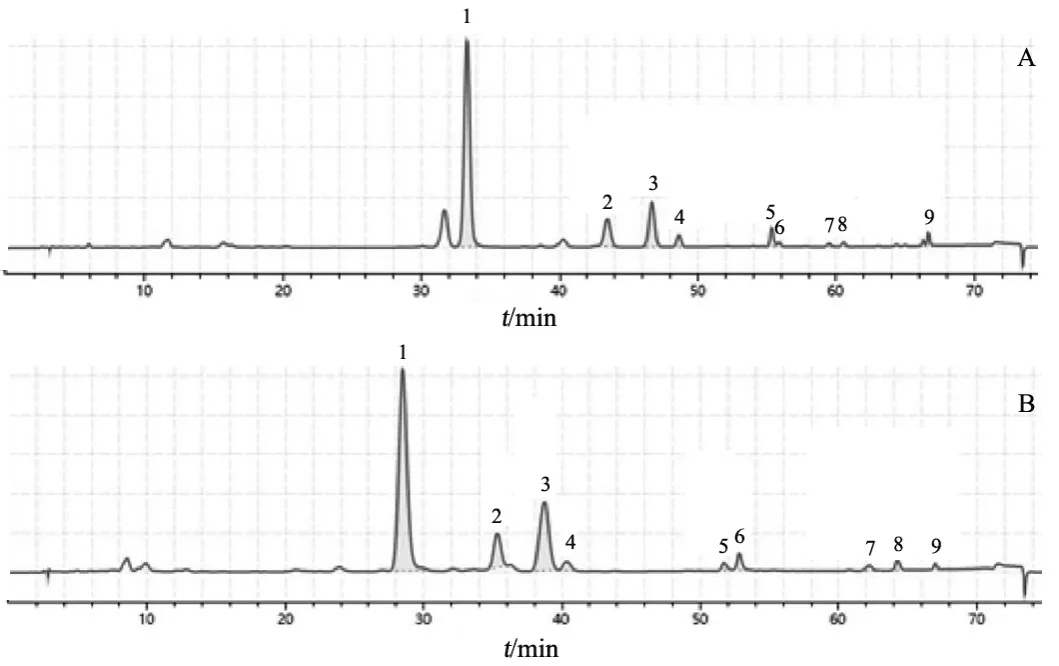
图1 正常色谱图与异常色谱图
2.5 双标线性校正法定性研究
将采集的色谱数据导入DRS Origin软件,通过关联对照品,设定双标化合物,进行双标线性校正法分析,得到保留时间回归偏差、保留时间预测正确率和色谱柱符合率。同时,与相对保留时间法进行优劣比较。
3 结果与讨论
在不同的C18色谱柱上,各个物质的保留时间具有线性关系[8-9]。通过采用对照品的保留时间进行色谱峰定位得到样品实际保留时间,以19根色谱柱得到的实际保留时间的算数平均值作为预测标准保留时间(standard retention time, SRT)。以5种成分的SRT为横坐标(X),分别为黄芩苷(32.08 min)、峰2(42.88 min)、千层纸素A-7-O-β-D-葡萄糖醛酸苷(45.81 min)、汉黄芩苷(47.54 min)、黄芩素(55.09 min);以实际保留时间为纵坐标,得到在各色谱柱上SRT与实际保留时间的拟合结果,各色谱柱的线性方程和相关系数见表2。由表2可见,上述5个成分在19根色谱柱上,SRT与实际保留时间线性关系良好(r>0.99)。

表2 不同色谱柱保留时间的线性方程及相关系数
3.1 双标选择与优化
以DRS Origin软件为平台,得到保留时间的双标线性校正结果,通过软件内部的数据分析筛选出了10种双标选择方案,其中峰1和峰5组合预测正确率和色谱柱符合率均为100 %。按双标化合物选择尽量分布在保留时间区域两端的原则[9-10],选择峰1(黄芩苷)和峰5(黄芩素)为双标化合物,双标线性校正法示意图见图2。
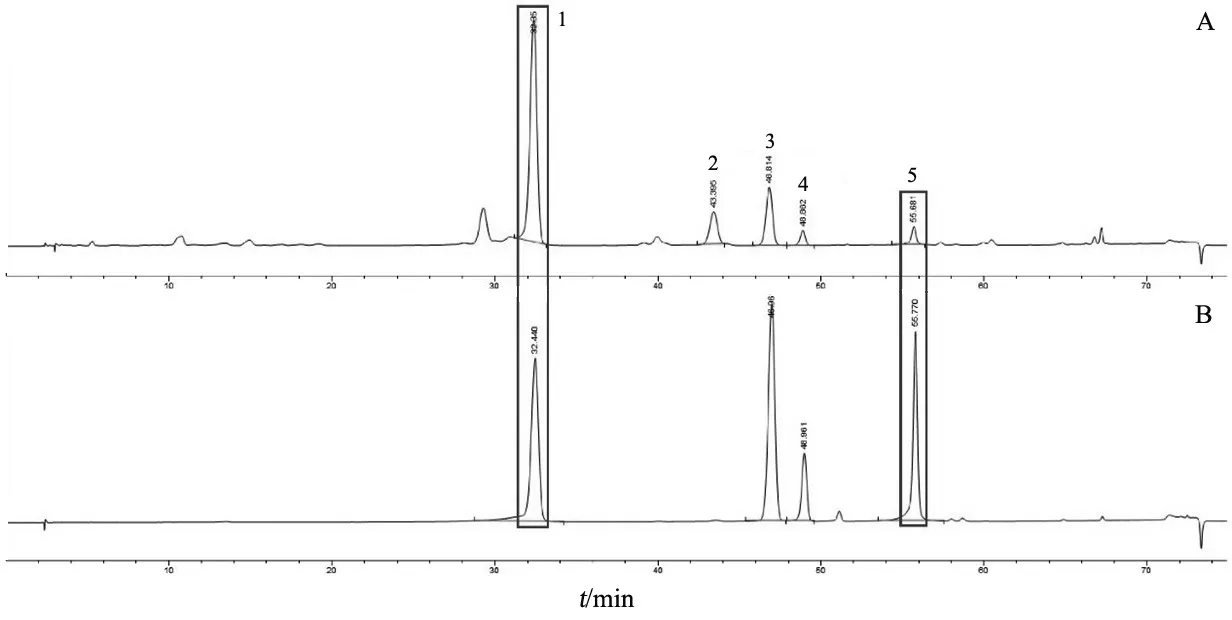
图2 双标线性校正法示意图
以双标化合物(黄芩苷和黄芩素)的SRT为横坐标,实际保留时间(以Col 7为例,黄芩苷27.91 min,黄芩素52.91 min)为纵坐标,得到线性拟合方程:Y=1.1144X-12.1613,然后将其余3个成分的SRT值代入方程,得到峰2、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷的保留时间偏差的绝对值依次为0.202,0.422,0.296 min,满足定性条件下SRT与实测保留时间的误差应不超过1 min的要求,说明该双标化合物的选择在Col 7上预测效果良好。
3.2 双标线性校正法与相对保留时间法的对比
对双标线性校正法与相对保留时间法在川黄芩液相色谱中定性的优劣进行比较。双标线性校正法以黄芩苷和黄芩素为双标化合物,相对保留时间法以千层纸素A-7-O-β-D-葡萄糖醛酸苷为参照物,两种方法对保留时间的预测结果见表3。由表3可见,双标线性校正法的保留时间预测值的绝对偏差波动范围较小,且绝对偏差较低,明显优于相对保留时间法。

表3 双标线性校正法与相对保留时间法保留时间绝对偏差比较
3.3 样品分析
按2.2.2项下方法,取3批川黄芩药材制备供试品溶液,用2根新的色谱柱(Col 21,Col22)进行检测,将数据格式文件导入DRS Origin软件中,加载已建立的方法体系,提取双标保留时间,并利用软件功能对目标物进行保留时间预测。同时也用相对保留时间法处理数据。对双标线性校正法预测结果和相对保留时间法结果进行比较分析,结果3批样品的双标线性校正法检测结果均满足要求(ΔtR<1 min),说明该体系可进行实际应用。见表4。
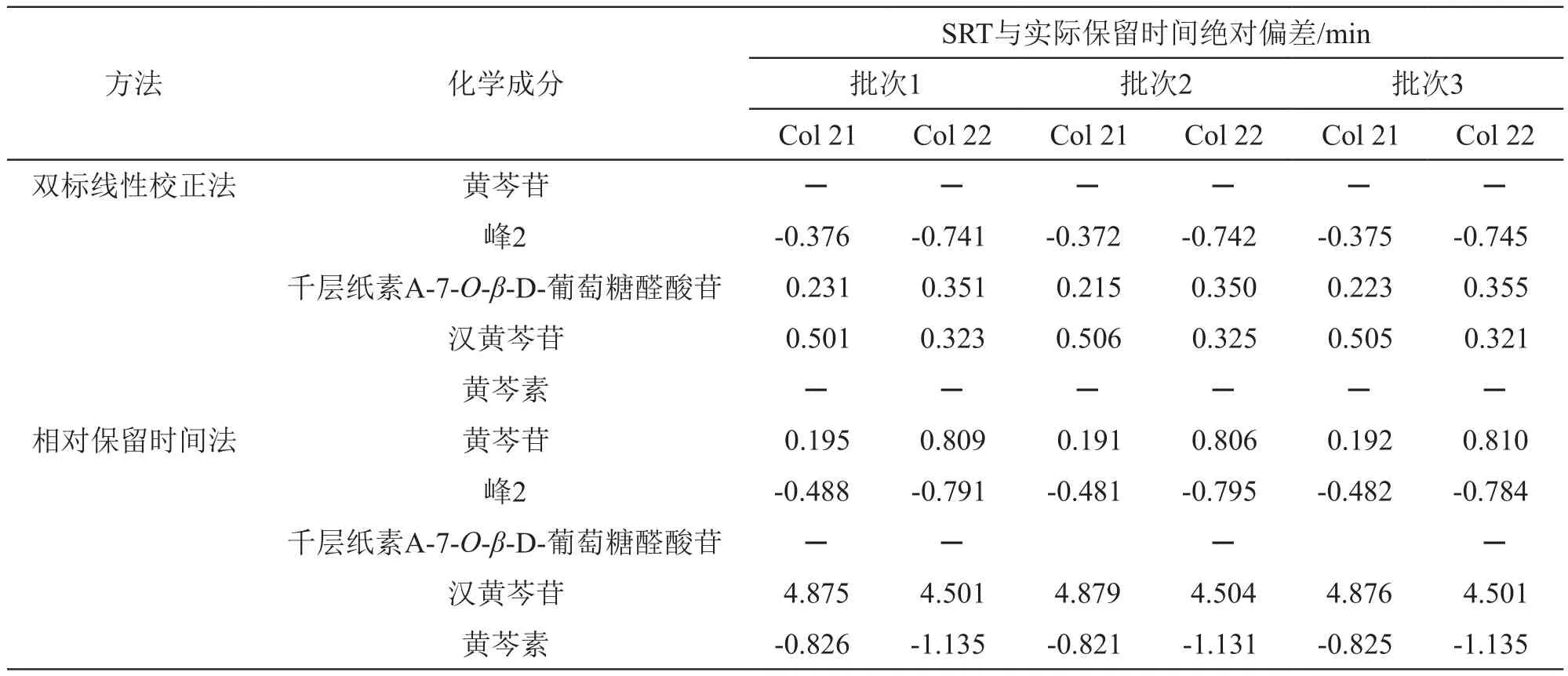
表4 双标线性校正法和相对保留时间法在新色谱柱上保留时间绝对偏差比较
4 结论
本研究采用双标线性校正法建立川黄芩的多组分定性鉴别方法,能快速、准确地定位川黄芩中5个成分。与相对保留时间法进行比较,双标线性校正法的预测精度更高,适用的色谱柱数量更多,明显优于相对保留时间法。本研究采用的双标组合,综合考虑了色谱柱适用率和预测准确度等因素,最终选择了黄芩苷和黄芩素两个位于色谱峰两端的色谱峰作为双标参照物,同时也满足廉价易得等优势。但目前,由于整个研究还处在试验阶段,下一步的应用和推广还有很多亟待解决的问题。
