Fe/Cu修饰氮掺杂碳纳米管的构筑及催化性能
2022-12-06王支国邓莹莹党姣娥张永伟张丽珊云斯宁
王支国 邓莹莹 党姣娥 张永伟 张丽珊 阿 鑫 云斯宁*,
(1西安建筑科技大学材料科学与工程学院,功能材料研究所,西安 710055)
(2青海省高原绿色建筑与生态社区重点实验室,西宁 810008)
0 引 言
染料敏化太阳能电池(dye-sensitized solar cells,DSSCs)作为第3代太阳能电池的典型代表,因其成本效益高、制备简单和理论转换效率高等优势而引起了人们的广泛关注[1]。其中,对电极作为DSSCs的重要组成部分,起着收集外部电路电子和催化I-3还原为I-的作用。高活性催化剂可以促进光伏器件中的碘还原反应,从而提高DSSCs的光电能量转换效率(power conversion efficiency,PCE)。理想的催化剂应具有优越的导电性、显著的化学稳定性、优异的催化活性和低廉的生产成本。Pt基材料是DSSCs中最常用的催化剂,但由于资源稀缺、成本高和易被碘体系电解液腐蚀等缺点,使得Pt基催化剂的应用受到限制。因此,开发高效耐用的非贵金属对电极催化剂对DSSCs的发展至关重要。
过渡金属因其丰富的储量和较高的催化活性,在不同技术领域(能量储存、能量转换以及催化等)具有广泛的应用价值[2-3]。其中,Cu修饰氮掺杂碳因其良好的催化活性而备受关注。Guan等采用Cu纳米颗粒修饰MOF衍生氮掺杂碳,其表现出比商用Pt/C更好的氧还原(oxygen reduction reaction,ORR)催化活性[4]。Kong等采用Cu修饰氮掺杂碳,获得比单纯的Cu和N-C更好的ORR催化活性[5]。Chen等采用Co纳米颗粒修饰氮掺杂多孔碳材料,其表现比N-C更好的氨硼水解催化活性[6]。但是,由于单一的Cu修饰氮掺杂碳的活性位点有限,且稳定性不理想,其催化活性有待进一步提高。研究发现,在氮掺杂碳中,氮原子的作用是约束和稳定金属颗粒。采用双金属修饰氮掺杂碳,一方面会使更多的金属-氮位点嵌入碳层,增加活性位点的数量,且2种金属-氮活性位点之间会产生协同效应,从而进一步提高催化活性;另一方面,更多的金属被氮限制和稳定后,能够进一步提高双金属修饰氮掺杂碳对电解液的耐腐蚀性,从而提升其稳定性。因此,双金属修饰表现出比单一金属修饰更优异的催化性能和稳定性[7-10]。Zheng等采用Cu和Co共修饰氮掺杂碳(Cu/Co@N-C)作为电解水产氢的催化剂,得益于Cu与Co之间快速的电荷转移,Cu/Co@N-C在电解水产氢装置中表现出较好的催化性能[11]。Du等采用Ni修饰Cu-MOF,其对葡萄糖的氧化具有良好的催化效果[12]。因此,采用双金属修饰氮掺杂碳对促进碳基材料催化性能进一步提升具有重要的研究意义。
碳骨架的导电性和形貌结构对催化剂的电子转移能力和电化学稳定性也起着关键作用[13]。碳纳米管(CNT)具有丰富的褶皱,可以大大增加催化剂的活性位点数量、促进电荷转移和提高催化剂的反应动力学过程[14]。研究表明:CNT对I3-的还原具有较好的电催化活性,是构建快速电子传输网络的理想基体材料[15]。此外,研究发现:Fe常被用作控制三聚氰胺衍生氮掺杂碳形成CNT的金属元素[16]。Li等通过在三聚氰胺衍生氮掺杂碳中引入Fe源,制备了具有竹节状形貌的CNT,对ORR和CO2还原反应都表现出优异的催化活性[17]。Yang等以三聚氰胺和硝酸铁为原料,通过控制退火温度,制备了管状CNT/Fe3C复合材料,与商业Pt/C催化剂相比,在0.1 mol·L-1KOH溶液中表现出更高的ORR活性、更好的稳定性和更好的甲醇耐受性[18]。Fe催化氮掺杂碳生成纳米管,主要取决于Fe吸附碳原子/碳簇的能力,其吸附碳原子/碳簇的能力与其粒度有关,粒度适中的Fe催化剂粒子能够使碳基材料表面的碳原子/碳簇的融入和析出达到平衡,从而形成CNT[19-20]。因此,我们采用Fe作为第2种金属制备双金属修饰CNT。首先,通过热解双氰胺和含铜金属盐的混合物,制备了Cu修饰氮掺杂碳(Cu-N-C),随后采用离子交换法制备Fe/Cu修饰氮掺杂CNT(Fe/Cu-N-C/CNT)。将制备的催化剂作为对电极,应用于DSSCs,并对其所组装电池的电化学性能、光伏性能以及稳定性进行了研究。
1 实验部分
1.1 材料制备
1.1.1 原位合成法制备Cu-N-C
Cu-N-C的制备过程如下:如图1所示,将乙酰丙酮铜(Cu(C5H7O2)2,0.500 0 g,阿拉丁,纯度 98%)和双氰胺(C2H4N4,1.300 0 g,阿拉丁,纯度99%)完全分散在无水乙醇(50 mL,阿拉丁,纯度97%)中。随后,将混合溶液保持在50℃连续搅拌4 h,得到的溶液在80℃烘箱中干燥、过夜。干燥后的样品在N2气氛下800℃下热解2 h,升温速率为5℃·min-1,样品随炉冷却,得到Cu-N-C。
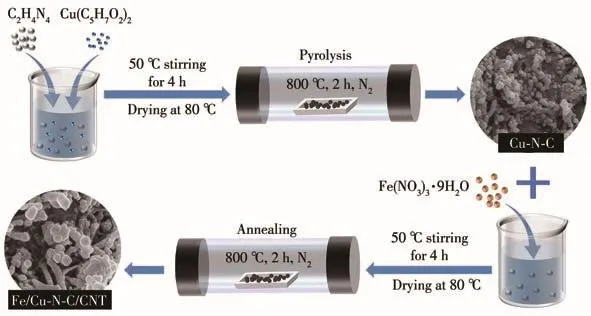
图1 Cu-N-C和Fe/Cu-N-C/CNT的制备示意图Fig.1 Schematic diagram of Cu-N-C and Fe/Cu-N-C/CNT preparation
1.1.2 离子交换法制备Fe/Cu-N-C/CNT
将九水合硝酸铁(Fe(NO3)3·9H2O,0.087 0 g,阿拉丁,纯度99.99%)分散于无水乙醇(50 mL)中,搅拌30 min直至完全溶解。然后加入上述制备的Cu-N-C(0.200 0 g),在恒定温度(50℃)下连续搅拌4 h,所得混合溶液在80℃的烘箱中干燥。所得混合物在N2气氛下800℃退火2 h,升温速率为5℃·min-1,即得Fe/Cu-N-C/CNT。依据课题组之前的研究结果,选用乙酰丙酮铜与九水合硝酸铁的物质的量之比为 2∶0.3[9-10]。
1.2 电极的制备和电池组装
光阳极:商用TiO2光阳极(0.196 cm2,购于江苏延长桑莱特新能源有限公司)在空气中500℃烧结30 min。待温度冷却到120℃后,将其浸入0.5 mmol·L-1的N719染料中(乙腈为溶剂,N719染料与乙腈体积比为1∶1),在黑暗条件下浸泡24 h后,用乙醇冲洗并干燥,得到染料敏化的TiO2光阳极。
对电极:将Cu-N-C或Fe/Cu-N-C/CNT粉末(40 mg)分散在异丙醇溶液(1 mL)中,加入6 g的ZrO2珠,球磨4 h。使用喷枪将混合均匀后的浆料涂在FTO玻璃的导电面上。然后,在N2气氛下400℃退火30 min,获得Cu-N-C或Fe/Cu-N-C/CNT对电极。将20 mmol·L-1H2PtCl6的异丙醇溶液涂覆在FTO玻璃的导电面上,在500℃退火30 min,得到的Pt电极作为参照。
电池的组装:采用2个相同的对电极组装成对称电池,用毛细滴管将I3-/I-电解质注入电极中,获得完整的DSSC,电池的有效面积为0.196 cm2。将对电极、染料敏化的TiO2光阳极和I3-/I-电解液组装成三明治形状的DSSC,用于光伏性能测试。I3-/I-电解质由 0.1 mol·L-1硫氰酸胍、0.06 mol·L-1LiI、0.03 mol·L-1I2、0.6 mol·L-11-丁基-3-甲基咪唑碘、0.5 mol·L-14-叔丁基吡啶和乙腈溶液组成。更多的电池组装细节请参考本课题组之前的报道[21-23]。
1.3 材料表征与电池性能测试
通过X射线粉末衍射仪(XRD,D/Max-2200,Cu Kα,λ=0.154 06 nm,工作电流:40 mA,工作电压:40 kV,扫描速率:10(°)·min-1,扫描范围2θ=10°~80°)和拉曼光谱仪(LabRAM HR Evolution,Horiba,激发波长:532 nm)分别确定Cu-N-C和Fe/Cu-N-C/CNT的物相组成和石墨化程度。通过场发射扫描电子显微镜(FESEM,JSM-6700F,JEOL,加速电压 0.5~30 kV)对不同样品的显微结构与形貌进行表征。使用X射线光电子能谱仪(XPS,Thermo ESCALAB 250XI)研究样品的表面元素组成及价态。使用电化学分析仪(CHI 660E辰华,上海)对制备的对电极催化剂进行循环伏安(CV)、电化学阻抗(EIS)和Tafel测试。在100 mW·cm-2的光照强度(AM 1.5G)下,使用太阳光模拟器(EASISOLAR-50-3A,美国)测量DSSCs的光伏性能。
2 结果与讨论
2.1 结构与形貌表征
图2a为所制备样品的XRD图。Cu-N-C的XRD图中能够明显看出金属Cu的衍射峰,表明存在金属Cu。值得注意的是,在Cu-N-C中,碳的26°左右的衍射峰不明显,这可能是由于Cu的高强度金属峰掩盖了碳峰。在Fe/Cu-N-C/CNT的XRD图中,除了Cu金属峰外,在45°和65.1°处出现金属Fe的衍射峰,在36°和47°出现Fe4N的衍射峰。Fe4N是Fe/Cu-N-C/CNT制备过程中的副产物,Fe较Cu更为活泼,在温度达到700℃时会出现Fe4N(PDF No.86-0231),在以往的报道中也出现过类似现象[24-25]。Fe4N的形成能够促进碘还原催化反应的进行,从而提高Fe/Cu-NC/CNT的催化活性,类似结果在Li等的报道中通过密度泛函理论计算已经证明[26-27]。此外,引入第2种金属Fe后,Cu的金属衍射峰强度明显降低,26°左右石墨碳衍射峰比较明显,这可能是由于Fe的掺入使催化剂的结晶度发生变化。以上结果表明制备的催化剂中存在金属和无定型碳。
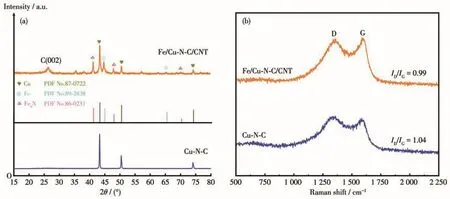
图2 Cu-N-C和Fe/Cu-N-C/CNT的(a)XRD图和(b)拉曼谱图Fig.2 (a)XRD patterns and(b)Raman spectra of Cu-N-C and Fe/Cu-N-C/CNT
图2b中为所制备催化剂的Raman谱图,在约1 354和约1 589 cm-1处出现2个峰,分别对应碳的D峰和G峰。D峰与G峰的峰强度比(ID/IG)可以反映碳材料的缺陷程度和石墨化程度。计算得到Fe/Cu-NC/CNT的ID/IG为0.99,小于Cu-N-C(ID/IG=1.04),表明Fe/Cu-N-C/CNT的石墨化程度更高。这可能归因于Fe4N、Cu和Ni多金属相的存在,促进了其石墨化程度的提高;另一方面,制备Fe/Cu-N-C/CNT时,经过2次高温烧结,进一步提高了碳材料的石墨化程度。在关于过渡金属修饰碳基催化剂的报道中,也发现了类似的现象[28-30]。Fe/Cu-N-C/CNT较高的石墨化程度可以促进电荷传输,进一步提高其电化学性能。
在图3a中,Fe/Cu-N-C/CNT的XPS总谱图呈现5个明显的主要特征峰,分别对应C1s、N1s、O1s、Fe2p和Cu2p,表明样品中存在C、N、O、Fe和Cu元素。在图3b中,C1s的XPS精细谱图包含3个主要的特征峰,分别对应 C=O(289.00 eV)、C—N(285.76 eV)和C—C(284.69 eV)键。C—N键的存在表明N原子被成功掺入碳材料中。N1s的XPS精细谱图如图3c所示,分为吡啶-N(398.55 eV)、金属-N(399.37 eV)、吡咯 -N(400.85 eV)、石 墨 -N(401.50 eV)和 氧 化 -N(404.79 eV)。相关研究已经证明:吡啶-N、金属-N和石墨-N能够提供更多的促进三碘化物还原的活性位点[11,31]。图3d中Cu2p在932.91 eV处的Cu2p3/2和952.60 eV处的Cu2p1/2的特征峰证实了金属Cu0的存在。同时,Cu2p3/2(934.56 eV)和 Cu2p1/2(954.48 eV)处出现的特征峰对应Cu2+[4]。图3e中,Fe2p的XPS精细谱图可分为6个特征峰:720.01 eV(Fe02p1/2)、723.83 eV(Fe2+2p1/2)、727.50 eV(Fe3+2p1/2)、707.38 eV(Fe02p3/2)、710.83 eV(Fe2+2p3/2)和 714.64 eV(Fe3+2p3/2)。以上结果进一步证实了催化剂中N和金属的成功掺入并形成金属—氮键。Cu2+、Fe2+和Fe3+主要以金属—氮位点和氧化物的形式存在,氧化物的导电性低于金属Cu和Fe。由于本研究中金属用量较少,以氧化物形式存在的Cu2+、Fe2+和Fe3+的含量极少,对氮掺杂碳导电性的影响较小,可以忽略不计,类似结果在之前的研究中已有报道[4,31]。
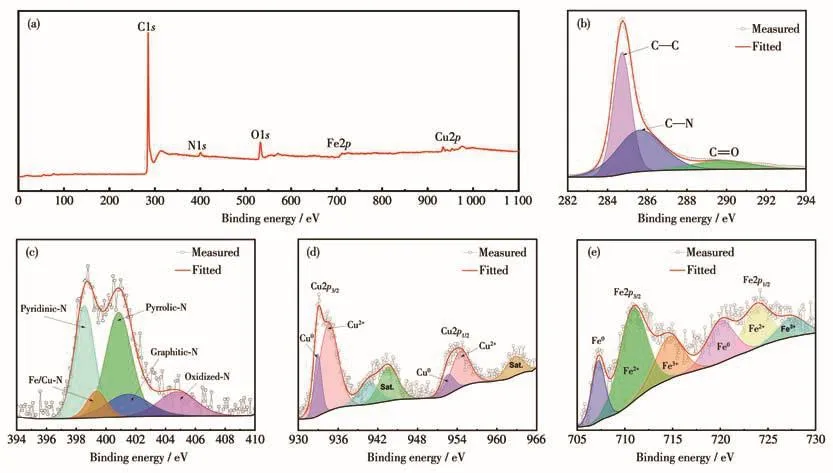
图3 Fe/Cu-N-C/CNT的(a)XPS总谱图及(b)C1s、(c)N1s、(d)Cu2p和(e)Fe2p的XPS精细谱图Fig.3 (a)XPS survey spectra and high-resolution(b)C1s,(c)N1s,(d)Cu2p,and(e)Fe2p XPS spectra of Fe/Cu-N-C/CNT
如图4a、4b所示,Cu-N-C为直径约50 nm的球形纳米颗粒。图4c为Cu-N-C的EDS(能谱)元素分布图,图中能够清晰地看到Cu、N和C元素均匀分布。图4d、4e中,Fe/Cu-N-C/CNT呈现出纳米管和纳米颗粒2种形貌,纳米管互相缠绕(直径为50~100 nm),表面负载有纳米颗粒(直径约50 nm)。纳米管的生成可能是由于在二次烧结过程中生成了Fe4N和Fe纳米颗粒,纳米颗粒进一步催化诱导碳的石墨层弯曲生长成CNT。类似现象在之前的文章中也有所报道[18,32]。相互缠绕的纳米管和球形纳米颗粒形成了随机取向的三维孔道,促进电解液与催化剂薄膜充分接触[14,33]。该结构有利于电子从外部电路通过催化剂材料传输至电解液中,从而加速I3-的还原反应,类似的结构在之前的文章中也有报道[9]。图4f中的EDS元素分布图表明,Fe、Cu、N和C元素在Fe/Cu-N-C/CNT中均匀分散,进一步证明碳基材料中均匀地掺杂了氮杂原子和金属原子。
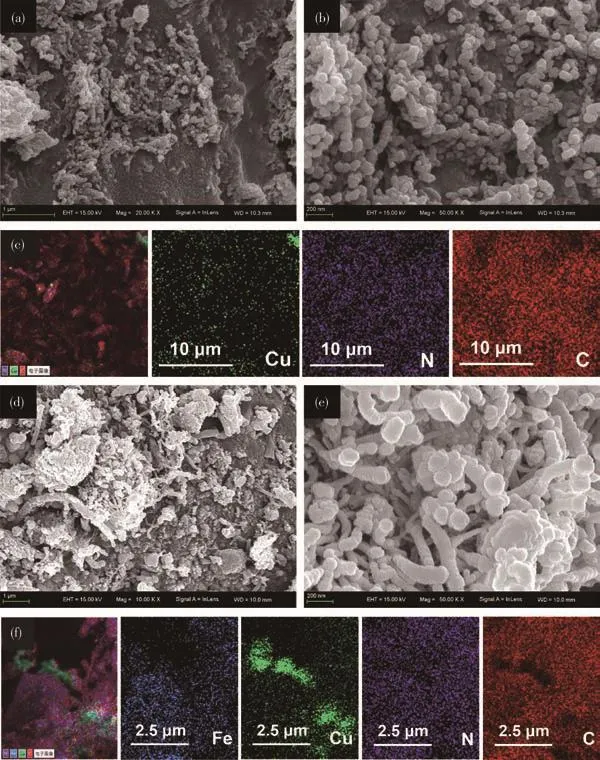
图4 Cu-N-C的(a、b)FESEM图和(c)EDS元素映射图;Fe/Cu-N-C/CNT的(d、e)FESEM图和(f)EDS元素映射图Fig.4 (a,b)FESEM images and(c)EDS element mappings of Cu-N-C;(d,e)FESEM images and(f)EDS element mappings of Fe/Cu-N-C/CNT
2.2 电化学性能表征
图5a展示了不同对电极在三电极系统中测试得到的CV曲线。表1给出了相应的电化学参数。每个对电极的CV曲线均有2对氧化还原峰,左边的氧化还原峰对应I3-/I-之间的氧化还原反应,如方程式1所示;右边的氧化还原峰对应I3-/I2之间的氧化还原反应[21],如方程式2所示:

表1 不同对电极的电化学参数Table 1 Electrochemical parameters of different counter electrodes
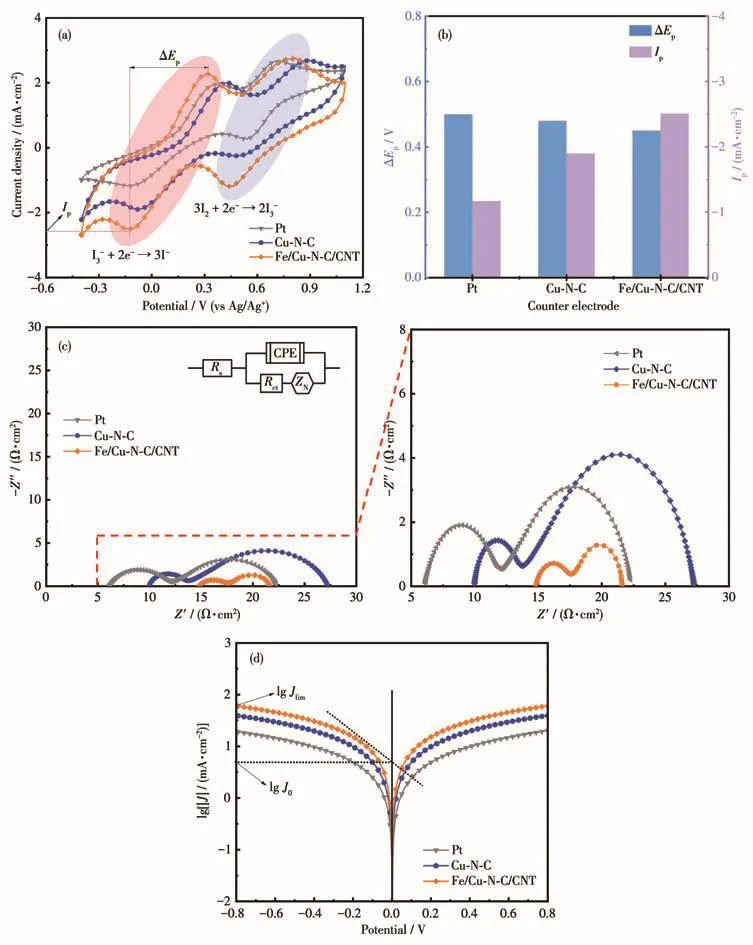
图5 (a)Cu-N-C、Fe/Cu-N-C/CNT和Pt对电极在50 mV·s-1扫描速率下的CV曲线;(b)不同对电极催化剂的ΔEp和Ip值;(c)不同对称电池的Nyquist曲线和(d)Tafel极化曲线Fig.5 (a)CV curves of Cu-N-C,Fe/Cu-N-C/CNT,and Pt counter electrodes at scanning rate of 50 mV·s-1;(b)Values of Ipand ΔEp for various counter electrodes;(c)Nyquist plots and(d)Tafel polarization curves for the symmetrical cells with as-prepared counter electrodes

CV曲线中,通过比较阴极峰电流密度(Ip)和氧化还原峰之间电位差(ΔEp)的大小,可以评价对电极材料的催化性能。较大的|Ip|和较小的ΔEp意味着对电极表面的氧化还原反应能够顺利进行,并且具有较高的氧化还原可逆性[34]。从图5b和表1可知,对电极的|Ip|值从大到小依次为Fe/Cu-N-C/CNT(2.51 mA·cm-2)>Cu-N-C(1.90 mA·cm-2)>Pt(1.17 mA·cm-2);ΔEp值从小到大依次为Fe/Cu-N-C/CNT(0.45 V)<Cu-N-C(0.48 V)<Pt(0.5 V)。其中,Fe/Cu-N-C/CNT 的|Ip|值最高、ΔEp值最低,表明Fe/Cu修饰使得氮掺杂碳具有优异的I3-还原催化活性[35]。
图5c显示了不同对电极组装的对称电池的Nyquist曲线,高频区在实轴的截距代表串联电阻(Rs),Rs值越小,表明该催化剂在导电玻璃上的附着力越强。曲线的左半圆半径代表电极/电解液界面的电荷转移电阻(Rct),Fe/Cu-N-C/CNT的Rct为2.18 Ω·cm2,小于 Cu-N-C(2.93 Ω·cm2)和 Pt(5.88 Ω·cm2)。一般情况下,催化剂的Rct越小,表明其对于I3-还原的催化活性越高。因此,Fe/Cu-N-C/CNT的电荷传输性能优于Cu-N-C和Pt。另一方面,Fe/Cu-N-C/CNT中纳米管互相缠绕可以暴露更多的边缘活性位点,增加催化剂与电解液之间的接触面积,从而提高电荷传输性能,类似结果在之前的研究中已经报道[36]。
Tafel极化曲线测试结果如图5d所示,极化曲线Tafel区(120 mV<|V|<400 mV)线性区域外推延长线与平衡电位线(图中零电位点与X轴垂直的实线)的交点在Y轴的截距为lg J0,交换电流密度(J0)反映了对电极催化剂对电解液体系中I3-的还原能力。理论上,J0与Rct呈反比关系,如方程式3所示:

其中,R为标准气体常数,T为绝对温度,n为电化学反应涉及的电子转移数目,F为法拉第常数。对电极的J0按Fe/Cu-N-C/CNT>Cu-N-C>Pt的顺序依次降低,表明Fe/Cu-N-C/CNT对I3-的还原具有较高的催化活性。阴极分支与Y轴的交点为lg Jlim,极限扩散电流密度(Jlim)反映了电解液中I3-的扩散速率。所制备的Fe/Cu-N-C/CNT对电极具有最高的Jlim,表明Fe/Cu-N-C/CNT具有最快的离子扩散速率。得益于Fe的引入和二次烧结,催化剂进一步生长为相互缠绕的纳米管状结构,这种结构具有大量的孔隙,有利于电解液的充分渗透,加快离子的扩散。
2.3 光伏性能测试
由Fe/Cu-N-C/CNT、Cu-N-C和Pt电极组装的DSSCs器件的J-V曲线如图6所示,相应的光伏参数如表2所示。其中,Fe/Cu-N-C/CNT对电极组装的DSSC获得7.55%的PCE和14.78 mA·cm-2的短路电流密度(Jsc),优于Cu-N-C(PCE=6.99%,Jsc=13.90 mA·cm-2)和Pt(PCE=6.76%,Jsc=14.29 mA·cm-2)电极。这一结果与之前报道的其他过渡金属修饰氮掺杂碳对电极的光伏性能相当。本文中报道的Fe/Cu-N-C/CNT作为对电极,得益于多组分(Cu和Fe金属纳米颗粒、Fe4N纳米颗粒与氮掺杂CNT)之间的协同作用以及独特的纳米管三维网络结构,其组装的DSSCs器件具有优异光伏性能,高于之前报道的CoNi@NC(3.58%)、Co-NPCD(7.28%)、Nb/Co-N-C(7.46%)和Fe-N-C(6.94%);与 Bi/Co-N-C(7.65%)和 Fe-NPCD(7.63%)对电极组装的DSSCs器件的PCE相当[37-40]。
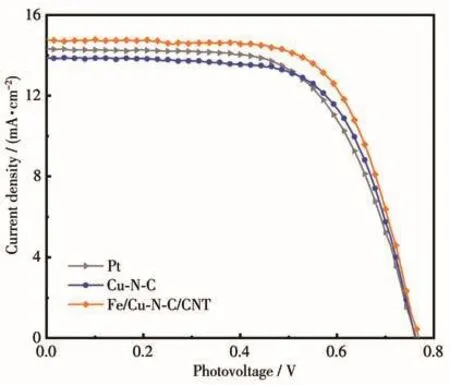
图6 Cu-N-C、Fe/Cu-N-C/CNT和Pt对电极所组装DSSCs的J-V曲线Fig.6 J-V curves of the assembled DSSCs with Cu-N-C,Fe/Cu-N-C/CNT,and Pt counter electrodes

表2 金属修饰氮掺杂碳作为对电极催化剂组装DSSCs的光伏参数对比Table 2 Comparison of photovoltaic parameters of DSSCs with the metal-modified nitrogen-doped carbon counter electrodes
综合以上分析,Fe/Cu-N-C/CNT的较高催化活性和良好光伏性能主要来源于以下几方面:(1)Cu与Fe金属之间的协同作用进一步降低了Fe/Cu-NC/CNT的Rct;(2)加入金属Fe盐并进行二次烧结,诱导碳的石墨层弯曲生长成互相缠绕的纳米管,有利于Fe/Cu-N-C/CNT催化剂与电解液的充分接触,进一步增强其催化活性;(3)Cu和Fe金属纳米颗粒、Fe4N纳米颗粒与氮掺杂碳及CNT共存,提高Fe/Cu-N-C/CNT的电催化活性。
2.4 稳定性测试
如图7a、7b所示,在50圈稳定性测试后,Fe/Cu-N-C/CNT的CV曲线表现出良好的重合性,而Cu-N-C的CV曲线出现较大偏移,这一结果表明Fe/Cu-N-C/CNT具有较好的电化学稳定性。图7c、7d显示了在不同扫描周期下Cu-N-C和Fe/Cu-N-C/CNT的氧化还原峰值电流密度。随着扫描周期的增加,Fe/Cu-NC/CNT的峰值电流密度没有显著变化,证明Fe/Cu-NC/CNT对电极在碘体系中表现出优异的可逆性和良好的电化学稳定性。类似结果在之前的文章中也有报道[9,41]。
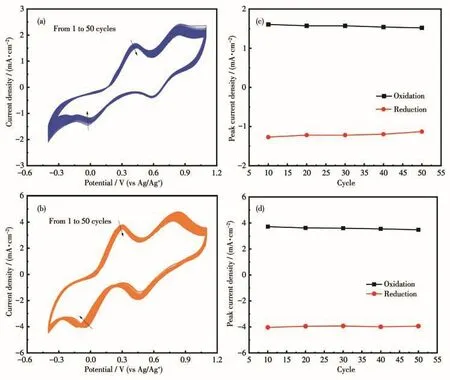
图7 (a)Cu-N-C和(b)Fe/Cu-N-C/CNT的50圈连续扫描的CV曲线(扫描速率:50 mV·s-1);(c)Cu-N-C和(d)Fe/Cu-N-C/CNT的CV循环扫描圈数与峰值电流密度之间的关系Fig.7 CV curves for 50 cycles continuous scans of(a)Cu-N-C and(b)Fe/Cu-N-C/CNT counter electrodes(scanning rate:50 mV·s-1);Peak current densities at various CV scanning cycles for(c)Cu-N-C and(d)Fe/Cu-N-C/CNT
3 结论
通过原位化学合成法结合离子交换法成功地制备了Cu-N-C和Fe/Cu-N-C/CNT催化剂。将其作为DSSCs的对电极,在其组装的对称电池中,Fe/Cu-N-C/CNT的电荷转移电阻为2.18 Ω·cm2,低于Cu-NC(2.93 Ω·cm2)和 Pt(5.88 Ω·cm2)。Fe/Cu-N-C/CNT 对电极组装的DSSCs获得了7.55%的PCE,高于Cu-NC(6.99%)和Pt(6.76%)。Fe/Cu-N-C/CNT对电极在连续50圈循环扫描中表现出了优于Cu-N-C的电化学稳定性。本工作中所制备的Fe/Cu-N-C/CNT催化剂在制备工艺、光伏性能和稳定性方面都具有明显优势,为合成低成本、高催化性能催化剂的设计提供了思路。
