改性生物质活性炭对水溶液中Cu2+的吸附研究
2022-12-01王培若刘艳娟
包 坤,王培若,刘艳娟
(唐山学院 a.新材料与化学工程学院,b.唐山市水环境生态修复技术重点实验室,河北 唐山 063000)
0 引言
重金属进入水环境中,会对生态环境产生持续的危害,并对社会经济产生重大影响。根据不完全数据统计,重金属污染每年给我国带来的直接经济损失高达200亿元[1]。同时,重金属通过生物链的作用会对人体造成很大的伤害,因此,对水体中的重金属污染进行治理在我国很受重视。目前,生物质活性炭吸附法是污水重金属处理中比较常用的方法,该方法操作便捷,性价比高,且处理效果好[2]。生物质活性炭是指利用农业废弃物(果壳、秸秆、木材等)和工业废弃物(如污泥)等制备而成的一种活性炭[3]。然而未改性的生物质活性炭的可选择性较差且吸附容量较小,因此,对改性生物质活性炭进行研究成为必然趋势。通过对生物质活性炭进行改性处理,可以有效扩大生物质活性炭的适用范围,并且可以提高其吸附容量。
目前,对于改性生物质活性炭的研究越来越多。石家豪等[4]利用Na2CO3与粉煤灰制备复合改性生物质活性炭,并就其对磷的吸附效果进行研究,发现改性后的生物质活性炭较未改性的粉煤灰吸附效果更强,磷的去除率可高达98.01%。肖瑶等[5]利用玉米芯残渣和膨润土制成生物质活性炭,并用氯化钙进行改性处理,改性后的生物质活性炭对水溶液中Pb2+的去除率高达98%,最大饱和吸附量为232.2 mg/g。Yin等[6]利用无水MgCl2对巨菌草秸秆进行改性,制备的改性生物质活性炭具有良好的去除水中Cd2+的能力,且吸附过程符合Langmuir等温吸附和准二级动力学吸附模型。Yan等[7]以小麦秸秆为原料,并用K2FeO4制备铁改性生物质活性炭,表征结果表明其对Cu2+和磺胺嘧啶吸附效果均较好,最大吸附量分别为46.85 mg/g和45.43 mg/g。Quyen等[8]利用咖啡渣为原料,并用NaOH进行改性,以此生物质活性炭为吸附剂考察了其对水中Pb2+,Cd2+的吸附性能,结果表明,此生物质活性炭能够去除废水中89.6%的Pb2+和81.5%的Cd2+,是一种高效且低成本的吸附剂。Wallacee等[9]利用改性后的奶牛粪制得一种衍生生物质活性炭,表现出对金属离子按Pb2+>Zn2+>Cd2+顺序具有竞争性去除的特征,Pb2+和Cd2+的去除率随pH值的升高而增大,而Zn2+的去除率在pH值≈7.5时达到最大。
我国是一个农业大国,秸秆资源十分丰富,仅2017年,我国的秸秆资源就达到了9.0×108t,但是其利用效率不足40%[10],利用秸秆这样一种具有优良的重金属去除性能的生物质活性炭,不仅可以解决生物质活性炭收集困难、来源不稳定等问题,还可以有效地提高其经济价值,达到高利用的目的。而且,对这些秸秆进行回收再利用,还可有效降低其对环境的负面影响。本研究以玉米秸秆为原料制备生物质活性炭,分别应用NaOH和HNO3对其进行改性,以提高其吸附水溶液中Cu2+的潜能,以此为利用改性生物质活性炭进行水污染处理的研究提供一定的理论借鉴。
1 实验材料和方法
1.1 试剂与仪器
试剂:铜标准贮备液(1.000 mg/mL),CuSO4,H2SO4,HNO3,NaOH均为分析纯。实验用水为去离子水。
仪器:原子吸收分光光度计(TAS-990,北京普析);电热恒温干燥箱(101-1AB,天津泰斯特);气浴恒温振荡器(SHZ-82,常州金坛良友);马弗炉(SX2-10-13,四川恩格);离心机(80-2,江苏中大);pH计(PHSJ-3F,上海精密科学)。
1.2 供试材料
实验所用玉米秸秆取自唐山市某农田。用去离子水对其冲洗三遍后,放入电热恒温干燥箱中干燥(80 ℃),将其粉碎后,放入马弗炉内700 ℃低氧分解120 min。利用干筛法进行过滤,获得三种不同粒径的生物质活性炭(0.15~0.30 mm,0.30~0.50 mm,0.50~1.00 mm)。按料液比1∶30[m(g)∶V(mL)]将生物质活性炭加入到0.1 mol/L的NaOH溶液(或3%HNO3溶液)中,再在40 ℃的水浴中保持240 min,过滤,洗涤到中性,50 ℃烘干,储存,由此获得改性生物质活性炭。
1.3 实验方法
在锥形瓶中,加入一定浓度的Cu2+溶液(20 mL),分别准确称取一定质量的NaOH改性、HNO3改性和未改性的生物质活性炭,用稀H2SO4和NaOH溶液调节pH值,恒温振荡后,0.45 μm水系滤膜过滤样品,原子吸收分光光度计测量滤液中的Cu2+浓度,并重复三次。
(1)
(2)
式中,η为Cu2+去除率,%;C0为Cu2+初始质量浓度,mg/L;C为吸附平衡时Cu2+质量浓度,mg/L;Q为Cu2+平衡吸附量,mg/g;V为溶液总体积,L;m为生物质活性炭用量,g。
2 吸附理论模型
2.1 等温吸附模型
本研究应用Langmuir和Freundlich等温吸附方程来表征恒温条件下生物质活性炭的表面吸附量与水溶液中Cu2+的平衡浓度之间的关系[11]。
Langmuir方程:
(3)
Freundlich方程:
(4)
式中,Qe和Qm分别为Cu2+平衡吸附量和饱和吸附量,mg/g;Ce为Cu2+平衡质量浓度,mg/L;K1为Langmuir常数,L/mg;K2为Freundlich中与吸附能力有关的常数,(mg1-1/n·L1/n)/g;n为Freundlich常数。
2.2 吸附动力学模型
应用Lagergren准一级动力学方程和准二级动力学方程对实验数据进行拟合,研究生物质活性炭对水溶液中Cu2+的吸附动力学特征[12-13]。
准一级动力学方程:
(5)
准二级动力学方程:
(6)
式中,Qe为Cu2+平衡吸附量,mg/g;Qt为t时刻Cu2+吸附量,mg/g;k1为准一级动力学反应速率常数,min-1;k2为准二级动力学反应速率常数,g/(mg·min)。
2.3 吸附热力学模型
应用Gibbs-Helmholtz方程计算ΔG0(吸附自由能)、ΔH0(吸附焓变)及ΔS0(吸附熵变),来分析温度对生物质活性炭吸附水溶液中Cu2+的影响[14]。
(7)
ΔG0=ΔH0-ΔS0T。
(8)
式中,Kd为平衡分配系数;R为气体常数,J/(mol·K);T为绝对温度,K;ΔG0为吸附自由能,kJ/mol;ΔH0为吸附焓变,kJ/mol;ΔS0为吸附熵变,J/(mol·K)。
3 结果与分析
3.1 生物质活性炭用量对吸附性能的影响
在35 ℃条件下,考察NaOH改性、HNO3改性以及未改性的生物质活性炭(粒径均为0.15~0.30 mm)的不同投加量(0.10 g,0.15 g,0.20 g,0.25 g,0.30 g,0.40 g,0.50 g和0.60 g)对浓度为40 mg/L的Cu2+溶液(20 mL)的吸附效果,溶液pH值为6.0,震荡吸附360 min,结果如图1所示。
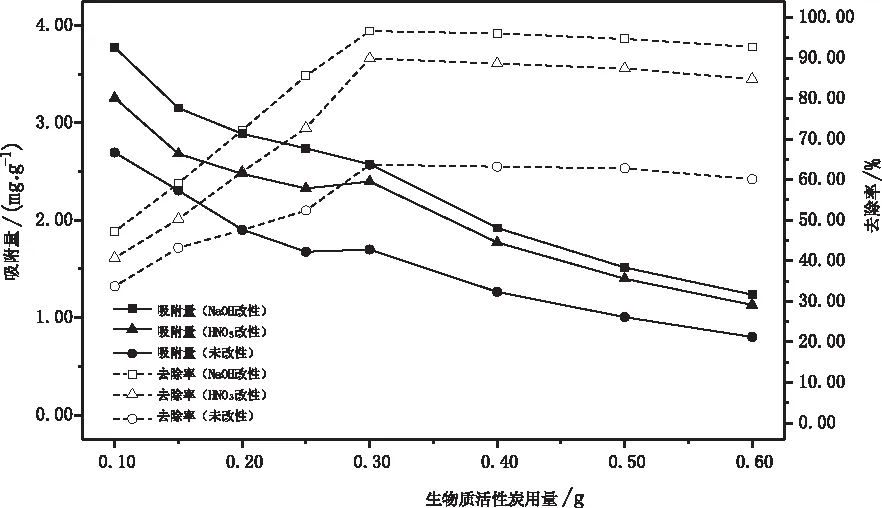
图1 生物质活性炭用量对吸附量和去除率的影响
由图1可知,生物质活性炭对Cu2+的吸附量随生物质活性炭用量的增加而下降,这是由于生物质活性炭的投加量越高,单位质量的生物质活性炭吸收的Cu2+的量减少,则吸附量就越小。当生物质活性炭用量由0.10 g增加到0.30 g时,Cu2+的去除率不断升高,当用量由0.30 g增加到0.60 g时,去除率逐渐稳定甚至降低,这是由于当吸附剂用量增加到一定程度后,过量的吸附剂无法得到充分的利用,从而形成诸多空位,此时生物质活性炭对Cu2+的吸附达到饱和状态[15]。从吸附量和去除率两个方面进行综合考虑,0.30 g为最适宜的投加量,此时生物质活性炭对溶液中Cu2+的去除率最高,分别为96.60%(NaOH改性)、89.90%(HNO3改性)和63.70%(未改性),吸附量分别为2.58 mg/g(NaOH改性)、2.40 mg/g(HNO3改性)和1.70 mg/g(未改性)。在生物质活性炭用量相等的条件下,三种生物质活性炭对水溶液中Cu2+的吸附性能表现为:NaOH改性>HNO3改性>未改性。
3.2 生物质活性炭粒径对吸附性能的影响
在35 ℃条件下,分别取0.30 gNaOH改性、HNO3改性以及未改性的生物质活性炭(粒径均为三种:0.15~0.30 mm,0.30~0.50 mm,0.50~1.00 mm),对浓度为40 mg/L的Cu2+溶液(20 mL)进行吸附,溶液pH值为6.0,震荡吸附360 min,结果如图2所示。

图2 生物质活性炭粒径对吸附量和去除率的影响
由图2可知,在三种不同粒径的生物质活性炭中,粒径在0.15~0.30 mm的生物质活性炭具有较好的吸附效果,NaOH改性、HNO3改性和未改性生物质活性炭对Cu2+的吸附量分别为3.88 mg/g,3.69 mg/g和2.58 mg/g,且对Cu2+的去除率也达到最大,分别为96.90%,92.20%和64.59%。这是缘于生物质活性炭的比表面积、孔隙结构等因素,它们决定了其吸附性能,即粒径较大的生物质活性炭具有较低的比表面积,其孔隙率越低,吸附性能也就越差[16]。故在探究其他因素对吸附效果的影响时,选用粒径在0.15~0.30 mm的生物质活性炭,可以达到较好的吸附效果。在生物质活性炭粒径相等的条件下,三种生物质活性炭对水溶液中Cu2+的吸附性能表现为:NaOH改性>HNO3改性>未改性。
3.3 pH值对吸附性能的影响
在35 ℃条件下,分别取三种生物质活性炭0.30 g(粒径均为0.15~0.30 mm,下同),吸附处理不同pH值(2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0)的Cu2+溶液(40 mg/L,20 mL),震荡吸附360 min,结果如图3所示。
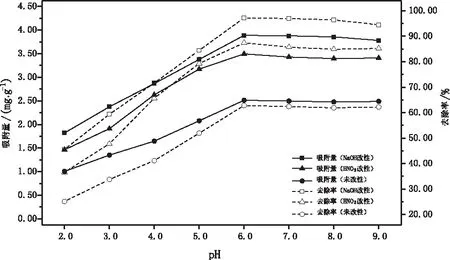
图3 pH值对吸附量和去除率的影响
由图3可知,pH值为2.0~6.0时,生物质活性炭对溶液中Cu2+的吸附量随pH值的升高而增大,且吸附量受pH值变化的影响较大,这主要是由于pH值为2.0~6.0时,pH值越小,溶液中H+浓度越高,高浓度的H+会与Cu2+形成吸附位点的竞争,对吸附过程产生不利影响,因此出现较低的吸附量,而随着pH值的升高,溶液中H+浓度降低,对吸附位点的竞争相对减弱,吸附量就会不断增加[17]。而当溶液pH值过高时会呈胶体状态,不易于固液分离[18]。当pH值为6.0时,NaOH改性、HNO3改性以及未改性的生物质活性炭对Cu2+的吸附量达到最大,分别为3.89 mg/g,3.50 mg/g和2.51 mg/g,此时对Cu2+的去除率也达到最大,分别为97.20%,87.40%和62.80%。在陈钰等[11]的研究中,在pH值为6.0时,玉米秸秆生物质活性炭对Cu2+的吸附量及去除率也达到最大,这与本研究结论一致。故在探究其他因素对吸附效果的影响时,控制实验条件pH值为6.0,能达到较好的吸附效果。在相同pH值条件下,三种生物质活性炭对水溶液中Cu2+的吸附性能表现为:NaOH改性>HNO3改性>未改性。
3.4 吸附时间对吸附性能的影响
在35 ℃条件下,分别取三种生物质活性炭0.30 g,对浓度为40 mg/L的Cu2+溶液(20 mL)进行吸附,震荡时间分别为0,60 min,120 min,180 min,240 min,300 min,360 min,420 min,480 min和540 min,溶液pH值为6.0,结果如图4所示。
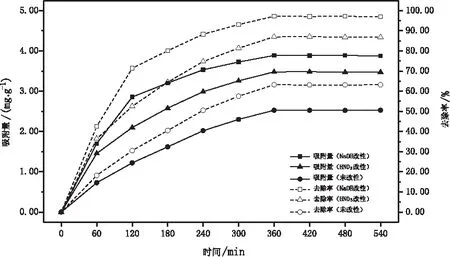
图4 吸附时间对吸附量和去除率的影响
由图4可知,在吸附开始的240 min内,吸附量呈现较大的增长速率,处于快速吸附阶段,这是由吸附剂与吸附质间的范德华力造成的,属于物理吸附占主导的吸附过程[19]。化学吸附过程主要发生在240~360 min内,这时的三种生物质活性炭对Cu2+的吸附速率趋于平缓,这是由吸附剂上活性位点被充分利用或者发生表面吸附引起的[11]。然后在360 min时达到了吸附平衡,此时NaOH改性、HNO3改性和未改性生物质活性炭对Cu2+的吸附量分别为3.89 mg/g,3.48 mg/g和2.53 mg/g,去除率分别为97.20%,87.00%和63.19%。与本研究相比,在陈钰等[11]的研究中,ZnCl2改性的玉米秸秆对Cu2+的吸附平衡时间为480 min,时间稍长。在相同吸附时间条件下,三种生物质活性炭对水溶液中Cu2+的吸附性能表现为:NaOH改性>HNO3改性>未改性。
3.5 等温吸附研究
在15 ℃,25 ℃和35 ℃条件下,分别取三种生物质活性炭0.30 g吸附处理不同浓度(0,10 mg/L,20 mg/L,30 mg/L,40 mg/L,50 mg/L,60 mg/L,70 mg/L,80 mg/L)的Cu2+溶液(20 mL),震荡吸附360 min后,测定Cu2+在不同平衡浓度时的吸附量。应用Origin软件分别对Langmuir和Freundlich模型进行拟合和分析。拟合参数和曲线如表1和图5-7所示。
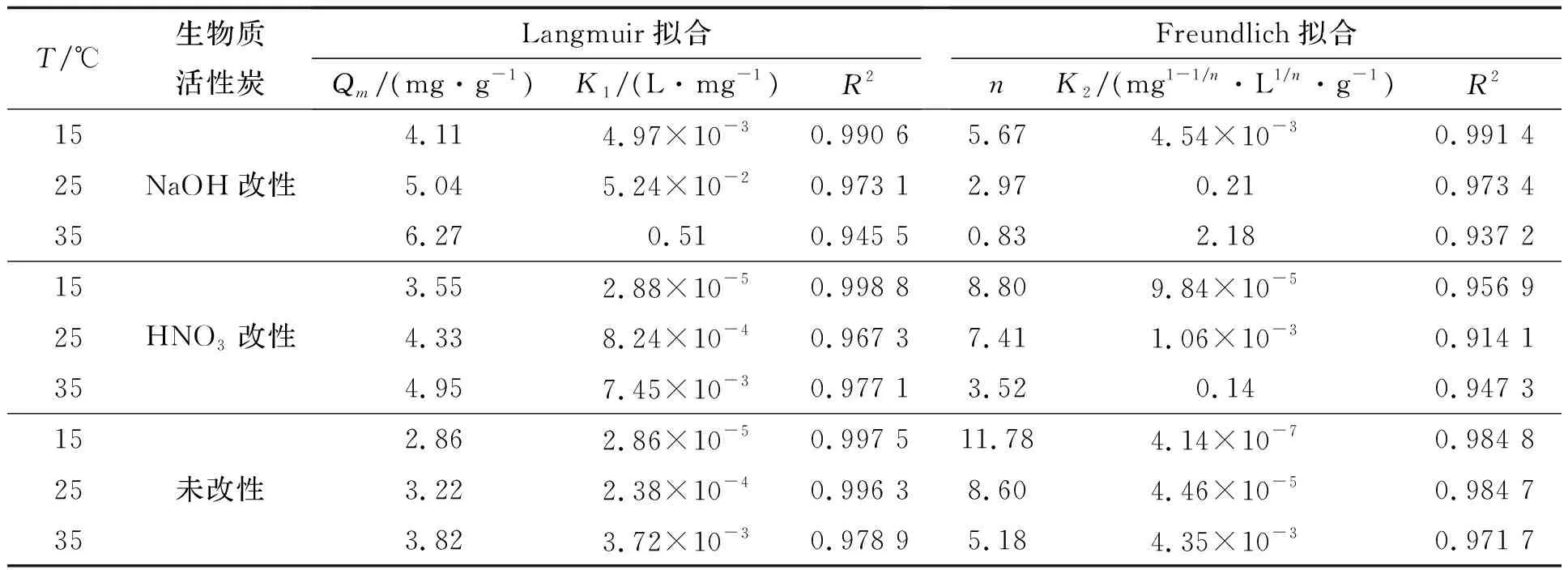
表1 Langmuir和Freundlich模型拟合参数

图5 等温吸附拟合曲线(NaOH改性)
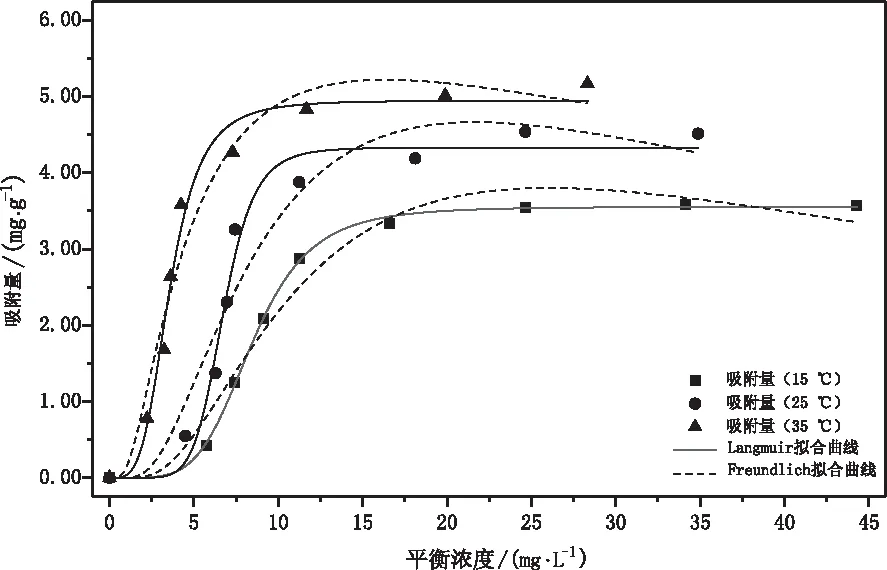
图6 等温吸附拟合曲线(HNO3改性)

图7 等温吸附拟合曲线(未改性)
Langmuir和Freundlich模型都能较好地表征三种生物质活性炭对Cu2+的吸附效果,最大吸附量与理论吸附量值都相差不大。随着温度的增加,Langmuir模型中最大的理论吸附量Qm值与K1值均增大,表明温度增加能促进Cu2+的吸附[20]。Freundlich模型的非线性程度基本上随着n值的增大而增大,表明在15 ℃,25 ℃和35 ℃的条件下,该吸附过程均基本呈现非线性吸附特征。Langmuir模型能更好地表征HNO3改性和未改性生物质活性炭对Cu2+的吸附效果。而对于NaOH改性生物质活性炭,在15 ℃和25 ℃时,Freundlich模型能更好地表征对Cu2+的吸附效果,在张华丽等[21]的研究中,Freundlich模型也能较好地表征碱改性玉米秸秆对Cu2+的吸附,这与本研究结论一致;而在35 ℃时,Langmuir模型能更好地表征对Cu2+的吸附效果,这与徐长伟和刘鑫娜[22]研究的NaOH改性玉米秸秆对Cu2+的等温吸附性能结论一致。
3.6 吸附动力学研究
利用Lagergren准一级动力学方程和准二级动力学方程[式(5)和(6)]来推断三种生物质活性炭对溶液中Cu2+的吸附机理,并应用Origin软件分别对两种动力学模型进行拟合和分析。吸附动力学的拟合参数和曲线如表2和图8所示。
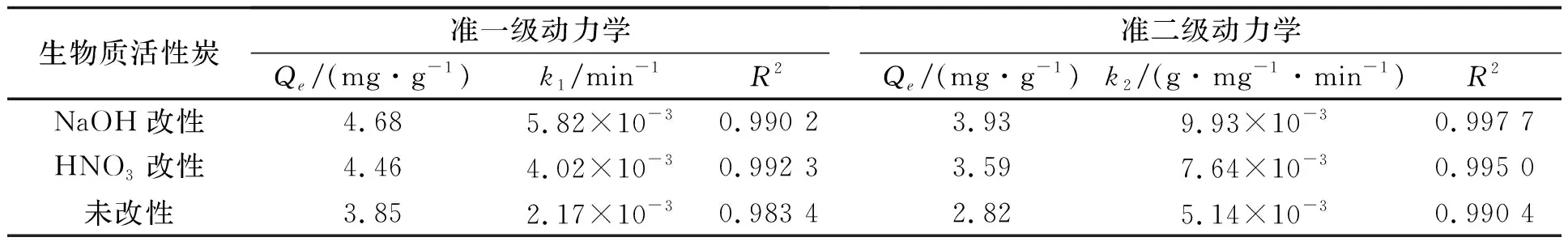
表2 吸附动力学拟合参数

图8 吸附动力学拟合曲线
通过准一级和准二级动力学模型拟合,可以看出两种模型的表征值都比较高,但与准一级动力学模型相比,准二级动力学模型能更好地描述生物质活性炭对Cu2+的吸附过程,这与汪怡等[23]研究的三种改性生物质活性炭对Cu2+,Pb2+的吸附动力学研究结论一致。准二级动力学模型包含了吸附的外部膜扩散、表面吸附和内扩散等所有过程,能更全面地描述生物质活性炭对Cu2+吸附的过程[24]。准二级动力学模型计算出的平衡吸附量(NaOH改性:3.93 mg/g;HNO3改性:3.59 mg/g;未改性:2.82 mg/g)与实验值(NaOH改性:3.89 mg/g;HNO3改性:3.48 mg/g;未改性:2.53 mg/g)相比较,二者相对误差分别为1.02%,3.06%和10.28%,说明吸附过程中有物理吸附和化学吸附两种形式存在,而且主要以化学吸附为主。
3.7 吸附热力学研究
在15 ℃(288.15 K),25 ℃(298.15 K)和35 ℃(308.15 K)条件下,分别取三种生物质活性炭0.30 g对浓度为40 mg/L的Cu2+溶液(20 mL)进行吸附,溶液pH值为6.0,震荡吸附360 min,测定Cu2+的平衡吸附量,并利用Gibbs-Helmholtz方程[式(7)和式(8)]对实验数据进行分析,计算参数见表3。
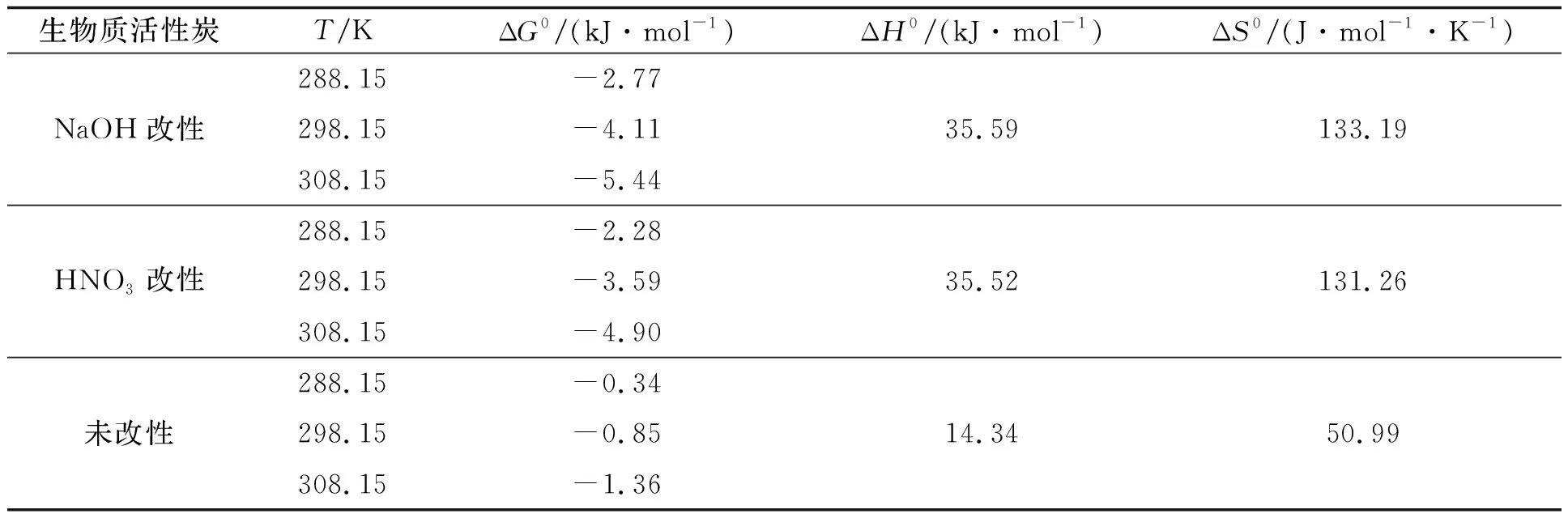
表3 吸附热力学参数
三种生物质活性炭吸附Cu2+实验的表征热力学参数中,ΔG0为负值,表明吸附Cu2+的过程为热力学自发过程[25-26];ΔH0为正值,表明该吸附过程为吸热反应,温度增加有利于吸附的进行[18],这与热力学实验结果一致;ΔS0为正值,固/液界面的无序程度增加,表明生物质活性炭对水溶液中Cu2+有较好的亲和力[27]。实验结果与郑小燕等[28]研究的酒石酸改性玉米芯对Pb2+,Cu2+的吸附热力学的实验结论一致。
4 结论
利用NaOH和HNO3对玉米秸秆生物质活性炭进行改性,并与未改性的生物质活性炭对水溶液中Cu2+进行对比吸附实验。结果表明,当投加量为0.30 g,粒径为0.15~0.30 mm,pH值为6.0,吸附时间为360 min时,生物质活性炭对Cu2+的吸附效果最佳。
三种生物质活性炭对水溶液中Cu2+的吸附均符合Langmuir和Freundlich模型。Langmuir模型中的Qm值和K1值随温度的增加而增大,表明温度增加能促进Cu2+的吸附。Freundlich模型的非线性程度随n值的增大而增大,吸附过程均基本呈现非线性吸附特征。
三种生物质活性炭对水溶液中Cu2+的吸附行为更加符合准二级动力学模型,吸附过程存在物理吸附和化学吸附,并且以化学吸附为主。
吸附热力学实验表明,三种生物质活性炭吸附Cu2+的过程为热力学自发的吸热过程,对水溶液中Cu2+均具有较好的亲和力。
三种生物质活性炭所表现出来的吸附性能均为:NaOH改性>HNO3改性>未改性。因此,NaOH改性生物质活性炭吸附性能最好。
