双轴驱动式人造肛门括约肌系统经皮无线供能
2022-12-01华芳芳颜国正王立超柴川页肖敦玺
华芳芳, 颜国正, 王立超, 柴川页, 肖敦玺
(上海交通大学 电子信息与电气工程学院; 医疗机器人研究院; 上海智慧戒毒与康复工程技术研究中心, 上海 200240)
肛门失禁(Fecal Incontinence,FI)是指机体对直肠内容物丧失蓄控的能力[1],包括感知肠道内容物的性状以及丧失对粪便、气体排出的自主控制能力,是一种临床表现为排便紊乱的非致命性病症,严重影响患者的生活质量.FI的主要治疗方法有药物及物理治疗[2]、括约肌修补术[3-4]、括约肌重建术[5]、骶神经刺激[6]、人工肛门括约肌(Artificial Bowel Sphincter, ABS)以及结肠造口术[7-8],具体治疗方案视患者的具体情况而定[9-10].根据Andromanakos等[11]的调查,美国FI患病率大约为8.41%,其中青少年肛门失禁患病率约为2.91%,而70岁以上老人发病率则高达16.16%,由此可见FI患病率较高且随年龄增加而显著增加.此外,受怀孕、分娩等生理现象影响,女性罹患FI的概率高于男性[12].结合我国人口老龄化加剧的事实,我国FI发病率也值得关注.因此,作为治疗FI新兴方向的人工肛门括约肌的研究显得尤为重要.Wilt等[13]受AMS800在治疗小便失禁中疗效显著的启发,研制了人工肛门括约肌并进行临床应用.随后,磁珠链人工肛门括约肌[14]、形状记忆合金型人工肛门括约肌[15]以及仿耻骨直肠肌式人造肛门括约肌[16]等装置应运而生.但人工肛门括约肌在医疗中的实用价值受到难以系统长期稳定供能的限制,因此,系统安全稳定且长期的能量供给尤为重要.现有的人造肛门括约肌系统在长期植入动物体内的能量供给方面仍有较大研究空间.
本文研究的双轴驱动式人造肛门括约肌(Biaxial Actuated Artificial Anal Sphincter,BAAS)系统作为一种原位植入式生物医疗器械,除了使得FI患者能像正常人一样感知排便需求,并可以选择合适的时间、地点进行排便外,还集成了压力数据采集、便意感知等多种辅助患者康复的功能,但相较其他括约肌系统功耗较高.基于系统较高的功耗和长期在体内工作的需求,BAAS体内执行装置使用可充电锂电池,并采用经皮无线供能[17-18](Transcutaneous Wireless Energy Transmission,TET)系统保证BAAS各项功能工作时稳定、充足的能量供应.TET技术的使用为人工肛门括约肌系统应用带来很多优势:
(1) TET系统可以减小电池尺寸,进而缩小体内无线能量接收端的体积,为系统植入提供便利,并提高系统生物安全性.
(2) TET系统不仅可为体内电池充电,还可替代体内电池直接为体内执行机构供能,双重保障增加系统可靠性.
(3) TET系统的搭建较为简单,并具有较高的传输效率,且便于随身携带,方便患者随时使用.
大量活体实验表明,TET系统接收线圈植入部位受增生包裹影响,发射线圈与接收线圈耦合性能明显低于体外实验,耦合距离不断增加,且存在传输角度等问题,传输效率明显下降并伴随发热现象,严重影响该系统生物安全性[19].因此,BAAS系统的TET供能在提高传输功率、降低发热等方面还有很多工作需要进一步研究.针对现有TET系统存在的增生包裹导致的传输角度等问题,本文对现有TET系统的参数进行分析研究,实现系统长期稳定的能量供给.
1 TET系统
BAAS系统的TET主要分为体内无线能量接收端与体外无线能量发射端,采用耦合谐振的能量传输方式为封装在体内控制模块的可充电锂电池充电[20-21].体内无线能量接收模块主要由整流滤波、体内控制电路组成,其中体内控制电路主要包括稳压模块和充电模块.为了便于患者随身携带,体外无线能量发射端通过可充电聚合物锂电池组供电,主要由稳压模块、方波发生模块、电压电流检测电路、全桥逆变模块组成.输出端通过LC串联调谐与线圈相连,体内能量接收部分为同样谐振频率的LC串联谐振电路,其等效模型如图1所示.图中:Lt为发射线圈电感;Ct为发射线圈电容;Vt为发射线圈电压;It为发射线圈电流;Rt为发射线圈等效电阻:Lr为接收线圈电感;Rr为接受线圈等效电阻;RL为负载电阻;Cr为接受线圈电容;Ir为接受线圈电流.
两线圈对心并保持较近的距离,通过磁感应耦合进行能量传递.最大耦合传输效率[22]为
(1)
(2)
(3)
α=RL/Rr
(4)
式中:α为负载因子;k为链路耦合系数;Q1为发射线圈空载品质因数;Q2为接收线圈空载品质因数;ω为谐振频率;M为互感.
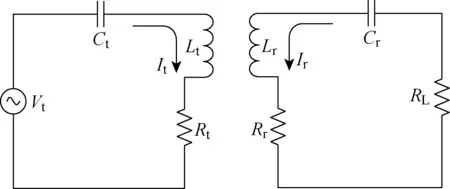
图1 TET系统等效模型Fig.1 Equivalent model of TET system
2 TET系统的测试实验及结果
在人工肛门括约肌系统中,TET系统的性能直接影响体内执行机构的能量供给能力,本文将接收线圈、锂电池、整流滤波模块以及体内控制电路等封装为直径约50 mm、厚度约5 mm的体内无线接收端,植入于动物腹部皮下组织.研究所使用的实验动物为小香猪,其体重约为25 kg,年龄为0.5 a.然而,在系统长期植入过程中,由于动物体自身的排异反应,体内无线接收端被组织增生包裹(见图2),导致发射线圈与接收线圈之间存在耦合角度且耦合距离增加,致使能量传输效率明显低于体外实验并产生发热等问题.
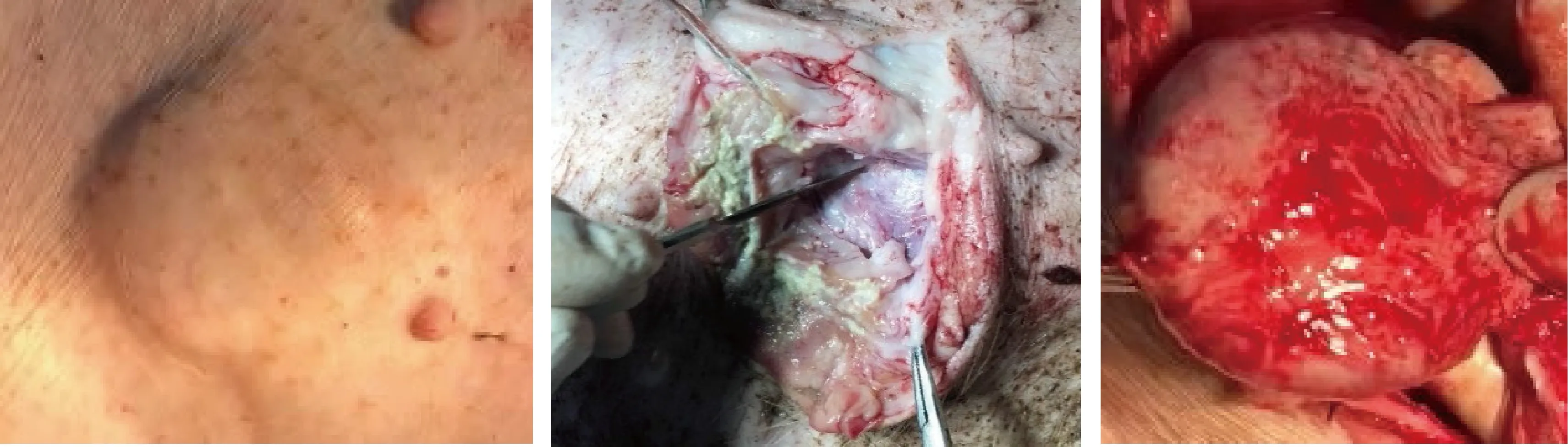
图2 体内无线接收模块组织增生包裹情况Fig.2 Hyperplasia of parcel of wireless receiving module in vivo
本文结合现有BAAS系统中TET系统的实验结果,对现有TET系统的参数进行分析并优化.同时,对TET充电模块充电过程中产生的热量进行分析,以确保TET充电模块符合生物安全要求.
2.1 接收线圈与发射线圈的参数确定
设TET模块的传输效率为
(5)
式中:P1为发射端的总功率;P2为接收端的总功率;U1为接收线圈与发射线圈之间发射端的互感电压;I1为发射端的电流;U2为接收线圈与发射线圈之间接收端的互感电压;I2为接收端电流.由文献[23]有:
U2=ωNAμH
(6)
式中:N为接收线圈匝数;A为接收线圈面积;μ为磁导率;H为磁场强度.
对同一线圈而言,增加铁氧体厚度有助于增加线圈产生的磁场强度以及线圈之间的耦合系数,且接收线圈面积A应尽量增大,以提高传输效率.
在确定了接收线圈的线圈结构以及线径、匝数、隔磁片厚度等参数的基础上,优化发射线圈的线圈结构.设Na和Nr分别为两个典型线圈匝数,每匝线圈的半径为ai和rj,其自感L由所有单匝线圈的电感值与各匝线圈之间的互感组成[24],表示为
(7)
式中:L0为各匝自感;R为单股铜线的线径×股数的总线径;M0为匝间互感;d为线圈间距;δi, j为各匝之间变化量.
而磁片对线圈的电感增强[25]为

(8)
式中:λ(t)为材料特性函数;μ0为空气磁导率;T(x)为几何函数,定义如下:
(9)
式中:J1为第一类一阶贝塞尔函数.其互感的增强[26]可表示为
(f(λ)+g(λ))dx
(10)
(11)
(12)
式中:t1为接收线圈磁片高度;t2为发射线圈磁片高度.
螺旋结构的铁芯材料为锰锌.针对现有BAAS中TET系统的参数进行进一步分析,接收线圈确定为由50股单股铜线(线径0.05 mm)组成的丝包Litz线,其线圈匝数为45,线圈外径为 48.6 mm,线圈结构为单层平面线圈,磁片厚度为 0.5 mm.发射线圈确定为由150股单股铜线(线径 0.05 mm)组成的丝包Litz线,其线圈匝数为30,线圈结构为螺旋线圈,铁芯尺寸为直径50 mm、高45 mm,其具体参数如表1所示.表中:D为磁片厚度.根据表1所示的线圈参数,绕制1组发射线圈与3组接收线圈,并使发射线圈对其3组接收线圈分别进行充电耦合试验,传输效率如图3所示.
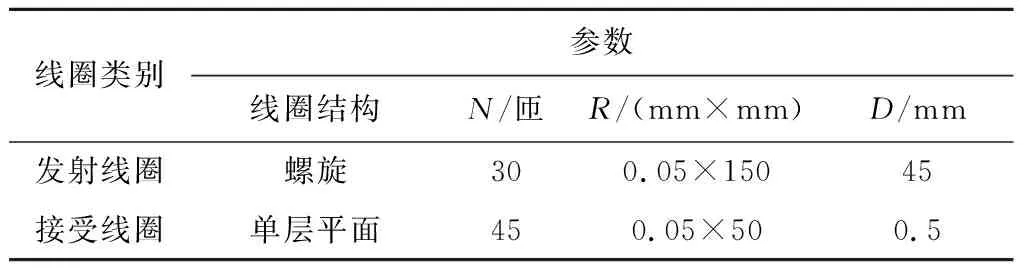
表1 发射线圈与接收线圈的具体参数
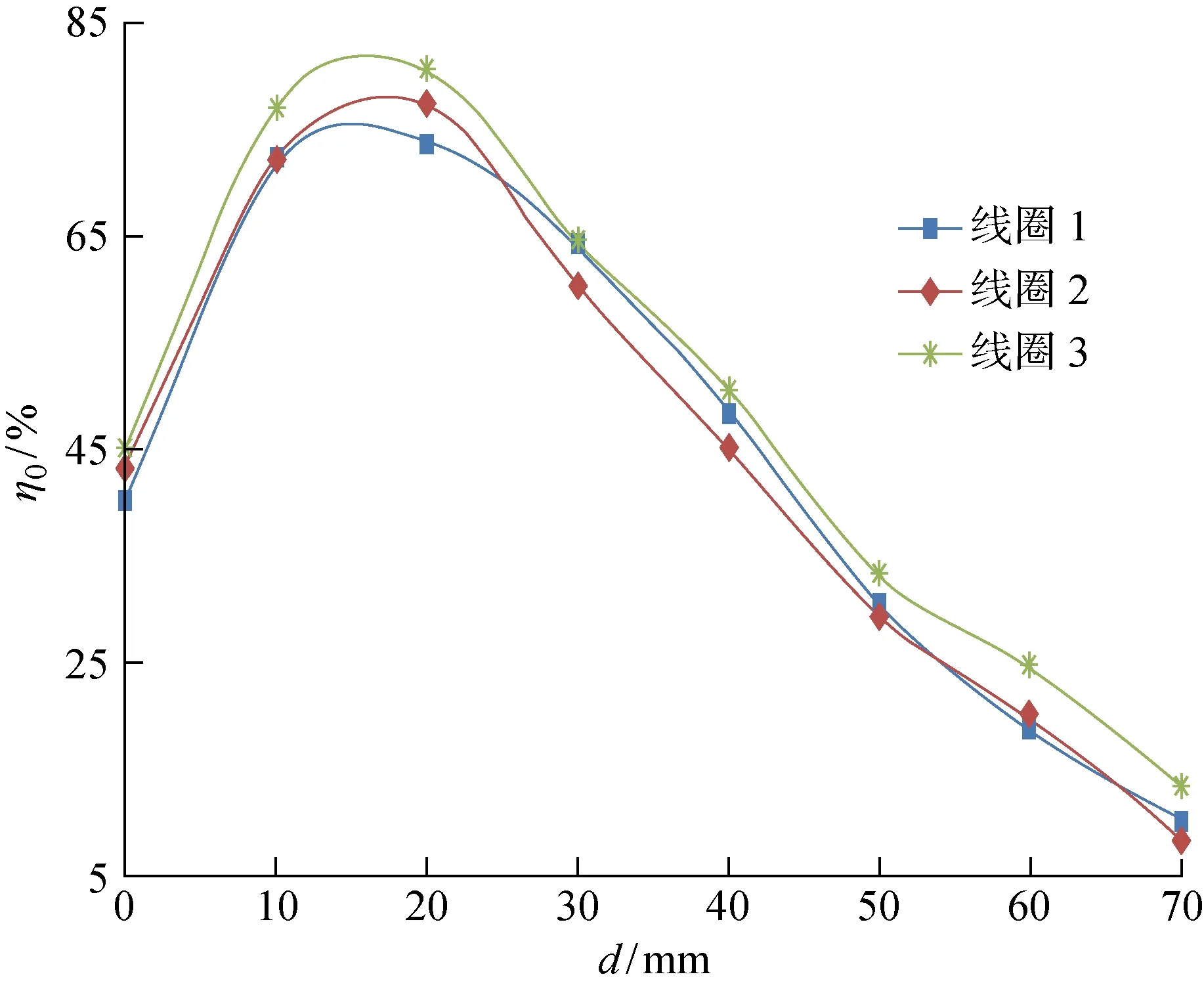
图3 接收与发射线圈的传输效率Fig.3 Transmission efficiency of receiving and transmitting coils
由图可见,在平行且对心状态下,当传输距离为20 mm时,线圈1、2、3的传输效率分别可达到73.88%、77.19%、80.35%.当传输距离为30 mm时,线圈1、2、3的传输效率仍分别达到64.38%、60.33%、64.38%.
2.2 传输角度的实验研究
TET系统的接收线圈植入活体后,由于组织增生的包裹,充电时不一定会达到完全平行对心状态,会产生一定的传输角度,所以保持发射线圈不变,改变接收线圈的接收角度,对TET系统进行传输角度实验.将传输距离设为30 mm,不同传输角度下的传输效率实验结果如图4所示.图中:Al为传输角度.
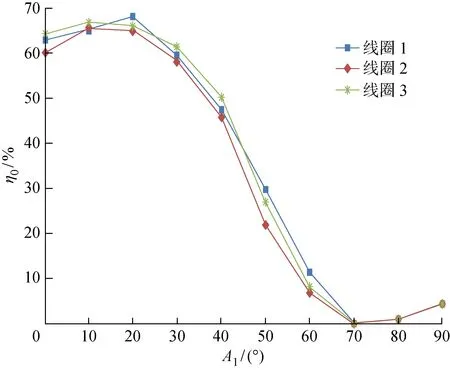
图4 不同传输角度下的传输效率实验结果Fig.4 Experimental results of transmission efficiency at different transmission angles
由图可见,3组实验结果表明,传输角度为20°时,线圈1、2、3的传输效率分别可达到68.19%、65.35%、66.42%,均值为66.65%.传输角度为30° 时,线圈1、2、3的传输效率分别可达到59.78%、58.67%、61.44%,均值为59.96%.当传输角度为70° 时,传输效率基本降为0%.由活体实验可知,动物腹部皮下组织较柔软,在实际充电过程中,可手动调整有组织增生包裹后的接收端位置,而组织增生包裹的角度一般不超过30°.因此参数满足BAAS系统性能要求.
3 TET系统的充放电实验
在设计TET系统时,为延长单次充电后系统的工作时间,并减少电池充电次数来延长电池寿命,提高临床患者的实用性,对BAAS系统采用较大容量的950 mA·h锂电池为体内执行机构供电,并设计了低功耗模式.将体内无线接收端包裹在带皮的小香猪肉内,体外无线发射端与猪肉表皮直接接触,并在体内无线接收端与体外发射端接触的猪肉部分安装温度计以便随时观察温度变化.由于研究所使用的实验动物为小香猪,在使用TET系统给体内执行机构充电的过程中配合度不高,所以选择持续性充电方式而减少充电次数.
利用TET系统对BAAS进行5次重复充放电实验,其中电池完全充满电(电池电压达到 4.15 V以上且稳定不变视为完全充满)与电池完全放电完成(电池电压达到3.6 V以下且机构不能正常运行视为完全放电完成)为一次充放电实验,充电距离设为20 mm,最终取其平均值绘制锂电池的充电放电过程曲线,如图5所示.图中:ti为充电时间;tj为放电时间;U为电压.
设充放电实验进行5次重复性实验,即Nm=5,总体标准差为
(13)
剩余误差εl为
(14)
由于充放电实验的数据样本满足3σ原则,即εl<3σ,所以充放电实验稳定性满足要求.
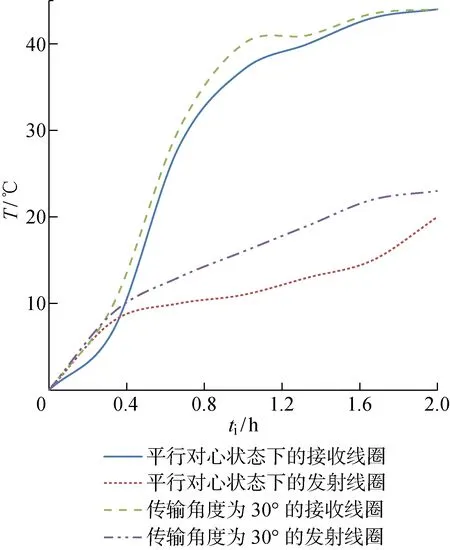
如图5(a)所示,系统充电时长约为2 h,主要分为涓流充电、恒流充电以及恒压充电3个阶段,其中 3.57 V≤U≤3.78 V为涓流充电,充电时间为0.4 h;3.78 V 图5 电池充放电实验结果图Fig.5 Charging and discharging test results of battery 线圈充电时的温度曲线如图6所示.图中:T为接受线圈温度.在平行且对心状态下,当传输距离为20 mm时,充电过程中体内接收线圈的温度变化范围为0~44 ℃,其中,温度增长较快的时间段为充电后的0.2~0.8 h,由3 ℃增长至35 ℃.体外发射线圈的温度变化范围为0~20 ℃,变化比较平稳.在传输角度为30°的状态下,充电过程中体内接收线圈的温度在充电后的1 h内,由0 ℃增长至40 ℃,体外发射线圈的温度比平行对心状态下的温度平均高 4.2 ℃,相对于平行对心状态下发射线圈充电时的温度增长了13%.人的体表温度为36.5 ℃,增长后的充电温度仍在人体可承受温度范围之内,不会造成低温烫伤的情况.体内接收线圈充电过程中的温度变化对生物体的影响会因生物体内自身的散热机制而降低,因此,在传输角度为30°时仍满足BAAS系统性能要求. 图6 接收线圈充电时的温度曲线Fig.6 Temperature curve of receiving coil 结合BAAS系统,针对受组织增生包裹导致的传输角度及发热等问题,本文对现有TET系统的参数进行分析研究.实验结果表明,在传输距离为30 mm条件下,传输角度为20° 时,实验的传输效率均值可达到66.65%;传输角度为30° 时,实验的传输效率均值可达到59.96%.在实际充电过程中,可手动调整有组织增生包裹后的接收端位置,而组织增生包裹的角度一般不超过30° .传输角度为30° 时,发射线圈充电温度最大值为23 ℃.人的体表温度为36.5 ℃,增长后的充电温度仍在人体可承受温度范围之内,不会造成低温烫伤的情况.因此参数满足BAAS系统性能要求,达到了在传输距离较远时仍可高效率传输能量的目的.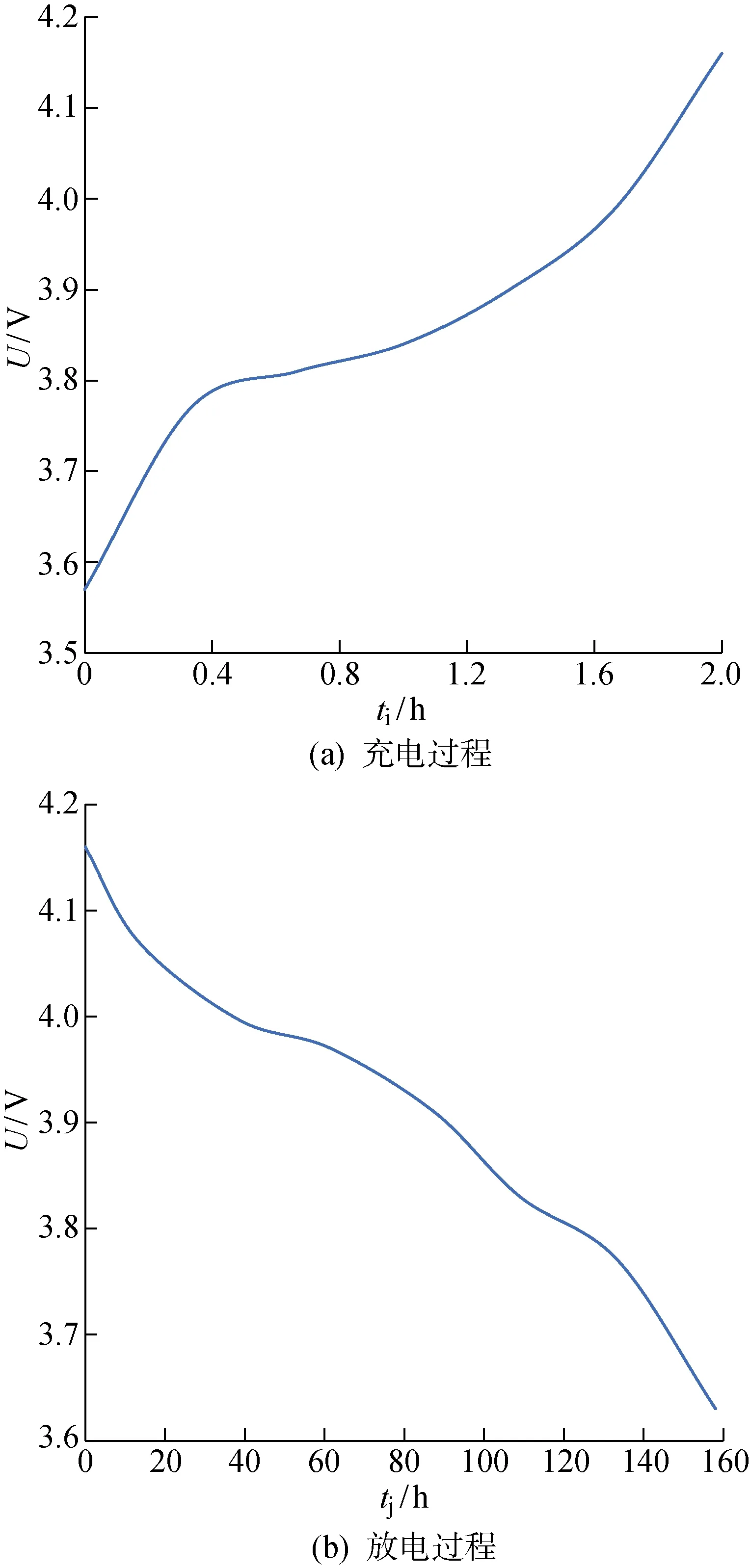
4 结语
