超声中心肌做功参数的正常参考值范围及临床应用研究进展
2022-11-29冯晓玄冯颖青
冯晓玄,冯颖青
1南方医科大学第二临床医学院,广东 广州 510515;2广东省医学科学院//广东省人民医院心内科//广东省心血管病研究所,广东 广州 510080
心肌收缩功能的评估有助于评价临床心血管疾病,评估心肌收缩功能的最优指标也一直在探索。目前最常用于评价收缩功能的参数是左室射血分数(LVEF)。心肌运动不是单纯的收缩和舒张,还包括了三维空间的扭转、旋转、圆周、径向、纵向运动等[1-2],LVEF是通过心室容量变化计算获得,在一些特定疾病或左心室收缩功能存在细微变化时并不能真实反映出心肌收缩力,且受左室后负荷的影响[3-4]。心肌应变技术主要通过整体纵向应变(GLS)参数评估心肌功能,对心肌梗死后患者左室收缩功能障碍具有较高的敏感度和特异性[5],在早期更客观地反映整体和局部心肌功能的变化,还能作为改善慢性心衰患者危险分层的工具[6]。但从研究结果上看,GLS仍然无法解决后负荷依赖的问题[7],心肌应变值降低,可能是由于后负荷的增加引起,而并不直接指向心肌收缩力下降。有学者以犬为实验对象进行研究,构建主动脉缩窄模型使左心室压力增加约30 mmHg,比较后负荷增加前后GLS和心肌做功(MW)的变化情况[8],发现GLS值有明显的受损(3%~4%),而左室压力-应变环(PSL)面积没有发生明显变化(<0.5%)。为了更准确评估心肌功能,心肌做功(MW)技术越来越受到重视[9]。MW克服了LVEF和GLS共同存在的负荷依赖问题[10],通过二维斑点追踪技术(2D-STE)、超声心动图、左上臂肱动脉血压数据,无创量化MW,为心血管疾病的诊断及预后评估带来新的应用前景。本文就目前对MW技术评价心血管疾病心肌功能的应用展开综述。
1 MW原理与主要参数
MW技术利用超声心动图在2D-STE的基础上与无创肱动脉血压结合来评价心血管疾病。2D-STE的原理是细小组织由于反射、衍射、干扰等原理,产生回声斑点,对心肌组织的斑点回声进行追踪,通过每一帧像之间的位置关系描述心肌的三维运动轨迹,此项技术相较于组织多普勒更准确、更客观[11]。为了消除后负荷对心肌功能的评价影响,有研究首先从心肌能量学角度出发,用氧耗代替心肌收缩的总机械能变化[12],提出心室的压力-容积环[13-14]形成的压力-容积面积可量化心室收缩总机械能,同时还可以估算节段心肌收缩的氧耗情况。然而压力-容积面积的获得是一项对于心室参数测量的有创操作,在动物实验上有一定的操作空间,临床实践上有极大的困难,因此利用常规超声心动图获得做功参数会更为现实和方便。
为避免有创性操作,有学者提出用无创方法得到的左室压力-应变环(PSL)代替,将负荷和应变均纳入到研究当中[15]。左上臂肱动脉血压非侵入性地估计得到无创左室压力曲线(力),利用2D-STE测量应变值(距离),二者建立起左室PSL,可计算出整个心动周期中左室各个节段随时间变化的MW。左室PSL与有创测量结果具有很高的一致性,可以反映出心肌代谢和耗氧量,与氟-脱氧葡萄糖正电子发射断层扫描对心肌糖代谢的描述显著相关(r=0.81,P<0.05),因此MW可以间接反映心肌能量代谢情况,通过心肌能量代谢情况定量评估左室的收缩功能。近来一些研究也证实了MW用于评估左室收缩功能的可行性[16-17],有学者总结了MW从理论到临床实践的路线图,其中涵盖了多种疾病,包括未发生心脏重构的高血压、心肌病、ST段与非ST段抬高型心肌梗死、心脏再同步化治疗、心肌淀粉样变性等,均支持使用MW评估左室收缩功能的可行性、可靠性以及临床的可实践性[18]。
无创左室压力曲线的获得依赖于左室压力参考曲线。首先,用超声心动图确定多个病种患者二尖瓣和主动脉瓣的打开与关闭时间,并获得他们单心动周期的有创左室压力曲线;再将获得的所有有创左室压力曲线沿时间轴进行拉伸或者压缩,使得所有有创左室压力曲线的瓣膜开闭时间重合;最后将所有有创左室压力曲线都按垂直方向进行缩放,使其具有相同的峰值,继而得到一条左室压力参考曲线[19]。因此,左室压力参考曲线通过汇集所有情况下的单周期左心室压力曲线,通过上述三个步骤利用瓣膜开闭时间对每个压力曲线进行平均化处理计算获得。无创左室压力曲线基于左室压力参考曲线,通过测量个体实际的瓣膜开闭时间,并通过拉伸或压缩左室压力参考曲线的时间轴来调整等容收缩期、射血期和等容松弛期的时间间隔,使之与个体测量的时间间隔相匹配,同时对左室压力参考曲线压力轴进行垂直方向的缩放调整,使之与个体测量的左上臂肱动脉血压相匹配,最后得到一条特定对象的左室压力曲线。因此,左室压力参考曲线可被用于预测特定对象的左室压力[19]。
左室应变的获取主要依赖于GLS。将采集到的标准心尖二腔、三腔及四腔心切面图像(至少3个心动周期,帧频>60帧/s)导入EchoPac软件进行自动分析,即可自动得到GLS。
因此,左室PSL是二尖瓣关闭至开放之间沿逆时针方向形成的闭环,其面积近似于整体的MW。实际上,通过对应变曲线进行微分得到应变率,与同步瞬时心室压力相乘得到瞬时功率,再将该功率进行随时间的积分即得到MW随时间变化的曲线函数,通过该曲线函数即可获得瓣膜开闭时间段的MW值。
通过对各节段的做功指数(WI)、有用功(CW)、无用功(WW)和做功效率(WE)进行平均值计算得到MW的4个主要参数:(1)整体心肌做功指数(GWI):二尖瓣关闭至开放之间,心室PSL区域内的总做功;(2)整体心肌有效做功(GCW):收缩期心肌收缩缩短所做功和等容舒张期心肌拉长的负功之和,有利于心肌射血;(3)整体心肌无效做功(GWW):与GCW相反,是收缩期心肌拉长和等容舒张期心肌缩短所做的功,不利于心肌射血;(4)整体心肌做功效率(GWE),计算公式为:GCW/(GCW+GWW)×100%,心肌在整个心动周期中的做功效率。根据以往文献报道,GWI与耗氧量密切相关(P<0.05),且与其它指标相比更为重要,而GCW次之[20-21];GWI=GCW-GWW,GWW可依赖GWI和GCW进行综合反映;心肌收缩功能降低时,由于GCW和GWW成比例增加[21],GWE可得到保留。
2 MW技术在健康个体中的研究
目前在不同健康人群中对MW参数正常值范围的研究进展(表1)[22-23]。其中多项研究[22-25,27]认为,GWI、GCW与收缩压呈正相关关系,与GLS呈负相关关系(P<0.05),有的研究结果显示GWI、GCW与GLS呈正相关关系(P<0.05)[26]。部分研究认为GWI和GCW与年龄具有显著相关性[23,29-31];在不同性别之间,有研究认为女性的GWI和GCW高于男性[22-23,26],且女性GWI随着年龄的增长而显著增加[23,29-30],然而这种性别差异在儿童及青少年群体中表现并不突出;更有学者提出在儿童群体中使用年龄和体表面积进行参数校正以计算GWI和GCW的正常值参考范围[32]。小样本量的数据提出的参考范围可能存在人群选择偏倚,希望未来可以有大样本的正常人群数据以供参考。
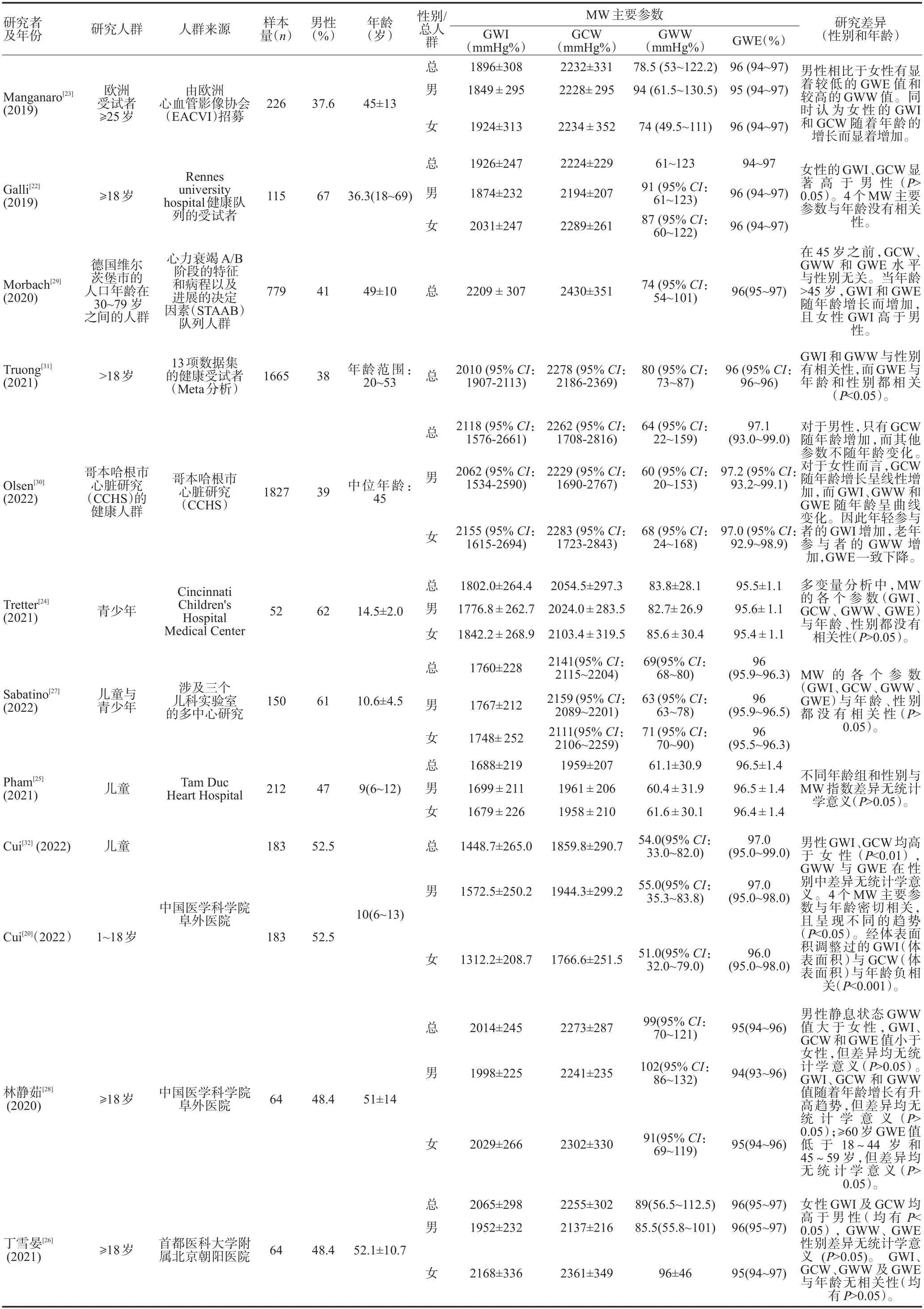
表1 不同健康人群中对MW参数正常值范围Tab.1 Normal value range of MW parameters in different healthy populations.
3 MW技术与心血管疾病的研究进展
3.1 MW技术与高血压疾病
在评估高血压患者左心室收缩功能时,通常考虑两方面因素的影响,一个是心肌重构(肥大和心肌损伤),另外一个是负荷条件(应变的负荷依赖性)[33],根据Frank-Starling机制和自动调节机制可知长期暴露于增加的后负荷,左室经历了结构和功能重塑,心肌耗能增加,而心肌收缩功能变化在高血压早期则难以被发现的。在评估高血压患者的整体左室收缩功能时,受到负荷条件的影响,常规检测指标LVEF和GLS显示正常值,但MW反映心肌耗能的结果有异常。研究发现,与健康人相比,中重度原发性高血压患者的GWI显著升高,由于GCW 和GWW 成比例增加,高血压患者的GWE才得以保留[21]。总体心肌收缩功能由于代偿的存在而表现正常,然而MW从区域应变值中可看到节段性心肌变形仍存在显著差异[34]。有研究计算了高血压患者整体和心尖、中部和基底区域的MW;在区域应变值中看到的心尖到基底部梯度保留在心肌功的分布中,心尖区域补偿了基底段的损伤,且这种功能重新分布在局部基底间隔肥大患者中更为明显;在这些患者中,节段MW分析揭示了与急性负荷条件无关的区域性工作的潜在损害[34]。因此,MW比GLS具有更高的敏感度,即使从整体上尚未发生心肌重构,MW仍能够检测亚临床左室收缩功能障碍[35],这是因为MW指标存在可评估节段性心肌功能的特性,更有利于克服负荷影响,在心肌重构发生的早期阶段对心肌收缩功能进行评估。
高血压可导致心肌重构的发生,应用MW参数对节段性心肌功能评估特点,可评估不同心肌重构类型的心肌工作情况。有学者将左室重构分为4种类型:正常构型、向心性重构、偏心性左室肥厚、向心性左室肥厚。研究发现,偏心性和向心性左室肥厚患者的MW高于正常左室几何结构和向心性重构患者,偏心性和向心性左室肥厚患者的GWI和GCW功高于正常左室几何结构和向心性重塑患者,不同左室几何结构组之间的GWW和GWE相似[36]。
有研究表明,MW与心肌峰值耗氧量有确切的相关性,与性别、年龄、BMI、左室结构和功能参数无关,高血压患者的心肌峰值耗氧量增加[20]。与健康组及控制良好的高血压患者组相比,未控制和顽固性高血压患者的GWI更高,所有高血压患者的GCW也高于健康组,而GWW和GWE在不同组之间相似。对顽固性高血压及血压控制欠佳的患者而言,完善MW检查可以更早发现心肌收缩功能障碍,并开始强化治疗,避免心脏功能恶化。
综上所述,当血压值在较高水平时,左室心肌需要更多的氧耗来满足增加的后负荷所产生的代谢能量。MW技术不仅能在早期检测高血压患者亚临床左室收缩功能障碍,评估不同心肌重构类型的心肌工作情况,还能评估高血压患者的血压控制情况,调整治疗方案。
3.2 MW技术与心肌病
心肌病是一大类累及心肌组织,临床以心脏结构异常、心力衰竭和(或)心律失常为特征的疾病,一般根据病理和解剖学标准进行分型分为三型,其中扩张型心肌病(DCM)和肥厚型心肌病(HCM)是临床上较为常见的两种类型[37]。
扩张型心肌病以左心室或双心室扩张并伴收缩功能受损为特征[38],病理基础是心肌变性、萎缩和纤维化,心肌纤维化与死亡、心律失常事件、住院和猝死的风险增加有关[39]。既往已有研究认为MW参数可以作为评价扩张型心肌病整体心肌收缩功能的指标[21,40-41]。近来有研究认为DCM患者治疗后与治疗前相比GWI升高(P<0.05),而GCW、GWW、GWE治疗后变化无统计学意义(P>0.05),LVEF和GLS在治疗后没有显著变化,因此未来可通过测量MW参数评估治疗效果[40]。心肌纤维化程度作为评估预后的重要指标,临床上一般使用心脏磁共振成像(CMRI)晚期钆增强作为金标准进行检验,然而在遇到显著慢性肾脏疾病、不兼容的金属设备或幽闭恐惧症等禁忌证患者时,CMRI晚期钆增强可能并不适用。有研究表明CMRI、GLS、GWI、GCW 和GWE与心肌纤维化均有独立关联性,且CMRI和GCW显示出比GLS更高的准确性、敏感度和特异性,根据预测左室心肌纤维化的准确性从高到低排名为CMRI、GCW、GWE、GWI 和GLS[42],在未来的进一步的研究中,MW有望作为评估DCM患者心肌纤维化程度的替代指标。
肥厚型心肌病以左心室和(或)右心室肥厚为特征,常为不对称肥厚并累及室间隔,典型者左室容量正常或下降,常有收缩期压力阶差[38],病理基础是心肌排列紊乱,间质纤维化的改变。HCM患者的心肌功能同样可以用MW参数进行评估,甚至还能预测不良事件(联合终点包括全因死亡率、心脏移植、心力衰竭住院、流产的心源性猝死和适当的植入式心律转复除颤器)发生率。有研究发现非阻塞性HCM患者相比健康者GCW、GWE和GWI显著减少,而GWW显著增加,GCW>1730 mmHg%(中值)的患者比总体GCW<1730 mmHg%的患者经历了更高的无事件生存率(P<0.001)[43]。HCM预后同样涉及心肌纤维化的评估[44],与DCM相似,MW有望成为评估心肌纤维化程度的一项替代指标。
未来,MW技术有望通过评估心肌纤维化程度为心肌病患者预后提供一定的临床参考价值,经过更多的研究证实成为对心肌病患者预后评估的一项替代指标。
3.3 MW技术与冠心病
急性冠脉综合征作为冠心病的重要组成部分,系不稳定性冠状动脉粥样硬化斑块破裂、血栓形成,引起急性心肌缺血的一组临床综合征;在临床实践中,具有病情变化快、临床表现及危险性差异极大的特点,加强早期识别、危险分层并采取积极、合理的干预措施显得尤为重要[45]。在一项评估ST段抬高型心肌梗死患者从基线检查(指数梗死)到3月随访期间MW参数的演变研究表明[46],ST 段抬高型心肌梗死患者GWI、GCW 和GWE的演变可能反映心肌顿抑,而GWW的稳定性可能反映永久性心肌损伤和不存活瘢痕组织的发展。
有学者纳入126名非ST段抬高型心梗患者,在冠状动脉造影前进行节段性应变分析,发现节段WI可以通过识别功能失调节段的数量来确定急性动脉闭塞,通过设置节段WI和应变的经验截断值判断心肌的节段性收缩功能障碍,且具有很高的敏感度和特异性,可作为急性冠状动脉闭塞的诊断指标,加强对冠心病的早期识别[8]。
ST段抬高型心肌梗死会发生心室重构,不良的左室重构与不良预后相关,因此早期识别左室重构具有重要作用。Lustaso团队在一项纳入已接受直接经皮冠状动脉介入治疗和最佳药物治疗的350例患者回顾性研究中发现,在早期左室重塑患者中,罪犯区域的WI显著降低,有利于从区域性识别早期的心室重构,采取积极合理的干预措施,改善预后[47]。一项纳入了197名接受经皮冠状动脉介入治疗且LVEF≤40%患者的研究发现,随访6月后,GWI值越高,LVEF正常化(≥50%)的可能性越大,且GWI≤750 mmHg%,全因死亡率高,因此MW参数还能应用在预后评估,使后续治疗方案具有预见性[48]。
由上述可见,MW技术不仅能评估梗死后心肌功能变化情况,还能加强对缺血节段心肌的早期识别和危险分层,有利于尽早采取积极、合理的干预措施,改善患者预后情况,MW参数还能对患者进行预后评估,为后续治疗方案提供参考价值。
3.4 MW技术与心脏在同步化治疗(CRT)
CRT是慢性心力衰竭一种不可或缺的治疗手段,在传统起搏基础上增加左心室起搏,目的是恢复心室间及心室内运动的同步性,协助心肌排血,有利于逆转心肌重构、降低心衰住院率和死亡率[49]。有研究显示,在我国临床实践中,即使严格按照指南选择患者,仍至少有30%患者对CRT治疗无应答,即临床表现、心脏结构及血流动力学情况均无明显改善[50]。目前尚缺乏对CRT术后反应率的评估,虽然已有大量临床证据表明,QRS的宽度和左束支阻滞波形是决定CRT术后反应率的重要因素[49],然而其预测判读尚未具有统一标准,且QRS宽度和左束支阻滞波形依赖心电图质量以及读图者专业水平。
一项纳入97名患者的研究表明GCW<1057mmHg%可识别85%的无反应者,阳性预测值为88%[51];另外一项纳入166名患者的多变量Cox回归分析研究表明[52]CW≤888 mmHg%是心脏死亡率的唯一独立预测因子(OR=4.23,P=0.03)。
有研究认为确定MW作为CRT反应预测因子背后的概念源于不同步心脏的特征性收缩模式:早期激活区域在主动脉瓣打开之前开始缩短,从而拉伸后期激活区域[53]。由于局部Frank-Starling 效应,这种早期收缩期的拉伸使晚期激活的区域收缩得更加有力,而这种更强的收缩导致早期激活区域在收缩中期拉伸。这种模式体现在间壁(S)和左室侧壁(LW)形成的相互作用,对侧间壁-左室侧壁相互作用的典型模式导致了左束支阻滞心脏的间壁-左室侧壁的功差异。换言之,间壁作为早期激活区域,侧壁作为晚期激活区域,当侧壁心肌功能足够强时,间壁心肌在收缩中期被拉伸。早期激活的间壁在收缩中期反弹拉伸导致无效做功(负值)增加,而收缩期预拉伸导致晚期激活的侧壁MW增加[54]。研究认为这种对侧拉伸和缩短的机械行为不仅表明电激活延迟,还强烈表明心肌具有良好的收缩功能。且间壁-左室侧壁做功差值越大,越能表现其良好的整体心肌活力和收缩功能。因此研究认为,间壁和侧壁MW之间的差值可预测CRT反应(6月后左室收缩末期容积减少>15%),且AUC为0.77(95%CI:0.70~0.84)。
因此,MW技术有望成为补充患者CRT治疗应答反应评估新的非侵入性工具,通过计算间壁和侧壁MW之间的差值,预测CRT反应。然而目前仍需要更大样本量及多中心的研究结果确定MW参数预测CRT反应阈值,才能使MW技术真正成为指导临床准确诊疗的可靠方法,降低患者不必要的手术操作和诊疗支出,为患者提供更有效的治疗指导。
3.5 MW技术与心脏淀粉样变性
淀粉样变性是一类以淀粉样蛋白异常沉积系统性疾病,可累及心脏,淀粉样物质沉积和浸润肌细胞外间质和血管周围[55],导致心肌细胞萎缩,心肌壁和室间隔肥厚[56],预后较差。
有研究发现,与健康对照组相比,静息状态下心脏淀粉样变性患者的GWI显著降低,在运动状态下,GWI差异更加显著,且GWE降低,表明心肌淀粉样变性患者心肌能量利用效率低下[57]。该团队在另一项纳入100名心脏淀粉样变性患者的前瞻性研究发现,GWI<1043 mmHg%的患者更容易发生主要心脏不良事件(HR=2.3,95%CI:1.2~4.3,P=0.01),而GWI<1039 mmHg%的患者拥有更高的全因死亡率(HR=2.6,95%CI:1.2~5.5,P<0.05),该研究还通过结合GWI和心尖-基底节段工作比值,建立预测模型:GWI<1039 mmHg%以及心尖-基底节段工作比值>3.0(高风险)相较于GWI>1039 mmHg%以及心尖-基底节段工作比值<3.0(低风险),预后更差(HR=6.4,95%CI:2.4~17.1,P<0.0001)[58]。
由上述研究表明,通过确立GWI诊断阈值可为心肌淀粉样变性患者进行风险分层,GWI和心尖-基底节段工作比值相结合可作为预测因子为心脏淀粉样变性患者预后评估提升临床参考价值。
3.6 MW技术与心力衰竭(HF)
HF是一个普遍且日益严重的公共卫生问题,在我国有着较高发病率和患病率,并呈不断增长的趋势,未来HF疾病负担随着我国老龄化社会的发展将会越来越重[59]。因此,HF的诊断、治疗和预后判断尤为重要。HF又分为射血分数保留的心衰(HFpEF)和射血分数降低的心衰(HFrEF)。
一项纳入126名急性HF患者的研究[60]发现,HF类型、N-末端脑钠肽前体的水平和MW参数密切相关。在住院期间N-末端脑钠肽前体水平降低的HFrEF患者中,GCW和GWI显著改善,GWW保持不变;在住院期间N-末端脑钠肽前体水平没有变化甚至升高的HFpEF 患者中,GCW和GWI没有变化,GWW却显著升高;而在所有的HF患者中,GWW值越高,出院后6月内死亡或再住院风险越高。这与另一项对HFpEF患者GWW与主要不良心血管事件发生率及全因死亡率关系的研究结果[61]保持一致。此项研究结果表明GWW 截断值为170 mmHg%(AUC 为0.80,P<0.01),当GWW>170 mmHg%,主要不良心血管事件发生风险增加4倍(HR=4.5,95%CI:1.59~13.12,P=0.005)和全因死亡率风险增加3倍(HR=2.9,95%CI:1.24~6.6,P=0.014)。此外,有研究纳入508名HFrEF的患者进行回顾性研究发现,GWI能为HFrEF提供预后评价的价值,GWI<750 mmHg%的HFrEF患者有更高的全因死亡率和HF住院风险(HR=3.33,95%CI:2.31~4.80,P<0.05)。上述研究结果从心肌能量学角度出发,提示HF类型不同,代偿与失代偿后的心肌反应不同,且GWW及GWI有望发展成为判断HF患者预后情况的无创指标[62]。
目前,还有学者利用机器学习对纳入MW参数后的HF诊断模型进行研究[63]。该研究将参与者分为4组(正常对照组、LVEF≥50%、40%≤LVEF≤50%、LVEF≤40%),探索MW参数能否高慢性HF患者提高临床评估准确性。根据研究结果表明,LVEF、GWI和LVEF+GWI 的多分类诊断性能分别为82%、88%和98%,即GWI+LVEF可以互补地提高四组分类的诊断准确性,提示在临床实践中,MW参数应与常规LVEF一起用于评估慢性HF患者的左室收缩功能,有助于在早期诊断中对HF患者的分类。
在评价HF患者药物疗效方面,MW参数也有一定的临床参考价值,目前研究结果主要集中在沙库巴曲/缬沙坦和螺内酯治疗中。研究结果显示[64-65],经沙库巴曲/缬沙坦治疗的HFrEF患者,GCW、GWE均呈现显著升高,而GWW变化不大;另有研究发现,若HFrEF患者在未经治疗前的GCW<910mmHg%,则发生主要心血管不良事件的风险更高(HR=11.09,95%CI:1.45~98.94,P<0.01)[66]。有研究从运动耐量与MW参数的关系角度出发[67],发现经螺内酯治疗6月后的HFpEF患者运动耐量的改善与GCW的升高变化呈独立相关,而GLS未表现出类似的改变。
综上所述,可以认为MW参数可以作为HF早期诊断、预后评估及指导其临床治疗的指标,尤其是GWW在HFpEF患者中的应用及GWI和GCW在HFrEF患者中的应用。未来,MW参数有望结合生物标志物利用拟合度更优异的模型对HF进行诊断、分型及预后评估,选择适当的治疗方案并对已有的治疗方案进行调整,提高患者的远期生存率。
3.7 MW技术与其他相关性心脏疾病
上述总结了目前MW技术与心脏功能直接相关疾病的研究进展,但在临床实践过程中,由其他原因引起的、与心肌损伤相关的心脏疾病同样不可忽视,MW技术在其他相关性心脏疾病上依然具有广阔应用前景。
3.7.1 糖尿病相关性心脏病 糖尿病尤其是2型糖尿病(T2DM)相关性心脏病,通常是以左室向心性重构和舒张功能减退为表现的限制性表型,并最后发展成为左室HFpEF,然而由于左室重构的发生,糖尿病相关性心脏病在早期即可发生心肌收缩功能受损[66]。现有研究表明,2型糖尿病患者组的GWI、GCW明显低于非2型糖尿病患者组[68-70],但并非所有研究都显示GWW、GWE在两组间存在明显差异;且在2型糖尿病患者中,空腹血糖与GWW呈正相关、与GWE呈负相关[68],HbA1c与GWI、GCW均呈负相关[69]。
因此,MW技术可在早期识别糖尿病相关性心脏病心肌收缩功能的改变,且与血糖水平及血糖控制情况相关。然而目前研究结果尚不一致,且仍缺乏利用MW参数预测糖尿病患者心血管事件发生率及评估糖尿病患者糖尿病相关性心脏病预后的临床研究,因此还需要更多的研究证据进行补充。
3.7.2 癌症治疗相关性心脏病 癌症治疗的风险/收益评估仍然具有挑战性,临床实践中仍需要权衡挽救生命的癌症治疗与可能癌症治疗相关的心脏功能障碍(CTRCD)之间的关系[71]。现指南已推荐使用GLS在早期对接受癌症治疗的患者进行心脏功能的评估,以尽早发现CTRCD[72]。由于MW参数相较于GLS的负荷依赖性小,因此已有研究利用MW参数对接受癌症治疗的患者进行心脏功能早期评估。在一项纳入136名用蒽环类药物和曲妥珠单抗治疗的乳腺癌患者的研究发现[73],GWI和GCW对检查时或随访中诊断CTRCD的应用价值更高,且当GLS与GWI联合序贯使用时,提升CTRCD发生的预测效果。另一研究结果也表现出与上述研究结果的一致性[74]。
尽管在未来仍需要更大的队列对MW参数的临床价值进行验证,然而在目前的研究中,对于接受癌症治疗患者的CTRCD评估,MW技术展示出可观的临床应用潜能。
3.7.3 慢性肾脏病(CKD)相关性心脏病 CKD通常与左心室肥大和左心室质量增加有关,这可能会增加心血管疾病和死亡的风险。由于MW技术加深了对不同负荷下左室重塑与心室壁应力增加之间关系的理解,因此已有研究观察MW参数与CKD之间的联系。研究结果均表明,相比于非CKD患者,CKD患者的GWW升高与GWE降低均具有显著性[75-77],在维持性血液透析患者的相关研究中同样支持这一研究结果[78]。有研究显示,GWE和GWW与GLS的AUC分别为0.87、0.878和0.72;ROC分析显示,GWE最佳截断值≤94%(特异性93.9%,敏感度68.6%);GWW最佳截断值>111 mmHg%(特异性93.9%,敏感度为68.6%),均显示出较高的特异性[77]。
因此,GWE和GWW对CKD患者心肌损伤诊断的准确性优于GLS,通过探索GWW及GWE的最佳截断值有助于在早期排除CKD 患者的心肌损伤,为降低CKD患者心血管疾病发生和死亡风险提供更好的诊疗思路。
除此之外,无创MW技术还被广泛运用在其他心血管相关疾病的心肌功能评价中。有研究者[79]发现当继发性二尖瓣反流患者GWI≤500 mm Hg%(HR=1.495,95%CI:1.074~2.081,P<0.05),GCW≤750 mmHg%(HR=2.011,95%CI:1.317~3.071,P<0.01),GWW<300 mmHg%(HR=1.591,95%CI:1.148~2.204,P<0.01)的全因死亡率高,1年、2年及5年的生存率低;同时有研究证实,GWI<482 mmHg%(AUC=0.882,P<0.01)的患者,行经皮二尖瓣缘对缘修复术预后不佳[80]。在主动脉瓣关闭不全患者的研究中[81]可以观察到GWI和GCW与主动脉瓣反流的严重程度及左心室收缩功能参数密切相关;且主动脉瓣关闭不全患者术后GWI可能在预测左室重构逆转起重要作用。再者,MW技术结合负荷超声心动图有望成为量化心肌收缩储备的评价工具之一,研究表明GWE与心肌收缩储备密切相关,在运动负荷时,GWE是左室存在收缩储备的强独立预测因子,这一发现在以耐力运动员及主动脉瓣返流患者为研究对象的研究中,均得到验证[82-83];更有研究发现若HFpEF患者在静息状态下GWE较低,不仅提示早期亚临床心肌损伤,而且这似乎与运动能力降低、肺充血严重程度的增加以及运动过程中左心室收缩储备减弱密切相关[84]。另外,MW技术还被用于研究心脏移植患者预测急性细胞排斥反应的发生,GWE被认为是急性排斥反应发生的独立预测因子[85]。
因此,MW技术不仅可用于心血管相关疾病早期左室收缩功能及收缩储备的定量评估,还可帮助临床医生识别可能在干预中受益的患者并尽早采取适当的干预措施改善预后。
4 MW技术的局限性与展望
MW技术能更早期、准确、简易地在临床心血管疾病中对心肌收缩功能进行评估。本文归纳了不同健康人群中MW 参数正常参考值范围研究成果,总结了MW技术对临床心血管疾病心肌收缩功能评估的相关研究;进一步证实MW技术临床实践性强、信息精确度高,且将后负荷融入心肌收缩功能评价中,弥补LVEF和GLS的不足,通过相对简单的无创性手段,即可为日后常见心脏病的诊断评估、预后评价、临床随访等提供了重要的发展方向。
然而,MW技术具有一定的局限性:(1)PSL使用的是左室压力估计值而非左室壁应力,忽略了左室的绝对尺寸以及室壁曲率的影响。根据LaPlace定律,室壁应力与球体或圆柱体的半径成比例增加;换言之,在较大的心室中,由于有较大的直径,收缩壁应力将较高;同时,曲率越小(壁越平,曲率半径越大),壁应力越高[86],心肌消耗的做功越高。而MW技术使用估计的左室压力而非左室壁应力,因此PSL并没有反映这部分的MW[86];(2)虽然结合了肱动脉血压测量无创替代左室压力测量,使MW参数对左室后负荷的敏感性低于GLS,但MW参数不能被认为与负荷无关,因为它们的值是通过心肌应变测量得出的,而心肌应变与负荷相关联[87];(3)目前针对MW的临床研究样本量较小,研究人群不一致,MW参数正常值参考范围不具有代表性。因此,仍需有更大的样本完善相关的研究,尤其是更大规模的前瞻性研究来提供更多的证据,建立适合不同人群的参考值范围,以期投入临床应用;(4)应变值的准确度依赖于2D-STE所提供图像质量,一方面是来自于图像采集机器、图像处理软件的精确度,另一方面是来自观察者内及观察者间的误差大小,若无法正确描绘心内膜边界,则难以扫描解剖结构,通常会导致心室缩短,这会影响心尖部的应变值(并因此影响MW参数)测量[87]。然而目前只有一个系统提供了计算MW的软件,限制了该方法的适用性[87],且尚未对图像质量、处理软件、专业素质等有明确要求。因此,在实际临床工作中应用MW,需要保证超声机器对图像识别的质量,提高时间分辨率,保证图像处理软件的准确性,不断优化机器和软件的功能,使其能准确跟踪帧与帧之间斑点运动的轨迹。还需要规范图像采集标准、提供图像采集模板,及对超声医生进行定期培训以获得观察者内、观察者间差异较小的图像和结果;(5)对某一些特定心血管疾病的患者如严重主动脉狭窄患者,由于瓣膜上方存在压力梯度,使得肱动脉收缩压和真实的左室压力相差较大,因此针对此类患者PSL并不适用,有学者为了弥补这一缺陷,运用新的无创估量方法,即无创收缩压袖带结合多普勒衍生平均主动脉梯度估计左室压力[88],这一方法具有开创性,其可靠性也得到了后续研究[89]进一步验证,然而这一新模型操作相对复杂,临床实践性相对较低。因此,针对一些特殊的心血管疾病(比如在显着变异的情况下难以获得应变迹线和MW参数估计的房颤患者),仍需要探索更优的估测方法获得可靠的MW参数。
MW在未来临床应用中前景广阔,利用超声心动图就能在早期阶段评估局部或整体心肌收缩功能,提供患者预后评价,随访观察心肌功能变化情况。然而目前仍缺乏针对不同人群的正常值参考范围,其测量方法及图像采集尚未标准化,对其他临床心血管疾病心肌收缩功能评估的研究证据也尚不充足;因此,仍需要大量的临床研究结果支持MW技术在实际临床工作中的应用和推广。