基于COMP报告的Eclipse计划系统验收测试
2022-11-28王美娇姚凯宁杜乙蒲亦晨蒋璠弓健吴昊岳海振
王美娇,姚凯宁,杜乙,蒲亦晨,蒋璠,弓健,吴昊,岳海振
北京大学肿瘤医院暨北京市肿瘤防治研究所 放疗科/恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142
引言
加拿大高质量放射治疗伙伴关系(Canadian Partnership for Quality Radiotherapy,CPQR)是指参与加拿大放射治疗的国家专业组织联盟,具体包括:加拿大放射肿瘤学协会、加拿大医学物理学家组织(Canadian Organization of Medical Physicists,COMP)和加拿大医学放射技术师协会。其中COMP与CPQR密切合作,为放射治疗设备制定了一系列技术质量控制指南,这些指南概述了设备应达到的性能目标,以确保辐射治疗质量达到可接受的水平。
COMP报告是基于Dunscombe等[1]之前的研究工作和van Dyk等[2]发布的文件进行归纳总结而来,具体方案的参数指标和标准可参考加拿大辐射治疗中心技术质量控制指南[3]。COMP报告内容包含外照射治疗计划系统(Treatment Planning System,TPS)的详细参数目标和安全标准,侧重于现代TPS的基本功能,旨在以质量控制测试的形式提供指南及其相关的性能标准。
放射治疗计划系统是癌症患者进行放射治疗的核心环节,包括CT图像采集、靶区体积的定义、照射技术的设计和优化、治疗计划的评估以及实施,TPS验收工作对于治疗计划方案的优化和辐射剂量的投递精度至关重要。美国医学物理学家协会TG 53号报告[4]制定了三维TPS验收方法以及临床使用过程中的质量保证方法。荷兰辐射剂量测定委员会报告[5]制定了TPS外照射光子束和电子束质量保证的实用指南,对TG 53号报告进行了补充。此外,其他研究者发表的报告[6-11]为TPS的验收测试提供了一个通用的框架;我国在2010年发布了YY/T 0798-2010《放射治疗计划系统质量保证指南》(以下简称质控指南)[12]。虽然目前关于TPS验收的报告已较多,但早期验收报告内容较多,项目繁杂,无法立即获取实用信息,因此不适用于精确放疗;最新报告内容又过于精简,且基本只介绍了操作项目,缺少具体的实际操作部分。
本文在COMP相关报告的基础上,以美国Varian公司Eclipse计划系统(V15.6)验收测试工作为例,对关键验收项目和具体实施过程进行了梳理和分析,旨在为相关验收工作提供全面可行的参考。
1 材料与方法
1.1 CT数据采集和功能性验收
1.1.1 CT相对电子密度
电子密度曲线用于CT图像灰度值(Household Unit,HU)到相对电子密度(Relative Electrical Density,RED)的转换,以便在辐射剂量计算时对组织不均匀性进行校正。ICRU 44号报告[13]和ICRU 46号报告[14]提出组织成分的变化对辐射剂量计算结果的影响较大。目前常用的电子密度模体为QRM-EDP(德国)[15]、美国Gammex(美国)[15]和CIRS 062M(美国)[16]。
本中心采用Somtom Sensation Open 40排大孔径CT定位机(西门子,德国)及Gammex_1467型头部和体部一体式模体。将模体摆放于CT床上并用激光灯进行定位,选择3种不同的扫描模式进行头部、胸部和盆部的扫描,重建层厚设置为1.5 mm。在扫描得到的图像上,对每个插件的中间位置取相同范围的几个像素的平均HU值作为该插件对应组织的HU值,电子密度模体的示意图如图1所示。

图1 电子密度模体(a)和对应的CT图像(b)示意图
1.1.2 图像几何方面
主要包括成像参数(如像素大小、扫描层厚、CT数字标尺和图像部分容积效应等)、图像伪影和失真[11]等。
1.1.3 CT数据传输方面
主要包括图像的几何位置和方向(左右和头脚方向)、所有文本信息、传输数据是否丢失、轮廓坐标及显示尺寸等。将不同厚度的固体水组成的水模体进行CT扫描并上传至TPS,并将水模体显示的轮廓尺寸与实际尺寸进行比较。
1.2 基础数据测量、导入与建模验收
1.2.1 基础数据建模参数
本研究采用TrueBeam型号医用加速器四档兆伏级光子束能量实测数据进行建模,包括均整和非均整模式(Flattening Filter Free,FFF)下的6 MV、10 MV在不同照射野条件下的百分深度剂量(Percentage Depth Dose,PDD)、射野离轴比(Field Off Axis Ratio,OAR)和输出因子(Output Factor,OF)等数据,具体测量过程及数据分析参考相关文献[17-18]。将测量的基础数据导入计划系统中进行建模和验证。
1.2.2 辐射束建模参数
根据IEC 61217[19]建议,辐射束参数主要包括机器型号/能量、机架角度、准直器角度、治疗床角度、多叶准直器(Multi-Leaf Collimator,MLC)型号和患者方向坐标显示一致性。此外,还包括各参数限值、照射技术、楔形方向、电子线限光筒、第三方托盘、射束坐标正确性和坐标值等。
MLC参数是辐射束建模的主要组成部分,主要包括叶片型号、叶片运动速度、非对称射野限值、MLC的透射和漏射、端面漏射(Dosimetric Leaf Gap,DLG)等。其中MLC的透射和漏射与DLG建模参数可以通过测量得到[20-21];同时可以检查MLC在TPS形成的叶片位置与加速器实际位置的一致性,TrueBeam型号加速器MLC建模参数测量值如表1所示。
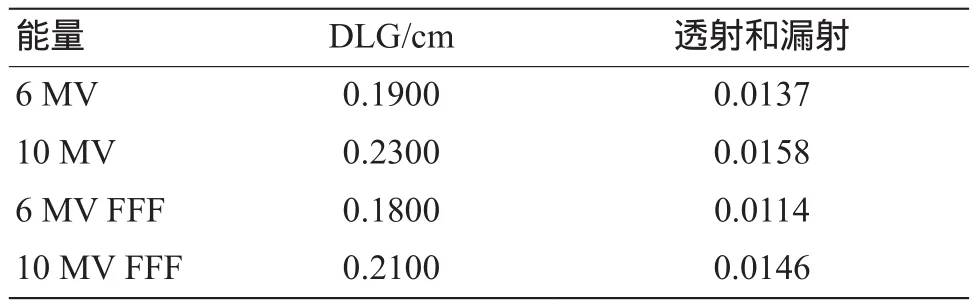
表1 实测MLC建模参数数据值
1.2.3 剂量计算模型精度验证
剂量计算模型精度的验证重点是基础数据验证、剂量计算算法本身精度的评价等,其中算法本身精度和可靠性的验证,已由相关的文献[22]报道,本研究利用Acuros XB算法进行剂量计算。
基础数据验证方法是在TPS中生成一个虚拟三维水模体(50 cm × 50 cm × 50 cm),添加机架角度和小机头角度均设置为0°的照射野进行垂直照射,分别形成与测量数据相对应的照射野尺寸合集,并获取相应深度处的OAR数据,与测量数据进行对比,得到两者之间的偏差。本研究仅展示标准照射野(10 cm×10 cm)的PDD和3个深度处的OAR的对比结果。OF的验证,包括1 cm×1 cm、1 cm×5 cm、5 cm×1 cm、5 cm×5 cm、8 cm×10 cm、10 cm×10 cm、10 cm×15 cm、15 cm×15 cm、20 cm×15 cm和30 cm×30 cm等多个方形野或矩形野的对比结果。
1.2.4 计划评估验收
计划评估用于显示计算测量剂量分布的一致性,包括剂量点显示、点坐标位置显示、剂量插值、射束显示(位置和照射野大小、方向、剂量分布)和剂量体积直方图(感兴趣的体积区域、体素剂量插值、剂量体积直方图计算等)。
1.2.5 其他项目验收
包括治疗计划数据导出(能否匿名化)、计划方案审核和确认、打印等基本功能的可用性。
1.3 临床计划实施和计划验证
1.3.1 临床计划实施验收
在实施临床计划方案之前,需要检查数据的传输和回传记录数据的完整性和可靠性。传输数据包括患者信息、坐标系和治疗参数等相关数据能否正确传输到加速器治疗端,保证患者的治疗信息准确无误;回传数据包括照射野信息、时间、治疗次数、机载影像图像和机载影像位置偏移等。
1.3.2 临床计划验证
本研究选取14个病例进行临床计划验证,其中头部4例、胸部5例、腹部盆腔5例,采用二维矩阵和机载电子射野影像系统(Electronic Portal Imaging Device,EPID)2种质控设备进行治疗计划方案的二维剂量验证,其中二维矩阵验证采用PTW OCTAVIUS 1500矩阵结合Octagonal模体(Oct1500)。计划验证以测量结果为参考,采用为γ 2 D分析方法,并以3 mm的位置误差和3%的剂量偏差作为评价策略,对TPS的计算结果进行评价和验证。
1.3.3 安全性测试验收
TPS主要由计算机硬软件系统、服务器和外围设备组成,用以监控磁盘空间、用户帐户、内存和其他资源,安全性测试也是TPS验收测试和质控的一部分。
安全性测试内容包括TPS和患者数据定期备份,具体包括日检(对所有新的或更改的文件进行增量备份)、周检(备份所有与治疗计划相关的文件)、月检(备份整个系统,包括系统软件、TPS软件、射束数据文件、治疗计划文件)、系统维护(系统硬件和软件、相关计算机网络和其他类型的计算机间通信)、安全性(计算机系统的安全,硬件、软件、网络和束流数据、网络安全)和版本兼容性/可用性(新版本的更新、质量保证测试需求、试运行)。
2 结果
参照COMP报告和国内质控指南,Eclips15.6计划系统对相关的CT图像采集和传输系统,计划评价和数据传输/回传记录等系统可靠性和安全性等项目的验证,均稳定可靠,不再赘述,研究仅对验收工作中较关键的验收项目结果进行分析。
2.1 定位CT图像验收
图2为Gammex电子密度模体在头部、胸部和盆部3种扫描模式下的CT图像HU值到RED的转换曲线。在临床实际应用过程中,将3种不同的CT图像RED转换曲线导入Eclipse计划系统中建模,可针对扫描部位的不同选择相对应的RED转换曲线分别进行剂量计算,以保证治疗计划剂量计算的精度和准确性,电子密度误差在0.02以内(基准值:0.02)[11]。

图2 Gammex模体在3种扫描模式下的CT图像的HU值到RED转换曲线
CT图像几何尺寸TPS中水模体的轮廓尺寸与模体实际尺寸如图3所示,偏差在±1 mm以内(标准值:2 mm)。

图3 Eclipse治疗计划系统水模体轮廓显示尺寸
2.2 剂量计算模型验证
以6 MV辐射能量为例,标准辐射野10 cm×10 cm的PDD和OAR的测量结果与TPS模拟计算偏差如图4所示。其中,OAR分别为水下5 cm和10 cm深度处的数据,均在最大剂量深度处进行归一化处理。采用γ 1D(Local Dose方法,剂量误差<3%,位置误差<3 mm)进行对比分析,结果显示PDD曲线最大偏差在水下280~300 mm,OAR曲线最大偏差在半影区,结果均<2%(标准值≤±2%)[22]。

图4 TPS计算与实测数据PDD(a)和OAR(b)的比较
以6 MV能量为例,射野输出因子的验收结果如表2所示,其中偏差的计算方式为:偏差=(OFTPS- OF测量)/OF测量×100%。结果显示,1 cm×1 cm的OF偏差最大(标准值≤±2%),其余射野均小于1%(标准值≤±1%)[22],原因是小尺寸辐射野测量精度对测量设备和方法依赖度较高。

表2 TPS计算与实测输出因子对比
2.3 临床计划验证
对于治疗计划方案验证,分别采用PTW二维矩阵和EPID两种设备对14个病例进行验证,在评价策略不同的情况下,评价结果略有差异,见图5。其中采用3 mm位置偏差和3%剂量偏差的条件下,2种设备的γ通过率均大于95%,满足临床要求。结果显示不同评价策略对同一验证设备的验证结果影响较大,建议在计划系统验收时选择相对较严格的评价策略,对于验证放疗流程的整体可靠性有帮助。

图5 二维矩阵(a)和EPID验证(b)不同评估策略下14个射野的通过率
3 讨论
Moyed 等[23]认为用于计算模型拟合的基础数据不准确、算法局限性、治疗计划过程中的错误或输出数据的不当使用可能会对患者构成安全隐患。因此,在治疗计划系统验收时,确保与其精度和安全性相关的各个组成部分的可靠性,如贯穿整个放射治疗过程的坐标系设置、模拟辐射束的方向和射野形状、治疗射束的剂量分布、CT图像的HU值到RED转换和基础数据的准确性等关键项目。执行治疗计划后需要检查数据的回传信息,当TPS和加速器的厂家不匹配时,数据的回传等也需要重点关注。
研究表明,不正确的CT图像的RED转换曲线会导致照射剂量偏差3%以上[24-26],因此由CT 图像的RED转换曲线引入的剂量误差不可忽略。在3种扫描模式下采集的CT值具有一定差异(图2),需要在计划系统里根据情况予以区分并合理选择。低原子序数材料CT值变化较小,对剂量计算和组织不均匀性的校正影响较小,而高原子序数材料CT值变化较大。在CT数据扫描前应对CT定位机进行验收,以保证图像质量、CT床和激光灯的精度等;在CT维修后需对CT 图像的RED转换曲线进行校准,以确保剂量计算精度。
基础数据采集的准确性是保证TPS剂量计算精确的重要部分。本研究中PDD和OAR的γ分析显示,在半影区的通过率较低,所以在测量半影区时,需要采用驻留点时间长、测量时间长、步长小的原则,且根据辐射野尺寸和需要测量的数据类型,选择较为合适的测量工具。不同厂家的加速器和MLC型号均不同,应在加速器上进行透漏射测量,并导入到TPS中进行建模。对于不同的TPS和能量,透漏射在0.5% ~ 4%之间变化,且能量越低,泄漏量越小[21]。
4 结论
瓦里安Eclipse放射治疗计划系统在经过严格的安装和调试后,其验收结果在精确性和安全性等方面均符合国家标准并满足临床应用要求,该研究可为本领域TPS验收工作提供参考。
