冷圈套器切除技术在结直肠息肉的临床应用进展
2022-11-26朱晓佳
朱晓佳,杨 力
朱晓佳,杨力,江西省景德镇市第三人民医院消化内科 江西省景德镇市333000
0 引言
内镜热圈套器息肉切除术(hot snare polypectomy,HSP)是结直肠息肉常用的治疗手段.近年来,随着技术的发展,冷圈套器息肉切除术(cold snare polypectomy,CSP)以及冷内镜黏膜切除术(cold endoscopic mucosal resection,C-EMR)已逐步应用于临床,并被欧洲、美国以及日本内镜学会推荐用于切除结直肠微小息肉(≤5 mm)和小息肉(6 mm-9mm),以及部分10 mm-19 mm的无蒂息肉[1-3].然而,在实际临床应用过程中,由于内镜医师的操作习惯以及对冷切除技术的认识尚不充分,使得冷圈套器切除技术在结直肠息肉中并未得到充分的应用[4,5].为更好的了解这一技术,本文现就其临床应用进展加以综述如下.
1 冷圈套器切除技术的应用现状
Willems等[4]于2017-07/2018-05对全球808名内镜医师进行了问卷调查,结果发现CSP的使用较前有大幅增加,分别有17.5%,67.0%,55.2%,4.6%的内镜医师报告首选CSP切除1 mm-3 mm,4 mm-5 mm,6 mm-10 mm,10 mm-20 mm结直肠息肉.Tate等[5]在2017-07问卷调查了707名欧美国家的内镜医师,对于3 mm,8 mm,10 mm,15 mm,20 mm结直肠无蒂息肉分别有65.6%,43.3%,23.9%,12.4%,3.3%的内镜医师会选择使用CSP.韩国学者Yang等[6]于2018-10/2019-01调查了154名亚洲地区的内镜医师,发现分别有16.9%,31.2%,3.9%的内镜医师报告选择CSP切除≤5 mm,6 mm-9 mm,10 mm-19 mm无蒂或平坦息肉.日本学者Hotta等[7]报道了一项2017-12/2018-01期间进行的大规模调查,共有790家医疗机构参与,发现近70%的癌症中心和大学附属医院以及约60%的社区医院采用了CSP,但不到1/2的诊所采用了CSP.国内长海医院王润东等[8]于2019-11/2020-01对国内207名内镜医师进行了问卷调查,结果显示分别仅有4.8%,19.3%,0%的内镜医师报告选择CSP切除3 mm,7 mm,15 mm无蒂息肉.基于上述的调查,可以初步发现我国内镜医师在冷圈套器切除技术的应用,特别是在<10 mm结直肠息肉中明显滞后于欧美及其它亚洲地区.值得注意的是,问卷调查中内镜医师自我报告的息肉切除情况与其实际临床操作是否一致,对此美国学者Kadle等[9]进行了研究,作者于2018-11对佛罗里达州立大学的26名内镜医师进行了问卷调查,之后回顾性分析2016-01/2018-09间所有参与调查的内镜医师实际的息肉切除记录,结果发现问卷调查中分别有10.5%与89.5%的内镜医师报告选择CSP切除1 mm-3 mm,4 mm-9 mm无蒂息肉,然而,在实际的切除记录中却发现仅有5.8%与26.6%的1 mm-3 mm,4 mm-9mm无蒂息肉使用CSP切除,显示自我报告的息肉切除情况与实际的临床实践之间存在显著差异.提示在真实世界的临床操作中,尽管已有多项相关指南出现,但冷切除技术的临床应用仍然还远远不足.
2 冷圈套器切除技术在结直肠息肉中的应用
2.1 结直肠微小息肉(≤5 mm) 一项包括5项随机对照试验(randomized controlled trial,RCT)共计721个息肉的荟萃分析,比较了CSP、大开口活检钳息肉钳除术(jumbo forceps polypectomy,JFP)与冷活检息肉钳除术(cold forceps polypectomy,CFP)治疗≤7 mm结直肠息肉,结果发现CSP的不完全切除率显著低于CFP,而JFP的不完全切除率趋向低于CFP但差异无统计学意义[10].另一项包括4项研究的荟萃分析进一步比较了CSP与JFP治疗≤5 mm的结直肠微小息肉,结果显示CSP的不完全切除率略低于JFP(7.2%vs10.2%),但两者并无统计学差异[11].因此目前推荐首选CSP切除结直肠微小息肉[1,2].在CSP操作困难,技术上难以实施时,欧洲内镜学会推荐1 mm-3 mm息肉可考虑CFP[1],而美国指南则进一步限定为≤2 mm息肉,并建议使用JFP[2].
2.2 结直肠小息肉(6 mm-9 mm) 目前已有7项荟萃分析评估了CSP与HSP切除<10 mm结直肠息肉的疗效(见表1),结果显示两者完全切除率并无统计学差异[12-18];CSP组即刻出血高于HSP组[15,16],但需要治疗的出血两组无统计学差异[16];两组术后延迟出血率无统计学差异[12,14-16];CSP的治疗操作时间明显少于HSP组[12-14,16];两组术后息肉标本回收率相似[14,15].另有一项包括7项RCT共计968个息肉的荟萃分析,评估使用专用冷圈套器与常规热圈套器进行CSP的疗效,发现使用专用冷圈套器行CSP的组织学完全切除率优于常规圈套器,但两者术后息肉标本回收率相似[19].

表1 7项荟萃分析比较CSP vs HSP切除结直肠小息肉
有文献报道CSP切除6 mm-9 mm结直肠息肉的不完全切除率明显高于常规内镜黏膜切除术(endoscopic mucosal resection,EMR)(8.5%vs1.5%)[20].C-EMR是在CSP技术基础上结合了黏膜下注射水垫,Li等[21]的一项前瞻性研究显示C-EMR与常规EMR切除6 mm-10 mm息肉的组织学完全切除率相似(97.7%vs100%).另有2项前瞻性非劣性研究比较了C-EMR与常规EMR切除≤10 mm结直肠腺瘤的疗效,结果显示C-EMR的组织学完全切除率并不劣于常规EMR,两组术后出血率亦无差异[22,23].
目前冷圈套器切除术多用于结直肠无蒂息肉,对于有蒂息肉亦有部分学者进行了有益的尝试.Arimoto等[24]的一项回顾性资料显示CSP切除<10 mm有蒂息肉的即刻出血率明显高于HSP(38.2%vs3.5%),但延迟出血率却低于HSP(0%vs4.7%).Fatima等[25]的一项前瞻性研究评估了CSP切除≤10 mm结直肠有蒂息肉的即刻出血情况,结果发现CSP的即刻出血率为30.1%,其中近一半无需内镜干预可自行止血,全组无延迟出血及穿孔发生.另一项前瞻性研究同样发现CSP切除<10mm结直肠有蒂息肉的整块切除率为100%,术后即刻出血率为28.9%,无延迟出血发生,其中息肉≥6 mm是即刻出血的独立危险因素[26].尽管CSP在<10 mm有蒂息肉中初步显示出较好的治疗前景,但由于目前的研究尚少,仍需进一步的前瞻性研究证实.
2.3 结直肠无蒂息肉(≥10 mm) 近年来已有4项系统评价及荟萃分析评估了冷圈套器切除≥10 mm结直肠无蒂息肉的疗效(表2),结果发现冷圈套器切除≥10 mm结直肠腺瘤的残留率达11.1%[27],考虑到局部复发的风险,不建议用于切除大的腺瘤[28];冷圈套器切除锯齿状病变(sessile serrated lesions,SSL)总体技术成功率、不良事件分别为100%、0.7%[29],总体SSL残留率为1.0%-4.3%[27,29,30],≥20 mm SSL的残留率高于10 mm-19 mm者[29,30],与常规EMR比较,C-EMR切除SSL的术后延迟出血率更低[30].近期来自日本的一项大样本的前瞻性研究,使用CSP成功切除474个≥10 mm SSL,即刻出血率为3%,无延迟出血,中位随访7 mo未见复发[31].Tate等[32]的一项多中心回顾性研究比较了C-EMR与常规EMR切除≥20 mm SSL,显示两组技术成功率相似(100%vs99%),随访结果表明两组6 mo(4.3%vs4.6%) 与18 mo(2.0%vs1.2%)的复发率并无统计学差异.进一步显示冷切除技术可有效的用于切除≥10 mm SSL.
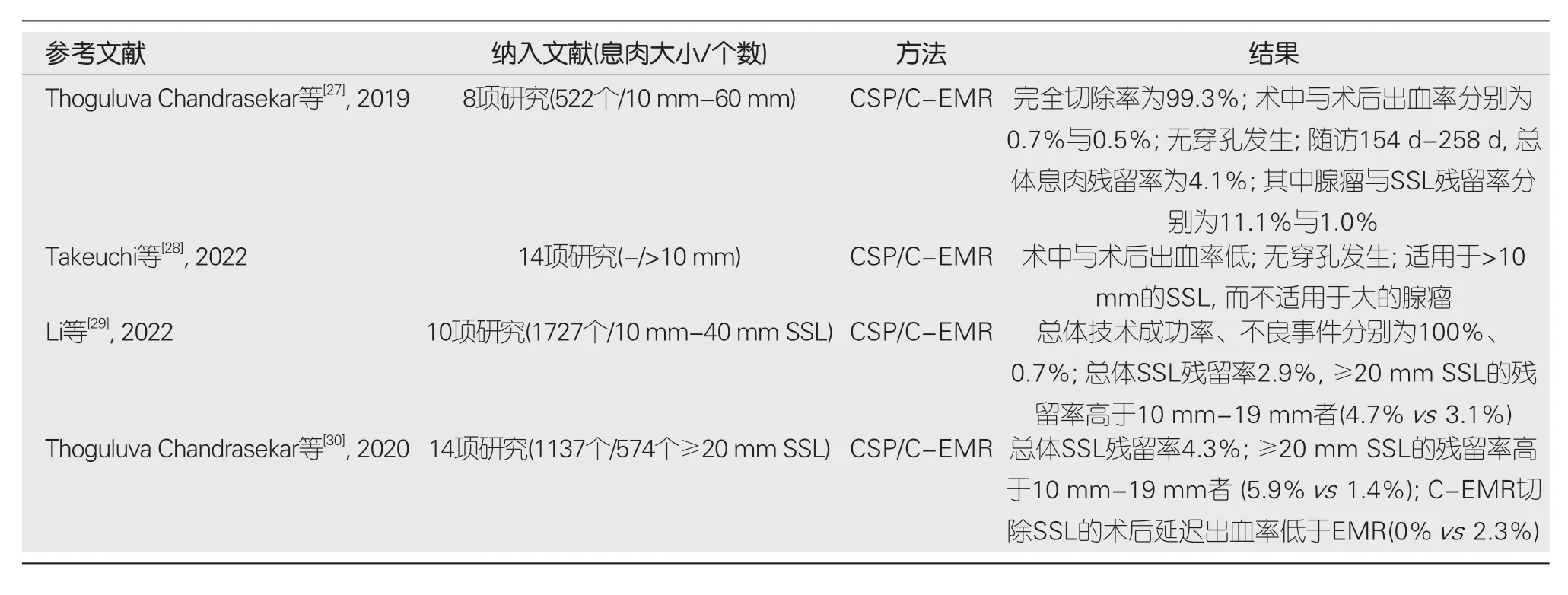
表2 4项系统评价评估冷圈套器切除≥10 mm结直肠无蒂息肉
3 冷圈套器切除技术在使用抗血栓药物患者中的应用
近年美国及欧洲均颁布了内镜检查围手术期抗血栓药物的管理,但其中并未针对冷圈套器切除提出具体的推荐意见[33,34].最新的一项包括17项研究的系统评价及荟萃分析,评估了CSP(96%的息肉<10 mm)围手术期抗血栓药物的安全性,结果发现CSP围手术期接受抗血栓药物的患者总体即刻出血率与延迟出血率分别为10.5%与1.6%,明显高于未使用者;接受抗血小板药物或抗凝剂可增加延迟出血的风险,接受直接口服抗凝药物(direct oral anticoagulants,DOACs)(2.5%)或多种抗血栓药物(3.9%)的风险更高;微小息肉或无需止血夹止血的简单病灶其延迟出血风险较低(0.4%与0.18%);围手术期使用或未使用抗血栓药物的血栓栓塞风险相似;CSP围手术期使用抗血小板药物和华法林是可行的,特别是对于微小息肉,但使用DOAC或多种抗血栓药物的患者即使应用止血夹也会出现较高的出血风险,应考虑停药[35].Lau等[36]的一项包括547例患者的大样本倾向匹配评分分析,评估了接受抗血栓药物患者息肉切除术后预防性使用止血夹的疗效,结果显示冷圈套器切除术后出血明显低于热切除方法,亚组分析表明预防性止血夹有助于降低使用DOAC患者息肉切除术后出血的风险,建议使用抗血栓药物的患者尽可能使用冷切除技术.日本学者同样认为接受抗血栓药物的患者CSP术后出血风险可能低于内镜热切除术[3].对于CSP术前停用DOAC的患者,Morita等[37]的一项包括468例患者(息肉<10 mm)的前瞻性队列研究,比较了仅在手术当天停用并在第2天恢复DOAC对CSP术后出血的影响,结果发现手术当天停用DOAC的即刻出血率(6.1%vs25.5%)与延迟出血率(0%vs8.5%)均明显低于继续使用DOAC者,表明仅在手术当天停用DOAC可以安全有效地实施CSP治疗.简而言之,基于现有的文献,在使用抗血栓药物的患者当中,相较于内镜热切除技术,冷圈套器切除显示出更有希望的应用前景.
4 冷圈套器切除技术后相关组织学改变
冷圈套器切除结直肠息肉后,有时部分未被切割的组织可残留于创面,形成一突出的组织物(cold snare defect protrusions,CSDPs)[38].多项研究报道CSP切除≤10 mm结直肠息肉术后CSDPs发生率为11.3%-34%[38-40],随息肉直径增大,CSDPs发生率趋向增加[40,41].多因素分析显示息肉直径≥6 mm、切除时间≥5 s是CSDPs发生的危险因素[38,39].CSDPs的活检组织学显示主要是黏膜下及黏膜肌层组织,并非血管结构或残留息肉[38].CSP术后CSDPs中94%存在黏膜下层组织,76%-81%存在黏膜肌层,认为术后创面出现CSDPs提示黏膜层可能切除不完全[38,39].
一项前瞻性研究比较CSP与HSP切除≤10 mm结直肠息肉,结果显示两者术后标本包含有黏膜肌层的比例相似(92%vs96%),但CSP术后标本包含有黏膜下层组织的比例明显低于HSP(24.0%vs81.5%),标本黏膜下层组织厚度CSP也明显低于HSP(51 µmvs933 µm)[42].另一项回顾性研究评估了CSP与HSP切除6 mm-9mm结直肠息肉术后标本的组织学深度,发现CSP术后标本包含黏膜肌层(57%vs92%)与黏膜下层组织(29%vs83%)的比例均明显低于HSP,标本黏膜下层组织厚度CSP也明显低于HSP(52 µmvs623 µm)[43].表明CSP切除深度较浅,仅少部分达黏膜下浅层.值得注意的是,尽管CSP术后标本多包含有黏膜肌层,有研究对CSP术后创面底部进行活检,发现62%的创面中仍可见残留黏膜肌组织[39].提示不少患者的黏膜肌层并未得到完整切除[3].近期来自日本的一项前瞻性随机对照研究,评估了黏膜下注射生理盐水是否提高≤10 mm结直肠息肉的黏膜肌层完整切除率以及切除深度,结果发现C-EMR的黏膜肌层完整切除率并不优于CSP(43.9%vs53.3%),术后标本包含有黏膜下层组织的比例两组亦无差异(17.5%vs23%)[44].显示黏膜下注射生理盐水并不能提高CSP的切除深度,临床切除更深层次的黏膜下组织可能需要使用高频电切除而不是单纯的黏膜下注射.
5 结语
总之,冷圈套器切除是不同于常规热切除的一种结直肠息肉切除技术,CSP或C-EMR为<10 mm息肉以及部分≥10 mm无蒂息肉提供了一种安全有效的治疗措施.随着该技术的进一步应用,以及对于其术后相关组织学特点的深入了解,将更有利于临床进一步的推广使用.
