射频消融对肝细胞癌患者的预后影响因素分析
2022-11-19吴建波黄俊梁强南部战区海军第二医院外一科海南三亚572000
吴建波,黄俊,梁强(南部战区海军第二医院外一科,海南 三亚 572000)
肝细胞癌(Hepatocellular carcinoma,HCC)被认为是世界范围内的常见恶性肿瘤,病死率仅次于肺癌、胃癌。HCC的发生与发展多与遗传、慢性乙型肝炎、吸烟、肥胖等因素密切相关,临床虽可通过影像学检查进行诊断,但由于HCC早期多无明显症状表现,大部分患者在确诊时多已至病情中晚期[1-2]。目前,临床针对HCC的治疗多采用介入治疗、肝移植术治疗、射频消融等方式,虽通过肝移植手术可在有效切除癌组织的同时去除肝基础性疾病,从而获得较好的预后,但由于手术费用相对较高、围术期并发症相对较多且供体肝的严重缺乏,难以成为临床首选的治疗方式[3-4]。射频消融是目前临床微创的治疗方式,其可适用于手术风险较大、无法通过手术切除及肝功能不良等范围的患者,且具有治疗反复性高的优势[5]。目前已有文献证实[6],射频消融应用于极早期肝癌患者中可达到与切除手术近乎相同的治疗效果,且在最大程度上减少并发症的发生,但随着HCC的恶性程度变高、发展迅速,故患者远期的预后仍欠佳。鉴于此,本探究将分析射频消融对肝细胞癌患者预后影响因素。报道如下。
1 资料与方法
1.1 一般资料 选取2017年8月至2021年1月我院接受射频消融治疗的肝细胞癌患者84例,其中男71例、女13例;年龄52~76(57.41±6.32)岁;肿瘤数量:1~3(0.85±0.14)个;肿瘤大小1.4~3.5(1.96±0.85)cm;肝功能(Child-Pugh)分级:A级49例、B级35例。本研究经我院医学伦理委员会审核批准。
1.2 纳入与排除标准 纳入标准:(1)符合HCC符合《原发性肝癌诊疗规范(2017年版)》[7]中相关标准,①有乙型肝炎或丙型肝炎;②至少每6个月行1次超声及甲胎蛋白(Alpha Fetoprotein,AFP)检测,肝内直径≤2 cm结节;③经动态增强核磁共振、动态增强CT、超声造影(CEUS)检查至少有2项为动脉期病灶明显强化、门脉或延迟期化下降的典型肝癌表现;④若肝内直径>2 cm结节则经上述影像学检查任一符合肝癌典型特征则可确诊。(2)均接受射频消融治疗且符合适应症。(3)临床资料完整。(4)均接受且签署知情同意书。排除标准:(1)近期内接受过相关治疗者。(2)存在肝内弥散性病灶者。(3)严重精神功能障碍无法配合治疗者。(4)合并其他恶性肿瘤者。
1.3 方法
1.3.1 治疗方法 所有患者均接受射频消融治疗,方法如下:采用美国柯惠射频组织消融系统ACT1020进行治疗,在治疗前经CEUS、超声等检查方式对患者的病灶位置、大小、数量及周围血供情况等进行确认。在发现病灶后应及时进行射频消融治疗,消融范围需完全覆盖病灶区域并>肿瘤边缘1 cm,若边界不清则需要扩大至1 cm以上;对直径>3 cm的病灶则需计算方案并执行重叠病灶区消融处理。
1.3.2 预后评估 在治疗后对所有患者进行1年的随访,以患者病灶消失,未出现新的病灶且相关血清肿瘤标志物水平维持在正常水平≥4周则为完全缓解;经治疗后肿瘤最长直径缩小>30%,且相关标志物水平维持正常水平≥4周则为部分缓解;经治疗后肿瘤最长直径缩小在20%~30%范围内,且相关水平维持正常水平≥4周则为稳定;经治疗后肿瘤最长直径未缩小甚至增加或有新的病灶出现则为疾病进展。将完全缓解及部分缓解视为预后良好,稳定及疾病进展视为预后不良。
1.3.3 资料收集 收集所有患者的一般资料[性别(男,女)、年龄(>60岁,≤60岁)、HBsAg(阳性,阴性)、AFP水平(>100μg/L,≤100μg/L)、肝功能(childpugh)分级(A级,B级)、肿瘤个数(单个,多个)、肿瘤大小(>3 cm,≤3 cm)及邻近脏器或血管(是,否)]等。HBsAg及AFP采用酶联免疫吸附实验法进行检测,其中HBsAg样品OD值/阴性对照平均OD值≥2.1判断为阳性,否则为阴性;child-pugh分级:A级表示肝功能良好,B级表示肝功能中等。
1.4 统计学处理 数据采用SPSS 23.0统计学软件进行处理。计数资料采用例(百分率)表示,行χ2检验;射频消融对肝细胞癌患者预后影响因素采用Logistic回归分析检验。P<0.05表示差异有统计学意义。
2 结果
2.1 预后情况分析 对治疗1年后患者进行随访评估,84例患者中预后良好的有57例(67.86%),预后不良的有27例(32.14%)。
2.2 单因素分析 射频消融对肝细胞癌患者预后不良不受性别、年龄、HBsAg、AFP水平及肿瘤个数的影响(P>0.05);但可能与Child-pugh分级、肿瘤大小及邻近脏器或血管有关(P<0.05)。见表1。
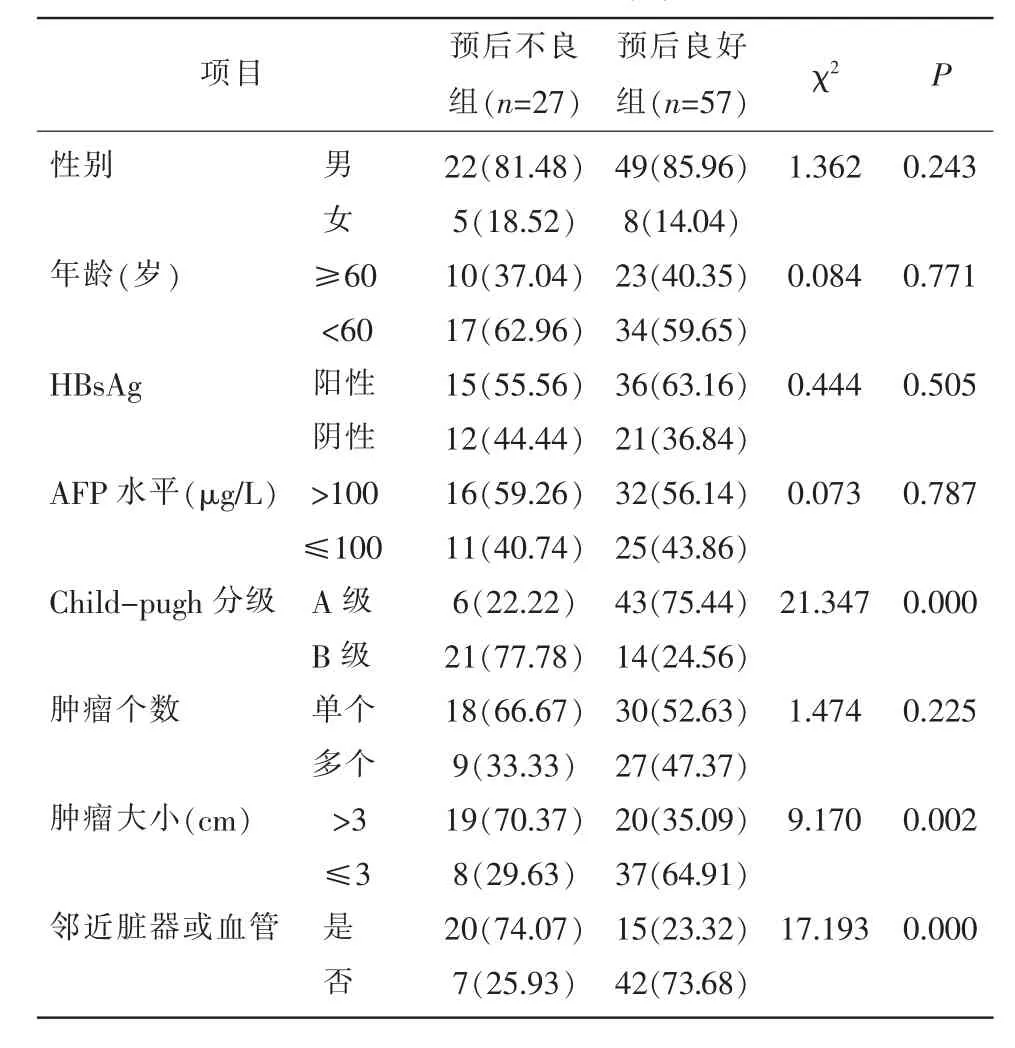
表1 单因素分析[n(%)]
2.3 多因素分析 将表1中比较结果显示差异有统计学意义的因素纳入自变量并为其赋值(见表2),将射频消融对肝细胞癌患者预后情况作为因变量(1=预后不良,0=预后良好),经非条件Logistic回归分析结果得出,Child-pugh分级为B级、肿瘤大小>3 cm及邻近脏器或血管均是影响射频消融对肝细胞癌患者预后不良的危险因素(OR>1,P<0.05)。见表3。
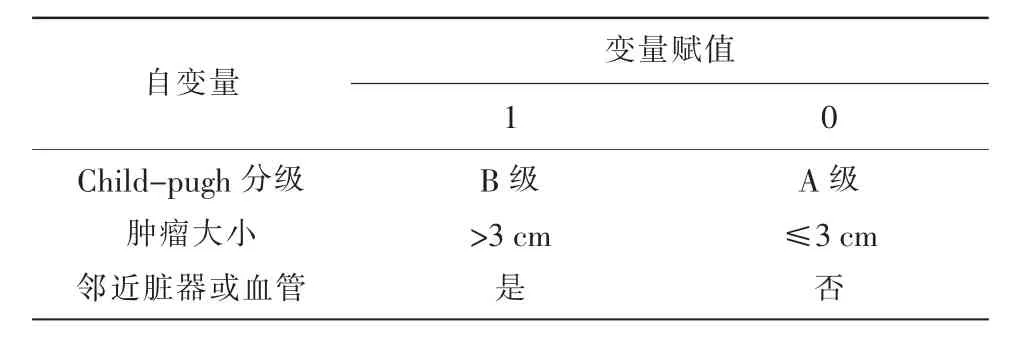
表2 自变量赋值表
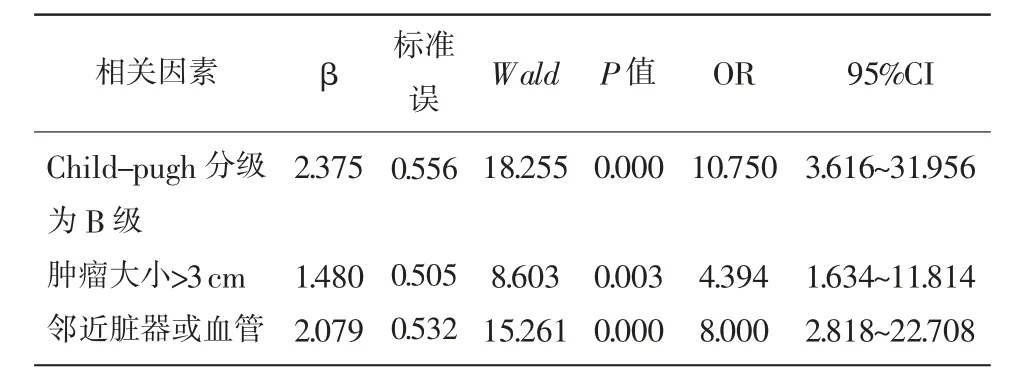
表3 影响射频消融对肝细胞癌患者预后不良的多因素分析
3 讨论
HCC具有起病急、病程进展快等特点,在早期多无明显症状表现,在出现显著临床症状是病情多已进入中晚期,仅部分患者可在早期的疾病筛查中确诊并接受切除手术,然而大部分患者仍会错过最佳的手术切除时机。目前,随着临床的治疗技术不断发展与进步,射频消融治疗凭借微创、并发症少等优势已被广大医患人员所接受,其治疗的机制主要是通过微波电加热对HCC患者的病灶组织进行加热,当射频电流>100 kHz时会引发局部组织所具有的电荷进行离子化运动,对肿瘤组织病灶起到毁损的目的。但目前临床仍有研究指出,射频消融治疗会受到局部病灶复发的多种因素影响导致患者的预后不佳。因此,分析影响射频消融对肝细胞癌患者预后不良的危险因素对制定防治措施、改善患者预后具有重要意义。
本次探究结果显示,经单因素及非条件Logistic回归分析结果得出,Child-pugh分级为B级、肿瘤大小>3 cm及邻近脏器或血管均是影响射频消融对肝细胞癌患者预后不良的危险因素(P<0.05)。逐条分析原因可能如下:(1)Child-pugh分级。Child-Pugh是综合评分方式,该分级最大的优势是通过有无肝性脑病、腹水、血清胆红素、白蛋白浓度及凝血酶原时间进行评分,具有计算简单、指标代表性强等优点被临床应用于肝功能的评价中。该分级越高则表示肝脏损害的程度越高,手术难度越大且预后越差。罗敏等[11]通过回顾性分析104例HCC患者的临床资料,共147个病灶,采用超声造影监测的方式对HCC患者的局部复发情况进行评估结果发现,术前肝功能Child-Pugh分级可影响超声引导下射频消融治疗术治疗HCC患者的术后生存率,与本次研究结果近似。(2)肿瘤大小。肿瘤越大往往在接受射频消融治疗时需要进行多次的重叠消融治疗,若消融范围未覆盖完全或定位不准确则会导致HCC患者的局部消融治疗不够彻底,故在治疗后预后仍较差。曾鹏等[12]通过对98例接受射频消融治疗的98例小肝癌患者临床资料进行回顾性分析发现,肿瘤直径≥3 cm的患者往往局部复发的几率更高,故预后相对较差。(3)邻近血管或脏器。已有研究证实[13-14],邻近大血管的HCC是射频消融治疗后肿瘤残留的独立危险因素之一,这主要是由于肿瘤靠血管或脏器越近,在进行射频消融治疗时对于较大的肿瘤升温较慢,肿瘤依靠血管较近则会被血流带走热量,即“热沉效应”,从而导致病灶残留的情况出现,影响预后。因此,在针对临近血管或脏器较近的病灶进行治疗时,可将射频针尽可能的靠近大血管,以减少热量的损耗,从而保证治疗的效果[15]。
综上所述,Child-pugh分级为B级、肿瘤大小>3 cm及邻近脏器或血管均是影响射频消融对肝细胞癌患者预后不良的危险因素,临床可针对上述因素制定防范措施,以改善预后。
