交流磁场对M-BTC材料电化学氮还原(NRR)性能的影响
2022-11-14高朋召张佩李玉玲马冯覃航刘小磐郭文明肖汉宁
高朋召 张佩 李玉玲 马冯 覃航 刘小磐 郭文明 肖汉宁





摘要:本文采用水热法合成了四种MOFs催化剂,分别通过XRD、SEM及IR表征了催化剂的组成和微观结构,进而研究了催化剂的NRR活性,最后探究了交流磁场对催化剂NRR活性的影响及作用机制.结果表明:四种催化剂中,Fe-BTC在-0.376 V(vs.RHE)和80oC时具有最高的氨产率和法拉第效率,分别为3.63×10 mol s cm和0.31%;在恒电位下,当交流磁场的强度为4.355 mT,频率为50 kHz时,催化剂的氨产率和法拉第效率最大,分别为3.61×10 mol s cm和5.67%,比无磁场时分别提高约10倍和18倍,这种增效一方面源于交流磁场增加了N在Fe-BTC表面的吸附量,另一方面,交流磁场产生的感应电动势与电场本身的电势的叠加作用,为NRR反应提供了额外能量所致.
关键词:电催化氮还原反应;金属有机框架;交流磁场;氨产率;法拉第效率
中图分类号:4599文献标志码:A
Effect of Alternating Magnetic Field on Electrochemical Nitrogen Reduction(NRR)Performance of M-BTC Materials
GAO Pengzhao1,ZHANG Pei1,LI Yuling1,MA Feng2,3,QIN Hang1,LIU Xiaopan1,GUO Wenming1,XIAO Hanning1
(1. College of Materials Science and Engineering,Hunan University,Changsha 410082,China;2. Hunan Zhongtai Special Equipments Co,Ltd. Changde 415211,China;3. College of Chemistry and Materials Engineering,Hunan University of Arts and Science,Changde 415000,China)
Abstract:In this paper,four kinds of MOFs catalysts were synthesized by hydrothermal method. The composition and microstructure of the catalysts were characterized by XRD,SEM and IR,respectively. Then,the NRR activity of the catalysts was studied. The results showed that Fe-BTC had the highest ammonia yield and Faraday efficiency at -0.376 V (vs.RHE)and 80℃,with values of 3.63×10 mol s cm and 0.31%,respectively. Under constant voltage,when the alternating magnetic field intensity is 4.355 mT,frequency is 50 kHz,the catalyst ammonia production rate and efficiency of Faraday's largest,were 3.61×10 mol s cm and 5.67%,respectively.This phenomenon is mainly due to the increase of the adsorption amount of N on the Fe-BTC surface by the alternating magnetic field,and the superposition of the induced electromotive force generated by the alternating magnetic field and the electric potential of the electric field itself,which provides extra energy for the NRR reaction.
Key words:electrochemical nitrogen reduction(NRR);MOFS;AC magnetic field;ammonia yield;Faraday efficiency
氨(NH)不仅是生产氮肥、药物、染料、炸药和树脂的重要原料[1],也是一种优异的氢能载体[2],对人类社会发展至关重要.目前工业合成氨主要采用Haber-Bosch工艺,然而该工艺需要高温高压,不仅消耗大量能源,而且会产生大量CO,因此,开发清洁高效合成氨新途径具有深远意义[2].目前氨的绿色合成方法主要包括电催化[3]、光催化[4]、光电催化以及生物催化等[3].其中,電化学合成氨(NRR)因具有节约能源、操作简便以及易于规模化、可实现分布式产氨等优点而成为研究的热点.然而,由于N键能较大(达945 kJ mol),因此需要高效电催化剂来还原N[5].目前常用的NRR催化剂中,贵金属电催化剂(Ru[6]、Au和Ag[7]等)表现出很好的催化活性,但是它们往往存在较强的析氢(HER)副反应,从而降低了NRR的法拉第效率(FE),并且贵金属昂贵,难以大规模应用;非贵金属或非金属催化剂主要有过渡金属氧化物类(FeO[8]、TiO[9]、CoO[10]等),过渡金属硫化物类(FeS[1]、MoS[12]等),非金属类(薄层黑磷纳米片[13]、MXene纳米片[14]、氮磷共掺杂多孔碳[15])等,这些催化剂不仅活性较高,而且价格低廉,因此受到较多关注.金属有机骨架(MOFs)具有高比表面积、可控的孔结构、均匀的结晶度,特别是它的不饱和金属阳离子或金属团簇可很方便设计成催化活性物种,是一类优异的催化材料[16],其中过渡金属- MOFs材料作为催化剂的研究受到了较多关注,Zhao等人[17]的研究表明,以MOF(Fe)为催化剂,在1.2 V时,氨产率和电流效率分别为2.19×10 mol s cm、1.43%.Zhang等人[18]报道了MOF衍生的梭状VO/C作为NRR催化剂,当电位为-0.6 V (vs.RHE)时,氨产率和法拉第效率分别为12.3 μg h mg和7.28%.Cui等人[19]报道了二维Mo基MOF作为NRR催化剂的密度泛函理论研究,结果表明,MOF对N的吸附能力要强于对HO的吸附能力,因此MOFs对氮气具有高选择性.
尽管电化学合成氨的研究已经取得了一定进展,但反应温度较高、氨转化率和法拉第效率较低等问题还没有得到彻底解决.同时,在电化学催化反应中,外磁场会影响催化剂的电子自旋和溶液中电荷的迁移,从而促进电催化过程的进行[20-22].如Koza等人的研究表明,磁场中洛伦兹力引起的磁流体对流可以促进电解液的循环,加速气泡与电极的分离[23-24].因此,本文以均苯三甲酸(1,3,5-BTC)为有机配體,通过改变金属中心,制备了四种MOFs材料(M-BTC,M=Fe、Co、Ni、Cu),测试了其低温NRR性能,进而探讨了外交流磁场强度对催化剂NRR性能的影响及相应的机理.
1实验部分
1.1试剂及材料
九水硝酸铁[Fe(NO)·9HO]、六水硝酸钻[Co(NO)·6HO]、六水硝酸镍[Ni(NO)·6HO]、六水硝酸铜[Cu(NO)·6HO]、均苯三甲酸(1,3,5- BTC)、氢氟酸(HF)、二甲基甲酰胺(DMF)、甲醇(CHOH)、去离子水(HO)等均为分析纯,疏水碳纸(HCP030P)和导电石墨(VXC72R)均采购自上海河森电气有限公司.
1.2催化剂制备
参考文献[25]中的水热法,并进行部分改进用于Fe-MOF的合成,具体步骤如下:室温下,分别将2.828 gFe(NO)·9HO和0.966 g 1,3,5-BTC超声分散于10 ml去离子水中,14 mmol HF超声分散于30 mL去离子水中,分别标记为A、B和C溶液,将B与C混合后搅拌1 h,然后将C溶液滴加入A和B的混合溶液中,再搅拌1h,最后将所得混合液转移到聚四氟乙烯水热反应釜中,在150℃下反应72 h后,自然冷却至室温.所得混合物用乙醇和去离子水分别离心洗涤3次,然后在60℃下烘干24 h,得到Fe-MOF.
Co-MOF[17]、Ni-MOF[26]、Cu-MOF[27]与Fe-MOF的合成方法类似,分别参考相关文献进行.
1.3材料表征
采用X射线衍射仪(XRD SmartLab 3 kW)对制备的催化剂进行物相分析,测试条件:Cu-Ka射线,扫描范围5°~80°,步长0.02,扫描速度8°/min.
采用场发射扫描电子显微镜(Hitachi S-4800)对催化剂进行微观形貌观察.
采用Thermo Scientific Nicolet 10在400~4 000 cm的范围内采集MOFs的傅里叶变换红外光谱,分析材料可能存在的官能团.
1.4电化学合成氨气测试
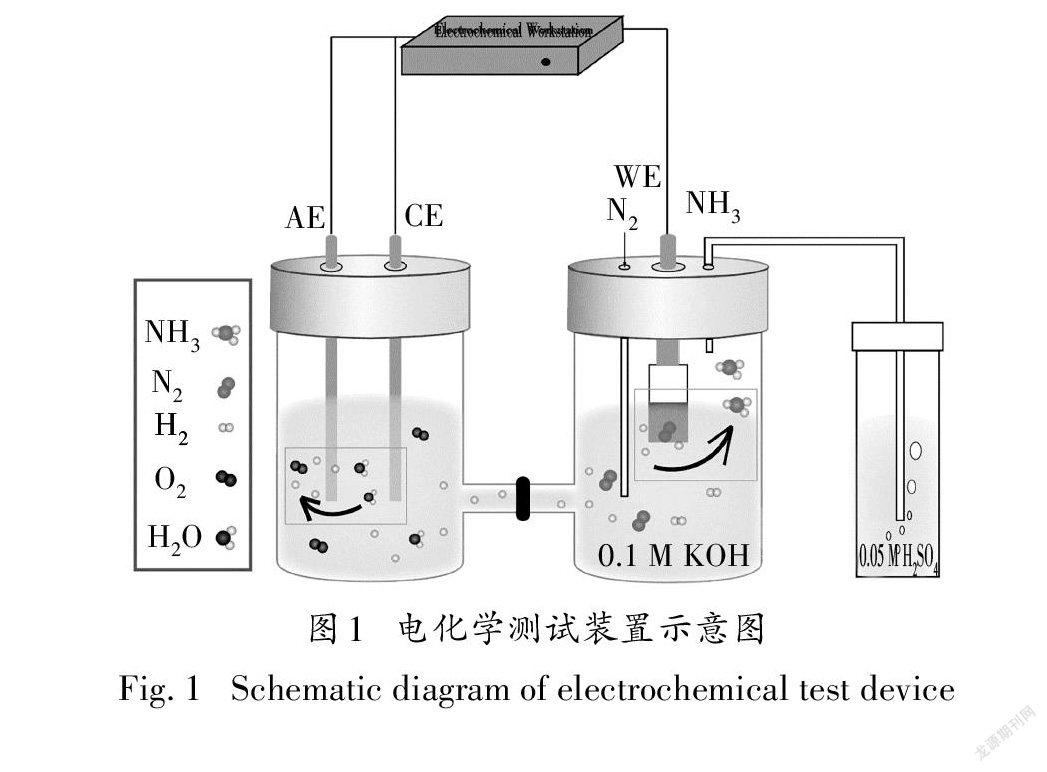
将疏水炭纸裁成1 cm×2 cm的大小,在无水乙醇中超声30min然后在80 ℃下烘干24 h备用.称取0.017 5 g催化剂,然后加入0.007 5 g导电石墨,1 mL无水乙醇,100 μL Nafion溶液,混合物在室温下超声30 min,得到黑色混合油墨.量取100μL混合油墨滴在疏水碳纸1 cm×1 cm的面积上,然后在室温下干燥24 h,得到工作电极[17].工作电极上催化剂的负载量均为1.59 mg cm.以1M KOH为电解液,在三电极的H型电解池中进行电化学合成氨实验,实验装置如图1所示.
采用Pt丝为阳极,Hg/HgO电极为参比电极,Nafion膜为质子导体,在CHI 760E电化学工作站测试催化剂的活性,用20 mL 0.05 mol/L HSO溶液收集产物.采用靛酚蓝分光光度法检测氨的浓度[28],采用Watt和Chrisp法进行副产物肼的检测[28].氨产率通过公式(1)得到[28]:
式中:C(NH)表示NH的浓度(mol mL);y表示HSO收集液的体积(mL);t表示反应时间(s);A表示工作电极上负载催化剂的面积(cm).法拉第效率由公式(2)得到[28]:
式中:F表示法拉第常数;Q表示用电量(C).
2结果与讨论
2.1催化剂的组成和微观结构表征
2.2.1四种催化剂的组成表征
四种MOFs材料的XRD图谱如图2所示,其中,Fe-MOF的主要衍射峰分别位于6.2°、10.2°、11.0°、20.1°附近,与Fe-BTC [MIL-100(Fe)]的模拟衍射峰基本一致[25].Co-MOF的主要衍射峰分别位于11.1°、17.8°、20.1°、27.3°、35.8°附近,与Co-BTC的模拟衍射峰基本一致[17].Ni-MOF的主要衍射峰分别位于12.0°、12.7°、14.4°、22.6°、26.5°处,与Ni-BTC的模拟衍射峰基本一致[26].Cu-MOF的主要衍射峰分别位于6.7°、9.5°、11.6°、13.4°、16.5°、17.5°、19.0°、20.2°、25.9°、27.5°,与Cu-BTC的模拟衍射峰基本一致[27].同时四种MOFs的衍射峰的强度均比较高.这表明合成的四种MOFs分别为Fe-BTC、Co-BTC、Ni-BTC、Cu- BTC,且具有良好的晶体结构.
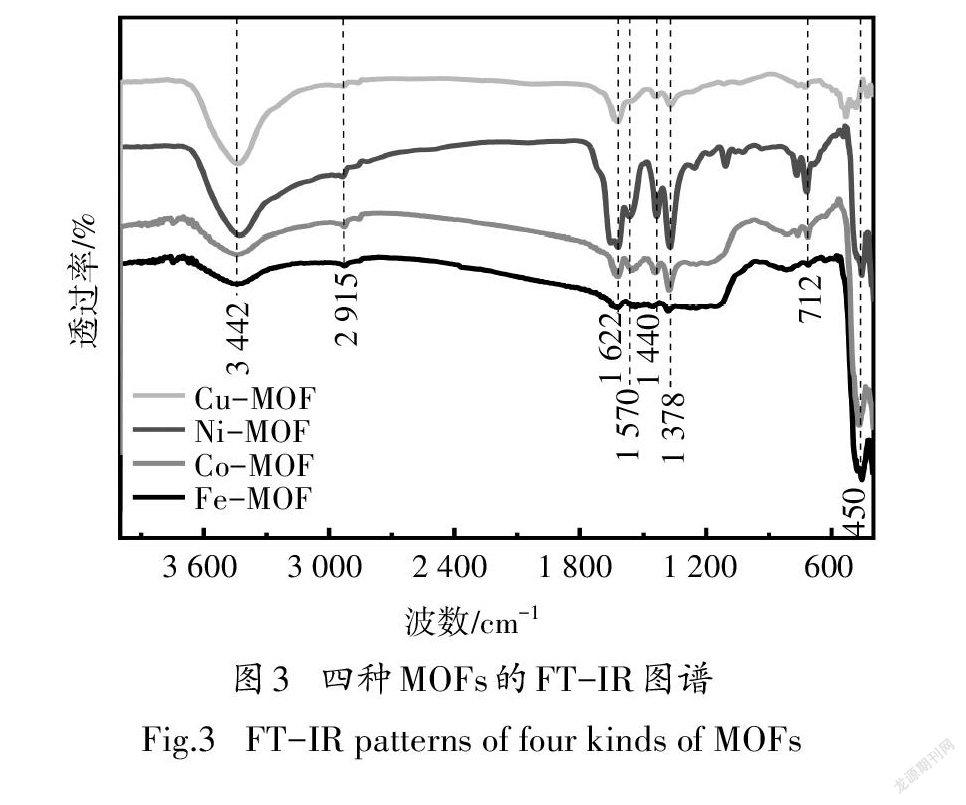
图3为四种MOFs材料的FT-IR图谱.可以看出,四种材料的吸收峰的位置基本一致,在3 442 cm附近的吸收峰为水中-OH的伸缩振动,2 915 cm附近的吸收峰为1,3,5均苯三甲酸中-CH振动,在1 622 cm和1 378 cm较明显的吸收峰分别为1,3,5均苯三甲酸中-COO键的非对称振动和对称振动,1 573 cm和1 440 cm處是苯环中C=C键的伸缩振动,712cm处的峰是苯环上1,3,5三处取代位置的吸收峰,而在420 cm有较明显的吸收峰,表明在该处存在Fe-O键、Co-O键、Ni-O键、Cu-O键的拉伸振动[17,29-30].表明合成的MOFs骨架结构中含有较为完整的均苯三甲酸有机骨结构,且具有良好的成键状态和分子结构特征.
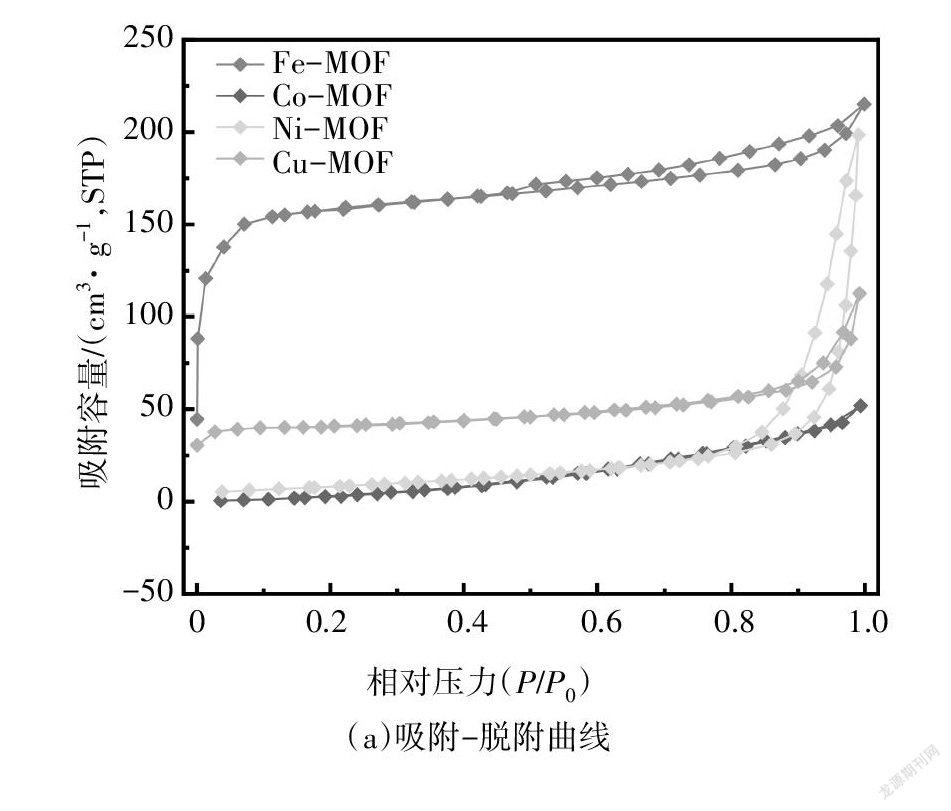
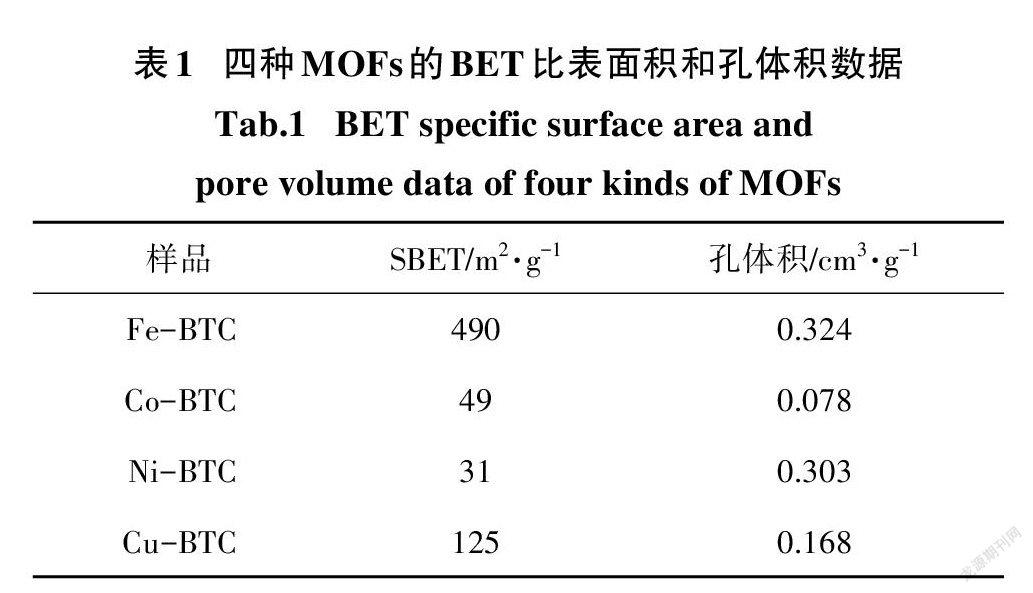
图4(a)和(b)分别为四种MOFs的氮气吸附-脱附曲线和孔径分布曲线,由图可以看出四种MOFs均表现出类I型氮气吸附-脱附等温曲线特征,其中Fe-BTC和Cu-BTC在低压下均具有N吸附量,并且Fe-BTC在低压下的N吸附量高于Cu-BTC的N吸附量,表明Fe-BTC和Cu-BTC均具有微孔结构,并且Fe-BTC的微孔要多于Cu-BTC.此外,四种MOFs均具有介孔和大孔结构.表1显示了四种MOFs(Fe- BTC,Co-BTC,Ni-BTC,Cu-BTC)的BET比表面积分别为490 m g、49 m g、31 m g和125 m g,四种MOFs中,Fe-BTC的BET比表面积最高.
2.1.2不同金属离子对MOFs材料微观形貌的影响
四种材料的微观形貌如图5所示,Fe-BTC和Cu-BTC主要由八面双锥的颗粒组成,其中Fe-BTC的粒径为320~350 nm,与报道的文献类似[25].CoBTC主要由菱形十二面体颗粒组成,粒径约为1.5 μm,与之前报道的文献类似[17].Ni-BTC则为片状结构,片层厚度为100~150 nm左右.与之前报道的文献类似[26].而Cu-BTC的粒径约为1μm,与之前的报道类似[27].
2.2MOFs的NRR性能研究
2.2.1四种催化剂的NRR性能比较
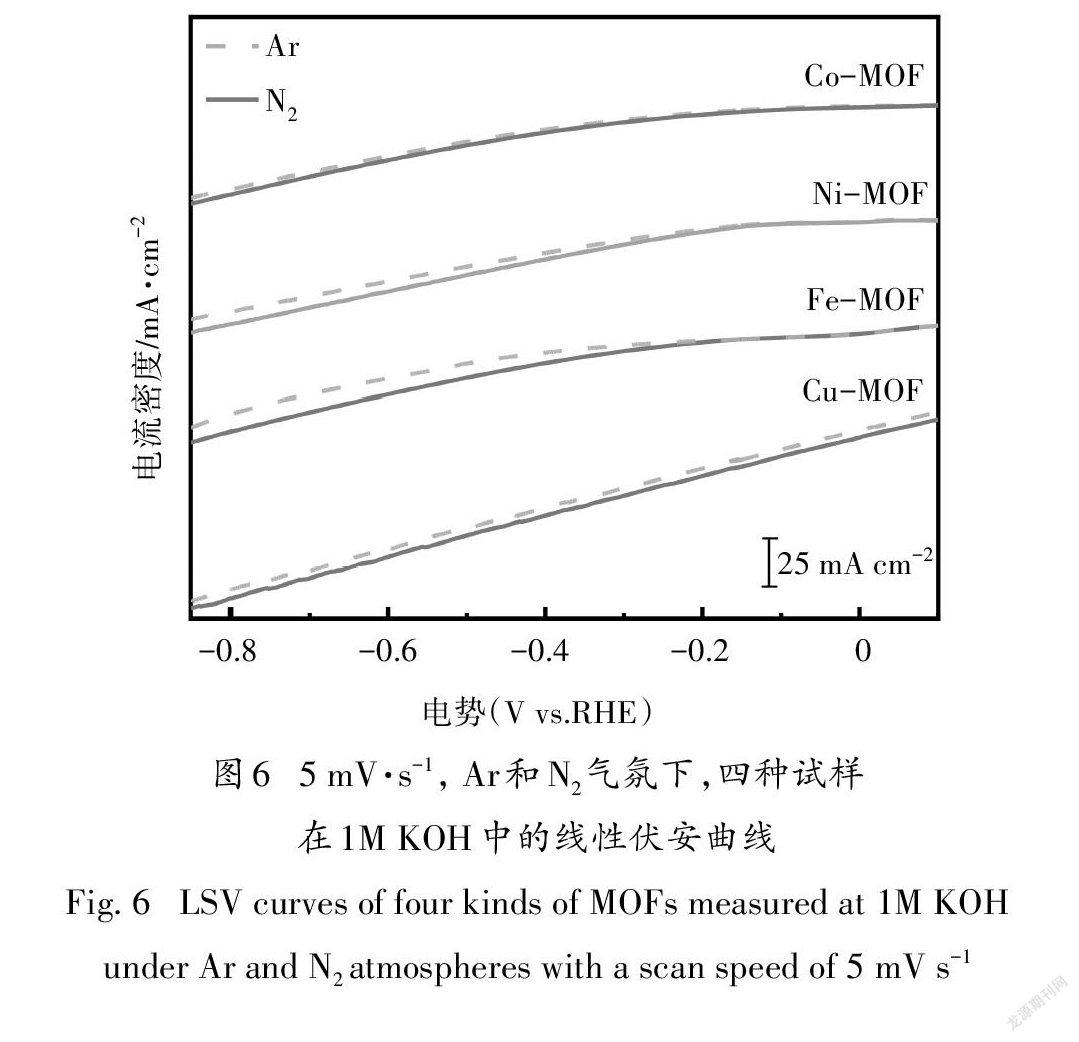
为测试四种MOFs的NRR活性,首先分别在N和Ar气氛下测试了催化剂的LSV曲线(见图6).由图中可以看出,四种MOFs在N气氛中的负电流明显高于Ar气氛下的相应数值,说明四种材料均具有NRR活性[32].对Fe-BTC来说,当电位低于-0.15 V时,N气氛下的电流密度值高于Ar气氛下的,说明从-0.15 V开始,该材料呈现出NRR活性;而其余3种催化剂,均是从0 V开始,M气氛下的电流密度值高于Ar气氛下的.同时比较N和Ar下四种材料的净电流密度,Fe-BTC在-0.758V(vs.RHE)时净电流密度最大,为9.70 mA cm,这表明:四种MOFs中,Fe-BTC具备最佳的NRR活性[32].
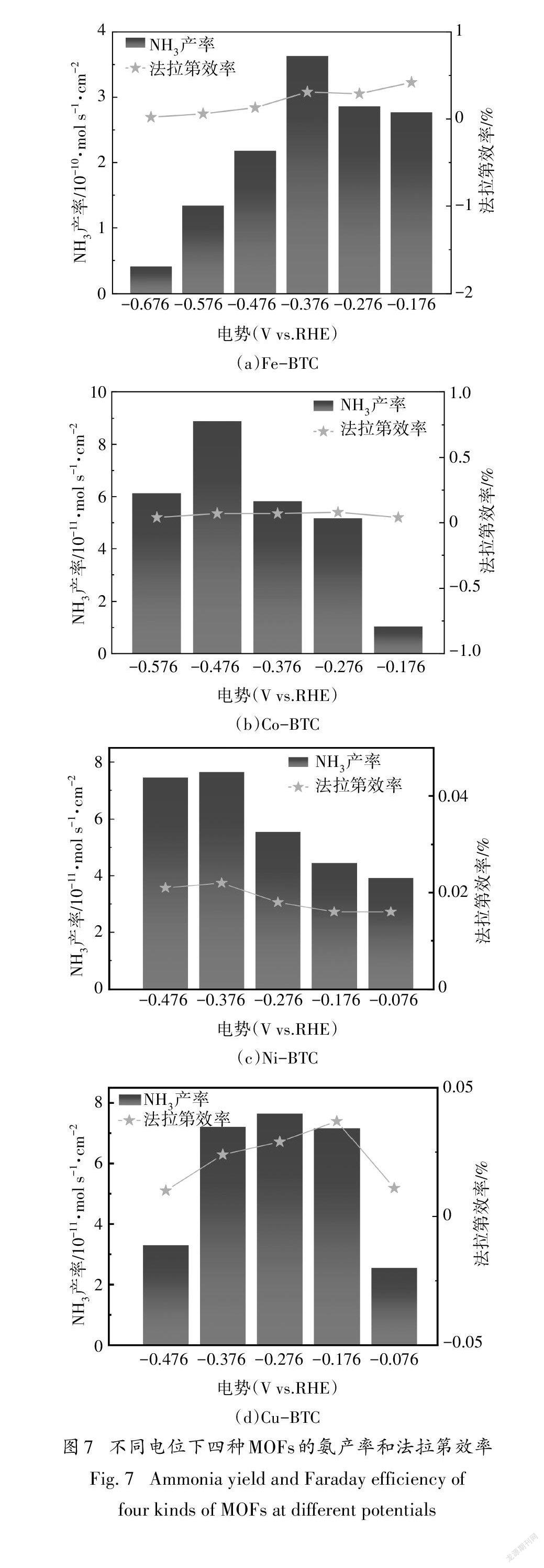
为进一步探究四种MOFs材料的NRR活性,分别将催化剂在一系列的电位下进行了2 h的测试,结果见图7.对比四种催化剂的氨产率和法拉第效率,Fe-BTC在-0.376V(vs.RHE)下显示出最高的氨产率和法拉第效率,分别为3.63×100mol·s·cm和0.31%,而Co-BTC在-0.176V(vs.RHE)时显示最低的氨产率和法拉第效率,仅为1.04×10mol s cm和0.04%,这归因于Fe-BTC较小的粒径和优异的N吸附能[19],以及相比其他三种MOFs,Fe-BTC具有较大的BET比表面积,同时在整个反应中没有副产物肼的生成[33].
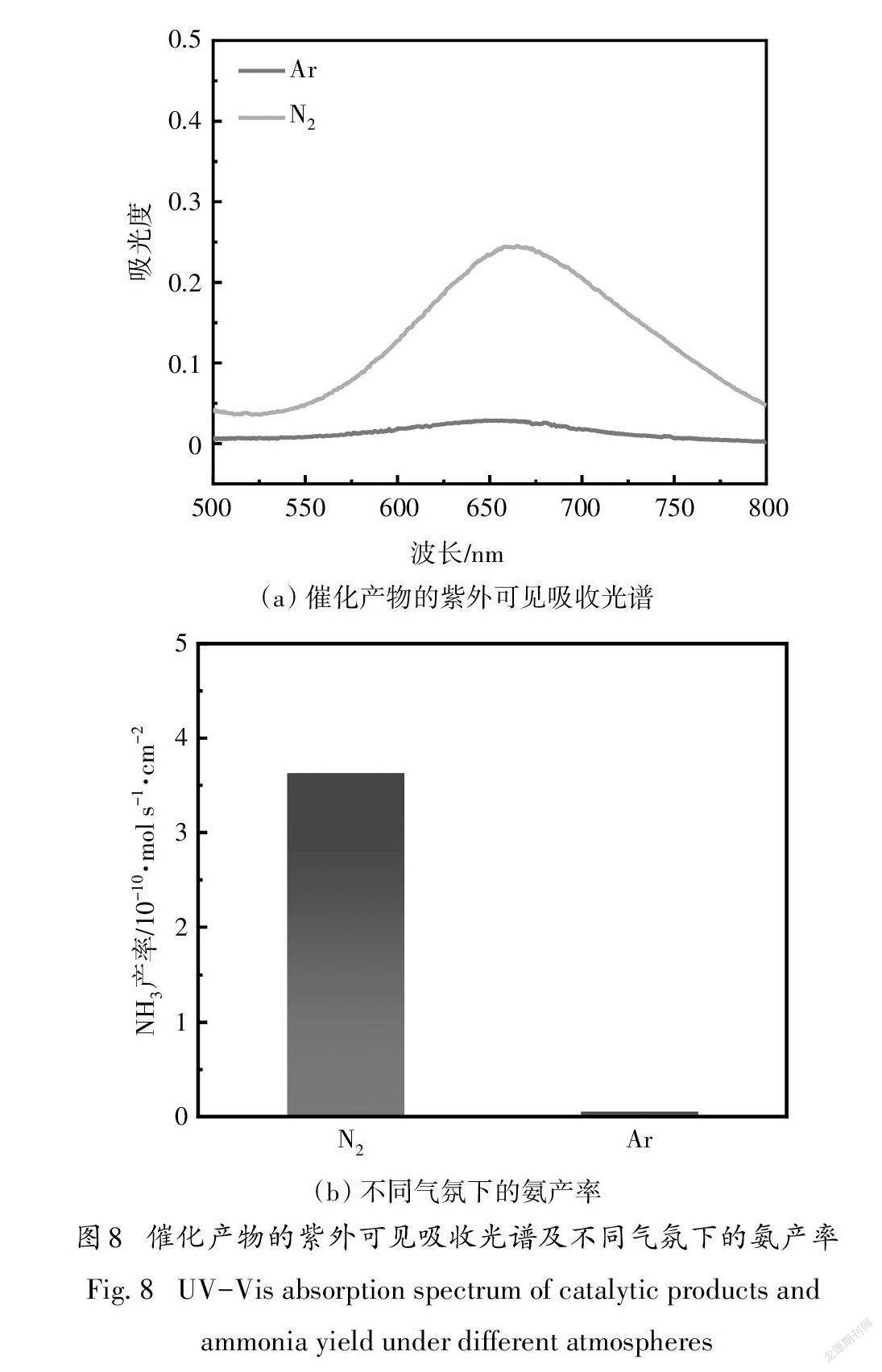
为了证实检测到的氨是N在Fe-BTC上面通过NRR过程产生的,以-0.376 V(vs.RHE)为恒电位,Fe-BTC为催化剂,分别在N和Ar气氛下进行了2h电催化实验,结果如图8所示.在电位为-0.376 V(vs. RHE)时,用Ar代替N进行2h的电催化实验,并用靛酚蓝分光光度法对收集装置里的液体进行NH检测,结果显示在Ar中几乎没有NH产生,因此说明NH的产生是由于N在Fe-BTC上面发生了NRR过程.
2.2.2温度对Fe-BTC NRR性能的影响
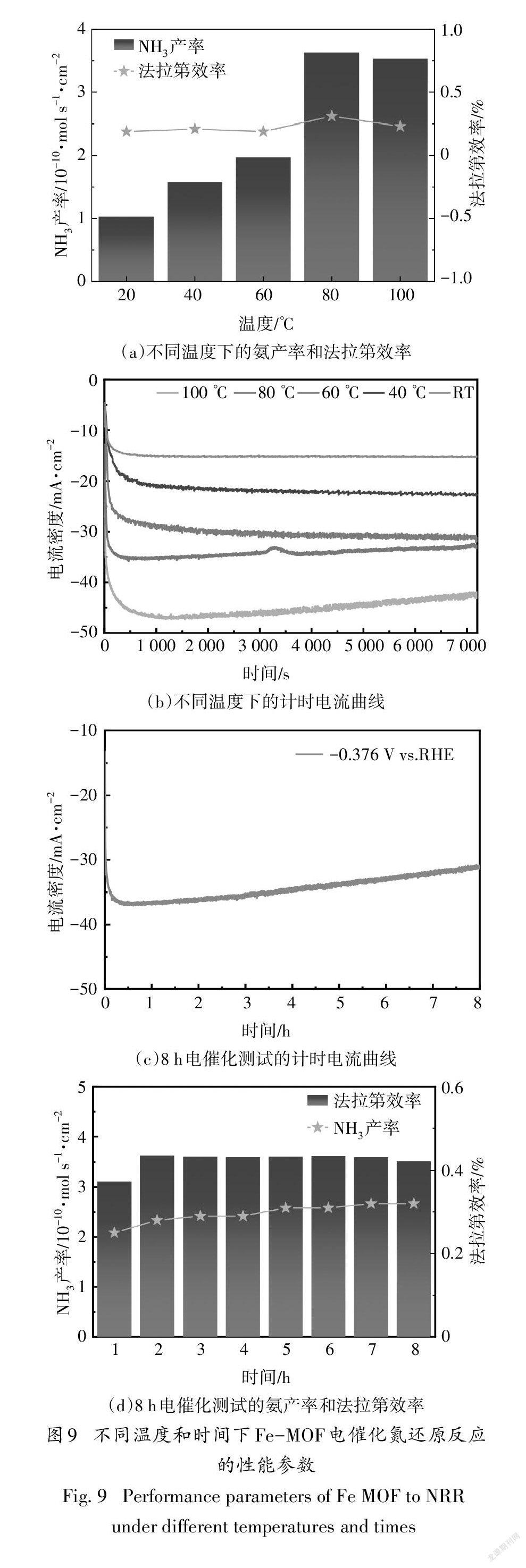
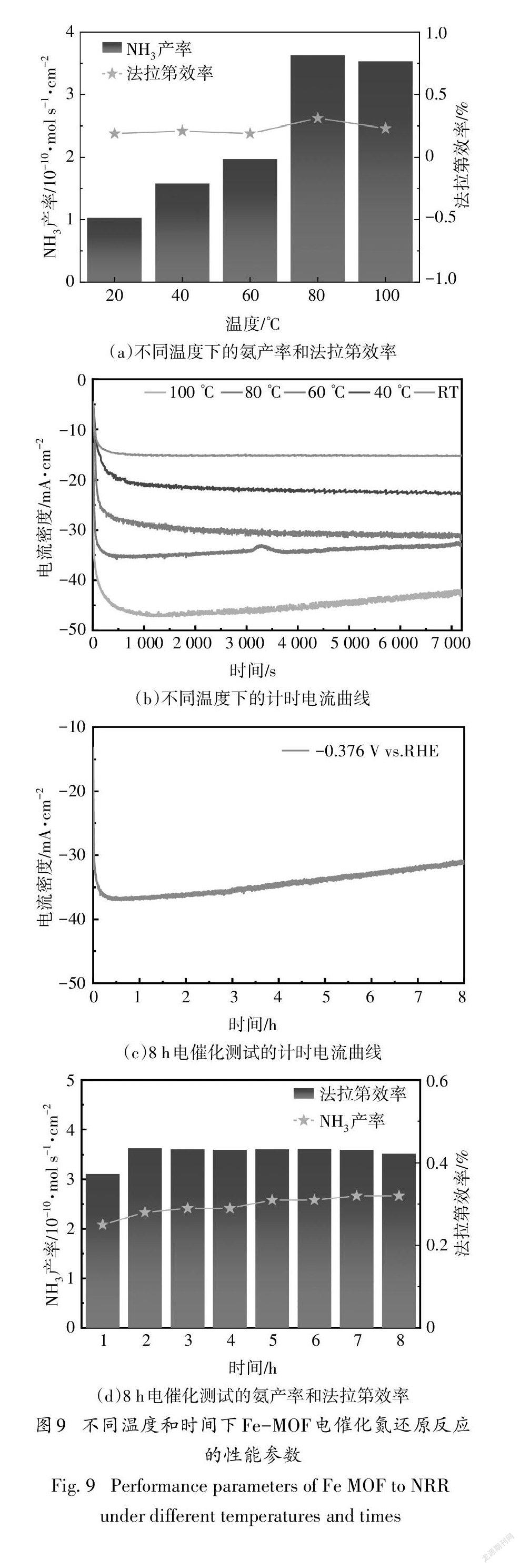
为了探究Fe-BTC的最佳反应温度,在不同温度下研究了催化剂的NRR活性.图9(a)为Fe-BTC在不同温度下的氨产率和法拉第效率,可以看出,从20 ℃到80 ℃,随温度的上升,氨产率增加,当温度达到80 ℃时,氨产率和法拉第效率最高,分别为3.63×10mol·s·cm和0.31%,约为20 ℃时的3.5倍和1.6倍,这是由于随温度升高,电解液的传质速率提高所致[17].图9(b)为不同温度下发生NRR的计时电流曲线.由图可知,从最初到1 000 s时,催化剂的电流急剧下降,这是由于电解液中+的阻塞效应[36-37],1 000 s以后,电流趋于稳定;随温度升高,稳定状态下的电流值逐渐增加.当温度为100 ℃时,3 000 s以后电流数值开始降低,这可能是由于过高的温度不仅导致Nafion质子交换膜的传质效率变差,同时催化剂的NRR活性衰减共同作用的结果[38].总之,从20 ℃升温到80 ℃,总电流随温度的升高而升高,一方面这是由于随着温度的升高,H的产生速度更快.这是由于阳极的反应为:
陽极产生的H通过质子交换膜转移到阴极得到电子后与活化氮结合,生成NH.而反应(3)会受到温度影响,当温度从20 ℃上升到80 ℃,随着温度的升高,阳极的H的产生速度加快,通过质子交换膜到达阴极后形成的H原子也相应增多,与活化氮结合生成NH的量增加,因此氨产率也就更高.另一方面,温度的升高使得质子交换膜的质子传导速率加快[36],但是当温度升到100℃时,质子交换膜的传质效率变差,并且H原子在阴极不仅与活化氮结合形成NH,还会形成大量的H作为副产物,而产生H也会消耗电流密度,因此氨产率和法拉第效率也相应降低.
2.2.3催化剂循环稳定性研究
稳定性是对催化剂性能的一个重要衡量指标. 对Fe-BTC进行了8h的循环稳定性测试,每隔1 h为一个循环,图9(c)和(d)为催化剂8 h的循环稳定性测试的计时电流曲线和氨产率及法拉第效率,图9(c)的计时电流曲线显示,在第5h后有轻微的电流衰减,因此也导致氨产率和法拉第效率有轻微的减小,这种减小与电解初始的氨产率和法拉第效率相比,可以忽略不计.由图9(d)可知,8h内,催化剂的氨产率和法拉第效率数值的变化非常小.
2.2.4交流磁场对Fe-MOF电化学氮还原性能的影响
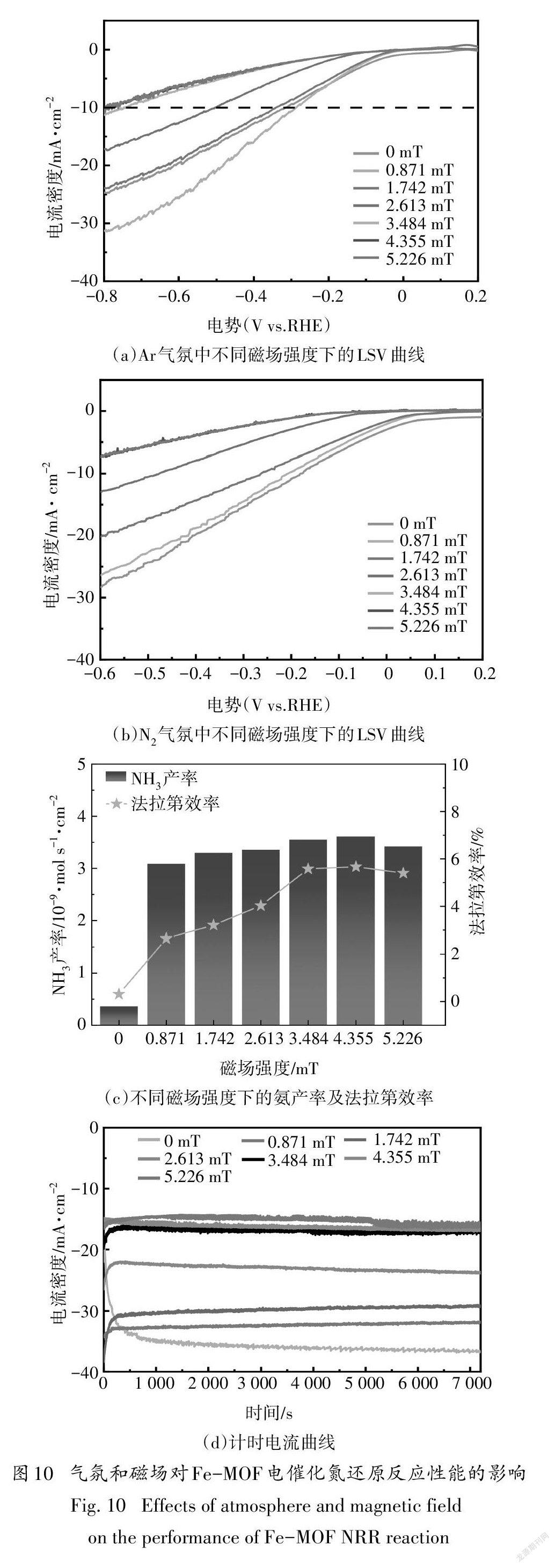
固定电压和温度(-0.376V,80℃),施加外交流磁场,测试磁场强度对催化剂NRR性能的影响.本实验测试了Fe-BTC在不同磁场强度下,Ar和气氛下的线性伏安曲线图,结果分别如图10(a)和(b)所示.由图10(a)可知,在Ar气氛中,当磁场强度从0 mT增大到0.871mT时,催化剂的过电位逐渐降低,这说明外磁场对析氢起到促进作用,当磁场强度进一步增加,催化剂的过电位开始增大,这说明外磁场开始对析氢起到抑制作用.已经有文献报道,析氢反应会受到交流磁场的的影响,在交流磁场中,其影响趋势是随着磁场强度的增大,析氢反应呈现低促高抑的趋势[34,35].
图10(c)为不同强度的交流磁场下,催化剂的氨产率和法拉第效率.与未引入磁场相比,上述数据均有提高,特别是当磁场强度为4.355 mT时,催化剂的氨产率为3.61×10 mol s cm,比不施加交流磁场时提高大约10倍,法拉第效率为5.67 %,比不加磁场时提高了约18倍.这种现象解释为:第一,在固液反应中,磁场会影响吸附量,并且最大的吸附量对应一定的磁场强度139],在本反应中,交流磁场的引入起到了增加N在Fe-BTC表面的吸附量的作用[31].在本反应中,交流磁场的引入可以增加N在Fe-BTC表面的吸附量[31],从而导致催化剂表面存在更多的活化氮,因此氨产率得到提升,在磁场强度从0mT增加到0.871 mT时,催化剂的过电位减小,对析氢反应起到促进作用,这样导致阳极处H浓度增加,从而通过质子交换膜扩散到阴极形成的H原子浓度同样增加,与此同时,磁场也导致阴极处催化剂表面存在更多的活化氮,从而导致N与H反应生成氨的转化率和法拉第效率相应提高;第二,交流磁场产生的感应电动势与施加的电势产生了叠加作用,相当于提供了额外的能量[40],并且磁场强度从0.871 mT增加到4.355 mT,交流磁场还对NRR的副反应HER起到了明显的抑制作用,因此NRR的氨产率和法拉第效率进一步提高.而当磁场强度从4.355 mT增大到5.226 mT时,磁场对HER的抑制作用不明显,而氨产率和法拉第效率的变化也就不明显.而由图10(d)可发现,在N中施加交流磁场时,当磁场强度由0 mT增加到4.335 mT时,催化剂的电流密度值随磁场强度的增大而减小;当磁场从4.335 mT增大到4.226 mT时,电流密度几乎无变化,这是由于交流磁场产生的感应电动势与施加电压的电势产生了叠加作用,从而使得极化电流发生变化所致[34],并且图10(d)中不同磁场下的计时电流曲线表明,在施加磁场时催化剂也具有较高的稳定性.
3结论
本研究通过水热法制备出了具有完整的晶型结构的Fe-BTC、Co-BTC、Ni-BTC、Cu-BTC四种MOFs,其中,Fe-BTC的NRR活性最佳,在-0.376V(vs. RHE)和80℃时具有最高的氨产率和法拉第效率,数值分别为3.63×100mol·s·cm和0.31%.选用NRR活性最佳的Fe-BTC,加入磁场后,催化剂的氨产率(为3.61×10 mol·s·cm)和法拉第效率(为5.67%),分别比之前提高了约10倍和18倍,这种现象主要由于交流磁场增加了N在Fe-BTC表面的吸附量,以及交流磁场产生的感应电动势与电场本身的电势的叠加作用,为NRR反应提供了额外的能量所致.
参考文献
[1] MARNELLOS G,STOUKIDES M. Ammonia synthesis at atmospheric pressure[J]. Science,1998,282(5386):98-100.
[2] LIU H Z. Ammonia synthesis catalyst 100 years:practice,enlightenment and challenge [J]. Chinese Journal of Catalysis,2014,35 (10):1619-1640.
[3] GUO C X,RAN J R,VASILEFF A,et al. Rational design of electrocatalysts and photo (electro)catalysts for nitrogen reduction to ammonia(NH3)under ambient conditions [J]. Energy & Environmental Science,2018,11(1):45-56.
[4] SCHRAUZER G N,GUTH T D. Photolysis of water and photoreduction of nitrogen on titanium dioxide [J]. Journal of the American Chemical Society,1977,99(22):7189-7193.
[5] KITANO M,INOUE Y,YAMAZAKI Y,et al. Ammonia synthesis using a stable electride as an electron donor and reversible hydrogen store[J].Nature Chemistr,2012,4(11):934-940.
[6] WANG Z Q,LI C J,DENG K,et al. Ambient nitrogen reduction to ammonia electrocatalyzed by bimetallic PdRu porous nanostructures[J].ACS Sustainable Chemistry & Engineering,2019,7 (2):2400-2405.
[7] SHI M M,BAO D,WULAN B R,et al. Au sub-nanoclusters on TiO,toward highly efficient and selective electrocatalyst for N,conversion to NH3 at ambient conditions[J].Advanced Materials,2017,29(17):1606550.
[8] MANJUNATHA R,KARAJIC A,GOLDSTEIN V,et al. Electrochemical ammonia generation directly from nitrogen and air using an iron-oxide/titania-based catalyst at ambient conditions [J]. ACS Applied Materials & Interfaces,2019,11(8):7981-7989.
[9] ZHANG R,REN X,SHI X F,et al. Enabling effective electrocatalytic N conversion to NH3 by the TiO nanosheets array under ambient conditions [J]. ACS Applied Materials Interfaces,2018,10(34):28251-28255.
[10] CHU K,LIU Y P,LI Y B,et al. Efficient electrocatalytic N reduction on CoO quantum dots [J]. Journal of Materials Chemistry A,2019,7(9):4389-4394.
[11] SULTANA S,MANSINGH S,PARIDA K M.Phosphide protected FeS2 anchored oxygen defect oriented CeO2NS based ternary hybrid for electrocatalytic and photocatalytic N reduction to NH3 [J].Journal of Materials Chemistry A,2019,7(15):9145-9153.
[12] ZHANG L,JI X Q,REN X,et al. Electrochemical ammonia synthesis via nitrogen reduction reaction on a MoS2 catalyst:theoretical and experimental studies[J].Advanced Materials,2018,30 (28):1800191.
[13] ZHANG L L,DING L X,CHEN G F,et al.Ammonia synthesis under ambient conditions:selective electroreduction of dinitrogen to ammonia on black phosphorus nanosheets [J]. Angewandte Chemie International Edition,2019,58(9):2612-2616
[14] ZHAO J X,ZHANG L,XIE X Y,et al. TiCT(T=F,OH)MX-ene nanosheets:conductive 2D catalysts for ambient electrohydrogenation of N to NH [J] Journal of Materials Chemistry A,2018,6(47):24031-24035
[15] SONG P F,WANG H,KANG L,et al Electrochemical nitrogen reduction to ammonia at ambient conditions on nitrogen and phosphorus co-doped porous carbon[J] Chemical Communications (Cambridge,England),2019,55(5):687-690
[16] KIRCHON A,FENG L,DRAKE H F,et al From fundamentals to applications:a toolbox for robust and multifunctional MOF materials[J] Chemical Society Reviews,2018,47(23):8611-8638
[17] ZHAO X R,YIN F X,LIU N,et al. Highly efficient metal - organic-framework catalysts for electrochemical synthesis of ammonia from N(air)and water at low temperature and ambient pressure[J] Journal of Materials Science,2017,52(17):10175- 10185
[18] ZHANG R,HAN J R,ZHENG B Z,et al Metal - organic framework-derived shuttle-like V2O3/C for electrocatalytic N2 reduction under ambient conditions[J]. Inorganic Chemistry Fron- tiers,2019,6(2):391-395
[19] CUI Q Y,QIN G Q,WANG W H,et al Mo-based 2D MOF as a highly efficient electrocatalyst for reduction of N to NH:a density functional theory study[J]. Journal of Materials Chemistry A,2019,7(24):14510-14518
[20] BUND A,KOEHLER S,KUEHNLEIN H H,et al Magnetic field effects in electrochemical reactions[J]. Electrochimica Acta,2003,49(1):147-152
[21] ZHU J H,CHEN M J,QU H L,et al Magnetic field induced capacitance enhancement in graphene and magnetic graphene nano- composites[J]. Energy Environ Sci,2013,6(1):194-204
[22] OKADA T,WAKAYAMA N I,WANG L B,et al The effect of magnetic field on the oxygen reduction reaction and its application in polymer electrolyte fuel cells[J]. Electrochimica Acta,2003,48(5):531-539
[23] KOZA J A,UHLEMANN M,GEBERT A,et al Desorption of hydrogen from the electrode surface under influence of an external magnetic field[J]. Electrochemistry Communications,2008,10 (9):1330-1333.
[24] KOZA J A,MUHLENHOFFS,UHLEMANN M,et al. Desorption of hydrogen from an electrode surface under influence of an external magnetic field —In-situ microscopic observations[J]. Electrochemistry Communications,2009,11(2):425—429.
[25] SONG G Q,WANG Z Q,WANG L,et al. Preparation of MOF (Fe)and its catalytic activity for oxygen reduction reaction in an alkaline electrolyte [J]. Chinese Journal of Catalysis,2014,35 (2):185—195.
[26]蘇燕平.Ni-BTC MOFs衍生材料及其性能研究[D].合肥:中国科学技术大学,2017.
SU Y P. The synthesis and applications of Ni—BTC MOFs derivatives [D]. Hefei:University of Science and Technology of China,2017. (In Chinese)
[27] LI L L,LIU Y Y,AI L H,et al. Synthesis of the crystalline porous copper oxide architectures derived from metal-organic framework for electrocatalytic oxidation and sensitive detection of glucose[J].Journal of Industrial and Engineering Chemistry,2019,70:330—337.
[28] DU H T,GUO X X,KONG RM,et al. Cr 2 O nanofiber:a high- performance electrocatalyst toward artificial N fixation to NH 3 under ambient conditions[J].Chemical Communications(Cambridge,England),2018,54(91):12848—12851.
[29] RANFT A,BETZLER S B,HAASE F,et al.Additive—mediated size control of MOF nanoparticles [J]. CrystEngComm,2013,15(45):9296.
[30] HASAN Z,JEON J,JHUNG S H.Adsorptive removal of naproxen and clofibric acid from water using metal—organic frameworks[J].Journal of Hazardous Materials,2012,209/210:151 —157.
[31]朱傳征,戴立益,杨宝林,等.常压下磁场对合成氨催化反应影响的研究[J].华东师范大学学报(自然科学版),1998(2):51—54.
ZHU C Z,DAI L Y,YANG B L,et al.Study on the effect of magnetic field on the catalytic reaction synthetic ammonia at the atmospheric pressure[J].Journal of Eastchina Normal University(Natural Science),1998(2):51—54.(In Chinese)
[32] LUO S J,LI X M,ZHANG B H,et al. MOF-derived Co O @NC with core-shell structures for N electrochemical reduction under ambient conditions [J]. ACS Applied Materials & Interfaces,2019,11(30):26891-26897.
[33] SHIPMAN M A,SYMES M D.Recent progress towards the electrosynthesis of ammonia from sustainable resources[J].Catalysis Today,2017,286:57-68.
[34] ZHENG H B,CHEN H H,WANG Y L,et al.Fabrication of magnetic superstructure NiFeO@MOF—74 and its derivative for electrocatalytic hydrogen evolution with AC magnetic field[J].ACS Applied Materials & Interfaces,2020,12(41):45987-45996.
[35] KORDALI V,KYRIACOU G,LAMBROU C. Electrochemical synthesis of ammonia at atmospheric pressure and low temperature in a solid polymer electrolyte cell[J].Chemical Communications,2000(17):1673-1674.
[36] LAN R,TAO S W.Electrochemical synthesis of ammonia directly from air and water using a Li/H/NH mixed conducting electrolyte[J].RSC Advances,2013,3(39):18016.
[37] MONTOYA J H,TSAI C,VOJVODIC A,et al. The challenge of electrochemical ammonia synthesis:a new perspective on the role of nitrogen scaling relations[J].ChemSusChem,2015,8(13):2180-2186.
[38] MALIS J,MAZUR P,PAIDAR M,et al. Nafion 117 stability under conditions of PEM water electrolysis at elevated temperature and pressure[J].International Journal of Hydrogen Energy,2016,41(4):2177-2188.
[39] ZRUNCHEV I A. Macrokinetics of catalyses with a ferromagneticcatalyst fluidized in magnetic field [J]. Dokl Bolg A kad Nauk,1974,27(10):1379-1382.
[40] WANG J H,MA Y W,WATANABE K.Magnetic-field-induced synthesis of magnetic γ-FeO nanotubes [J]. Chemistry of Mate- rials,2008,20(1):20-22.
