ATP生物荧光法在乳品企业清洗效果评价方面的应用
2022-11-11丘勒红梁俊健林淑仪林夏纯杨爱君
丘勒红,梁俊健,林淑仪,林夏纯,何 瑛,杨爱君
广东燕塘乳业股份有限公司,广东广州 510700
0 引言
牛奶中富含营养物质,非常容易滋生细菌等微生物,而清洗可以去除生产线上的牛奶残留,切断微生物滋生所需的营养,同时减少生产线上的牛奶与微生物形成的生物膜或生物顽垢,让后续的消毒无附着物的遮蔽,而且彻底的清洗是有效消毒的基础[1]。因此,有效清洗是卫生管控的重要措施之一,对清洗效果进行验证则是卫生管控的重要环节。
目前,乳品企业常用感官检查法(如肉眼检测、嗅觉检查等)、传统微生物检测法和ATP生物荧光法进行清洗效果验证。然而,感官检查法需达到工作人员肉眼或嗅觉可辨别的限量,其结果不能量化,且主观因素影响较大;传统微生物检测法耗时长,操作繁琐,检测结果滞后,而且反映的是“无菌”程度,而非“清洗”效果[2]。因此,判断清洗效果不应测量活体微生物的存在,而应通过测量清洗后残留的污染物数量来确定。ATP生物荧光法弥补了感官检查法与传统微生物检测法的局限性,具有快速、准确、灵敏、简便、可靠等优点,能在几十秒内获得检测结果,是目前清洁验证最有效的技术之一。
1 三磷酸腺苷(ATP)生物荧光法的基本原理
三磷酸腺苷(Adenosine Triphosphate,ATP)是含高能磷酸键的有机化合物,是生命过程的主要能量来源。在细菌、酵母菌和霉菌以及所有的动物和植物体中,包括食物和食物残渣中都含有ATP。ATP生物荧光法就是通过脱去1 个或多个磷酸基来释放能量,荧光素获得ATP释放的能量后发光,ATP荧光检测仪把光转化成光电信号,产生读数,检测结果表示为相对光单位(RLU)[3],和ATP的总量成正比,RLU数值越高,表明ATP的量越多,也意味着生物量残留越多。
ATP水平和微生物数量有着密切的相关性,但不能直接将ATP荧光检测仪测定的RLU数值和标准平板计数相对比,因为ATP数值所反映的生物残留,不仅仅是微生物,还包括残留污垢,而残留的污垢是微生物生长的营养源,例如刚生产完灭菌乳而尚未清洗的生产设备,如果采用传统微生物法进行检测,几乎检测不到活菌,但它的RLU数值却会很高,因为残留在设备上的灭菌乳也有ATP。
因此,ATP生物荧光法可以快速判定各个环节的清洁程度,从而达到卫生控制的目的。
2 ATP清洁验证方案的建立、
乳品企业可通过“风险分析,确定采样位点→标准化操作,采集参考数据→设定检测限值→制定采样计划,实施监测→检出异常,分级管控→数据分析,持续改善”等方面建立清洁验证方案。
2.1 风险分析,确定ATP采样位点
乳品企业应根据工艺流程,识别出需要进行清洁效果监测的相应设施设备,以鲜牛奶为例,涉及的设施设备包括奶槽车、收奶管、净乳机、储奶罐、杀菌机、灌装机等,同时要对各设施设备的功能、特性、结构、与产品接触面等信息进行评估,梳理出各设施设备的所有潜在采样位点,如储奶罐,潜在的采样位点包括储奶罐上盖、储奶罐内壁、取样口、搅拌叶、探针、排液口等。最后根据各潜在采样位点对产品质量影响显著程度以及清洗的难易程度建立风险矩阵(图1)进行分析,确定采样位点。
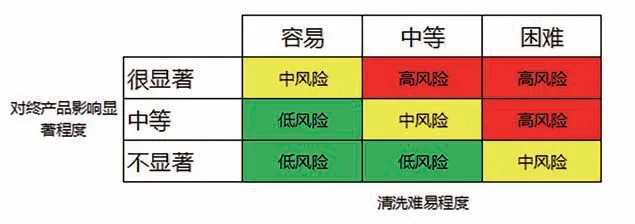
图1 风险矩阵图
采样位点应选择对最终产品质量与卫生影响显著以及清洗难度大的地方,尤其要重点关注表面抛光不佳、焊接点、管道联接处、密封垫圈、清洁死角等位置。
2.2 标准化操作,采集参考数据
采样位点确定以后,便可开始采集检测数据,正确使用采样棒是采集检测数据的基础。常用的采样棒有两种:一种是表面采样棒,专门用于检测清洁后表面清洁程度的测试工具,可以直接对清洁后的设备、器械表面进行涂抹采样。另一种是水质采样棒,专门用于检测难以用涂抹棒采样的区域清洁后的冲洗水样,如在位清洗(CIP)系统,无需拆卸部件,通过对冲洗水的检测来指示相应水中的生物含量。
2.2.1 表面采样棒的使用
将涂抹棒从采样管中抽出,用食指和拇指握住涂抹棒手柄,注意不要碰触采样头。涂抹采样时,使采样棒与待测表面成30°夹角,用力轻压采样棒使采样头紧贴待测位点,水平、上下重复涂抹,直至涂抹完待测区域整个表面。涂抹完成后将采样棒插回并完全按入采样管中,充分混合试剂,激活ATP发光反应,立即将采样管放入检测仪中进行检测[4]。
2.2.2 水质ATP采样棒的使用
用洁净且无菌的容器采集水样,将采样棒从采样管中旋转取出,将采样棒头部完全浸入水样内,保持5 s进行采样。采样完成后将采样棒直立手持,重新旋转插回并完全按入采样管中,激活ATP发光反应,2 min内将采样管放入检测仪中进行检测[5]。
2.2.3 建立统一的操作标准SOP
ATP表面采样棒的采样面积一般为(10×10)cm2,然而并不是所有的检测位点都适合该采样面积,如出奶口、灌注管等检测位点应根据实际结构和性状,制定采样面积[6],采取相应的有效涂抹手法,各位点涂抹手法可以不同,但同一位点每次涂抹时手法必须一致。因此,乳品企业应建立统一的操作标准SOP(图2),明确各采样位点的具体采样位置、采样面积、采样手法等,并做好相关人员的操作培训。

图2 ATP采样操作标准参考模板
一个检测位点应至少重复涂抹采样5 次,对于检测结果波动较大的位点,则需要增加检测数据量。每次采集参考数据时,应对检测位点“清洗前”“清洗后”和“深度清洗后”三方面的检测数据进行采集。“清洗前”的检测数据,即初步冲洗后,开始清洁前采集的检测数据,反映清洁前的表面污染水平;“清洗后”的检测数据,即完成清洁后,消毒杀菌之前采集的检测数据,反映常规清洁后的表面清洁水平,检测时应确保无肉眼可见的污垢;“深度清洗后”的检测数据,即比常规清洁更严格的方式处理后采集的检测数据,反映可实现的目标水平[7]。
2.3 设定检测限值
不同的检测位点可能由于表面材质、老化/损蚀程度、清洗方式等差异表现出不同的RLU水平。乳品企业可根据采集到的参考数据,通过与微生物检验的比对,再结合自身的质量安全控制要求和相应的法律法规,设定相应的限值,一般设置3 个水平:合格、警告、不合格(图3)[8]。
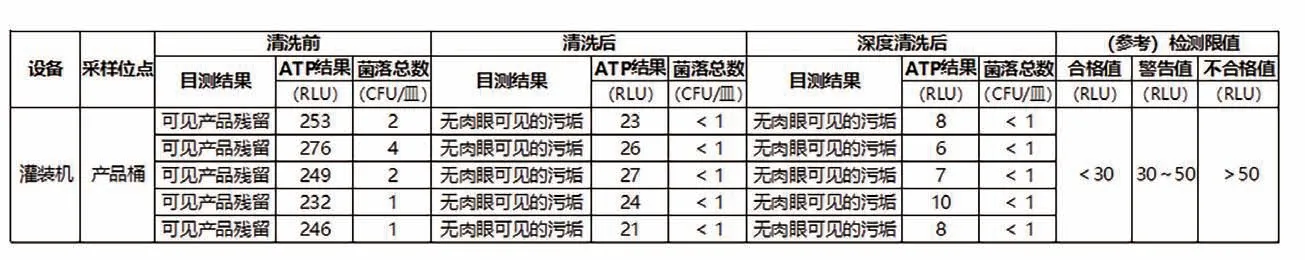
图3 设定检测限值
2.4 制定采样计划,实施监测
乳品企业应根据各检测位点的风险分析结果制定采样监测计划,明确各检测位点的风险等级、采样频率、合格限值等,其中风险越高的检测位点,采样频率越高。
2.5 检出异常,分级管控
在实施清洁验证的过程中,如出现“警告”和“不合格”时,要根据该检测位点风险等级的高低,采取相应的措施:①若出现“警告”,是低风险的检测位点,可进行生产,但同时要查出问题原因,下次清洗后再检测;②若出现“警告”,是高风险的检测位点,则不应生产,须重新清洗,再次检测;③若出现“不合格”,一律不许生产,须重新清洗后检测合格方可生产。
不管是“警告”还是“不合格”,现场管理人员都应予以重视,找出影响设备清洗质量的因素,并将之纠正。
2.6 数据分析,持续改善
乳品企业可根据ATP检测结果结合实际的生产情况调整清洗工艺,如采用一碱一酸、两碱一酸(即前两次采用热碱清洗,第二次采用热酸清洗)、选用复合清洗剂,甚至酶清洗技术[9]等。
此外,现在市面上大部分品牌的ATP检测仪都配套有数据管理系统,乳品企业可以通过连接检测仪和电脑,把检测仪里面的一个个检测数据传输到数据管理系统当中,对所有的数据进行有效管理,将零散的数据整合为集成信息。管理人员通过系统可以查看每个检测位点在一段时间内的检测情况,评估清洗效果的稳定性、一致性和有效性等,分析出现不合格检测结果的原因,精确查明导致污染的问题所在,分析设备、员工和生产过程的变化趋势,预测可能发生的问题,当观察到趋势向着不良结果发展时,应快速识别现有的和可能发生问题的位点,立即采取措施进行改善,优化清洗工艺和资源分配。
3 讨论
3.1 关于ATP检测的温度影响
生物荧光测定本质上是一个酶促反应,温度对检测结果也会产生影响,一般体现在两个方面:一方面是温度可直接影响样品的活性状态,在低温状况下,细菌生物活性降低,体内ATP浓度也明显降低。另一方面荧光素酶活性受温度影响明显,温度越高,酶促反应越快[10]。樊广华[11]等的研究表明,荧光素酶反应的最佳温度是23~25 ℃。然而涂抹棒可低温存放也可室温存放,如果采用低温存放的,测试前应提前取出,待回升至室温再进行检测。如果是采集水样进行ATP检测,应确保水样温度不超过30 ℃。
3.2 关于ATP检测限值的设定
由于表面材质的不同、老化/损蚀程度的差异,甚至不同品牌的ATP检测设备都会造成检测结果的差异。目前,对于检测限值没有统一的判断标准,大部分乳品企业都是根据经验制定本企业的判断标准。
3.3 关于数据的趋势分析
ATP检测不仅仅只是判定清洁情况的合格与否,它更可以通过数据分析预测趋势发展,(图4),虽然所有的检测结果都在合格范围内,但是不难看出其有一个向着不合格发展的趋势,此时就应该调查原因,找出问题,采取纠正措施。

图4 ATP检测数据趋势图
4 总结
ATP生物荧光法的精确测量可以指导及时的清洗评估和长期的管理决策,通过有效地收集检测数据并对数据进行整合及分析,发现隐藏的风险,及时提出应对措施,进行科学决策,为优化清洗工艺、保证清洗效果提供专业依据。乳品企业应根据自身实际情况建立清洁验证方案,在确保感官检查合格的情况下,结合ATP生物荧光法监测清洁效果,同时定期用微生物检测法进行验证。
