雷公藤甲素脂质体粉雾剂的处方工艺筛选与评价*
2022-11-09史亚玲李淼兰谢立颖姚志喻
史亚玲,李淼兰,谢立颖,姚志喻,陈 卉
(桂林医学院药学院,广西 桂林 541199)
肺癌是发病率和死亡率增长最快的恶性肿瘤之一,对人类健康构成严重威胁。根据2018 年WHO统计数据显示,全球新发肺癌病例超过200万人,因肺癌导致的死亡人数超过170万[1-2],给家庭和社会带来巨大挑战。
雷公藤甲素(Triptolide,TP)是从卫矛科植物雷公藤的主要活性成分,具有抗炎、免疫调节和抑制肿瘤等药理作用[3-5]。TP可通过抑制肺癌细胞增殖、诱导肺癌细胞凋亡以及抑制癌细胞转移等发挥治疗肺癌作用[6-7]。虽然TP具有高效治疗肺癌活性,但给药后主要在肝脏代谢,肝毒性明显,化学结构修饰和脂质体等纳米递药系统等方法一定程度上可降低其全身毒性[8],仍需要根据疾病情况开发新型给药方式。
肺部给药是一种非侵入性的局部给药方式,可直接作用于病灶,避免全身给药造成的生物利用度低和毒副作用,可减小给药剂量[9]。而以脂质体为载体的粉雾剂给药后可形成储库,达到长效缓释效果;并具有给药剂量小、肺部靶细胞药物沉积量高等特点,降低毒性的同时提高治疗指数[10]。因此,围绕增效减毒的目的,本实验制备雷公藤甲素脂质体,冻干后得到了雷公藤甲素脂质体粉雾剂,为雷公藤甲素治疗肺癌提供了新策略和实验基础。
1 仪器与材料
1.1 仪 器
LC-20AD高效液相仪,日本岛津;Evolion201紫外可见分光光度计,赛默飞世尔;TGL-16C高速离心机,上海安亭;ME204E电子天平,梅特勒-托利多;S10-3磁力搅拌器,上海司乐;N-1300旋转蒸发仪,日本东京理化;Nano ZS激光粒度仪,英国马尔文;SCIENTZ-IID超声波细胞粉碎机,宁波新芝;ALPHA1-2冻干机,德国Christ;显微镜,日本 OLYMPUS。
1.2 材 料
雷公藤甲素原料药(纯度>95%),桂林三棱生物科技有限公司;蛋黄卵磷脂,北京索莱宝;胆固醇,上海阿拉丁公司;吐温80,北京索莱宝;乙腈(TEDIA,色谱纯);磷酸二氢钾、氢氧化钠、无水乙醇、甲醇等试剂(分析纯),西陇科学。
2 实验与结果
2.1 雷公藤甲素含量测定
2.1.1 色谱条件
色谱柱:Agilent HC-C18(250 mm×4.6 mm, 5 μm);流动相:乙腈:水=35:65(V/V);检测波长:217 nm;流速:1.0 mL/min;温度:30 ℃;进样量20 μL。
对照品溶液精密称取TP对照品11 mg,用无水甲醇溶解,置于10 mL容量瓶中定容,制成1.1 mg·mL-1标准品的储备液。
供试品溶液取雷公藤甲素脂质体溶液,加无水甲醇超声破乳离心,取上清液过0.22 μm的滤膜,取续滤液即得。
空白对照溶液 取空白脂质体溶液,加无水甲醇超声破乳离心,取上清液过0.22 μm的滤膜,取续滤液即得。
2.1.2 专属性
取对照品溶液、供试品溶液及空白脂质体溶液1 mL于液相瓶中,按“2.1.1”项色谱条件进行分析。
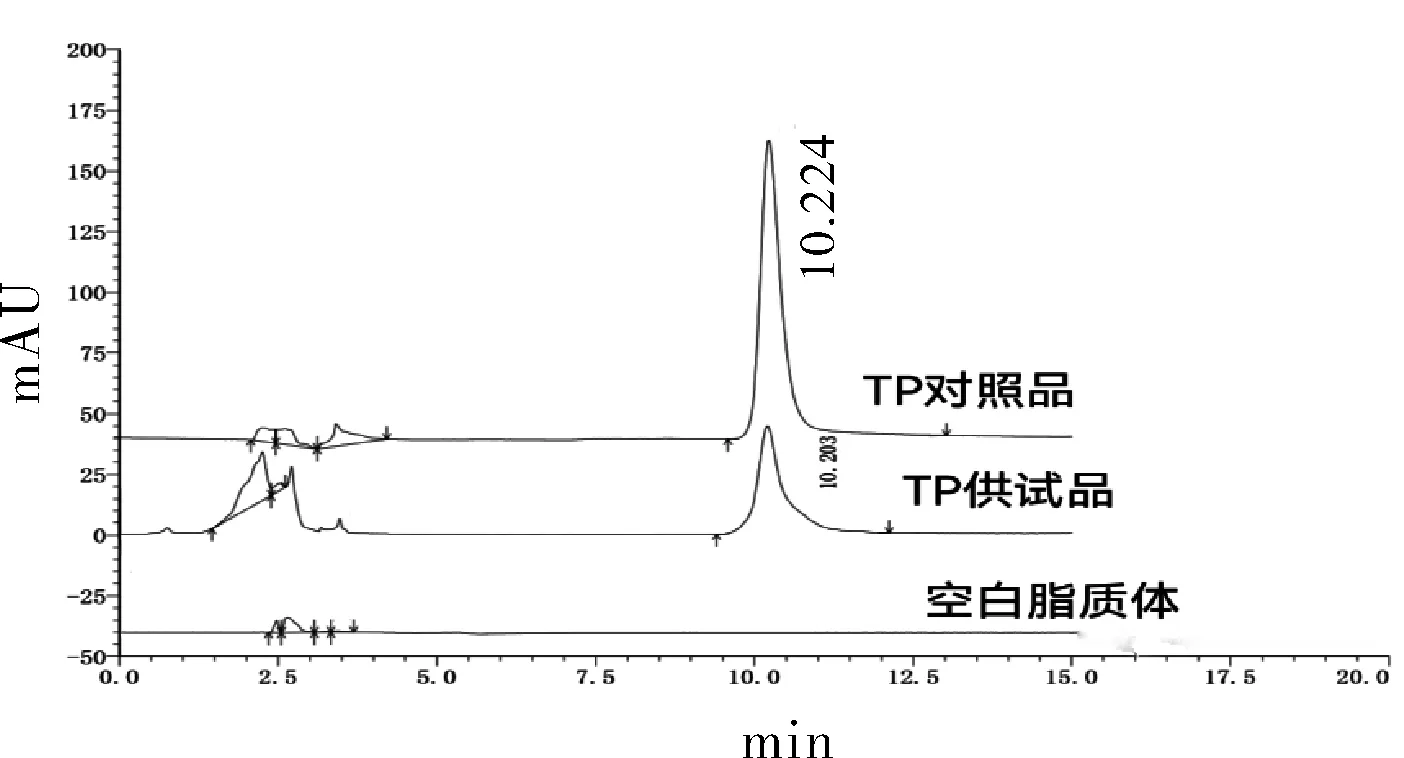
图1 TP对照品、TP供试品、空白脂质体的HPLC图谱Fig.1 HPLC diagram of TP,TP-L,blank liposome
结果显示,使用HPLC检测TP含量,TP峰型较佳,出峰时间在10 min左右,空白脂质体无干扰,表明此方法测定TP含量的专属性良好。
2.1.3 TP标准曲线的绘制
精密吸取TP标准品储备液,配置成浓度为0.0226、0.0679、0.0905、0.1131、0.1357、0.1810、0.2262 mg·mL-1TP标准系列溶液。根据“2.1.1”项色谱条件进行测定,以浓度(C)为横坐标、峰面积(A)为纵坐标绘制标准曲线,并进行线性回归,得到回归方程为A=14927316C+260982(r2=0.999),该结果说明TP溶液其浓度在0.0226~0.2262 mg·mL-1范围内相关性良好。
2.1.4 精密度试验
将浓度为20、40、100 μg·mL-1的TP标准溶液,于“2.1.1”项下的色谱条件重复分析5次进样,测出其峰面积,并计算RSD。其峰面积RSD值分别为1.03%、0.98%、1.06%,均小于2%,表明精密度良好。
2.1.5 加样回收率
往空白脂质体溶液中加入不同体积的雷公藤甲素溶液,用甲醇分别配制成15、50、100 μg·mL-1的不同浓度的样品,依据“2.1.1”项的色谱条件,对所制备的样品进行5次进样,测定峰面积,计算雷公藤甲素浓度和加样回收率。加样回收率结果分别为:99.38%、101.96%、98.73%,RSD <2%,表明该方法测定TP的准确度高。
2.2 乙醇注入法制备TP脂质体
2.2.1 载药及空白脂质体的制备
称取适量卵磷脂、胆固醇、雷公藤甲素于烧杯中,加入2 mL无水乙醇搅拌使完全溶解;将此溶液缓慢滴入10 mL纯水中,在磁力搅拌器上以300 rpm搅拌0.5 h,用超声波细胞破碎仪处理10 min,旋蒸回收乙醇溶剂,透析后得到雷公藤甲素脂质体混悬液(TP-L),于4 ℃条件下保存。采用相同方法制备其空白脂质体。
往上述脂质体样品中加入冻干保护剂,溶解摇匀后置西林瓶中,冻干12 h,过180目筛即可得到TP-LD,置干燥器内保存备用。
2.2.2 处方工艺
单因素考察:以包封率及载药量为指标对Tween-80用量、药脂比、反应温度、反应时间4个因素进行考察。
冻干保护剂:根据冻干粉外观、粒径和流动性等指标,筛选不同种类及合适比例的冻干保护剂。
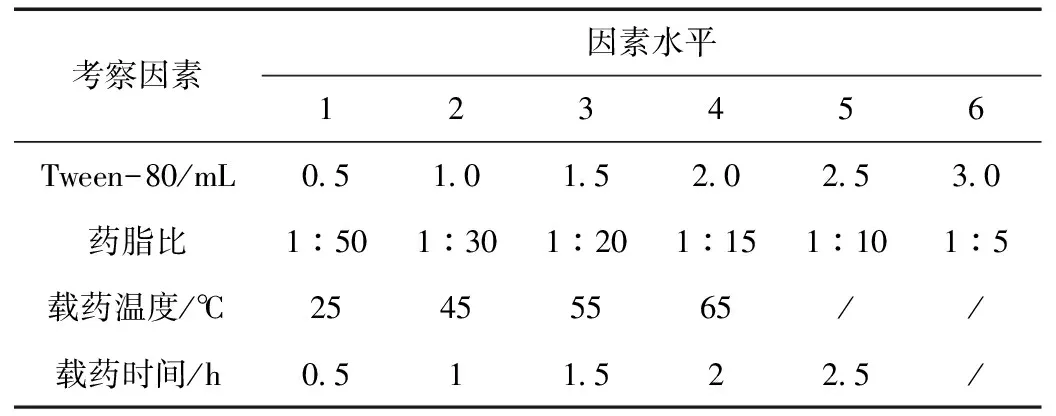
表1 单因素设计水平表Table 1 Single factor design level table

表2 冻干保护剂种类筛选Table 2 Screening of freeze-drying protective agents
通过对雷公藤甲素脂质体的处方和工艺进行单因素筛选,可以得出用乙醇注入法制备雷公藤甲素脂质体的较优处方为蛋黄卵磷脂16 mg、胆固醇4 mg、雷公藤甲素原料药2 mg。雷公藤甲素属于脂溶性药物,主要是嵌入在脂质层中,药物量过多会影响脂质层的分子结构,从而包封率降低,保持磷脂比例不变,增加原料药的投入量,可以发现当投入药量增加到2 mg时,脂质体的包封率和载药量都有明显的提高。适量的0.5%Tween-80-乙醇溶液可以促进雷公藤甲素的溶解,减少因雷公藤甲素不完全溶解造成包封率低的误差,并起到润滑和乳化的作用。乙醇注入法制备雷公藤甲素脂质体,载药温度和载药时间对包封率的影响也较大。经过考察,发现随着载药温度的升高,雷公藤甲素脂质体的包封率也有明显增高的趋势,而载药时间则对雷公藤甲素脂质体的包封率影响不大,考虑到耗时耗材问题,最终选择载药温度55 ℃、载药时间0.5 h来制备雷公藤甲素脂质体。
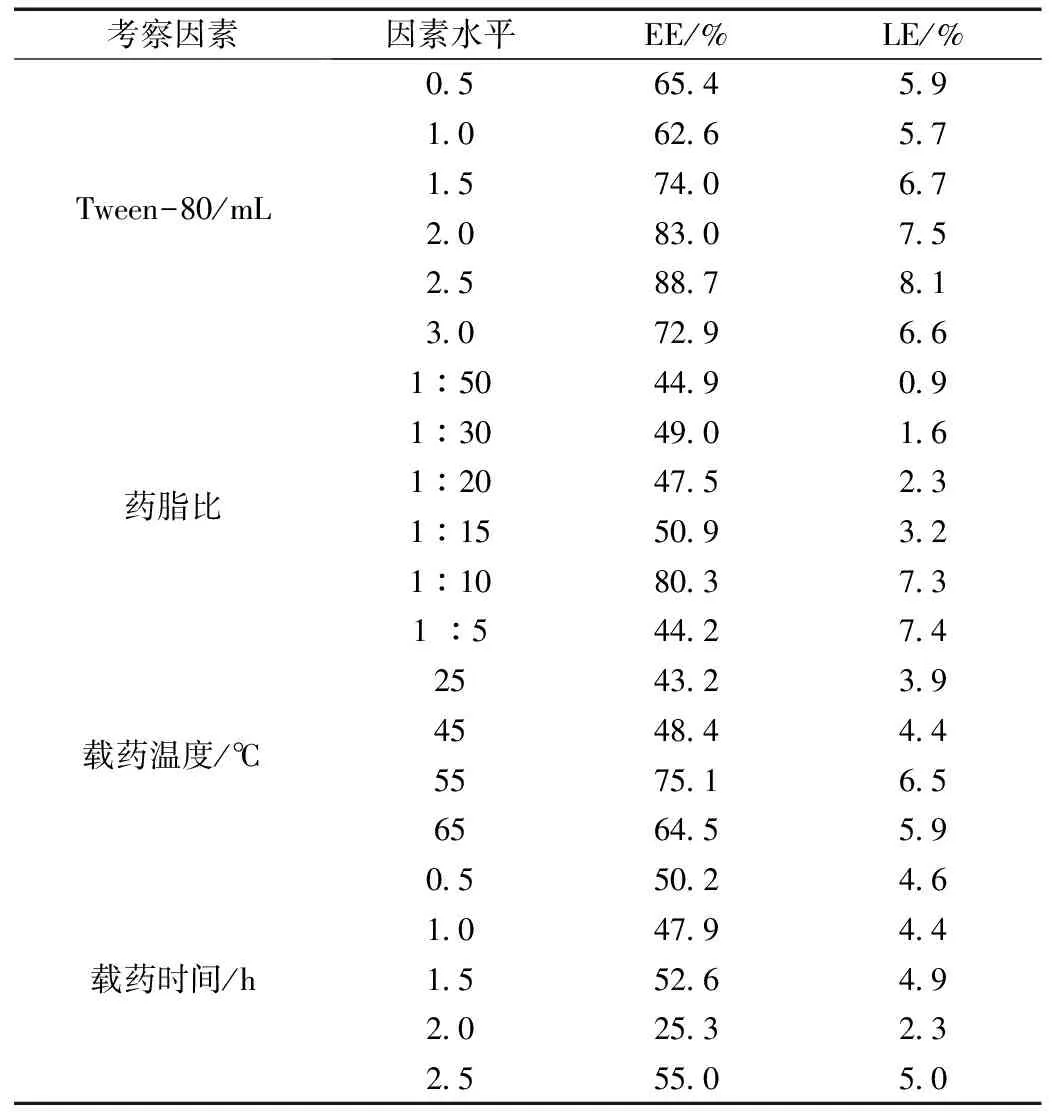
表3 单因素考察结果Table 3 Results of single factors
2.2.3 工艺验证
根据上述单因素实验中得出制备TP-L的条件,即Tween-80 2.5 mL、药脂比为1:10、载药温度55 ℃、载药时间0.5 h,按此法制备3批较优的TP-L样品,按“2.2”项下方法测定TP-L包封率及RSD。

表4 验证试验结果Table 4 Verification of test results
2.3 制剂学评价
2.3.1 外观形态

图2 加入不同冻干保护剂的粉雾剂外观Fig.2 Appearance of powder mist with different types of lyophilized protectants
加入不同的冻干保护剂,观察样品的外观、复溶速度。从图2可以看出,加入甘露醇冻干保护剂的TP脂质体冻干粉呈白色,且饱满,加入蔗糖的TP脂质体冻干粉呈白色,贴壁,萎缩。不同冻干保护剂对粉雾剂外观、复溶速度有影响,从表5结果可知,甘露醇对脂质体粉雾剂保护效果较好,样品复溶速度较快。
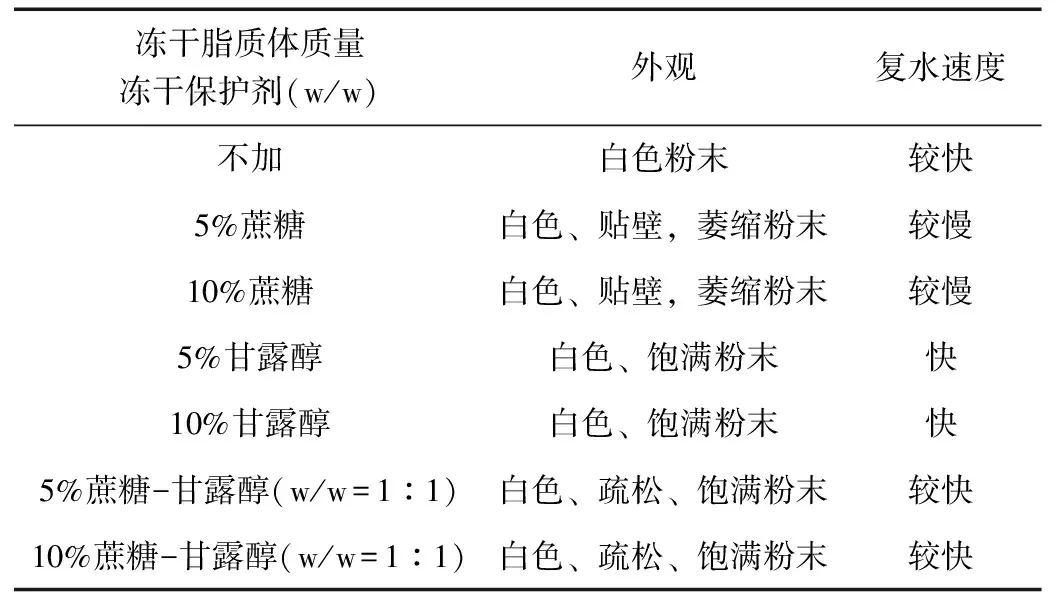
表5 不同冻干保护剂对脂质体冻干粉的影响Table 5 Effects of different lyophilized protectants on lipid body freeze-drying powder
2.3.2 流动性、松密度
将TP-LD通过下孔径为5 mm的玻璃漏斗,并从10 cm的高度缓慢、均匀地落入平板上,形成圆锥体。测量圆锥体的高度(h)和基底的半径(r),按公式计算休止角(θ,tanθ=h/r)。粉末休止角为38.7°,说明粉末流动性较好。取量筒,以自由落体方式装入脂质体冻干粉,记录质量与体积,计算得松密度约0.24 g/mL。
2.3.3 包封率和载药量的测定
取适量TP-L溶液和TP-LD复溶后样品,加甲醇破乳、离心取上清液过0.22 μm滤膜,续滤液按“2.1.1” 项下色谱条件进样测定。计算总药量(W总)、包封率(EE)和载药率(LE),计算公式如下。
(1)
(2)
2.3.4 粒径及Zeta电位
取适量TP-L和复溶后的TP-LD 样品溶液,用超纯水稀释10倍,利用马尔文激光粒度分析仪测定其粒径大小及Zeta电位值。取适量TP-LD样品,加液体石蜡充分搅拌分散后,于正置显微镜下观察并测定粉雾剂粒径大小,平均粒径为(1.17±0.047) μm,显微镜下粉雾剂形状见图3(C)。复溶前后包封率、粒径及Zeta电位变化结果见表6。
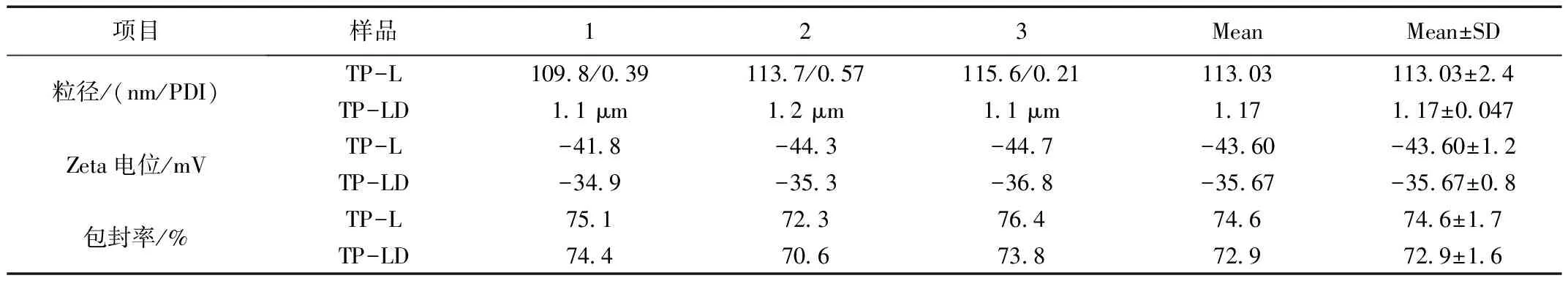
表6 LTP及LTPD复溶后包封率、粒径、电位结果Table 6 Results of entrapment efficiency, particle size and potential of LTP and LTPD after redissolution
按照筛选的方法制备的脂质体包封率约74.6%,冻干后的包封率约为72.9%,冻干前后包封率数据差别不大。于马尔文粒径仪下检测,结果显示冻干前的溶液粒径约为113 nm,电位约为-43 mV,冻干后的电位约为-35 mV。 取TP脂质体冻干粉复溶液适量,用纯化水再次稀释到约100倍,在电镜下测得冻干后的粒径为1.17 μm左右。

图3 TP-L 粒径图(A),TP-L Zeta电位图(B),TP-LD粒径图 (C,100×R=1.1 μm),复溶后的TP-LD Zeta电位图(D)Fig.3 TP-L particle size distribution (A),TP-L zeta potential(B),TP-LD particle size distribution (C,100×r=1.1 μm),TP-LD zeta potential(D)
2.3.5 肺部沉积率的测定
分别称取30 mg雷公藤甲素脂质粉雾剂装入3号羟丙甲纤维素胶囊中, 然后取上述胶囊10粒, 逐粒置于药粉吸入器内, 连续吸入10粒, 每次10 s, 停泵后打开测定仪, 用10 mL无水乙醇清洗每个接收盘 (装置、喉部、1~8级共10个接收盘), 连续2次, 合并后转入50 mL量瓶, 将量瓶中的液体用无水乙醇定容,参考“2.1.1”项色谱方法测定每个接收盘中雷公藤甲素的含量, 按公式计算药物肺部沉积率 (FPF),测得FPF为20.57%。
(3)
2.3.6 体外释放度评价[11]
对于多数固体剂型来说,药物的溶出速度直接影响药物的吸收速度。采用动态透析法进行原料药TP与TP-LD体外释药评价。
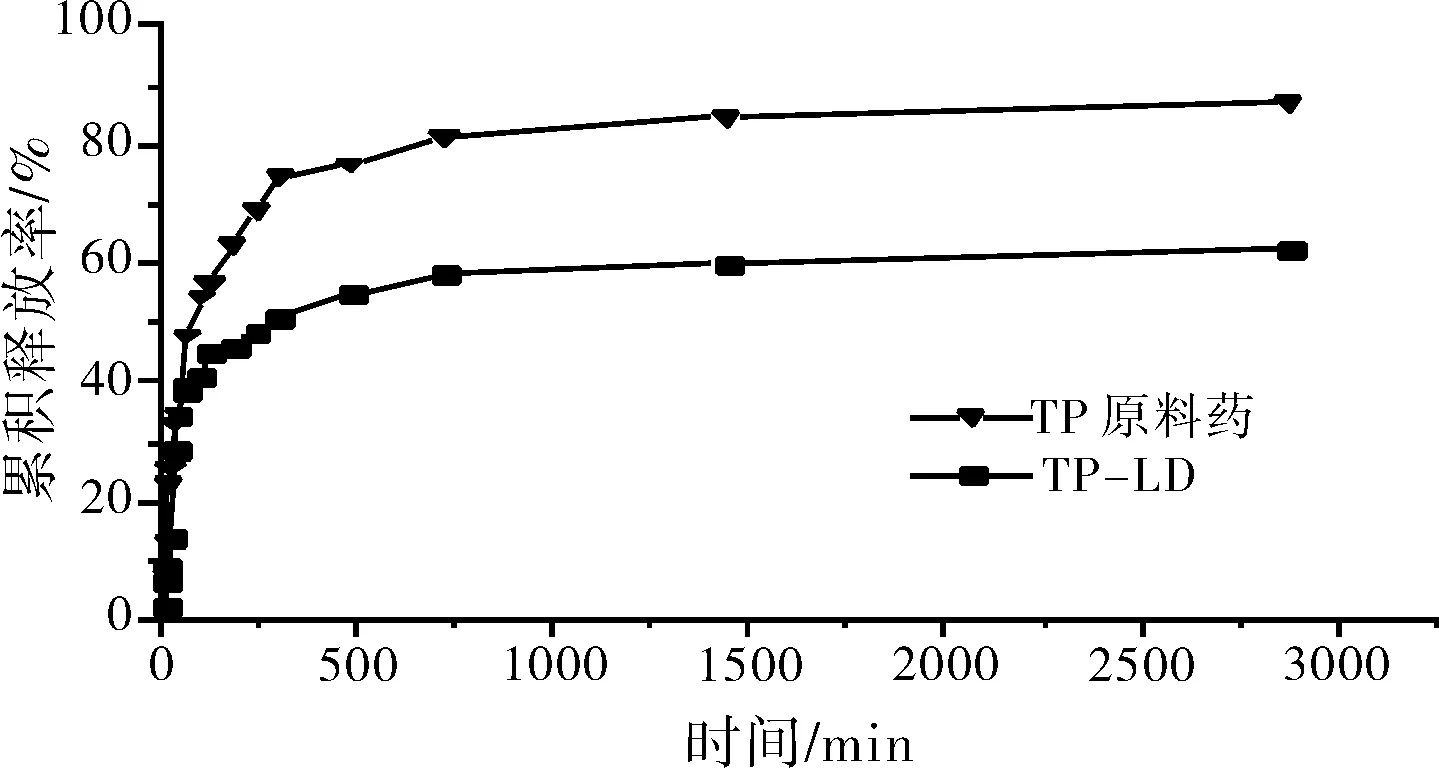
图4 TP-LD和TP原料药的体外释放图Fig.4 In vitro release diagram of TP-LD and TP
分别取TP原料药和LTPD适量,用3 mL人工肺液完全分散后置于透析袋(截留相对分子质量8000~14000),以50 mL含0.2%Tween-80的人工肺液为释放介质,控制温度为37±0.5 ℃,转速100 r·min-1,分别于5、10、15、30、40、60、90、120、180、240、300、480、720、1440、2160、2880 min取样1 mL,同时补充同温等量释放介质。采用“2.1.1”项所建立的HPLC法测定TP含量并计算制剂的溶出度。以时间为横坐标,以药物累积释放百分率为纵坐标绘制体外释放曲线。
由以上结果表明,雷公藤甲素脂质体粉雾剂和雷公藤甲素原料药在24 h后,体外释放曲线趋于平缓。雷公藤甲素脂质体粉雾剂在人工肺液里释放24 h后,累计释放量达到约62.5%,而雷公藤甲素在24 h后,累计释放量达到约87.1%。由此可见在人工肺液中,雷公藤甲素脂质体粉雾剂同原料药相比,具有明显的缓释效果。
3 结 论
雷公藤甲素具有抗炎和抗肿瘤等药理活性,但常规制剂的全身毒副作用较大。吸入粉雾剂与其他肺吸入剂型如气雾剂、雾化吸入溶液相比,具有携带方便、稳定性更好以及靶向递送病灶等优势,适合肺癌治疗。根据文献以及预实验结果,本实验采用乙醇注入法和冷冻干燥法制备的雷公藤甲素脂质体粉雾剂,冻干前和复溶后粒径、Zeta电位及雷公藤甲素包封率变化不大,处方工艺简单可行,稳定性和粉体学参数良好。接下来,本项目将进一步评价粉雾剂的空气动力学参数特征,并进行体内外抗肺癌疗效评价,为雷公藤甲素脂质体粉雾剂的开发提供更充足的实验数据。
