生半夏秫米汤与法半夏秫米汤的急性毒性研究*
2022-11-09尚春光张亚楠刘西建
张 艳,尚春光,张亚楠,刘西建
(山东中医药大学中医学院,山东 济南 250355)
“失眠第一方”半夏秫米汤由半夏。秫米组成。半夏辛温,燥湿化痰安神,是临床治疗失眠常用药[1]。秫米,张锡纯云“秫米即芦稷之米(俗名高粱)”,临床亦有不少医家认为是高粱[2]。《中华本草》曰:“高粱,甘涩温,健脾止泻,化痰安神。”原方中二药用量比例为1∶2,现代临床常用此方加味治疗各型失眠,效果良好。前期实验研究[3]证实了该方的镇静、催眠作用。原方所用半夏实为生半夏[4],临床不少医家认为不会引起不良反应[5],但碍于生半夏之毒,临床亦有许多医家改用法半夏[6-7]。鉴于半夏不同炮制品的半夏秫米汤毒性研究尚未见报道,本研究就生半夏与法半夏组成的半夏秫米汤的急性毒性进行探讨,以期为临床应用和实验研究提供参考依据。
1 材料与方法
1.1 实验动物 2个月龄SPF级健康昆明小鼠120只,体质量(20±2)g,雌雄各半,购于济南市朋悦实验动物繁育有限公司,实验动物质量合格证编号:N0.37009200014164。实验动物使用许可证号:SYXK(鲁)2017-0022,动物饲养于SPF级动物房,温度为20~25 ℃,相对湿度40%~60%,12 h明暗周期,自由摄食、饮水。本研究方案符合国家实验动物伦理的相关指导原则[8],通过山东中医药大学实验动物伦理委员会批准,批准号:SDUTCM20201216001。
1.2 药物与试剂 生半夏、法半夏饮片均购自郑州瑞龙制药股份有限公司,高粱购自山东鹤来香食品有限公司,经山东中医药大学中药鉴定室的刘红燕教授鉴定,生半夏、法半夏均为天南星科植物半夏Pinellia ternata(Thunb.)Breit.干燥的块茎,高粱乃禾本科植物高粱Sorghum vulgare Pers种仁。
丙氨酸转氨酶(alanine transaminase,ALT)试剂盒(批号:200706KE4)、天冬氨酸转氨酶(aspartate aminotransferase,AST)试剂盒(批号:200706KE3)、肌酐(creatinine,CrE)试剂盒(批号:200706KE6)、尿素氮(blood urea nitrogen,BUN)试剂盒(批号:200706KE5)均购自江苏晶美生物科技有限公司;石蜡(批号:YA0013)、伊红(批号:E8090)、苏木素(批号:G1140)均购自solarbio公司;无水乙醇(批号:10009218)、碳酸锂(批号:20022818)、冰醋酸(批号:10000218)均购自国药集团化学试剂有限公司。
1.3 主要仪器 WT11001R型电子天平(江苏省常州市万得天平仪器厂);GNP-908型隔水式恒温培养箱(上海精宏实验设备有限公司);352型酶标分析仪(芬兰Labsystems Multiskan MS);BC-2800vet型全自动血液细胞分析仪(深圳迈瑞生物医疗电子股份有限公司);TKD-TSF型自动组织脱水机、TKD-TK型摊片烤片机(湖北康强医疗器械有限公司);TB-718L型生物组织包埋机(泰维科技实业股份有限公司);RM2235型石蜡切片机、DM1000型白光显微镜(徕卡显微系统有限公司)。
1.4 半夏秫米汤的制备 生半夏秫米汤与法半夏秫米汤方中的半夏与高粱用量均按1∶2称取,加8倍体积冷水浸泡1 h,加热煮沸后煎煮1 h,减压低温50 ℃浓缩,浓缩至生药浓度为3 g/mL水煎液,置于4 ℃冰箱避光保存备用。
1.5 动物分组 将120只小鼠按随机数字表法分为生半夏秫米汤组、法半夏秫米汤组、空白组,每组40只,均雌雄各半。
1.6 实验给药 根据《中药、天然药物急性毒性研究技术指导原则》(编号:[Z]GPT2-1),采用最大给药量试验,24 h内3次灌胃给药。给药前12 h及给药期间禁食不禁水,以药物最大生药浓度3 g/mL水煎液,小鼠最大给药体积为0.4 mL/10 g灌胃给药,24 h内给药3次,每次间隔3 h。空白组小鼠灌胃给予等量生理盐水。
1.7 观察指标
1.7.1 一般情况 第1天密切观察小鼠每次给药后1 h情况,观察动物皮毛、饮食、进水、运动、眼睑指征、呼吸、分泌物和排泄物等,之后每天观察1次,连续14 d。记录动物出现中毒反应的开始时间、中毒症状、严重程度及持续时间等。
1.7.2 体质量 每组小鼠给药前称体质量,给药后第14天对剩余20只小鼠称体质量。
1.7.3 死亡情况 观察并记录各组小鼠死亡情况,记录死亡时间、濒死前反应。对出现濒死及死亡的小鼠,立即进行大体解剖,肉眼观察脑、肺脏、心脏、胃、肝脏、脾脏、肾脏等主要脏器的体积、颜色、质地的变化。
1.7.4 ELISA法检测血清ALT、AST、CrE、BUN含量 实验第2天,各组随机抽取20只小鼠(雌雄各半),摘眼球取血,ELISA法检测血清ALT、AST、CrE、BUN含量。第14天,将剩余的各组全部小鼠按上述方法检测。
1.7.5 全自动血液细胞分析仪检测血常规 按照“1.7.4”方法取血后,分别于实验第2天、第14天检测血浆中白细胞计数(WBC)、淋巴细胞计数(Lymph)、淋巴细胞百分比(Lymph%)、单核细胞计数(Mon)、单核细胞百分比(Mon%)、中性粒细胞计数(Neu)、中性粒细胞百分比(Neu%)、血红蛋白含量(HGB)、红细胞平均血红蛋白浓度(MCHC)、红细胞计数(RBC)、平均红细胞体积(MCV)、红细胞压积(HCT)、平均红细胞血红蛋白量(MCH)、红细胞分布宽度(RDW)、血小板计数(PLT)、血小板分布宽度(PDW)、血小板压积(PCT)、平均血小板体积(MPV),共计18个项目。
1.7.6 脏器观察及组织病理学检测 实验第2天,将取血后的小鼠脱颈椎处死,先进行大体解剖,肉眼观察胸腔、腹腔是否存在积液、是否光滑;观察主要脏器及腺体体积、色泽、质地的变化;然后取出脑、肺脏、心脏、胸腺、脾脏、肝脏、肾脏、胃,用4%多聚甲醛固定、冲洗后,进行脱水石蜡包埋,切片、展片、烤片、HE染色;显微镜下观察上述器官组织实质细胞有无变性、坏死,间质有无水肿、充血、炎症细胞浸润,有无纤维组织增生等。14 d观察期结束后,将每组剩余小鼠按照上述同样方法进行观察与检测。
1.8 统计学方法 采用SPSS 26.0软件进行统计分析,计量资料以“均数±标准差”表示,多组间的比较采用单因素方差分析,组间两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结果
2.1 一般观察 给药后1 h及给药后14 d期间,空白组、生半夏秫米汤组、法半夏秫米汤组小鼠的精神状态、行为、皮毛、眼睑指征、呼吸、分泌物、排泄物等均未发现异常变化。
2.2 死亡情况 实验期间无小鼠死亡。
2.3 各组小鼠体质量比较 给药前,空白组、生半夏秫米汤组、法半夏秫米汤组小鼠体质量比较,差异无统计学意义(P>0.05);实验第14天,3组小鼠体质量均较给药前有所增长,但3组小鼠间体质量比较,差异无统计学意义(P>0.05)。(见图1)

图1 各组小鼠体质量比较()
2.4 各组小鼠血清ALT、AST、CrE、BUN含量比较 实验第2天,与空白组比较,生半夏秫米汤组、法半夏秫米汤组小鼠血清ALT、AST、CrE、BUN含量均明显升高(P<0.01);与生半夏秫米汤组比较,法半夏秫米汤组小鼠血清AST含量明显升高(P<0.01),ALT含量明显降低(P<0.01);法半夏秫米汤组小鼠血清CrE、BUN含量与生半夏秫米汤组比较,差异均无统计学意义(P>0.05)。(见图2)
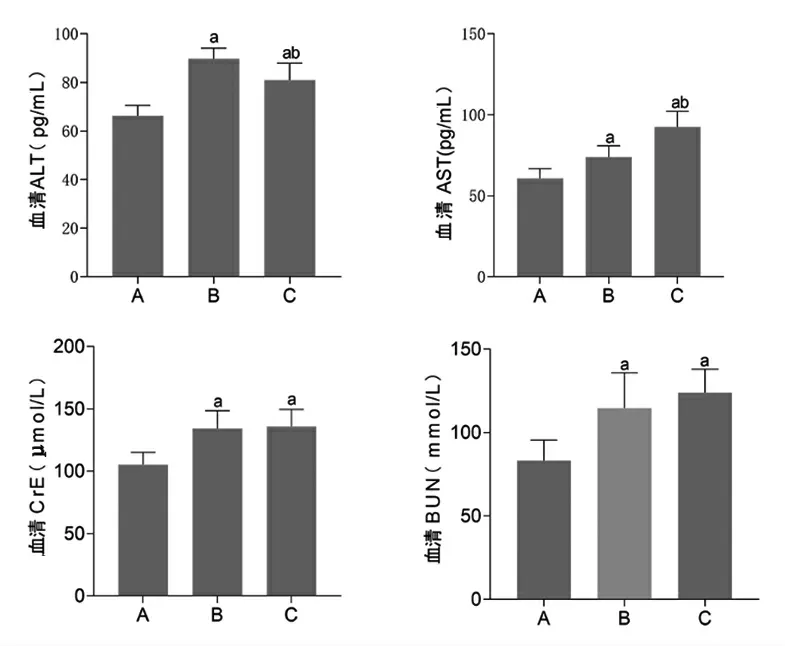
图2 实验第2 天各组小鼠血清ALT、AST、CrE、BUN 含量比较(,n=20)
实验第14天,与空白组比较,生半夏秫米汤组、法半夏秫米汤组小鼠血清ALT、AST、CrE、BUN含量均明显升高(P<0.01或P<0.05);与生半夏秫米汤组比较,法半夏秫米汤组小鼠血清ALT、AST、CrE、BUN含量均明显升高(P<0.01)。(见图3)
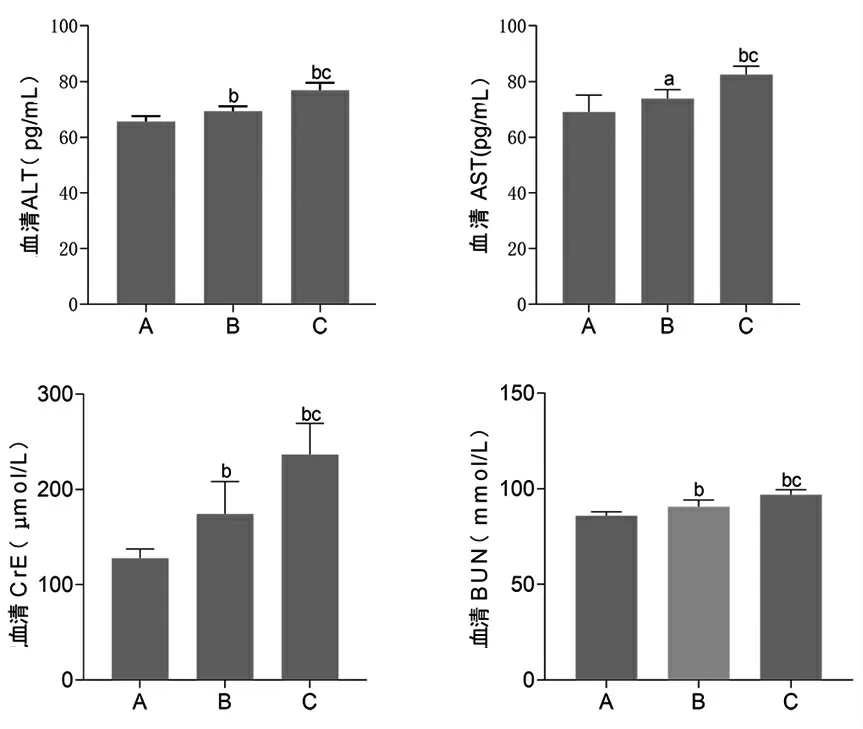
图3 实验第14 天各组小鼠血清ALT、AST、CrE、BUN 含量比较(,n=20)
2.5 各组小鼠血常规比较 实验第2天,与空白组比较,生半夏秫米汤组小鼠HCT明显升高(P<0.05),3组小鼠间其余17项指标比较,差异均无统计学意义(P>0.05)。(见图4)

图4 实验第2 天各组小鼠血常规比较(,n=20)
实验第14天,与空白组比较,法半夏秫米汤组小鼠RDW明显升高(P<0.05),3组小鼠间其余17项指标比较,差异均无统计学意义(P>0.05)。(见图5)
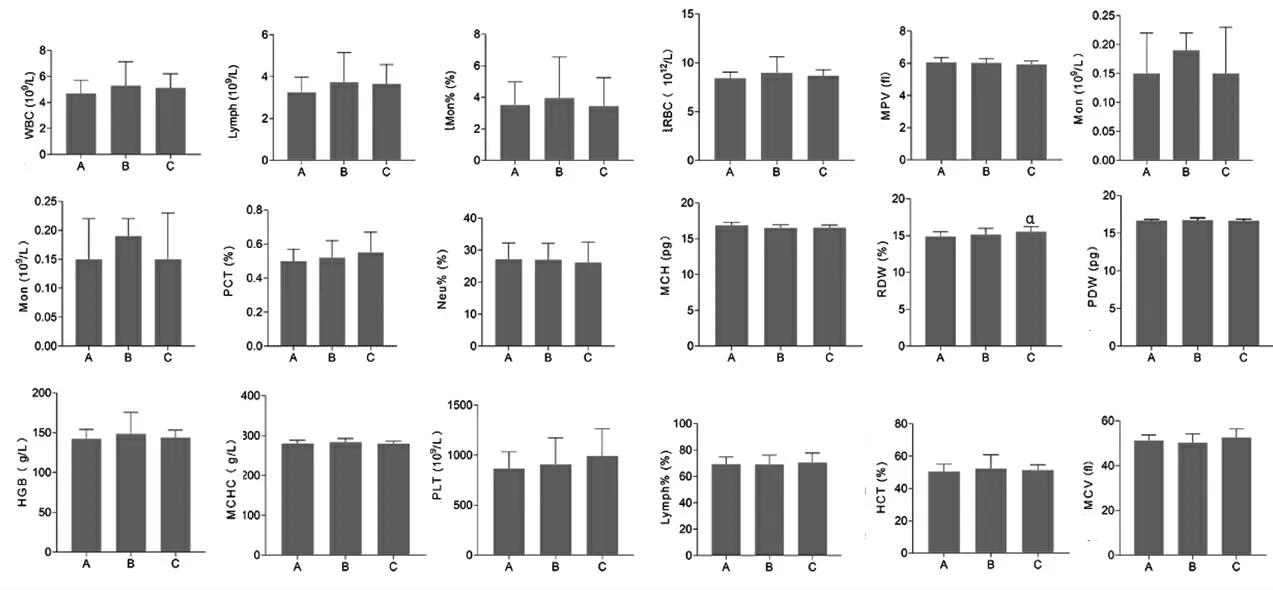
图5 实验第14 天各组小鼠血常规比较(,n=20)
2.6 脏器观察及组织病理学检查 实验第2天及第14天各组小鼠胸腔、腹腔浆膜光滑、无积液,各重要脏器体积、色泽、质地均未见异常。
病理组织学检查发现,各组小鼠胸腺均未见异常变化,皮质、髓质的比例正常,皮质区可见淋巴细胞均匀分布,髓质区未见异常变化;脾脏的组织结构正常,被膜无增厚而完整,脾窦未见扩张,脾小体未见异常改变,红白髓比例正常;心脏组织结构未见异常变化,可见排列整齐的心肌纤维,卵圆形核居中,间质内血管未见扩张或狭窄的异常变化,未见炎症细胞浸润;肺脏组织结构未见与药物有关的异常变化,各级支气管结构无异常,肺泡腔未见扩张或缩小的异常改变,未见炎症细胞浸润,间质血管未见扩张或狭窄;脑组织学检查无异常,未见异常形态的神经细胞,未见到小胶质细胞的增生及血管扩张,间质均匀;胃组织检查未见异常变化,胃黏膜无明显变化,胃黏膜腺管排列整齐,呈单柱状,壁细胞、主细胞界限清楚,固有层内胃腺体排列紧密整齐,未见炎症细胞,黏膜下层无水肿。
实验第2天,生半夏秫米汤组与法半夏秫米汤组小鼠均可见汇管区周围的肝细胞细胞核圆而居中,无明显肿胀;中央静脉周围肝细胞体积增大,染色变浅,疏松肿胀,肝细胞索排列紊乱;法半夏秫米汤组小鼠除上述变化外,还可见点状坏死灶。实验第14天,生半夏秫米汤组与法半夏秫米汤组小鼠均可见肝小叶结构不清,肝血窦扩张充血,大部分肝细胞疏松肿胀,呈现明显的细胞水肿;生半夏秫米汤组小鼠部分肝细胞核溶解消失,出现点状坏死灶,可见体积较大、染色深、双核、再生的肝细胞;法半夏秫米汤组小鼠则多数肝细胞核溶解消失。(见图6)

图6 实验第2 天及第14 天的肝脏病理学变化图(HE,×100)
实验第2天,生半夏秫米汤组小鼠可见肾小球毛细血管扩张充血明显,肾小管上皮细胞肿胀、部分出现细胞溶解;法半夏秫米汤组小鼠可见肾小管变形,局部高度扩张,肾小管上皮细胞体积增大,染色变浅,出现明显的细胞水肿,部分肾小管上皮细胞核溶解消失,可见蛋白管型,肾小球毛细血管扩张充血,部分肾小球萎缩。实验第14天,生半夏秫米汤组小鼠可见肾小管上皮细胞水肿,细胞胞质疏松,部分细胞核溶解,细胞脱落,同时管腔变窄消失,管形不规则;肾小管管腔内可见蛋白管型;肾小球毛细血管扩张充血明显,出现肾小球集中现象。法半夏秫米汤组小鼠肾小管上皮细胞也呈现水肿、坏死,部分细胞胞质出现疏松溶解而脱落,管腔狭窄甚至消失,仅保留肾小管轮廓,管形不规则。肾小管管腔内可见细胞或者蛋白管型。肾小球毛细血管扩张充血明显,出现肾小球集中现象。(见图7)

图7 实验第2 天及第14 天的肾脏病理学变化图(HE,×100)
3 讨论
半夏秫米汤始载于《黄帝内经》。《灵枢·邪客》云:“目不瞑者,饮以半夏汤一剂,覆杯则卧。”明·张景岳谓:“治久病不寐者神效。”本研究通过研究不同半夏炮制品(生半夏、法半夏)组成的半夏秫米汤的急性毒性,以期为今后的实验研究及临床应用提供实验基础。
肝、肾是药物代谢和排泄的器官,同时也是药物安全性评价的重要器官。世界卫生组织统计证实,药源性肝损伤引起的死亡率居全世界疾病死亡率的第五位,而中药则是导致肝损害的主要药物之一,位居第三[9]。因此肝损害是中药安全性研究的重点之一。而血清ALT和AST是肝损伤程度的重要评价指标[10]。肝细胞膜受损后,细胞内的ALT、AST进入血液,则会引起血液中ALT、AST的升高[11]。本研究中生半夏秫米汤呈现一定程度肝损害,实验第2天生半夏秫米汤组小鼠血清ALT、AST升高,肝组织病理显示肝细胞受损,与张丽美等[12]的报道相似。实验第14天,ALT值虽仍处于高水平状态,但比第2天含量有所降低,表明肝功能有一定程度恢复,同时肝组织病理学检查也发现了再生的肝细胞。由于本研究周期较短,未能观察到肝功能是否完全恢复,今后可适当延长实验周期进行相关观察。法半夏为生半夏用生石灰和甘草炮制后制得,本为减毒,但目前法半夏毒性成分存在去除不彻底和炮制过度的现象,直接影响了法半夏用药安全[13],这与本研究认为法半夏秫米汤有肝损害较一致。本研究还认为法半夏秫米汤的损害程度重于生半夏秫米汤,表现为法半夏秫米汤组实验第2、14天两次AST值、实验第14天ALT值明显高于生半夏秫米汤组;虽然实验第2天法半夏秫米汤组ALT水平低于生半夏秫米汤组,但肝组织病理形态学却显示点状坏死灶,而这在生半夏秫米汤组却未见到,而且实验第14天的病理表现也重于生半夏秫米汤组。因此,本研究认为两种半夏秫米汤均通过损害肝细胞导致ALT、AST升高,以法半夏秫米汤损害较重。
肾脏对于体内电解质的稳态和细胞外环境的调节有重要作用。肾近端小管上皮细胞富含各种转运蛋白、受体,可活化外源性化合物的代谢酶,是外源性毒物诱发肾损伤的重要靶点[14]。BUN和CrE分别是体内蛋白质和肌肉代谢的主要产物,主要通过肾脏排泄。血清BUN、CrE含量高低是肾实质受损的重要标志,能够反映肾小球滤过功能,是肾脏生理功能的重要反映指标,在评价肾功能方面具有重要意义[15-16]。当肾功能下降时,肾小球滤过率降低,排泄减少,血清BUN及CrE含量则会明显升高。本研究显示生半夏秫米汤及法半夏秫米汤均有肾损害。实验第2、14天,两组小鼠血清BUN、CrE升高,与严晓莺等[12]报道生半夏造成肾损害相符。但本研究结果显示法半夏秫米汤造成的肾损害较重,实验第14天法半夏秫米汤组小鼠血清BUN、CrE明显高于生半夏秫米汤组;病理学显示法半夏秫米汤组的肾小球、肾小管损害程度较重。这表明两种半夏秫米汤均通过损害肾小球及肾小管,引起排泄功能下降,从而导致BUN和CrE升高。
王潮奎等[17]研究表明加热虽能一定程度降低半夏刺激性,但毒性成分草酸钙针晶、生物碱即使100 ℃加热3 h,也不能被破坏[18]。本研究中生半夏秫米汤与法半夏秫米汤水煎液之所以表现出一定肝肾毒性,除了半夏加热后毒性并未完全消除,主要原因还是在于半夏剂量超大,与靳晓琪[19]提出的大剂量半夏会出现肝损害一致,而半夏正常或低剂量没有明显肝肾毒性。如岳苹等[20]证实小剂量生半夏水煎液2.275 g/kg(相当于成人15 g/d)灌胃小鼠给药,1次/d,连续14 d,无毒性反应。严晓莺等[21]研究也表明小剂量(1 g/kg)生半夏水煎液灌胃小鼠后,病理学检查肾脏无明显变化。而本研究中半夏秫米汤的小鼠每日最大给药剂量为360 g/kg,其中生半夏每日给药剂量为120 g/kg,根据人鼠剂量换算,约相当于70 kg体质量成人933.1 g/d的剂量,是《中华人民共和国药典》规定成人最大用量(9 g/d)的103.7倍,远远超过临床实际用量,因而呈现肝肾毒性。但是,本研究认为生半夏秫米汤和法半夏秫米汤毒性较小,较为安全,表现为各组小鼠在给药后无死亡现象,肉眼未见小鼠主要器官异常改变,小鼠体质量均较给药前增加,且与空白组比较,差异无统计学意义(P>0.05)。病理学检查显示,脾、心、脑及胸腺无异常变化;肺、胃未见药物相关异常变化。虽然实验第2天的血常规中生半夏秫米汤组小鼠HCT升高,实验第14天法半夏秫米汤组小鼠RDW升高,但是无其他相关指标变化,因而可能与用药无关。
本研究认为生半夏秫米汤和法半夏秫米汤大剂量用药能够损害肝细胞、肾小球、肾小管从而引起肝肾功能下降,具有一定肝肾毒性,以法半夏秫米汤造成的损害较重,但毒性较低。生半夏秫米汤造成的肝损害是否能够恢复,尚需进行相关研究。为降低毒性,保证安全,临床使用上述两方时,不宜使用超大剂量,并需开展临床实际用量的毒性研究;另外,还需规范半夏炮制品的加工制作以提高炮制品质量;或去除有毒成分,运用现代技术提取无毒的安全有效成分制成现代制剂使用。但鉴于目前对半夏毒性物质基础、安全的用量界限并不明确[9],因此,函需就半夏及其炮制品开展深入系统的相关研究。
