美国移植和细胞治疗学会系列指南3:造血干细胞移植后巨细胞病毒感染和巨细胞病毒病的防治策略
2022-11-07王春娟,孙毅
巨细胞病毒(cytomegalovirus,CMV)感染可能是潜伏的,也可以是活动性的。在造血干细胞 移 植(hematopoietic cell transplantation,HCT)相关的免疫抑制背景下,潜伏的CMV 可能会再激活,导致活动性感染,并可迅速进展为危及生命的CMV 病,其特征表现为CMV 复制导致的器官特异性组织损伤。本指南以常见问答(frequently asked questions,FAQ)的形式,聚焦于CMV 临床感染的防治,包括针对CMV DNA 血症的预防和抢先治疗(preemptive therapy,PET)。指南的最后章节则总结了尚未解决的问题和未来的发展方向。本指南根据循证医学级别对专家推荐意见进行了分类推荐,推荐强度(A~E)和证据质量分级(Ⅰ~Ⅲ级)见表1。

表1 推荐强度和证据质量分级
1 FAQ
FAQ 1 :什么是CMV 活动性感染,如何评估CMV活动性感染?
移植受者CMV 感染和CMV 病的定义已经在相关文章发表。简而言之,和所有疱疹病毒一样,CMV 感染可能是活动的或潜伏的。对于HCT 受者,术语“CMV 感染”通常被用于描述活动性感染(病毒复制),确定方法可以通过聚合酶链反应(PCR)检测到CMV 核酸(DNA 或RNA)阳性、检测CMVpp65 抗原阳性或培养阳性。通常术语“CMV病毒血症(CMV viremia)”也用来描述CMV 活动性感染,但由于目前大多数PCR 检测是测定CMV DNA 片段,因此,“CMV DNA 血症”可能是一个更合适的表述。
CMV 潜伏性感染的经典定义是有能维持复制能力的病毒基因组,而没有活跃的病毒复制,一般可通过检测CMV 特异性免疫球蛋白G(IgG)来评估。CMV IgG 检测阳性且证实曾接触过CMV的患者即为CMV 血清学阳性者。CMV 再激活(reactivation)指血清学阳性受者体内既往潜伏病毒发生的活动性感染,需要与血清学阴性受者的初次感染相区别。
FAQ 2 :CMV 感染的后果是什么?
在HCT 后频繁的CMV 监测的条件下,在此期间诊断的CMV 感染往往无明显症状。但是,如果不进行抢先治疗,这类CMV 活动性感染往往会发展为CMV 病。在没有抗病毒措施和采用抢先治疗策略之前,CMV 肺炎是CMV 病最常见的临床表现类型;而在抢先治疗时代,CMV 相关胃肠道疾病成为CMV 病最常见的临床表现,其原因可能是,与肺炎相比,CMV DNA 血症和胃肠道疾病之间的关联性相对较差。此外,CMV 病还可波及其他任何器官,包括肝脏、视网膜和中枢神经系统等。
即使在抢先治疗时代,没有发生CMV 病的情况下,CMV 感染也会增加HCT 后的非复发死亡率,这提示了CMV 感染或其治疗的负面间接效应。同时,莱特莫韦的一项Ⅲ期临床试验观察,CMV病无关的死亡率获益与莱特莫韦预防没有相关性,也证实了CMV 的负面间接效应。未来仍需进一步研究来明确间接效应对HCT 后结局的影响。
CMV 再激活与血液恶性肿瘤在HCT 后复发风险降低的相关性仍有争议,2 个大型CIBMTR研究均未能证实其有保护作用。因此,CMV 感染对复发的任何假定的有益影响都可能被其导致的非复发死亡率和总死亡率的增加所否定。
FAQ 3 :异基因HCT 后CMV 活动性感染和CMV病的相 关危险因素有哪些?
异基因HCT 后CMV 感染和CMV 病的主要危险因素包括:CMV 血清学阳性受者、急性移植物抗宿主病、使用泼尼松≥ 1 mg·kg-1·d-1(或同等剂量激素治疗)、去T 细胞移植(包括阿仑单抗或ATG)、单倍体相合移植、脐带血移植、HLA 不相合或无关供者、淋巴细胞减少、高龄、HCT 后使用环磷酰胺,CMV 感染风险可能因选择去T 细胞移植还是T 细胞保留移植而发生变化,但仍需要更多的研究。移植前受者CMV 血清学状态仍然是异基因HCT 后CMV 感染最重要的预测因子。所有供者和受者都应在HCT 前常规进行CMV 特异性IgG 检测(A-Ⅱ)。由于母体抗体可能经胎盘传输,对于小于12 月龄的患儿血清学阳性结果需要谨慎解释。可通过PCR 检测尿液或唾液CMV 来识别那些移植前CMV 真阳性的患者。目前没有足够的证据推荐其他免疫检测方法来确定CMV 的潜伏感染状态。
在美国,种族和社会经济差异被认为是可影响CMV 血清阳性率和先天性CMV 感染率的因素。另外的一项研究发现,非白种人HCT 受者在移植后有发生更加严重CMV 感染(CMV pp65 抗原血症>10 细胞/20 万外周血白细胞,或CMV DNA>1 000 拷贝/mL 血浆)的风险。然而,这一发现的机制仍不清楚,移植相关的混杂变量可能起到了一定的作用。这些危险因素与HCT 后CMV 感染间的复杂关系仍需进一步研究。
FAQ 4 :哪些非药物策略可以预防HCT 受者CMV感染?
对于CMV 血清学阴性的HCT 受者,首选血清学阴性供者以降低经移植物传播的原发性CMV感染风险和非复发死亡率(A-Ⅱ)。选择血清学阴性供者或去白细胞的血液制品可降低经输血传播CMV 感染的风险(A-Ⅰ)。选择病原体灭活血小板也可降低输注血小板感染CMV 的风险(A-Ⅰ)。
对于血清学阴性的HCT 受者,存在原发性社区获得性感染的长期风险。由于CMV 可通过口咽和泌尿生殖道间歇性排出,照护者需保持良好的手卫生习惯,尤其在更换尿布或与幼儿接触时。除此之外,目前没有降低原发性社区获得性CMV感染风险的其他建议。
对于CMV 血清学阳性受者,如果选择血清学阴性供者实施保留T 细胞移植,较选择血清学阳性供者,更易出现CMV 特异性免疫重建受损、CMV 病毒载量增加、CMV 再激活风险增加、迟发性CMV 感染及CMV 病等负面影响。选择无关供者和清髓预处理方案的HCT 时,CMV D-/R+ 较CMV D+/R+ 总生存率更低。针对无关供者HCT 的研究表明,HLA 匹配程度和供者年龄是最重要的生存预测因素。因此,对于CMV 血清学阳性受者,如果有多个HLA 匹配度相近且年龄差在10 岁以内的供者,可以考虑CMV 血清学阳性供者(B-Ⅱ)。
由于缺乏益处,不推荐预防性使用静脉注射免疫球蛋白或富含CMV-IgG 制剂(E-Ⅰ)。疫苗接种和过继性免疫治疗将在后续部分讨论。
FAQ 5 :CMV 预防和抢先治疗的策略有何不同?
所有进行异基因HCT 的移植中心都应执行CMV 预防和抢先治疗策略,这两种策略是互补而非互斥的关系(A-Ⅰ)。预防性策略指对有CMV感染风险但无活动性感染的患者进行抗病毒治疗。在感染发生前实施的预防为一级预防;在抢先治疗后或CMV DNA 血症清除后防止感染复发的治疗为二级预防。
抢先治疗是指常规监测血浆或全血中CMV 病毒载量,并在病毒载量超过阈值时启动抗病毒治疗。抢先治疗依赖于灵敏且快速的检测方法,以便及早开始治疗并防止疾病的发展。定量PCR(qPCR)具有灵敏度高(尤其在白细胞减少时)以及更好的定量性能,因此推荐通过qPCR 检测病毒载量而非检测pp65 抗原来监测CMV 活动性感染(A-Ⅱ)。
抢先治疗一般从诱导治疗开始,通常持续到CMV DNA 血症清除或病毒载量大幅下降为止(表2)。一旦诱导治疗后病毒载量下降,即可采用“维持剂量”(表2)继续治疗DNA 血症,同时减少毒副作用(见FAQ 17),具体方案会因移植中心和患者个体差异有所不同。
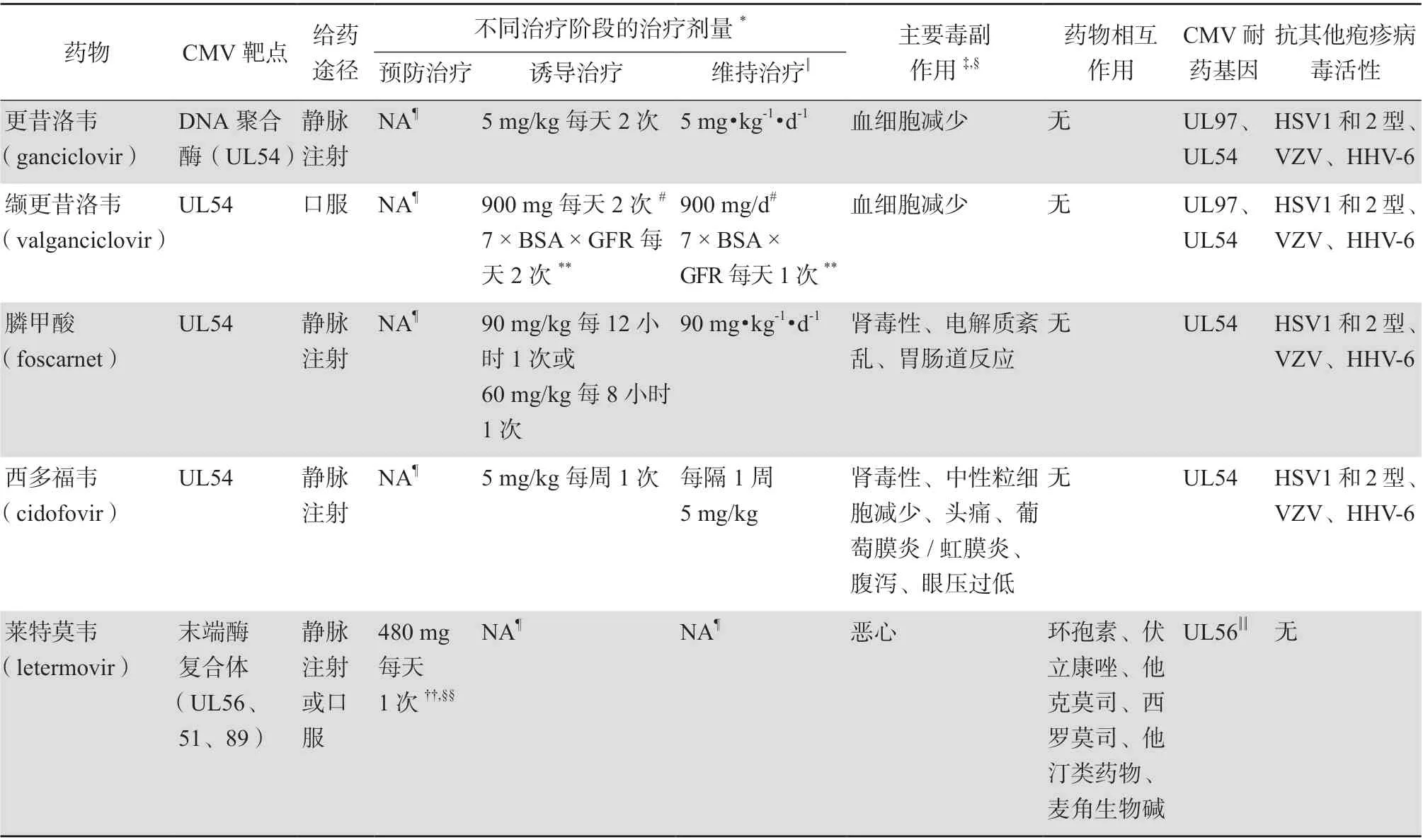
表2 HCT 受者CMV 感染和CMV 病的防治药物
曾经CMV DNA 血症清除后防止复发的持续低剂量抗病毒治疗也用“维持治疗”来描述,但目前认为使用二级预防来描述更为准确,因此本指南将使用二级预防进行表述。
由于抢先治疗和CMV 病的治疗策略不同(将在单独的指南中讨论),因此,所有CMV DNA 血症患者都应进行评估是否存在CMV 病。我们不推荐允许CMV 再激活的预防策略,比如采用抢先治疗而不是为了减少疾病复发的预防措施(E-Ⅱ)。
FAQ 6 :推荐哪些抗病毒药物用于CMV 感染预防或治疗?
CMV 感染防治的药物见表2。只有莱特莫韦和更昔洛韦被美国食品药品监督管理局(United States Food and Drug Administration,US-FDA)批准用于HCT 受者CMV 相关适应证。缬更昔洛韦、膦甲酸和西多福韦获批用于实体器官移植受者和获得性免疫缺陷综合征患者的CMV 相关适应证。此外,上述药物均未被批准用于儿童。然而,本指南中描述的这些药物在成人和儿童中的超适应证使用是基于数十年的临床经验和已发表数据。FAQ 12 讨论了大剂量阿昔洛韦和伐昔洛韦的作用。
FAQ 7 :对于CMV 血清学阳性的成人异基因HCT受者,推荐什么药物预防?
莱特莫韦于2017 年获US-FDA 和欧洲药品管 理 局(European Medicines Agency,EMA) 批准,用于CMV 血清学阳性成人异基因HCT 受者的一级预防。这一适应证的获批基于莱特莫韦的Ⅲ期随机临床试验结果。建议在HCT 后28 d 内对CMV 血清学阳性的异基因HCT 成人患者进行莱特莫韦预防,并持续至移植后第100 天(A-Ⅰ)。
根据现有临床证据并权衡成本效益等问题,部分移植中心仅对莱特莫韦Ⅲ期临床试验中定义的高危HCT 受者进行莱特莫韦预防(见FAQ 12)。在莱特莫韦预防前,应行qPCR 评估CMV DNA水平(A-Ⅱ)。如果检测到可定量的CMV DNA血症,应考虑行抢先治疗(FAQ 15)。严重肝功能损伤(Child-Pugh C 级)患者应谨慎使用莱特莫韦(C-Ⅲ),对于肌酐清除率<10 mL/min 患者,目前缺乏足够的数据来指导莱特莫韦调整剂量。
目前,莱特莫韦未被批准用于18 岁以下儿童,但一项针对儿童HCT 受者的莱特莫韦的Ⅱb期开放性标签研究(NCT03940586)正在进行中,该研究对接受治疗的患儿将按年龄进行分层分析(12~18 岁及12 岁以下)。
FAQ 8 :莱特莫韦预防期间,需要注意与哪些药物间的相互作用?
莱特莫韦可增加他克莫司、西罗莫司和环孢素的血药浓度,可降低伏立康唑的血药浓度。与莱特莫韦联用时,应对上述药物进行治疗性药物监测(TDM)并及时调整剂量(A-Ⅱ)。莱特莫韦对泊沙康唑和艾沙康唑的血药浓度无显著影响。
由于有机阴离子转运体OATP1B1 和OATP1B3 介导的药物相互作用,接受环孢素治疗的患者,莱特莫韦的剂量减少为240 mg/d。除环孢素外,目前尚不建议在联用其他可产生相互作用的药物时,对莱特莫韦的常规剂量进行调整(D-Ⅱ)。服用麦角生物碱的患者禁用莱特莫韦,建议同时接受他汀类药物和环孢素的患者常规咨询临床药师(A-Ⅱ)。
FAQ 9 :在接受莱特莫韦预防时,是否需要监测CMV 活动性感染?
需要,目前建议在莱特莫韦预防期间常规监测CMV 活动性感染,并根据各移植中心设定的阈值启动抢先治疗(见FAQ 15)(A-Ⅱ)。在一项Ⅲ期临床试验中,24 例(7.7%)患者因突破性CMV DNA 血症而启动抢先治疗,其中12 例(3.7%)接受了莱特莫韦预防。后续的观察性研究显示,对于高危和低危CMV 血清学阳性的HCT 受者,使用莱特莫韦预防后发生有临床意义的CMV 感染率约为0~20%,但患者群体差异和抢先治疗启动阈值差异,限制了这些研究的解释。最新数据表明,某些情况下,莱特莫韦预防期间低水平CMV DNA血症可能不需要中止预防和启动抢先治疗。未来仍需更多的临床经验来明确莱特莫韦预防期间对突破性CMV DNA 血症的监测和最佳治疗方法。
FAQ 10 :在移植第100 天停止莱特莫韦预防后,应如何监测CMV 活动性感染?
莱特莫韦Ⅲ期临床试验的结果显示,在停止莱特莫韦预防后(第14 周)至移植后第24 周,所有患者中约有10%、CMV 感染高风险人群中约有20%出现了有临床意义的CMV 感染。因此,推荐各移植中心监测CMV 活动性感染至HCT 后6 个月(第180 天),必要时启动抢先治疗(A-Ⅱ)。与CMV 监测和抢先治疗相比,莱特莫韦预防可能因为抑制CMV 再激活,CMV 抗原暴露减少,从而延迟CMV 特异性细胞免疫重建。
FAQ 11 :接受莱特莫韦预防的患者是否需使用阿昔洛韦、伐昔洛韦、泛昔洛韦预防单纯疱疹病毒(HSV)和水痘带状疱疹病毒(VZV)?
需要,莱特莫韦对HSV 或VZV 无活性,因此需要使用其他药物预防HSV 和VZV(A-Ⅰ)。
FAQ 12 :若由于医疗成本、可及性、年龄或其他问题,CMV 血清学阳性的成人异基因HCT 受者不能使用莱特莫韦进行预防,怎么办?
推荐通过CMV 监测和抢先治疗来预防CMV病(A-Ⅰ)。不推荐使用缬更昔洛韦、更昔洛韦或膦甲酸等药物进行一级预防(D-Ⅰ)。
HCT 后早期使用更昔洛韦进行一级预防可有效预防CMV 感染,但并没有产生明显的生存获益。另外有研究显示,对于CMV 血清学阳性的异基因HCT 受者,采用pp65 抗原血症指导的抢先治疗策略,一旦检测抗原阳性则启动更昔洛韦抢先治疗并持续到移植后100 d。这种方法和更昔洛韦预防策略(从植入开始一直用到第100 天)一样,均能有效预防CMV 病。但考虑到骨髓抑制的风险,以及可采用高灵敏度qPCR 检测来指导抢先治疗,目前不推荐使用缬更昔洛韦或更昔洛韦进行一级预防。同样,HCT 后早期使用膦甲酸也可有效预防CMV 感染和CMV 病,但由于不良反应,不推荐常规使用。
与成人不同,儿童使用更昔洛韦或膦甲酸进行一级预防更为常见。对于特定儿童HCT 受者(C-Ⅲ),可以考虑使用缬更昔洛韦、更昔洛韦或膦甲酸作为一级预防,但目前无法就最佳患者群体和方案提出建议。
使用大剂量静脉注射阿昔洛韦(肾功能正常患者,1 500 mg·m-2·d-1)和伐昔洛韦(肾功能正常患者,8 g/d)一级预防可降低CMV 活动性感染的风险,但不能降低CMV 病的风险。大剂量阿昔洛韦和伐昔洛韦预防联合CMV 监测和抢先治疗已用于某些高危人群,如脐带血移植和单倍体相合HCT 受者。不建议常规使用大剂量阿昔洛韦或伐昔洛韦单药预防CMV 感染(E-Ⅱ),若使用上述药物进行CMV 预防,应始终结合CMV 监测和抢先治疗策略(A-Ⅰ)。
FAQ 13 :其他异基因HCT 受者人群,应该实施CMV 监测和抢先治疗策略吗?
由于CMV 可通过移植物从供者传播给受者,因此,所有CMV D+/R- HCT 受者都应实施CMV监测和抢先治疗策略(A-Ⅰ)。相比之下,CMV D-/R- HCT 受者感染CMV 风险相对较低,目前尚没有评估D-/R-移植状态下的预防策略的随机试验。一项单中心研究表明,对CMV D-/R- HCT 受者实施CMV 监测和抢先治疗策略可有效预防输血传播引起的CMV 病,感染发生率为3%。因此,对于D-/R- 受者,尚不清楚 CMV 监测是否具有成本效益,但对HCT 后很可能需输血治疗的患者可以考虑进行CMV 监测(C-Ⅱ)。
FAQ 14 :何时开始监测CMV,应该多久监测1 次?
从移植开始或移植后第二周开始,每周监测1 次,并持续至HCT 后第100 天或更长时间(见FAQ 20)(A-Ⅱ)。因非恶性疾病而接受HCT 的CMV 血清学阳性患者,如果在入院前几周使用T细胞耗竭药物(如ATG 或阿仑单抗)预防移植物抗宿主病(GVHD)时,则应从入院时便开始监测CMV(C-Ⅱ)。一项针对CMV 血清学阳性脐带血移植受者的研究,提到每周进行2 次CMV 监测,但目前尚无足够的证据来支持这种策略,尤其在使用莱特莫韦进行一级预防的脐带血移植人群。
FAQ 15 :何时启动抢先治疗?
目前尚无经过验证的统一的病毒载量标准作为启动抢先治疗的阈值。该阈值可能因移植中心而异,并根据患者潜在的CMV 风险特征而各有不同。基于近期的Ⅲ期临床试验,可有效预防CMV病的启动抢先治疗病毒载量阈值为:低危患者300~1 000 拷贝/mL(约274~909 IU/mL),高危患者150 拷贝/mL(约137 IU/mL)。建议每个移植中心根据患者风险类别和中心特定数据来确定病毒载量阈值(A-Ⅱ)。病毒载量的动态变化可以预测并指导启动抢先治疗,但将该策略推荐为常规使用仍需要额外的临床数据。
FAQ 16:抢先治疗的一线药物是什么?有什么注意事项?
一般建议口服缬更昔洛韦或静脉注射更昔洛韦,而非膦甲酸作为抢先治疗一线药物(B-Ⅱ)。由于口服缬更昔洛韦更易于给药,且与静脉注射的更昔洛韦具有临床等效性,因此是抢先治疗的首选一线治疗药物。若存在口服障碍或口服药物吸收障碍,如严重的胃肠道GVHD,则不推荐使用缬更昔洛韦(D-Ⅱ)。
中性粒细胞减少是HCT 受者使用缬更昔洛韦和更昔洛韦治疗的常见并发症,因此,需定期评估中性粒细胞绝对计数(A-Ⅲ)。同时,应注意避免联用霉酚酸酯、甲氧苄啶-磺胺甲唑等骨髓抑制药物。在抢先治疗期间,如果出现中性粒细胞减少,一般不建议减少缬更昔洛韦和更昔洛韦剂量(除非符合FAQ 17 中所述的调整为维持剂量的标准)(D-Ⅲ),而是应给予粒细胞集落刺激因子(G-CSF)治疗或改为膦甲酸治疗,直至中性粒细胞绝对计数恢复正常。
对于植入前存在CMV DNA 血症,或植入后早期、伴血细胞减少或患者不耐受等不适合使用缬更昔洛韦或更昔洛韦的情况,推荐使用膦甲酸作为初始抗病毒药物(A-Ⅰ)。在膦甲酸治疗期间,应注意监测肾功能和电解质水平。由于西多福韦易出现肾毒性且疗效不确切,目前仅作为三线药物(C-Ⅱ)。无论选择何种药物,都应在抢先治疗起始治疗时给与诱导剂量(表2),并根据肾功能调整药物剂量。
FAQ 17 :抢先治疗应该持续多久?
尽管临床实践中存在差异,但抢先治疗诱导治疗一般持续2 周,直至CMV DNA 血症清除(B-Ⅱ)。若诱导治疗1~2 周后病毒载量下降,则可以考虑过渡至维持治疗(表2),并持续到CMV DNA 血症清除(B-Ⅱ)。
FAQ 18 :接受抢先治疗时,如果病毒载量增加怎么办?
在抢先治疗诱导治疗的14 d 以内,常常观察到病毒载量无明显变化或轻度增加(≤1 log10),特别是接受全身糖皮质激素治疗的急性移植物抗宿主病患者或接受去T 细胞移植的患者。对于初治患者,耐药的可能性很低,通常无需改变治疗方案(B-Ⅱ)。难治性或耐药性感染的诊疗将在另一个单独的指南中讨论。
FAQ 19 :抢先治疗结束后,患者应如何管理?
接受过第一个疗程抢先治疗的HCT 受者仍存在CMV DNA 血症复发的风险,可能需要再次抢先治疗。因此,抢先治疗结束后,推荐使用缬更昔洛韦900 mg/d(肾功能正常)或莱特莫韦(剂量同一级预防)进行二级预防,或实施CMV 监测和抢先治疗策略(A-Ⅱ)。如果选择实施CMV 监测和抢先治疗,应根据移植中心界定的病毒载量阈值,对复发性CMV DNA 血症患者重新启动抢先治疗。在第1 疗程抢先治疗中使用的药物仍可以用于第2 疗程抢先治疗(B-Ⅱ)。
FAQ 20 :哪些患者在HCT 第100 天后,仍需要继续给予药物预防?
如FAQ 10 中所讨论的,建议对接受莱特莫韦预防至第100 天的患者,进行CMV 监测到HCT后180 d。此外,建议对于移植第100 天以后存在至少以下1 个CMV 感染危险因素的患者,实施CMV 监测和抢先治疗策略,或继续使用缬更昔洛韦或莱特莫韦进行预防(A-Ⅱ):
①淋巴细胞减少(<100 个/mm3);② 移植第100 天以前出现的CMV 感染;③因GVHD 需要大剂量泼尼松(≥0.5 mg·kg-1·d-1)或同等剂量激素治疗;④ 缺乏CMV 特异性T 细胞免疫。
基于目前的数据,对于符合以上标准的患者,尚无法就移植第100 天后的预防持续时间给出建议,这可能会因患者个体差异而有所不同。
FAQ 21 :HCT 前CMV 病患者的最佳预防策略是什么?
HCT 前CMV 病很少见,但与HCT 后CMV病的早期复发和不良预后有关。一般应延迟HCT以充分治疗移植前CMV 病(B-Ⅲ)。针对HCT前CMV 病患者已经提出了积极的二级预防策略,包括HCT 后使用膦甲酸或更昔洛韦进行二级预防,或更频繁(即每周2 次)的CMV 监测以指导抢先治疗。CMV 血清学阳性HCT 受者可以选择莱特莫韦预防替代上述策略。然而,对于HCT 前出现CMV 病,但在HCT 后无法使用莱特莫韦预防的患者,可以考虑采用上述二级预防策略(C-Ⅲ),尽管此类患者的最佳预防方案仍未确定。
FAQ 22 :在异基因HCT前进行CMV预防是否有用?
一般不建议在HCT 前进行CMV 预防(D-Ⅱ)。虽然更昔洛韦或缬更昔洛韦已用于HCT 前的一级预防,但是,由于患者差异和HCT 后预防策略的不同,这种预防的益处尚不明确。最近的一项研究表明,CMV 血清学阳性的脐带血移植受者在HCT 前8 天至HCT 前2 天期间接受更昔洛韦预防,和移植后接受相同的预防策略相比,对HCT 后的结局无影响。
FAQ 23 :自体HCT 受者如何预防CMV 感染?
由于自体HCT 受者发生CMV 病的风险非常低,大多数情况下无需采取预防策略(D-Ⅱ)。但是,对于接受CD34 选择性移植的自体移植受者,CMV 感染和CMV 病的风险较高,可以从CMV监测和抢先治疗中获益(C-Ⅱ)。
2 尚未解决的问题/未来的发展方向
2.1 填补在儿童中使用新型抗病毒药物有关的知识空白
儿童HCT 受者通常经历与成人HCT 受者相似的CMV 感染、CMV 病和耐药性风险。然而,新型抗病毒药物在儿童HCT 受者中的安全性和有效性尚缺乏相关数据。莱特莫韦目前还没有获批用于儿童患者。但是,目前已有研究报道莱特莫韦在儿童HCT 受者中超适应证使用的情况,然而,仍需要进一步的数据进行验证。正如FAQ 7 中提到的,一项莱特莫韦在儿童HCT 受者中的Ⅱb 期研究正在进行中。在获得更多数据之前,建议18岁以下的儿童参加临床试验(A-Ⅲ)。
2.2 优化莱特莫韦预防策略
2.2.1 进一步明确莱特莫韦疗效和死亡率获益 尽管在Ⅲ期临床试验中观察到莱特莫韦预防可以降低死亡率,但并非所有的高危HCT 受者都有同等的代表性。Ⅲ期临床试验中,单倍体相合移植受者占总人数的14.3%,脐带血受者占4%,体外去T 细胞移植受者占2.5%。因此,仍需要更多的研究来明确莱特莫韦预防对不同CMV 风险的HCT 人群的疗效和生存获益,尤其是Ⅲ期临床试验中占比例相对较低的高风险患者,似乎可从莱特莫韦预防中最大获益。
2.2.2 确定莱特莫韦预防的最佳疗程 在Ⅲ期预防试验中,从移植后第14 周(停用莱特莫韦时)至第24 周期间,所有患者中约有10%、CMV 高危人群中约有20%发生了临床意义CMV 感染。因此,需要确定莱特莫韦预防的最佳疗程。目前,一项旨在比较莱特莫韦预防疗程100 d 和200 d 的Ⅲ期临床试验正在进行中,主要疗效结局指标为HCT 后第28 周的CMV 感染率(NCT03930615)。
2.3 确定其他药物在抢先治疗中的作用
Maribavir:近期,一项Ⅱ期研究表明,对于全血或血浆CMV 载量≤100 000 拷贝/mL 的HCT和实体器官移植受者,接受Maribavir 作为抢先治疗的疗效并不差于缬更昔洛韦。另一项Ⅲ期临床试验旨在比较Maribavir(400 mg,每日2 次)与缬更昔洛韦,用于治疗年龄≥16 岁的HCT 受者首次发作的无症状CMV 感染的疗效,目前该研究正在进行中(NCT02927067)。
莱特莫韦:由于缺乏疗效数据且体外试验发现容易耐药,目前不推荐将莱特莫韦作为抢先治疗单药治疗。一项Ⅲ期预防研究发现,在随机分配至接受莱特莫韦预防时检测到CMV DNA 血症(未达到抢先治疗标准)的患者中,约31%出现有临床意义的CMV 感染,需要停用莱特莫韦并启动标准抢先治疗;然而,该试验报道的耐药发生率相对较低。未来仍需更多的研究来确定莱特莫韦作为抢先治疗的疗效。
2.4确定CMV 特异性细胞介导免疫(cell-mediated immunity,CMI)的作用
目前有几种评估CMV 特异性T 细胞反应的方法。在实体器官移植受者中,这些检测方法在评估CMV 感染风险和指导预防疗程方面显示出潜在的价值。这些检测方法证实了在异基因HCT 患者中CMV 特异性免疫建立与感染保护之间的关系。小规模单中心研究表明,使用CMV 特异性免疫检测可能有助于指导HCT 后的抢先治疗。在推荐这一策略之前,仍需进一步研究。
2.5 CMV 疫苗接种策略
研发一种有效的CMV 疫苗用于移植受者是一个挑战,目前尚无获批的疫苗可供使用。近期一项针对CMV 血清学阳性HCT 受者的安慰剂对照Ⅲ期临床试验,一个很有希望的候选疫苗ASP0113 未能达到主要或次要终点。目前正在评估其他几种候选疫苗。
2.6 CMV 细胞疗法
过继性免疫治疗指通过分离供者T 细胞、体外增殖并将其输注给受者以重建CMV 特异性T 细胞应答的治疗方法。一些小的研究显示,过继性免疫治疗作为预防和抢先治疗的辅助治疗已在HCT受者中安全使用。另外,使用HLA 部分匹配的第三方细胞解决了T 细胞制备中固有的几个局限性。但仍需随机研究来明确过继性免疫治疗在HCT 受者预防CMV 或抢先治疗的疗效和安全性。免疫治疗作为难治性/耐药性CMV 感染和CMV 病的辅助治疗策略将在另一个指南中单独进行讨论。
专家点评:陈心传教授(四川大学华西医院血液内科医疗副主任,医学博士,硕士生导师,副主任医师)
CMV 感染是异基因HCT 后最常见的感染并发症之一。在我国,CMV 感染极为广泛,血清学阳性率高达95%。CMV 感染对HCT 受者的影响包括两个方面,即直接效应和间接效应。前者主要是CMV 病,后者包括GVHD、机会性感染、免疫抑制以及死亡率增加。
长期以来,CMV 感染的防治策略主要包括预防和抢先治疗两种方式。由于目前中国市场可及的抗CMV 药物主要是更昔洛韦、缬更昔洛韦和膦甲酸(西多福韦未在国内市场上市),而现有的这些可获得的药物可导致粒细胞缺乏、继发性植入功能不良和肾损害等不良反应,它们的疗效或安全性不尽人意,且均未获批HCT 受者CMV 预防适应证。因此,目前国内大多数移植中心仍然选择抢先治疗。
然而,令人遗憾的是,即使在积极的抢先治疗下,CMV 再激活仍然会导致HCT 受者GVHD、机会性感染以及死亡风险增加。此外,对于抢先治疗,除了对其骨髓毒性等不良反应在移植患者中的担忧之外,目前尚没有统一的启动抢先治疗的病毒载量阈值,抢先治疗无法解决CMV 反复再激活、难治性/耐药性CMV 等问题,加之频繁的CMV 监测也会增加患者的痛苦和经济负担。因此,对于HCT 受者而言,预防是一个非常重要的CMV 管理手段,尤其在中国,CMV 血清学阳性率高达95%的背景下,CMV 预防更应该受到足够的重视。
CMV 预防这一概念是针对CMV 再激活提出的。HCT 受者发生GVHD 时,往往会更容易出现CMV 再激活,特别是二次再激活、多次再激活的问题,这些是非常棘手的临床问题。我国相关研究显示,CMV 二次再激活的比例高达30.3%,而这类反复再激活的CMV 感染,即使是接受了抢先治疗,仍然表现出对预后的不良影响。另外的研究显示,积极的CMV 预防可能减少CMV 反复再激活以及难治性CMV 感染的发生。因此,预防与抢先治疗是互补,而非互斥的关系,预防同样是一种非常重要的管理CMV 的方法。
莱特莫韦,一种新型抗CMV 药物,通过抑制CMV DNA 末端酶复合体阻断病毒的复制。于2017 年在美国和欧洲、2021 年在中国获批上市,批准用于CMV 血清学阳性的成人异基因HCT 受者预防CMV 感染和CMV 病。一项Ⅲ期临床试验显示其可以显著降低CMV 感染率和24 周全因死亡率。因此,2017 年欧洲白血病感染会议(ECIL 7)血液系统恶性肿瘤和干细胞移植后CMV 感染的管理指南、2021 年美国移植和细胞治疗学会(ASTCT)造血干细胞移植后CMV 感染的防治策略均推荐莱特莫韦用于CMV 血清学阳性的成人异基因HCT受者预防CMV 感染。另外,CMV 疫苗、过继性免疫治疗作为CMV 非药物预防目前处于进一步研究中。期待未来有更多新的防治CMV 的方法,帮助临床医师解决CMV 管理的困境。
致谢:感谢默沙东(中国)投资有限公司为本文翻译提供学术支持,感谢上海北翱医药科技有限公司为本文提供辅助编辑工作。
版权声明:本文原文“American Society for Transplantation and Cellular Therapy Series :#3-Prevention of Cytomegalovirus Infection and Disease After Hematopoietic Cell Transplantation”,首次发表在Transplantation and Cellular Therapy,2021,27(9):707-719;本次二次发表已取得版权所有者Elsevier 的同意,对原文进行翻译,不涉及一稿多投及侵犯版权等问题。
