改性地瓜皮对刚果红的静态吸附效果研究
2022-11-01史薇,罗莺
史 薇,罗 莺
(武汉市生态环境局 江岸区分局,湖北 武汉 430019)
在染料废水吸附研究中,学者们把研究重点集中于新型吸附材料[1],尤其是利用农林废弃物制备新型吸附材料[2-5],并且在环境污染处理方面越来越多地关注廉价和有效的替代技术及其实际应用。
农林废弃物因含有大量木质素、纤维素和半纤维素等成分,具有较强的吸附性能,同时又易于进行改性处理以制备新型吸附剂,且其具有来源广泛、价格低廉等优点,所以研究者们对农林废弃物的应用进行了广泛而深入的研究。Amarasinghe等[6]研究了茶叶渣对水溶液中Cu2+和Pb2+的吸附,在温度22 ℃,pH值5.10~6.10时,吸附量达到最大,对Cu2+和Pb2+的最大吸附量分别为48.10 mg·g-1和65.10 mg·g-1。
地瓜皮作为农林废弃物,因其具有成本低廉、易于得到且吸附性能力良好等特点,常常被用作染料废水处理的吸附剂。而利用乙二胺对地瓜皮进行改性后,大大提高了其吸附废水中阴离子染料的能力,进一步降低了废水处理的成本。
笔者通过静态吸附实验,研究乙二胺改性地瓜皮对刚果红的吸附效果,并进一步探讨改性地瓜皮的吸附机理和作用,以期为开发廉价易得的农业废弃物吸附材料提供充分的理论基础。
1 实验试剂与仪器
1.1 实验试剂
实验过程所用到的试剂如表1所示:

表1 主要实验试剂
1.2 实验仪器
实验所用到的仪器与设备如表2所示:

表2 主要实验仪器与设备
2 实验部分
2.1 地瓜皮的预处理
地瓜皮原料取自湖北洪湖地区。将水洗干净后的地瓜皮晾干,用研磨机将晾干的地瓜皮研成粉末,过60目筛,再用去离子水洗净,置24 h恒温烘箱中于55 ℃烘干至恒重,保存于干燥器中待用。
2.2 改性地瓜皮的制备
取30 mL蒸馏水、10 mL无水乙二胺、2 g水洗地瓜皮粉末混合于500 mL烧瓶中,置于80 ℃恒温水浴锅中反应2 h。待反应结束后,用蒸馏水反复冲洗,抽滤,至中性。洗净后放入恒温烘箱中于55 ℃烘干至恒重,得改性后地瓜皮粉末,置于干燥器中待用。

图1 实验装置
2.3 地瓜皮形貌的电镜扫描
扫描电子显微镜形貌如图2所示:

图2 地瓜皮扫描电子显微镜图像
从图2(a)可以看出,地瓜皮表面呈多孔隙结构,这种孔隙结构有利于吸附的进行;从图2(b)可以看出,乙二胺改性后的地瓜皮表面孔隙更立体,结构更饱满,这种立体结构更有利于吸附的进行,由此图可得出,乙二胺改性地瓜皮对吸附结构有促进效果。
2.4 静态吸附实验
2.4.1 静态实验步骤
将1 g/L的改性地瓜皮粉末放入到100 mL锥形瓶中,加入一定浓度的刚果红溶液50 mL,置于水浴恒温振荡器,0.5 h后取上清液,离心,用分光光度法测定剩余染料浓度。
2.4.2 标准曲线的绘制
根据实验测得的吸光度和标准溶液的浓度,分别以吸光度和标准溶液浓度为横纵坐标,绘制刚果红溶液标准曲线。
2.4.3 吸附剂平衡吸附量及吸附率的计算
取离心后上清液,用分光光度计测定反应后溶液的吸光度,然后采用下式计算地瓜皮粉末对刚果红的吸附量:
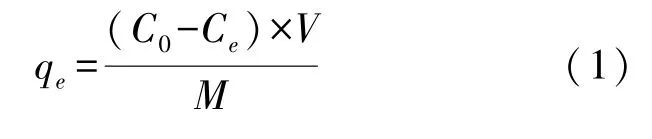
用下式计算地瓜皮粉末对刚果红的吸附率:

式中:C0——刚果红溶液的初始浓度,mg/L;Ce——吸附达到平衡时染料的浓度,mg/L;V——刚果红溶液的体积,L;M——吸附剂地瓜皮质量,g;qe——吸附量,mg/g;m——吸附率,%。
3 实验结果分析
本实验主要研究了溶液pH值、吸附剂用量、染料浓度和反应时间4个影响因素对乙二胺改性地瓜皮吸附刚果红染料效果的影响。
3.1 pH值对吸附刚果红的影响
为研究溶液pH值对乙二胺改性地瓜皮(MPS)对刚果红(CR)吸附效果的影响,首先取50 mg的MPS,再移取50 mL的初始浓度为100 mg/L的CR溶液,置于100 mL锥形瓶中,并调节pH值分别在4.00~10.00之间变化,在298 K下连续振荡24 h后,测量溶液中CR的浓度,计算其单位吸附率,实验结果如图3所示:
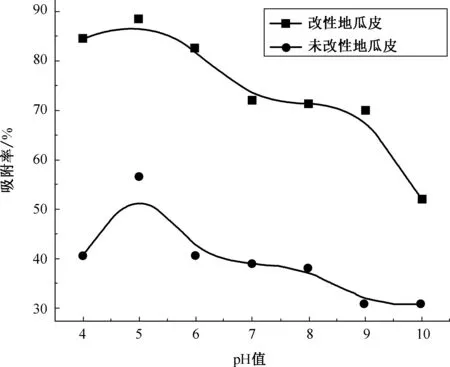
图3 pH值对地瓜皮吸附CR效果的影响
由图3可以看出,对于MPS吸附CR的体系,pH值在4~5之间时,CR的吸附率是缓慢增加的;当pH值=5时,MPS对CR的吸附率达到最大值;当pH值在5~6之间时,CR的吸附率是缓慢下降的;而pH值在7~10时的吸附率明显低于pH值在4~6时的。总体来看,在酸性条件下吸附效果优于碱性条件。
改性地瓜皮吸附刚果红实验结果表明,pH值在4~6之间时,溶液中与刚果红竞争结合改性地瓜皮表面吸附点位的质子较多,吸附活性点位较多,所以改性地瓜皮对刚果红的吸附量较大,吸附率也较大;当pH值在7~10之间时,刚果红解离带负电荷,然而此时溶液中质子数目较少,只能中和一部分带负电荷的刚果红,因此单位吸附量比pH值在4~6时减小;溶液中的质子数随pH值的增大而减少,能吸附刚果红染料的吸附点位也减少,单位吸附量减小,因而去除率呈下降趋势。当pH值大于9时,改性地瓜皮与刚果红带同种电荷,都是负电荷,他们之间产生静电斥力,因此单位吸附量有大幅度降低。因此,本实验对MPS吸附CR吸附体系采取最佳pH值为5。
3.2 吸附剂用量对吸附刚果红的影响
吸附剂的用量对溶液中染料的吸附量有着重要的影响。
本实验采用0.3~2.0 g/L的改性地瓜皮粉末,置于100 mL锥形瓶中,加入100 mg/L的刚果红溶液50 mL,在298 K恒温水浴振荡器中振荡24 h,达到吸附平衡后取出,测出吸附后染料的浓度。计算其单位吸附率,所得实验结果如图4所示:
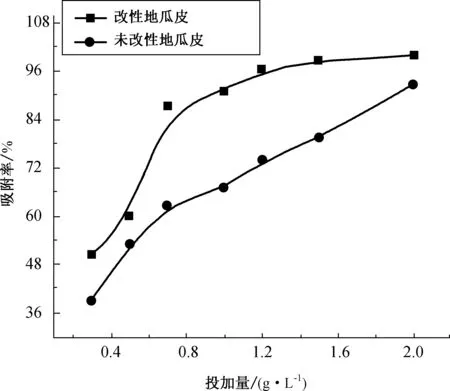
图4 吸附剂用量对吸附刚果红效果的影响
由图4可以看出,MPS-CR吸附体系的吸附率随吸附剂用量的增加而增加,MPS对CR的吸附,当改性粉末投加量由0.5 g/L增加到0.7 g/L时,CR的吸附率由60%增加到87%,吸附率大幅增加;当吸附剂用量继续增加后,吸附率增幅减缓,而吸附剂用量为2.0 g/L时,CR吸附率达99.82%。
从实验结果中发现,当吸附剂用量逐渐增大,吸附率则逐渐增加。分析其主要原因是,改性地瓜皮粉末用量增加后,用于吸附染料的活性点位也在增加,从而可以吸附更多的吸附质,所以吸附率是逐渐增加的;在吸附剂用量小于0.7 g/L时,增幅较大的原因在于吸附剂提供的吸附染料的活性点位尚未达到吸附所有染料所需的饱和点位数,所以随吸附剂用量的增加,CR吸附率大幅增加;吸附剂用量大于0.7 g/L时,吸附剂吸附点位可吸附大部分染料,使吸附率达90%以上。
综合考虑MPS对CR的吸附结果,吸附剂用量选用取1 g/L时吸附率已达90%,有较好的吸附效果,所以实验中采用1 g/L作为吸附剂的最佳浓度。
3.3 染料浓度对吸附刚果红效果的影响
本实验中,吸附剂用量为1 g/L,配制浓度为20~500 mg/L的刚果红溶液,取50 mL置于100 mL锥形瓶中,于298 K恒温水浴锅中振荡24 h,达到吸附平衡后取出,测出吸附后染料的浓度。实验结果如图5所示:
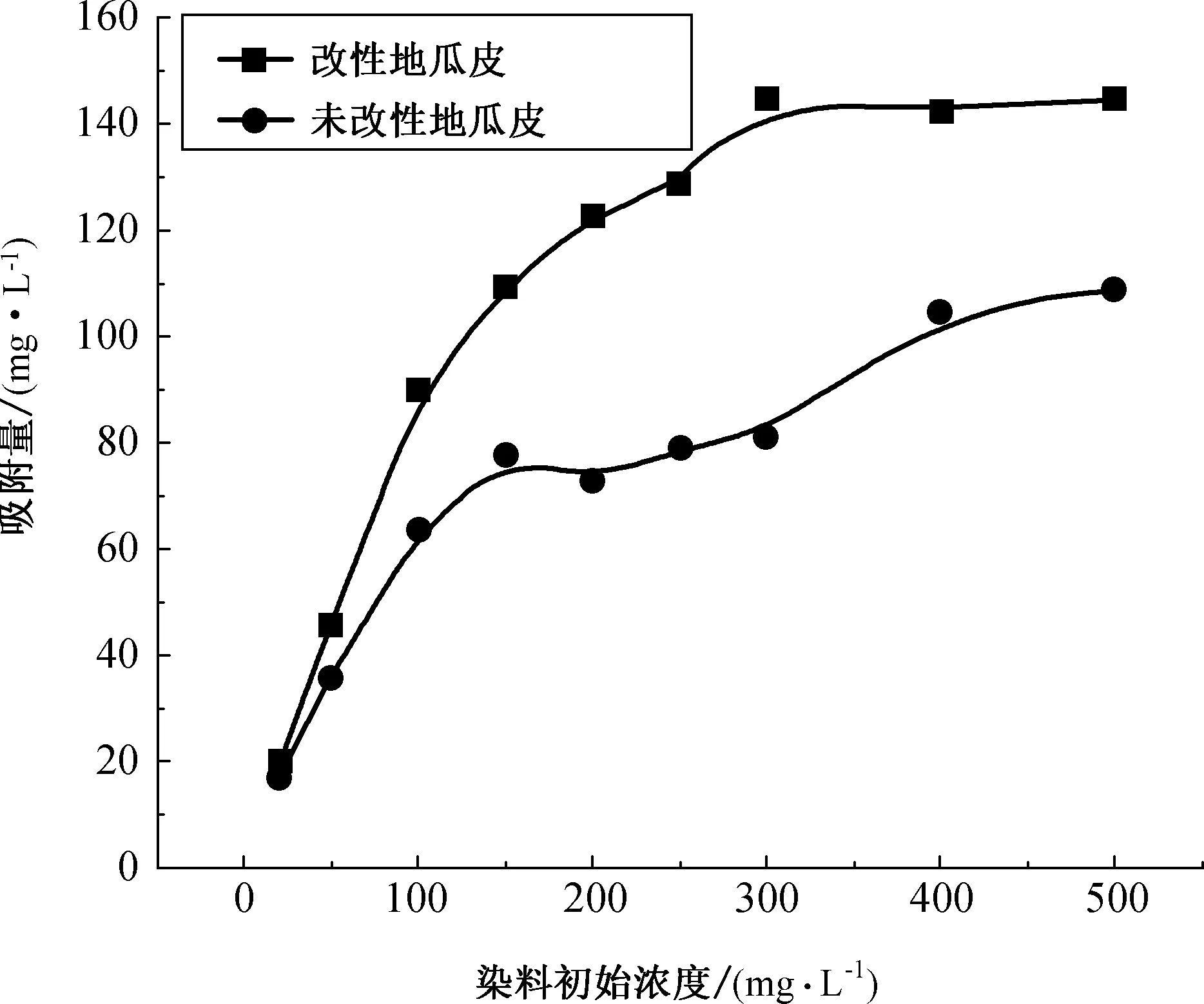
图5 染料浓度对吸附刚果红的影响
由图5可以看出,改性地瓜皮吸附CR时,随着平衡浓度的增加,单位吸附量也随之增加,并且刚开始增加幅度较大,随后逐渐达到吸附平衡。由图5可以看到,刚果红溶液浓度为300 mg/L时,改性地瓜皮对刚果红的吸附量达到最大值,在300~500 mg/L之间呈现吸附平衡状态。改性地瓜皮粉末最终达到的吸附平衡的吸附量为145 mg·g-1。染料浓度的高低对吸附效果有一定的影响。
3.4 时间对吸附刚果红的影响
首先取50 mg的MPS,再移取50 mL的初始浓度为100 mg/L的CR溶液,置于100 mL锥形瓶中,于298 K下,置于振荡器中进行吸附实验。每隔一段时间取出锥形瓶,测量溶液中CR的浓度,算出吸附率。所得实验结果如图6所示。
由图6可以看出,MPS对CR的吸附可分为开始较短时间内的快速吸附和以后的慢速吸附两个过程。在0~180 min时,吸附速率快,吸附快速进行;在180~480 min时,吸附速率开始减慢,吸附过程减缓;在480 min之后,吸附曲线逐渐趋于平稳,呈现缓慢吸附状态,吸附基本达到平衡。该趋势符合吸附基本规律。
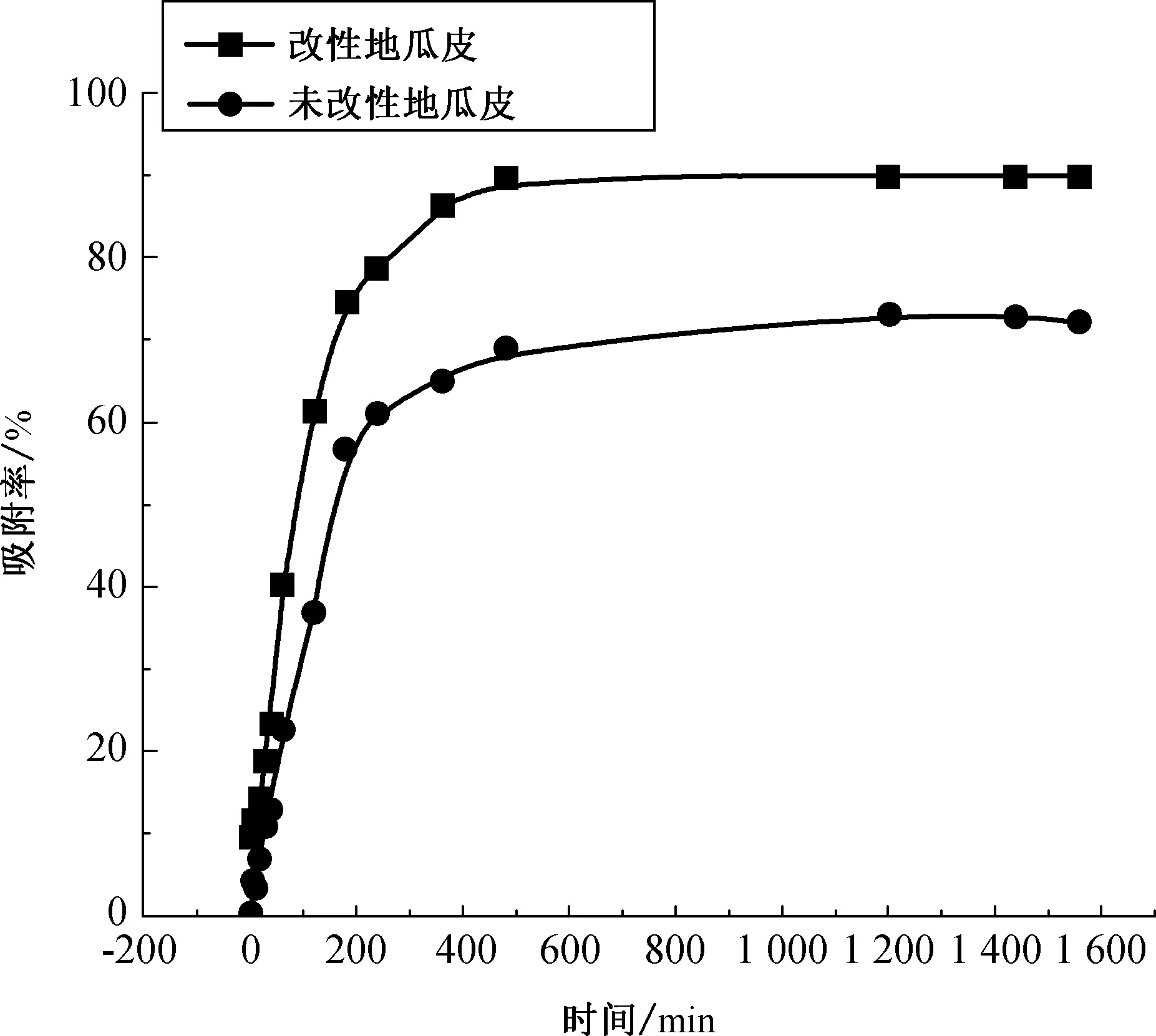
图6 时间对地瓜皮吸附刚果红效果的影响
本实验表明,吸附平衡时间为8 h。综合考虑MPS对CR的吸附,为达到较好的吸附效果,实验取24 h作为吸附平衡时间。
4 结论
本研究以廉价的农业废弃物地瓜皮为基本原料,使用乙二胺对其进行改性,研究其对阴离子染料刚果红的吸附性能。探讨了其吸附机理,实验结论如下:
(1)通过电镜扫描发现地瓜皮表面存在多孔结构,有利于吸附进行;改性地瓜皮表面较天然地瓜皮表面接入乙二胺,并且表面孔隙增多,证明地瓜皮改性在地瓜皮表面引入乙二胺,乙二胺改性地瓜皮制备成功。
(2)静态吸附实验中,研究了改性地瓜皮和未改性地瓜皮对刚果红的静态吸附效果。探究了pH值、吸附剂用量、染料浓度和反应时间等吸附条件对吸附的影响,结果表明,改性地瓜皮在吸附剂浓度为1 g/L,pH值为5,吸附时间为24 h时,对100 mg/L刚果红溶液的吸附率可达到90%以上,而未改性地瓜皮在相同条件下的吸附率只有67%左右。改性地瓜皮对染料的吸附效果明显优于未改性地瓜皮。
