铁锌合金在离子液体中的电沉积行为及其在Hank’s溶液中腐蚀性能研究*
2022-11-01崔祥忠王伟强于凤云许雅南
崔祥忠,王伟强,于凤云,许雅南,齐 民
(大连理工大学 材料科学与工程学院,辽宁 大连116024)
0 引 言
Fe及Fe合金因其良好的力学性能和生物相容性,在生物可降解支架研究领域中备受关注[1-5]。Fe作为人体重要的微量元素之一,参与氧转运、酶的合成和电子传递等多种细胞代谢过程。目前,可降解Fe合金支架的临床试验表明,Fe合金支架既保留了传统的永久支架的优良的物理性能,也展现出良好的生物相容性和完全可吸收的特质,在两年的随访数据显示,无死亡、心梗、以及血栓案例[6]。然而,相较于其他可降解金属支架,缓慢的腐蚀降解速率仍然是铁基生物降解材料在实际应用中面临的主要问题[7-9]。因此改善纯铁基体的腐蚀速率是非常重要的,而合金化也是首选的手段,因为相比于表面改性来说,合金化后的材料组织和性能更加均匀。
目前关于Fe合金化方面的研究很多,如添加合金元素Mn[10],Ga[11],N[12],W[13],这些合金元素改变Fe的固有标准电位和微观结构(如多相体系、晶粒尺寸),引起了耐蚀性的变化。Zn是人体中含量第二高的金属微量元素,仅次于Fe。它是酶最重要的组成部分,参与大多数细胞代谢[14]。Zn的标准电位为-0.76 V,低于Fe (-0.44 V)[15],以Zn作为第二组元合金化Fe理论上可以降低Fe基体的腐蚀电位,从而提升Fe合金腐蚀降解速率。但是目前关于Fe-Zn合金的研究较少,这可能是由于纯Fe的熔点为1 538 ℃,纯Zn的沸点为907 ℃,用传统的冶金方法很难制备Fe-Zn合金。而电沉积过程是常温、原子级的互竞共沉积过程,通过调整电源参数和电解液的成分,可以在室温下获得成分可控的二元甚至三元合金,而无需考虑各组分之间的熔沸点差。
目前已经有研究者在水溶液体系中通过电沉积制备出了Fe-Zn二元合金[16-19],但是水的电化学窗口较窄,以水作为溶剂在电沉积过程中存在着阴极析氢反应明显的问题[20-21],因此以离子液体作为溶剂进行电沉积成为了新的研究方向。在离子液体中,低共熔溶剂(deep eutectic solvents,DESs)因具有电化学窗口宽、导电性良好和易制备[22-25]等诸多优点备受关注。DESs通常是由一定比例的氢键受体和供体通过氢键结合而成的两组份或三组份的低共熔混合物,其凝固点远低于各个组份的熔点[26-27]。氯化胆碱-尿素(ChCl-Urea)是目前应用最普遍且研究最充分的DESs体系之一,通常ChCl和Urea的摩尔比为1∶2[28]。已经有研究者在这种DES体系研究了电沉积Fe及Fe合金[29-31]或Zn及Zn合金[32-34],在低共熔溶剂中电沉积Fe-Zn合金有望为Fe-Zn合金的制备提供一条新的可行途径。
本文在氯化胆碱-尿素低共熔溶剂(ChCl-Urea DES)中电沉积制备出Fe-Zn二元合金,探索了在ChCl-Urea DES中Fe、Zn离子的电化学还原行为,合金的成核生长行为。分析了沉积电位对Fe-Zn合金的微观形貌和元素含量以及相组成的影响,并且对不同组织和成分的Fe-Zn合金在Hank’s溶液中的腐蚀性能进行了研究。
1 实 验
1.1 电解质制备
氯化胆碱(ChCl,≥98.0%)、尿素(Urea,≥99.0%)、氯化锌(ZnCl2,≥98.0%)购自麦克林化学试剂有限公司,氯化亚铁(FeCl2·4H2O,≥99.0%)购自国药集团化学试剂有限公司。所用试剂使用前在80 ℃真空条件下干燥24 h,实验用水皆为去离子水。将ChCl和Urea按照摩尔比1:2的比例混合,在80 ℃油浴锅中磁力搅拌直至得到无色透明的ChCl-Urea DES,然后将一定质量的FeCl2·4H2O和ZnCl2加到ChCl-Urea DES中,继续80 ℃搅拌24 h直至形成深红棕色电解液,即得到ChCl-Urea-FeCl2-ZnCl2DES。
1.2 电化学测试及电沉积
使用电化学工作站(M204,Metrohm Autolab,Netherlands)对电解液进行循环伏安(CV)和计时电流(CA)测试,对ChCl-Urea DES中Fe-Zn合金的电沉积电化学行为和成核行为进行研究。电化学测试及电沉积过程均采用三电极体系。电化学测试过程中玻碳电极(GC)(直径3.00 mm)为工作电极,铂片电极(Pt)(1 cm×1 cm)为对电极,银/氯化银电极(Ag/AgCl)为参比电极。CV的测试区间为-1.8~1 V,扫描速率为50 mV/s。CA的测试电位为-1.15,-1.25和-1.35 V;电沉积过程中紫铜片(1 cm×1 cm)为工作电极,纯铁片1×1 cm为对电极,Ag/AgCl电极为参比电极。工作电极与对电极在使用前用不同型号的砂纸和抛光膏打磨并抛光至光滑镜面,所有电极在使用前使用丙酮、无水乙醇和去离子水充分清洁并干燥。电沉积过程的沉积电位根据CV曲线分别选取为-1.15,-1.25和-1.35 V,沉积时间为30 min。电化学测试及电沉积都在80 ℃条件下进行。本文所提到的纯铁(≥99.99%)和紫铜(≥99.9%)均为厚度为0.5 mm的冷轧薄板,购自中国封腾金属制品有限公司。
1.3 铁锌合金镀层表征
使用场发射扫描电子显微镜(SEM,Supra55,Zeiss,Germany)对沉积层的表面形貌进行观察。使用场发射电子探针(EPMA,JXA-8530F PLUS,Jeol,Japan)检测了沉积层的元素组成,加速电压为15 kV,在样品表面的不同位置上选取5个点进行测试后取平均值。通过X射线衍射仪(XRD,Empyrean,PANalytical B·V,Netherlands)在40 kV下使用Cu-Kα辐照(λ=0.154056 nm),步长为0.04°,扫描范围为20°~100°(2θ)确定沉积物的相结构。使用Tafel极化曲线测试方法对合金沉积层在室温下的腐蚀性能进行分析(选择冷轧纯铁作为对照),所用腐蚀介质为Hank’s溶液,Fe-Zn合金为阴极,Pt为阳极,饱和甘汞(SCE)电极为参比电极,样品测试面积为1 cm2,测试前将样品浸入Hank’s溶液中静置30 min。
2 结果与分析
2.1 铁锌离子在低共熔溶剂中的还原行为
ChCl-Urea DES电解液中FeCl2·4H2O和ZnCl2的CV曲线如图1(a)所示。ChCl-Urea DES中含0.1 mol/L FeCl2·4H2O的CV曲线在负扫至-1.30 V时和正扫至0.38 V时,各出现一个还原峰和一个氧化峰,这分别对应着铁的还原(Fe2++2e-→Fe)和氧化(Fe-2e-→Fe2+)过程。ChCl-Urea DES中含0.1 mol/L ZnCl2的CV曲线在负扫至-1.60 V时和正扫至0.85 V时,各出现一个还原峰和一个氧化峰,这分别对应着锌的还原(Zn2++2e-→Zn)和氧化(Zn-2e-→Zn2+)过程。在整个扫描过程中,可以观察到两条CV曲线都只有一对氧化还原峰,可以说明Fe(Ⅱ)和Zn(Ⅱ)在ChCl-Urea DES中为一步还原及氧化。
ChCl-Urea DES 电解液中含0.1 mol/L FeCl2·4H2O和0.05 mol/L ZnCl2的CV曲线如图1b所示。负扫过程中可以在-1.50和-1.30 V处观察到两个明显的还原峰Ⅰ和Ⅱ,分别对应Zn(Ⅱ)和Fe(Ⅱ)在DESs中的还原电位。在正扫过程中在-0.40 V处出现一个氧化峰位a,氧化峰a则表明在两种金属离子的还原过程中出现了二者共析的产物,即Fe-Zn合金。
2.2 铁锌离子在低共熔溶剂中的形核行为
图2显示了不同电位下的电流的瞬变过程。每条CA曲线的初始状态的特征是电流的急剧下降,这与电极上第一个Fe/Zn核的形成相对应。其后的电流增加是由于Fe/Zn核的形成和生长,直到出现峰值。电流的上升过程中的最大值为im,im在时间轴上的位置tm取决于电势阶跃的大小。最后,根据科特雷尔定律,电流收敛到平面电极线性扩散所对应的极限电流。随着电势的增加,im增大,而tm缩短。这可以解释为由于核密度增加,扩散层重叠所需的时间减少。
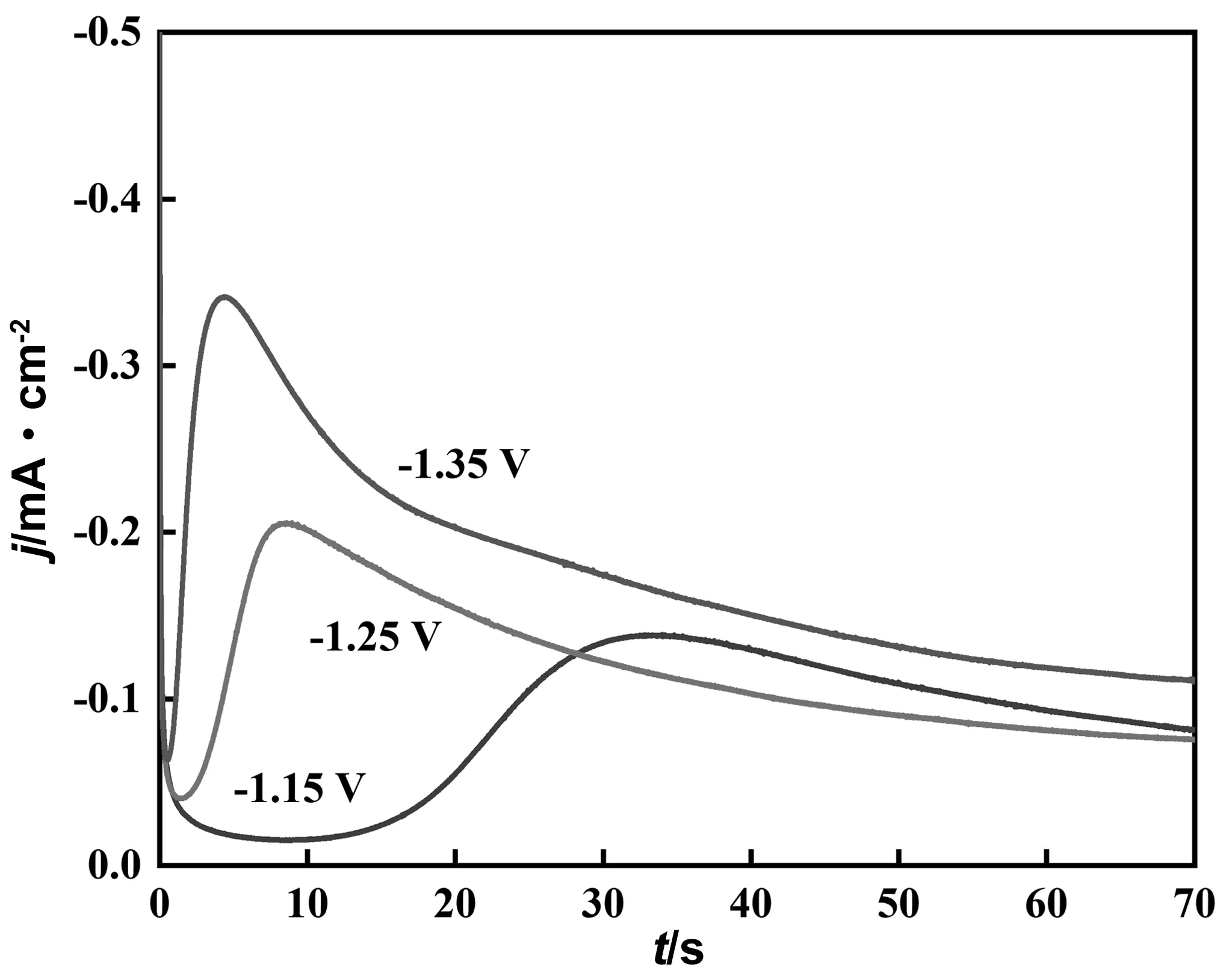
图2 不同沉积电位条件下电流随时间变化曲线Fig.2 Curves of current vs. time under different deposition potentials
Scharifker和Hills提出了一种方便的方法来识别成核机理[35]。描述电流-时间瞬态最常用的模型是三维瞬时形核模型(式(1))和三维渐进形核模型(式(2))。其中瞬时形核所有的Fe/Zn核在电解开始时同时产生,渐进成核则是在整个电解过程中不断产生新的晶体。
瞬时:(i/im)2=1.9542(t/tm)-1{1-exp[-1.2564(t/tm)]}2
(1)
渐进:(i/im)2=1.2254(t/tm)-1{1-exp[-2.3367(t/tm)2]}2
(2)
式中:im、tm分别为电流和时间的峰值坐标。


图3 由图2和式(1),式(2)得到的曲线Fig.3 curves obtained from Fig.2 and equations (1) and (2)
2.3 镀层的元素组成分析
表1显示了用EPMA测定的合金成分组成。随着沉积电位从-1.15 V降低到-1.35 V,Zn的质量百分比从2.3%增加到了7.4%,这是因为电位越负,越接近Zn的还原电位,从而增大了镀层中的Zn含量。沉积镀层中含有微量的O元素,这是由于镀层与空气接触氧化导致的[30]。

表1 EPMA测定的合金元素成分表 (%质量分数)
2.4 镀层的物相分析
图4为不同沉积电位下镀层的XRD衍射图谱。因为经30 min电沉积后,合金镀层厚度约为11 μm,所以,图中Cu所对应的衍射峰应是基底的衍射峰。在-1.15,-1.25,-1.35 V的沉积电位下镀层的衍射峰均为α-Fe的衍射峰,且存在(110)方向的择优取向。不同沉积电位下镀层的衍射峰均为α-Fe的衍射峰,这与图1(b)中含有两种金属盐离子的电解液的CV曲线只有一个明显的氧化峰相符;并随着沉积电位变负,α-Fe的衍射峰强度逐渐降低。根据Fe-Zn平衡相图,在室温下,Zn在Fe中的溶解度<2%[36],但图4中电沉积合金的XRD结果表明,所有Fe-Zn合金均呈现出单一的α-Fe衍射峰,这表明在ChCl-Urea DES中电沉积得到的Fe-Zn合金形成了过饱和固溶体。
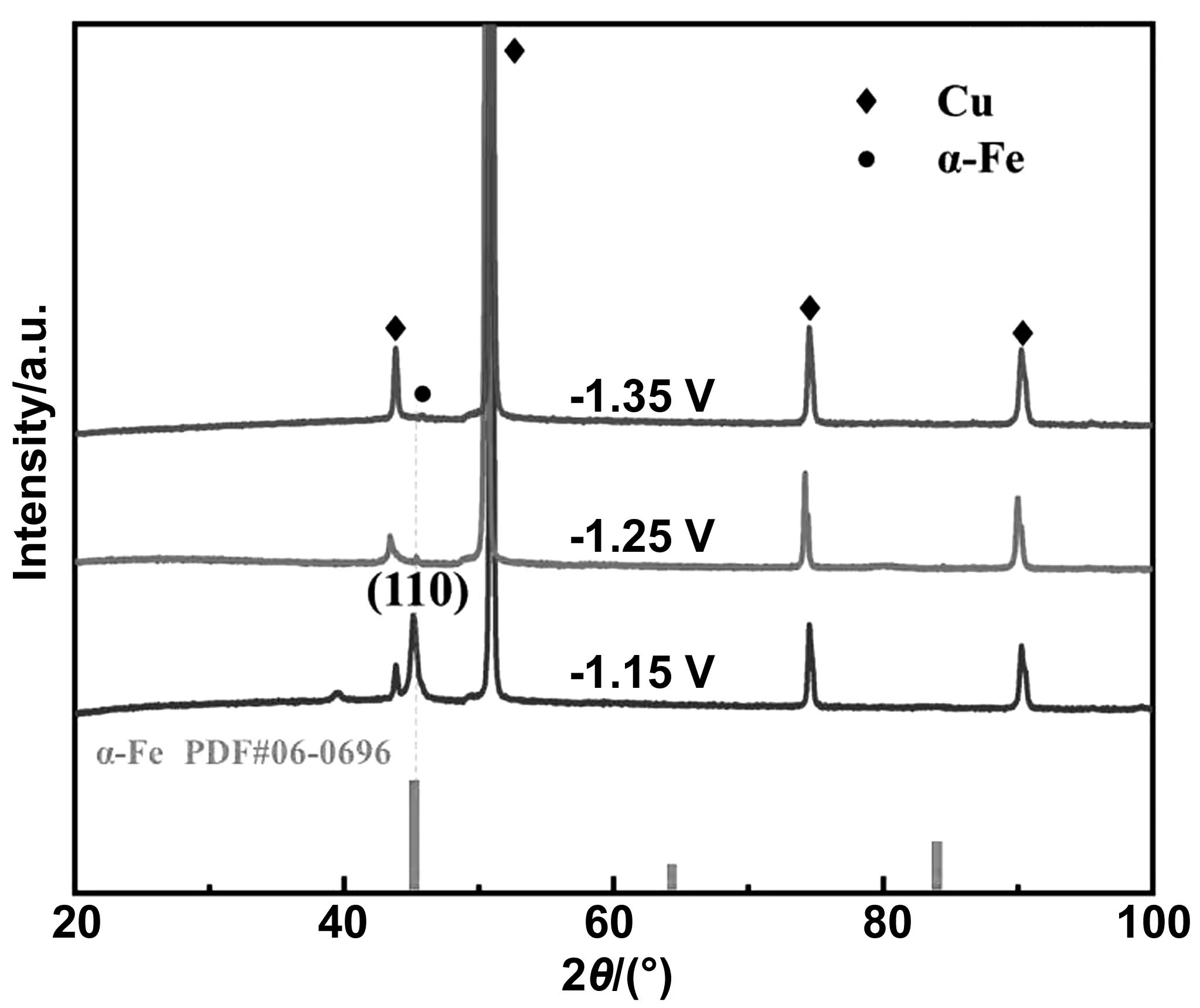
图4 在不同电位下沉积的Fe-Zn合金的XRD图谱Fig.4 XRD patterns of the Fe-Zn alloys deposited at different potentials
2.5 镀层的微观形貌分析
图5为在-1.15,-1.25,-1.35 V电位下,在ChCl-Urea-0.1 mol/L FeCl2·4H2O-0.05 mol/L ZnCl2镀液中沉积30 min的Fe-Zn合金的表面形貌。在不同的电位下,Fe-Zn合金镀层表面致密,无裂纹。高电位下晶粒呈分散的半球状生长,表面突起较少,随着沉积电位的负移,表面突起增多,合金晶粒逐渐呈不规则团簇状生长。这是由于合金的形核方式为三维渐进成核,合金在生长过程中会不断产生新的晶核,随着沉积电位负移,合金的形核能变大,形核率增加,所以沉积电位负移时合金表面的突起更多并聚集在一起呈不规则团簇状。同时结合合金的成分和物相结果可知,沉积电位越负,更多的Zn原子进入到铁的晶格中形成了过饱和固溶体,使Fe基体晶格畸变程度增大,这也为结晶提供了更多的形核位点,最终表面形成团簇状生长形态,如图5(c)所示。随着合金晶粒的细化和晶格畸变程度的增大,合金的择优取向减弱,在图4 XRD中也对应更低的衍射强度。

图5 在不同沉积电位下制备的Fe-Zn合金的表面形貌:(a)-1.15 V; (b)-1.25 V; (c)-1.35 VFig.5 Surface morphology of the Fe-Zn alloys deposited at different potentials: (a)-1.15 V; (b)-1.25 V; (c)-1.35 V
2.6 镀层的腐蚀性能分析
图6为纯铁与不同Zn含量的Fe-Zn合金的Tafel极化曲线。从曲线中测得的腐蚀电位Ecorr和腐蚀电流密度Jcorr的值列于表2。表2中还列出了腐蚀速率CR,该值由方程(3)[37]计算得出,式中EW为当量(相当于相对原子质量除以通常价态;铁为27.92 g),ρ是材料密度(铁为7.87 g/cm3):
(3)
金属在同一腐蚀介质中的腐蚀电流密度越大即腐蚀速率越快。表2中Zn含量为2.3%和4.3%的Fe-Zn合金的Jcorr均大于纯Fe,这表明Zn含量为2.3%和4.3%的Fe-Zn合金的腐蚀降解速率相较于纯Fe有所提升,其中Zn含量为4.3%的Fe-Zn合金的Jcorr最大,为5.70 μA/cm2,是纯Fe的2.7倍。Zn含量为7.4%的Fe-Zn合金的Jcorr小于Zn含量为2.3%和4.3%的Fe-Zn合金,这表明Fe-Zn合金的腐蚀速率会随着Zn含量的增加先增加后降低。这一结论与许等[19]的研究结论相符,许等的研究表明Fe-Zn合金的腐蚀产物中含有Zn(OH)2,Zn的含量越高腐蚀产物Zn(OH)2越多。Kasai等[38]的研究表明,Zn(OH)2的积累形成了细小的结构,起到了良好的防腐作用,这或许解释了为什么随Zn含量从4.3%增加到7.4%,合金的Jcorr降低。

图6 不同电位下制备的Fe-Zn合金的动电位极化曲线Fig.6 Potentiodynamic polarization curves of Fe-Zn alloys deposited at different potentials

表2 根据极化曲线和计算的腐蚀速率(CR)得到电化学数据
3 结 论
(1)以ChCl-Urea DES为基础液,铜作为阴极基体,Fe(Ⅱ)和Zn(Ⅱ)可以在-1.15~-1.35 V沉积电位下共沉积得到Fe-Zn合金。
(2)Fe-Zn合金镀层中含Fe,Zn,O 3种元素,其中O为镀层与空气中的O2反应掺入。Zn元素质量比例随着沉积电位的负移(-1.15~-1.35 V)而提升(2.3%~7.4%)。
(3)在XRD衍射图中不同Zn含量的Fe-Zn合金的衍射峰均显示为单相的α-Fe,说明均生成了过饱和固溶体,且具有沿(110)晶面生长的择优取向。
(4)在ChCl-Urea DES中沉积得到的Fe-Zn合金膜的表面致密,无裂纹。低电势下呈分散的半球状生长。随着沉积电位的负移,合金晶粒呈不规则团簇状生长。
(5) Fe-Zn合金的腐蚀速率较纯Fe相比更快,且合金的腐蚀速率随着合金中Zn含量的增加呈现先升高后降低的趋势。
