不同起始浓度肠内营养液在胃癌根治术后肠内营养中的应用效果
2022-10-21吕小芹王佳佳金玉涵张玉花安冉冉滨州医学院附属医院山东滨州256600
吕小芹,王佳佳,金玉涵,张玉花,安冉冉 (滨州医学院附属医院,山东 滨州 256600)
中国国家最新癌症中心数据显示胃癌(GC)在癌症发病率居恶性肿瘤第二位,死亡率居第三位[1]。我国胃癌的发病率居癌症发病率的第二位[2]。胃癌根治术是治疗胃癌、延续患者生命的主要手段。胃癌术后患者受手术及胃肠减压的影响,往往不能经口摄入充足的目标需要量。最近美国肠外营养和肠内营养(EN)协会指导推荐术后EN24 h内可行。早期肠内营养(EEN)的生理益处已得到充分证明,可以维持胃肠道的结构完整性、降低肠道通透性和增加肠系膜血流量[3],从而降低患者感染发生率、术后并发症、死亡率、住院时间和费用[4]。在肠道在无禁忌证的患者中EEN是首选[5]。但EN喂养过程中常常出现腹胀、腹泻等胃肠道不良反应,EN喂养难以顺利进行,导致喂养不足。我国胃癌围术期营养治疗中国专家共识,提倡胃癌术后EEN应从低剂量、低浓度开始[6]。但其具体浓度无明确规定,本研究旨在探讨不同起始浓度EN液在胃癌根治术后早期肠内营养中的应用效果。
1 对象与方法
1.1研究对象:选取本院2015年1月~2020年12月行胃癌根治术的患者为研究对象,纳入标准:①符合胃癌诊断标准。②患者生存时间>1个月。③择期行胃癌根治术,术后早期应用肠内营养。④年龄≥18岁。⑤患者知情同意,并签署知情同意书。排除标准:①中途停止EN者。②存在肠道功能障碍。③合并转移、肠道手术患者。④住院期间自动出院、死亡患者。根据纳入与排除标准,其中早期肠内营养浓度为5%的患者107例、10%的患者45例、20%的患者30例,根据研究配比原则,最终选取5%浓度组、10%浓度组、20%浓度组各30例。两组患者一般资料比较,差异无统计学意义(P均>0.05)。见表1。本研究经过本院医学伦理委员会同意。
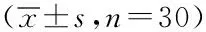
表1 两组患者一般资料比较
1.2EN喂养方法
1.2.1输注浓度:两组患者术中留置鼻肠管(16F)或空肠营养管(16F),营养管管路末端均位于位置空肠上端。患者自术后第1天上午8:00开始EN,EN制剂采用整蛋白型EN制剂(能全素),生产厂家:纽迪希亚制药(无锡)有限公司,每100 g能量462 kCal,术后第1天根据用电子秤称取12.5 g(能量57.75 kCal)营养粉剂,5%浓度组使用带刻度的量杯取净化水,水温40℃,将营养粉剂溶于净化水中,搅拌均匀,配置成浓度5%的能全素营养液。10%浓度组取净化水500 ml,配置成浓度为10%的能全素营养液。20%浓度组采用同等方法,配置成浓度为20%的能全素营养液。第1天EN液输注结束后,评估患者的反应,若患者无腹胀[7]、腹泻、恶心[8]呕吐等不适,当天可适当增加营养量。以后每天将输注浓度在原基础上增加5%,营养制剂输注克数采用逐步增加,即:第2天营养制剂量50 g(能量231 kCal),第3天营养制剂量目标量100 g(能量462 kCal),第4天营养制剂量200 g(924 kCal),直至患者达到50%目标需要量。若患者在EN过程中出现腹胀、腹泻、恶心等不耐受情况,则第2天仍采取前1 d的输注速度及输注浓度,若患者出现恶心、腹胀、呕吐等情况,则降低患者输注浓度,直至患者不再出现胃肠道不良反应。若患者出现严重并发症,则终止EN。
1.2.2输注速度:输注管路采用EN泵入管均采用营养泵持续定速泵入,起始速度为20~30 ml/h,若患者使用过程中出现腹胀、恶心、呕吐等不耐受情况,则督促患者下床活动,若下床活动后腹胀、恶心不缓解,则调节泵速,以降低患者不适反应。若患者当天肠内营养输注结束后无不适,则第2天输注速度提高10~20 ml/h,若患者存在恶心、呕吐、腹胀等胃肠道不良反应,输注速度为前一天速度或降低输注速度10~20 ml/h,直至患者无不适。输注过程中均使用可移动式输液悬挂支架,督促患者每天至少4次下床活动,每次活动量不少于20 min。
1.3评价指标
1.3.1EN提供机体所需50%目标能量的过渡时间:计算患者自EN输注开始至EN提供机体所需50%目标能量的时间。根据体重设置50%目标需要量。50%EN目标热量[6]=50%×20 kCal×体重。
1.3.2患者每天EN输注克数、能量及完成情况:第二天上午由责任护士评估患者昨天EN实际输注克数及完成情况。若患者第二天8∶00之前按照原定计划完成EN。则定义为完成计划目标量。
1.3.3观察患者肠道功能恢复情况:观察患者首次排气、排便时间,起始时间为患者术后返回病房时间。
1.3.4患者肠内营养输注期间耐受情况:观察两组患者在EN过程中每天腹胀、腹痛、恶心、呕吐的情况。
1.4统计学方法:采用SPSS23.0统计学软件进行χ2检验,不同浓度间比较采用方差分析。
2 结果
2.1EN提供机体所需50%目标能量的过渡时间:5%浓度组患者达到50%目标能量所需时间为(6.40±1.88)d,10%浓度组患者达到50%目标能量所需时间为(7.7±1.53)d,20%浓度组达到50%目标能量所需时间为(8.5±2.43)d,三组比较,差异有统计学意义(F=8.548,P=0.000)。
2.2不同起始浓度患者EN输注克数及完成情况:不同浓度EN患者术后第1天EN输注速度及输注时间比较,差异有统计学意义(F=13.239,P=0.00;F=30.507,P=0.00)。患者术后第2天EN输注克数及速度比较,差异有统计学意义(F=12.377,P=0.00;F=14.481,P=0.00)。见表2。
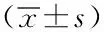
表2 不同起始浓度患者EN每日实际输注情况
2.3不同起始浓度患者肠道功能恢复情况:不同起始浓度患者观察患者首次排气、排便时间比较,差异无统计学意义(F=1.355,P=0.265;F=0.387,P=0.680)。
2.4患者肠内营养输注期间耐受情况:不同起始浓度患者营养过程中第1天、第2天胃肠道不良反应比较,差异有统计学意义(F=12.073,P=0.015;F=8.353,P=0.015)。不同起始浓度患者营养过程中第3天、第4天、第5天胃肠道不良反应比较,差异无统计学意义(P均>0.05)。见表4。
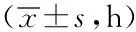
表3 不同起始浓度患者肠道功能恢复情况
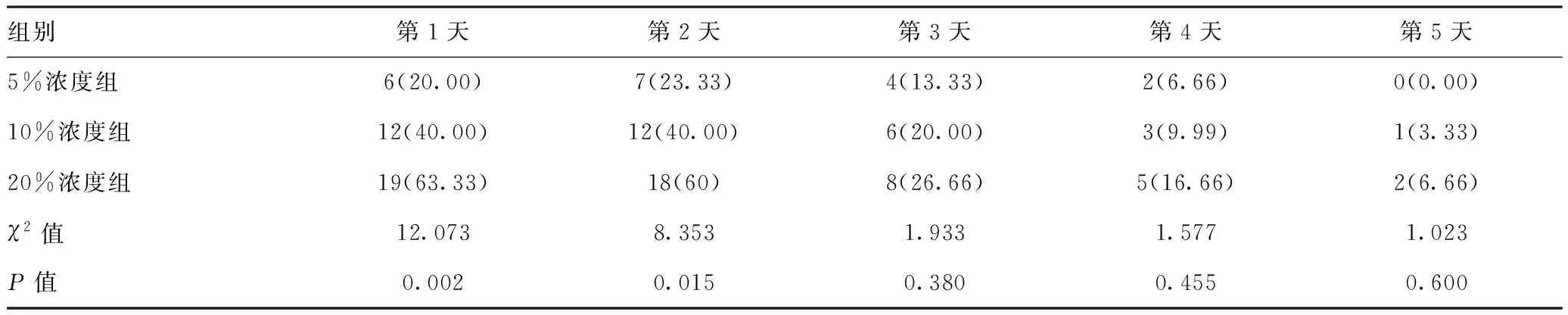
表4 不同起始浓度患者EN输注期间耐受情况[n(%),n=30]
3 讨论
最新研究调查显示,我国胃癌发病率呈快速增长状态,其5年生存率却远低于发达国家[9]。临床研究数据显示,胃癌患者往往合并营养不良[10]。肠外营养与EN为主要的营养补充方式,但肠外营养对血管造成损害,增加患者感染的发生率[11],且有增加胆汁淤积症的风险[12]。EN相对肠外营养具有价格低廉,并能够降低患者术后死亡率,缩短患者住院时间[13]的优点。欧洲肠外营养与EN协会关于外科临床营养的指导原则,建议不能开始早期口服营养,口腔摄入不足超过7 d[14]的患者,在术后24 h内进行EN治疗。以往研究报告EEN在改善胃肠手术患者的临床疗效方面优于全肠外营养(TPN)[15]。欧洲指南中指出,胃部分切除或全胃切除的患者术后经口摄入安全、可行,对于不能早期经口进食、经口摄入不足(<50%)且持续时间>7 d 的患者应尽早开始管饲(24 h内)[6]。EN是功能性胃肠道营养支持的首选方法[16]。尽管加速康复外科ERAS理念患者早期经口进食,但由于手术麻醉、胃肠道不良反应等多种原因,患者往往营养摄入不足,影响患者早期康复,因此EN。
最新专家共识建议,胃癌术后患者允许相对低热量供能15~25 kCal/(kg·d),有利于降低感染及相关并发症的发生率。指南建议对耐受良好的患者,喂养量应在72 h内达到目标需要量,以优化营养治疗的疗效。对胃肠道耐受性较差的患者,喂养量可7 d内逐渐达到目标需要量。但对于EN的目标能量,不建议用EN覆盖全部能量目标。研究中采用20 kCal/(kg·d)的低热量目标值,以50%作为目标量符合低热量标准。本研究发现,对耐受良好的患者,喂养量可在72 h内达到50%目标需要量。对胃肠道耐受性较差的患者,喂养量可在7~10 d内逐渐达到50%目标需要量。患者达到50%EN目标需要量,维持1~3 d后,其EN量呈下降趋势,其主要原因在与患者术后3 d胃肠减压已解除,自主进食量逐渐增加,患者能量的摄入由管饲逐渐转化为经口进食。经口进食成为机体营养的主要供应来源,EN转换为次要营养供应方式。
EN能有效改善胃肠功能,但可增加术后腹胀、腹泻等并发症[17]。术后腹胀的发生主要与手术因素、麻醉因素等多种原因导致有关。首先,手术对胃肠道或支配胃肠神经的刺激,导致患者神经内分泌被激活,反射性引起胃肠蠕动抑制,加剧了患者胃肠道功能障碍[18]。麻醉诱导期患者吞咽大量空气;术中使用的麻醉药品及术后使用镇痛泵等,亦可引起腹胀。此外由于患者术后水、电解质平衡紊乱,特别是低钾血症,使胃肠蠕动减弱。且患者胃癌根治术后胃动素、胃泌素及饥饿素均显著下降,胃动素可加速胃肠道的排空;胃泌素可刺激胃酸、胃蛋白酶分泌,促进胃肠道运动及胃黏膜的生长;饥饿素能够刺激患者食欲、调节能量代谢[19],胃癌根治术后,患者重建消化道,机体不能及时适应重建的消化道,患者早期胃肠道功能难以有效恢复,致使患者早期胃肠道出现恶心、腹胀等不良反应。而腹胀、恶心是延迟EN进度的主要原因,而腹泻是终止EN的主要原因[20-21]。因此胃癌根治术患者EEN应从低浓度、低剂量开始。本研究设置5%浓度组、10%浓度组、20%浓度组低浓度剂量。在EEN起始阶段,指南中建议缓慢启动EN(10~20 ml/h),一旦以前的症状得到缓解,没有新的症状出现,就慢慢增加EN。本研究中以20~30 ml/h为EN的起始速度,根据患者的反应及时调整速度,保证EN顺利输注的同时减轻患者不适。本研究发现,腹胀是影响EN增加量的主要影响因素。在患者术后EEN早期,腹胀的发生率高达40%,采取积极应对措施后,腹胀症状能够缓解,腹泻是关系到EN能否继续实施的关键因素,其主要原因可能与患者个人体质及对营养液不耐受有关。通过浓度和速度的综合调整,研究发现术后1~2 d患者5%浓度组胃肠道不良反应最少,患者早期胃肠道负担减轻,胃肠道吸收利用率增加,且能全素中含有丰富的维生素以及膳食纤维,可以促进胃肠道的蠕动,有助于患者胃肠道的早期恢复。5%浓度营养液渗透压低于20%浓度营养液,对胃肠道的刺激影响小。而20%浓度营养液患者腹胀最为明显。但研究中患者术后首次排气时间和排便时间没有差异,可能与患者实施多种促进胃肠道活动的措施有关。患者术后第3~5天,由于手术及麻醉影响因素逐渐减少,患者自身能力修复,早期排气与排便,胃肠道功能已恢复,其并发症无差异。
综上所述,在胃癌根治术后EEN支持过渡阶段,建议以5%EN液为起始速度,每天将输注浓度在原基础上增加5%,以首次喂养量为10~15 g,输注速度20~30 ml/h为宜。在输注过程中密切观察患者恶心、呕吐、腹胀、腹泻等并发症,并根据患者个体化情况及时调整。但本研究局限于患者的目标需要量及并发症,其不同浓度患者的生化指标有待于进一步探讨,从而为胃癌术后患者提供更加可靠的依据。
