磁控溅射法制备医用钛表面含银抗菌涂层的研究进展
2022-10-20常培亮吴明超
游 立,常培亮,冯 能,吴明超,黄 雷,喻 成
应用研究
磁控溅射法制备医用钛表面含银抗菌涂层的研究进展
游 立,常培亮,冯 能,吴明超,黄 雷,喻 成
(武汉船用电力推进装置研究所,武汉 430064)
本文分析探讨了三种含银复合抗菌涂层的相关科研成果,先后对含银抗菌涂层的抗菌机理、不同体系的抗菌涂层基材与纳米银微粒制得的复合涂层的抗菌性能、成骨性能及相关问题进行分析探讨,为高杀菌活性、高品质含银复合抗菌涂层的研制开发提供更好的理论指导。
磁控溅射 纳米银 医用钛表面 抗菌涂层 成骨性能
0 引言
采用磁控溅射技术制得含银复合抗菌涂层在医用钛及及其合金方面具有广泛的用途,含银复合抗菌涂层大体上可分为三大类:第一类是银/陶瓷基复合抗菌涂层,常见的有Ag-TiO2、TaN-Ag等;第二类是银/聚合物基复合抗菌涂层,聚合物材料主要有聚四氟乙烯等;第三类是银与其他金属元素复合抗菌涂层,例如与Ta、Ti等元素复合来拓展复合涂层的功能。
钛及其合金因具有优良的生物相容性、耐腐蚀性和机械性能,在临床上被广泛用作骨骼、牙齿等人体硬组织的修复与替换材料[1-3]。然而,钛及其合金植入体表面通常会由于细菌粘附、增殖形成生物膜(biofilm)[4-5],对医用抗生素和人体免疫系统具有极强的耐药性,从而有可能导致术后细菌感染和进一步的并发症,造成手术失败[6],甚至导致患者的死亡。因此,实现钛及其合金植入体表面的抗菌性能,不仅有利于预防植入手术术后感染,而且对于有效减轻病患的痛苦、植入体有效使用寿命的延长均具有重要意义。
近年来,涉及在医药用钛及其合金的外表面通过磁控溅射技术制得含银复合抗菌涂层取得长效进步,并被广泛报道[7-8]。纳米银是一种广为人知的光谱抗菌材料,其主要是通过溶解释放出银离子与细菌的酶蛋白接触进行有效杀菌,或通过直接对细菌的细胞壁进行有效破碎实现杀菌,当前已经在医疗器械、净化水质处理、无菌棉纺织品、美容护肤、无菌包装等民生医疗领域取得广泛地应用[9-11]。与此同时,含银复合抗菌涂层在医药钛植入体的应用前景十分明朗,相关研究结果表明,植入体在生物体内溶解释放出合适浓度纳米银微粒可促进生物体的成骨细胞增殖,大大增强植入体在生物体内的成骨活性。
当含银复合抗菌涂层在医用钛及其合金的外表面应用技术比较成熟,不仅具备植入体材料结构性高强度的特点,同时具备功能涂层的杀菌活性及促进成骨生长的功效,因而备受医疗领域地广泛关注。其制备方法大体上包括有化学水热还原法、旋转喷涂法、化学气相沉积法、阳极氧化法、磁控溅射法等技术。
1 含银抗菌涂层抗菌机理
金属钛及其合金作为植入体往往会存在术后细菌感染等后遗症,植入体手术失败的罪魁祸首主要由于细菌及其他生物交容易粘附于金属钛及其合金外表面形成生物膜,容易对植入体进行感染侵蚀。据统计,在关节置换手术病例中,大约有1%会发生假肢感染,而在牙科领域,种植体周围炎的发生概率在前五年就高达14.4%,因此,病患需要进行长期的抗生素治疗(可能持续数年),而植入体手术后由于生物膜和有机抗生素产生的耐药性带来的细菌感染等并发症造成手术失败,重新移植植入体产生高昂的费用同时会给病人带来身理和心理上的痛苦。含银抗菌涂层作为无机抗菌材料的重要代表,凭借其广谱杀菌活性、良好的生物相容性、低毒性及不易产生耐药性等独特优势而广泛受到关注。
关于含银抗菌涂层的杀菌机理在学术界还没有形成权威的统一说法,但是相关人员普遍认为含银抗菌涂层的纳米银微粒的杀菌性能主要与两方面的因素有重要影响:银离子释放的数量/程度以及银纳米颗粒的活性(取决于纳米银颗粒的大小和形状)。这两大因素与控制细菌的增殖/生长机制直接相关,因为进入细菌的银离子可以通过与某些组分(如酶)中的主要官能团结合而与细胞中的巯基(-SH)相互作用,从而阻止细菌分裂并破坏细胞膜[12];而尺寸较小的银纳米颗粒能够直接与细胞接触,破坏细胞膜,从而杀灭细菌。当前相关领域研究人员大多数采用磁控溅射技术将纳米银微粒与有机聚合物体系或陶瓷基体进行复合,并于医用钛及其合金的外表面制得含银复合抗菌涂层。基体材料结构的高强度和耐磨性使得复合涂层不仅具有良好的机械耐磨性能,而且功能层中溶解释放的纳米银会对机体的局部产生抗菌消炎的效果。
2 磁控溅射制备含银复合抗菌涂层
作为典型的物理气相沉积技术的鲜明代表磁控溅射技术,其具有操作简单易控、沉积速率高、成膜致密均匀、涂层与基材结合力强、适合大批量规模化生产以及工艺绿色环保等优点,更由于能够方便的调节纳米银在基相中的尺寸大小和空间分布,被广泛应用于制备不同尺寸、不同功能应用领域的含银复合抗菌涂层。磁控溅射技术的主要原理是利用外界电场的作用,将其施加在在真空室的两个电极之间,注入真空室的工作气体(一般是氩气),可通过对工作气体的电离,使得电离后的气体离子可通过对靶材(阴极)上的原子或分子在衬底材料商进行喷射沉积(相关的磁控溅射技术的原理及过程如图1所示)[13]。电场可以通过直流模式、射频模式或者脉冲模式进行,取决于靶材的电导率和成膜质量要求。
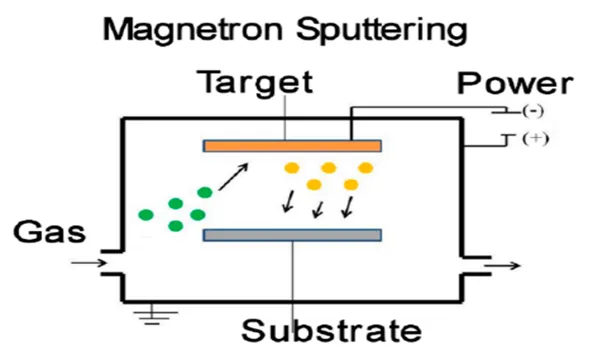
图1 磁控溅射过程示意图[13]
由于含银抗菌涂层中纳米银微粒普遍存在粒径小、比表面积大、活性高等特点,将其通过磁控溅射技术负载于不同的基体材料(有机聚合物、陶瓷)中会存在不同的分布情况,例如在银/陶瓷基复合涂层中,会出现较严重的纳米银表面偏析现象,而在聚合物基中则不会。因此,对不同基体材料中含银复合抗菌涂层的性能研究及相关差异性等问题的分析显得十分重要。
2.1 银/陶瓷基复合抗菌涂层
二氧化钛(TiO2)是最早被用来磁控溅射制备含银复合抗菌涂层的陶瓷基相材料之一。Ag-TiO2复合涂层可以采用Ag靶和TiO2陶瓷靶在氩气氛围制备,也可以利用反应磁控溅射技术,采用Ag靶和Ti金属靶进行共溅射得到。Uhm等首先通过等离子体电解质氧化法在医用钛金属表面生长TiO2纳米管阵列,随后在二氧化钛(TiO2)纳米管阵列上采用磁控溅射技术将纳米银微粒沉积在改基体上,可通过对银靶材的溅射功能的调控来对沉积的纳米银微粒的形貌、大小及含量进行可控性调节,同时相关的抗菌性测试试验结果表明,沉积有纳米银的TiO2纳米管杀菌性能显著优于单纯的TiO2纳米管[14]。F. Faupel等等通过同时采用二氧化钛(TiO2)靶和银靶,通过同时磁控溅射技术成功制得Ag-TiO2三维结构复合涂层,同时通过对含银复合抗菌涂层中银离子的溶解释放速率进行表征来判定其抗菌性能[15]。该工作最大的亮点是系统研究了Ag-TiO2复合涂层抗菌的银离子浓度“治疗窗口”,即通过控制涂层中纳米银的颗粒分布与含量控制银离子释放速率,使其既具有抗菌性能,又不对人体正常细胞造成损害。Doo-Hoon Song等采用适宜于工业大批量大面积制备的反应磁控溅射技术,利用金属Ti靶和Ag靶在医用钛表面共溅射沉积了Ag-TiO2复合涂层并表征其抗菌性能,其测试的银离子释放量均超过抗菌最低要求浓度0.1 ppb,显示出涂层对大肠杆菌等具有优良的抗菌性能[16]。然而,在溅射沉积制备Ag-TiO2复合涂层中,由于沉积的纳米银微粒与二氧化钛(TiO2)之间存在键合作用不明显,反应活性较低等问题,使得纳米银微粒在基材表面表现出较强的流动性,磁控溅射沉积一旦停止,基材表面的纳米银微粒会自主发生团聚,进而表现出明显的表面偏析现象[17](如图2所示),导致银颗粒在TiO2基相中的分布不均匀不可控,大量大尺寸银颗粒富集的涂层表面无序释放银离子,可能对人体正常细胞造成潜在危害。严重制约了Ag-TiO2复合涂层的进一步应用。类似的磁控溅射技术过程中也常会出现在银陶瓷基复合涂层中,纳米银微粒表现出表面偏析或富集的现象,例如(氮化钽)TaN-Ag复合涂层[18],Ag-Hap(羟基磷灰石)[19]复合涂层和(二氧化锆)ZrO2-Ag复合涂层等,虽然这些复合涂层都表现出优良的抗菌性能,但纳米银表面偏析导致的银离子无序释放的风险仍然存在[20]。Xiong等针对反应磁控溅射制备Ag-TiO2复合涂层中如何抑制纳米银表面偏析现象进行了深入、系统的研究。研究发现,在Ag-TiO2复合涂层表面原位沉积一定厚度二氧化钛屏障层(barrier layer)可以有效抑制银的表面偏析现象,而屏障层的致密程度越大,抑制效果越好[21]。

图2 纳米银表面偏析现象[17]
2.2 银/聚合物基复合抗菌涂层
有机聚合物基体自身表现出优艺的可加工性、耐高温高湿性、耐酸碱腐蚀性等特点,在作为含银抗菌复合涂层基相材料上具有较大优势。付元静采用磁控溅射法,在聚四氟乙烯(PTFE)膜上沉积纳米银膜,随着纳米银溅射时间增加,银离子在抗菌过程释放总量增多,在杀菌活性测试试验过程中可明显看出其对金黄色葡萄球菌、大肠杆菌等均表现出抗菌性能随着银离子释放总量的增多而逐渐增强[22]。而M. Irfan等采用磁控溅射法将银与六甲基二硅氧烷(HMDSO)单体进行等离子体聚合,形成的Ag/HMDSO复合涂层对表皮葡萄球菌(一种革兰氏阳性菌)具有显著的抗菌效果[23]。尤其值得关注的是,由于有机聚合物材料良好的延展性、高弹性及可改性加工等特点,纳米银在其中流动性较弱,导致在含银聚合物基复合涂层中基本没有纳米银表面偏析现象被观察到[24],主要归因于纳米银微粒在有机聚合物体系中表现出高分散性,从而在制备医用抗菌涂层方面具有较为广阔的前景。
2.3 银与其他金属元素复合抗菌涂层
近些年来,相关科研人员通过磁控溅射共掺杂技术将金属银与其他金属元素进行共沉积,制得功能型含银复合抗菌涂层的报道越来越多。Wu Jun等通过射频磁控溅射,在医用钛表面制备了Ag、Ta共掺杂的无定型磷酸钙涂层,其所制得的Ag-Ta复合抗菌涂层不仅具有高效的杀菌活性,而且还具有良好的成骨性能。与此同时,研究人员首次发现金属Ta的掺入可有效地抑制降低含银复合抗菌涂层中银离子的溶解释放速率,一定程度上拓宽了含银复合抗菌涂层的应用前景[25]。Thangavel等通过磁控溅射在钛合金表面沉积了镍钛合金与银的复合涂层,形成的复合涂层在摩擦系数、抗腐蚀性能等方面具有优异性能,不仅如此,Ni-Ti/Ag复合涂层对人类皮肤成纤维细胞展现出极高的细胞活性,显示该复合涂层具有良好的成骨活性[26]。杭瑞强等以金属钛为基体,通过磁控溅射技术将金属Ag和Ti实现共掺杂,实现Ti-Ag复合抗菌涂层,其中金属Ag的质量分数在1.2%~21.6%范围内,相关杀菌活性试验结果表明,不同质量分数的银对复合抗菌涂层的形貌表现出明显的差异性,随着银含量的增加,复合涂层的形貌从密集的一维柱状结构慢慢转变为稀疏柱状结构。所制得的金属Ti-Ag复合抗菌涂层在杀菌活性试验中对金黄色葡萄球菌表现出显著的杀菌活性。此外,得益于涂层独特的一维柱状结构,Ti-Ag复合抗菌涂层显示出良好的生物相容性和成骨活性[27]。He Xiaojing等通过磁控溅射在钛金属表面沉积了含有锶(Sr)、Ag两种金属元素的TiO2复合涂层,其中金属锶是能够促进新骨形成的重要元素。该研究发现适量浓度的银离子可进一步促进医用钛植入体的成骨活性,而锶的存在亦可有效减轻过量银离子潜在的对人体的细胞毒性[28]。
3 结论与展望
开发自身具有抗细菌感染能力的医用钛植入体,避免病患因植入感染造成的二次手术痛苦,并改善植入材料成骨性能,是一项极具挑战且意义重大的研究工作。在医用金属钛及其合金外表面通过采用磁控溅射技术将单一或多种功能性金属元素沉积在基体上制得含银复合抗菌涂层是避免植入体手术术后细菌感染的最为有效地技术手段。本文主要深入分析探讨了三种含银复合抗菌涂层的相关科研成果,先后对含银抗菌涂层的抗菌机理、不同体系的抗菌涂层基材与纳米银微粒制得的复合涂层的抗菌性能、成骨性能的相关研究进展进行了综述,总结如下:
1)在银/陶瓷基复合抗菌涂层中,需有效抑制纳米银的表面偏析现象,从而实现对银离子释放速率的精准调控,使其在有效抗菌的同时,又能避免细胞毒性。
2)在银/聚合物基复合抗菌涂层中,应大力开发具有优良生物相容性和细胞活性的新型聚合物基体,促进银/聚合物基复合抗菌涂层的进一步发展。
3)在银与其他金属元素复合抗菌涂层中,当前的研究热点仍然是对含银复合抗菌涂层的成骨性能的拓展研究,在掺杂不同金属元素的同时,应关注涂层表面形貌、结构对成骨细胞黏附、生长的促进作用。
[1] 于振涛, 余森, 张明华, 等. 外科植入物用新型医用钛合金材料设计、开发与应用现状及进展[J]. 中国材料进展, 2010, (12): 35-51.
[2] Geetha M, Singh A K, Asokamani R, et al. Ti based biomaterials, the ultimate choice for orthopedic implants A review[J]. Progress in Materials Science, 2009, 54(3): 397-425.
[3] Javed F, Al-Hezaimi K, Almas K, et al. Is Titanium Sensitivity Associated with Allergic Reactions in Patients with Dental Implants A Systematic Review[J]. Clinical Implant Dentistry and Related Research, 2013, 15(1): 47-52.
[4] Arciola C R, Campoccia D, Speziale P, et al. Biofilm formation in Staphylococcus implant infections. A review of molecular mechanisms and implications for biofilm-resistant materials[J]. Biomaterials, 2012, 33(26): 5967-82.
[5] Zimmerli W. Clinical presentation and treatment of orthopedic implant-associated infection[J]. Journal of Internal Medicine, 2014, 276(2): 111-119.
[6] Harris L G, Richards R G. Staphylococci and implant surfaces: a review[J]. Injury, 2006, 37(2): S3-S14.
[7] Zhang P, Zhang Z, Li W. Antibacterial coating incorporating silver nanoparticles by microarc oxidation and ion implantation[J]. Journal of Nanomaterials, 2013, 2013: 1-8.
[8] Zheng Y, Li J, Liu X, et al. Antimicrobial and osteogenic effect of Ag-implanted titanium with a nanostructured surface[J]. Int J Nanomedicine, 2012, 7: 875-84.
[9] Chernousova S, Epple M. Silver as antibacterial agent: ion nanoparticle, and mental[J]. Angewandte Chemie International Edition, 2013,52(6): 1636-1653.
[10] Marambio-Jones C, Hoek E M V. A review of the antibacterial effects of silver nanomaterials and potential implications for human health and the environment[J]. Journal of Nanoparticle Research, 2010,12(5): 1531-1551.
[11] Morones J R, Elechiguerra J L, et al. The bactericidal effect silver nanoparticles[J]. Nanotechnology, 2005, 16(10):2346-2353.
[12] Lee S H, Jun B H. Silver nanoparticles: synthesis and application for nanomedicine[J]. International Journal of Molecular Sciences, 2019, 20: 865.
[13] Benetti G, Cavaliere E, Banfi F, et al. Antimicrobial nanostructured coatings: a gas phase deposition and magnetron sputtering perspective [J]. Materials, 2020, 13: 784.
[14] Uhm S H, Kwon J S, et al. Long-term antibacterial performance and bioactivity of plasma-engineered Ag-NPs/TiO2nanotubes for bio-implants[J]. Journal of Biomedical Nanotechnology, 2016, 12(10):1890- 1906
[15] Hrkac T, Rohl C, Podschun R, et al. Huge increase of therapeutic window at bioactive silver/titania nanocomposite coating surface compared to solution [J]. Materials Science and Engineering C, 2013, 33: 2367-2375.
[16] Song D H, Uhm S H, Lee S B, et al. Antimicrobial silver-containing titanium oxide nanocomposite coatings by a reactive magnetron sputtering [J]. Thin Solid Films, 2011, 519(20): 7079-7085.
[17] Calderon V S, Cavaleiro A, Carvalho S. Functional properties of ceramic-Ag nanocomposite coatings produced by magnetron sputtering. Progress in Materials Science, 2016, 84: 158-191.
[18] Huang H L, Chang Y Y, Lai M C, et al. Antibacterial TaN-Ag coatings on titanium dental implants [J]. Surface and Coatings Technology, 2010, 205(5): 1636-1641.
[19] Trujillo N A. Antibacterial effects of sputter deposited silver-doped hydroxyapatite thin films[J]. Disserta- tions & Theses-Gradworks, 2007, 32(8): 2135-44.马福秋. 镍钛合金表面银基复合镀层的制备与性能研究[D]. 哈尔滨工程大学, 2012.
[20] Xiong J, Ghori M Z, Henkel B, et al. Controlling surface segregation of reactively sputtered Ag/TiOxnanocomposites[J]. Acta Materials, 2014,74: 1-8.
[21] 付元静. 基于磁控溅射法制备AG/PTFE复合膜及其性能的研究[D]. 2018.
[22] Irfan M, Polonskyi O, Hinz A, et al. Antibacterial, highly hydrophobic and semi-transparent Ag/plasma polymer nanocomposite coating on cotton fabric obtained by plasma based co-deposition[J]. Cellulose, 2019, 26(16): 8877-8894.
[23] Mishra Y K, Mohapatra S, Chakravadhanula V S K, et al. Synthesis and characterization of Ag-polymer nanocomposites[J]. Journal of Nanoence & Nanotech- nology, 2010, 10(4): 2833.
[24] Wu J, Ueda K, Narushima T. Fabrication of Ag and Ta co-doped amorphous calcium phosphate coating films by radiofrequency magnetron sputtering and their antibacterial activity[J]. Materials Science & Engineering C, 2020, 109:110599.
[25] Thangavel E, Dhandapani V S, Dharmalingam K, et al. RF magnetron sputtering mediated NiTi/Ag coating on Ti-alloy substrate with enhanced biocompatibility and durability[J]. Materials Science and Engineering: C, 2019, 99: 304-314.
[26] Zhao, L Z, Hang R Q, Gao A, et al. Nanostructured titanium-silver coatings with good antibacterial activity and cytocompatibility fabricated by one-step magnetron sputtering[J]. Applied Surface Science, 2015, 355: 32-44.
[27] He X J, Zhang X Y, Bai L, et al. Antibacterial ability and osteogenic activity of porous Sr/Ag-containing TiO2coatings[J]. Biomedical Materials, 2016, 11(4): 045008.
Research progress of silver containing antibacterial coatings on medical titanium surface prepared by magnetron sputtering
You Li, Chang Peiliang, Feng Neng, Wu Mingchao, Huang Lei, Yu Cheng
(Wuhan Institute of Marine Electric Propulsion, Wuhan 430064, China)
TM272
A
1003-4862(2022)10-0105-05
2021-12-06
游立(1991-),男,工程师。研究方向:超细银粉、电子浆料。E-mail: nickyou_cssc712@126.com
