HPLC-Q-TOF-MS在线筛选鉴定牡丹花中的抗氧化成分
2022-10-18田璇刘宇朱文卿郑振佳
田璇,刘宇,朱文卿,郑振佳
(山东农业大学 食品科学与工程学院 山东省高校食品加工技术与质量控制重点实验室, 山东 泰安 271018)
牡丹(PaeoniasuffruticosaAndr.)是毛茛科芍药属木本植物,有“花中之王”的美誉,是较好的天然营养保健资源,其中凤丹牡丹花被国家卫计委批准为新食品原料[1-2]。现代研究发现牡丹具有抗肿瘤、抗炎、抗过敏、抗血栓和预防动脉粥样硬化等作用[3-6],牡丹花具有清除超氧阴离子、羟基自由基和过氧化氢,保护DNA,防止低密度脂蛋白氧化损伤等作用[7-9],其主要抗氧化物质是黄酮类和花色苷类成分[10-11],分析其黄酮、花色苷类成分需要多种对照品进行比对,成本较高。前期有研究尝试通过高效液相色谱-电喷雾质谱联用技术分析牡丹花中的部分成分[12],但无法同时实现对其抗氧化活性成分的同步筛选。
高效液相色谱-飞行时间质谱(high performance liquid chromatography-quadrupole time of flight mass spectrometry,HPLC-Q-TOF-MS)技术的优点是速度快、灵敏度和选择性高,目前在食品和中药方面已有较多应用[13-15]。基于1,1-二甲苯-2-三硝基苯肼(1,1-diphenyl-2-picrylhdrazyl,DPPH)在线清除结合高分辨质谱鉴定抗氧化成分的方法,现已广泛应用于天然产物中抗氧化成分的快速筛选与鉴定[16-19]。该方法的主要流程为抗氧化成分与自由基反应在517 nm处形成负峰,结合高分辨质谱获得的精准分子量进行化合物的鉴定,从而实现样品中抗氧化成分的快速、定向和准确识别。
本研究以牡丹花为研究对象,在线筛选鉴别其抗氧化成分,为牡丹花的成分分析及其资源利用提供参考。
1 仪器与材料
1.1 材料与试剂
牡丹花干制品(山东省菏泽市康普生物科技有限公司)。DPPH(美国Sigma公司),乙腈(色谱纯,瑞士Oceanpak公司),纯净水(娃哈哈集团有限公司)。
1.2 仪器与设备
Rigol L-3000泵(北京普源精电科技有限公司),Thermo Fisher UltiMate 3000高效液相色谱仪(美国赛默飞世尔公司),Waters ACQUITY UPLC H-CLASS 超高效液相色谱仪(美国沃特世公司)和Bruker impact Ⅱ高分辨飞行时间质谱仪(德国布鲁克科技有限公司)。
1.3 实验方法
1.3.1 样品与DPPH反应液的制备
牡丹花粉碎后过80目筛,精密称取1.0 g样品,加入80 mL 95%乙醇溶液回流提取30 min,转移至100 mL容量瓶中并用95%乙醇定容,混匀,过0.45 μm有机滤膜,冷藏贮存。
将DPPH用80%乙腈溶解并配制成溶液,浓度为6×10-5mol/L,备用。
1.3.2 牡丹花中抗氧化成分在线筛选与分析
采用UltiMate 3000高效液相色谱系统对牡丹花样品进行在线抗氧化成分筛选。实验流程参照文献[20]方法进行改良,样品经过色谱柱分离后与L-3000泵输出的DPPH溶液混合,混合液在反应池中反应后流入图像二极管阵列检测器(DAD,photo-diode-array-detector)进行检测。鉴于DPPH自由基在517 nm处被抗氧化活性成分清除后形成倒峰,对比样品最佳吸收波长下的液相图和DPPH自由基反应后的液相图可以筛选出抗氧化成分,结合获取的精准分子量,实现牡丹花中抗氧化成分的在线筛选与鉴定。
1.3.3 仪器及工作条件
液相色谱工作条件:色谱柱Waters X-Bridge C18(250 mm×4.6 mm,5 μm);乙腈(A)-水(0.1%甲酸),梯度洗脱程序 0~6 min(5%~10%A),6~7 min(10%~12%A),7~22 min(12%A),22~27 min(12%~13%A),27~28 min(13%~19%A),28~45 min(19%~20%A),45~60 min(30%~35%A);流速1.0 mL/min;检测波长280 nm;进样量5 μL;柱温25 ℃。
DPPH溶液反应条件:反应器为PEEK盘管(10 m×0.25 mm),流动相为DPPH-甲醇溶液。
质谱工作条件:分别采用电喷雾正、负离子模式;全扫描范围m/z50~1 500,离子源ESI,毛细管电压3 500 V,雾化气压0.2 MPa,干燥气流速8 L/min,干燥气温度200 ℃,碰撞能量90 eV。
2 结果与分析
2.1 高效液相色谱条件优化
以乙腈-水(0.1%甲酸)为流动相,进行分析条件的摸索。分别考察了等度洗脱和梯度洗脱在不同检测波长下对牡丹花样品的分离情况。实验表明等度洗脱难以实现样品中化合物的有效分离,采用梯度洗脱的方式可以实现牡丹花样品中多组分的有效分离。分析过程中分别比较了280 nm和350 nm下样品的吸收情况和出峰数量,结果显示280 nm下样品中的响应值较好,色谱峰数量多于350 nm。因此,液相分析条件选用乙腈-水(0.1%甲酸)为流动相,在280 nm下进行梯度洗脱的分析条件。
2.2 抗氧化活性成分在线筛选
高效液相色谱仪进行抗氧化活性成分的筛选,其液相色谱分析结果见图1。图1(a)为牡丹花样品的高效液相色谱图,图1(b)为在线清除自由基液相色谱图,根据图1(b)结果显示牡丹花提取物中的化合物6、8、10、14和15共5种成分具有抗氧化活性。
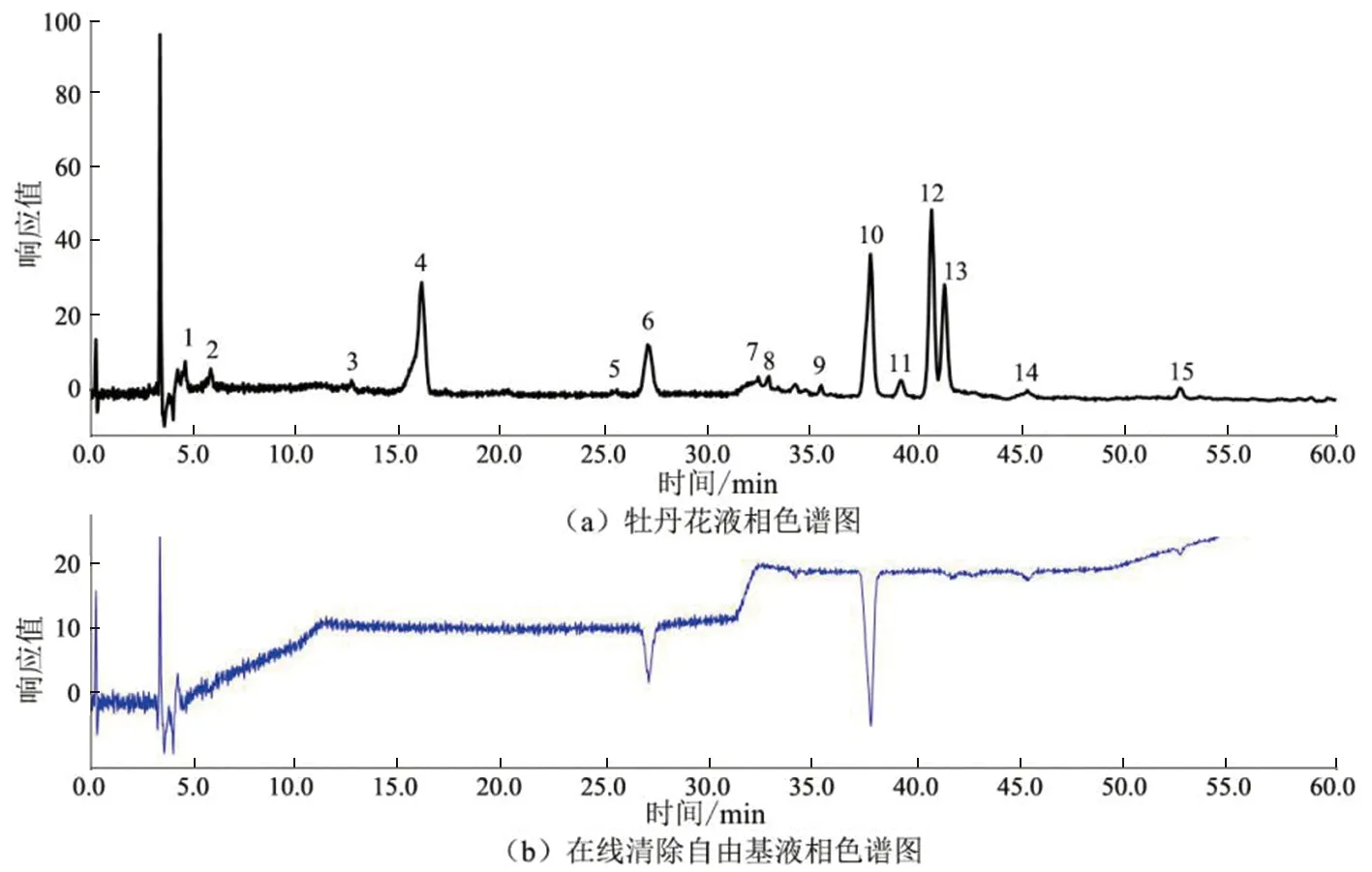
图1 牡丹花与在线清除自由基的HPLC图Fig.1 HPLC chromatograms of peony flower and on-line free radical scavenging
2.3 质谱条件优化
分别考察正、负两种离子模式下待测样品的总离子流图,分析结果见图2。对总离子流图进行比较后发现,牡丹花中的主要待测组分在负离子模式下的响应值略高于正离子模式,在负离子模式下杂质的干扰程度低于正离子模式。因此为获得最佳的分析结果,本研究选取负离子模式为牡丹花成分分析的质谱条件。

图2 正负离子模式下牡丹花样品的总离子流图Fig.2 Total ion flow diagram in positive and negative ion modes of peony flower samples
2.4 牡丹花组分及其抗氧化成分的鉴定
在优化后的色谱分析条件下,采用飞行时间质谱对牡丹花中的化学成分进行鉴定。根据获得的化合物的精确分子量信息与参考文献相对比,进行化合物的推测,结果见表1。参考相关文献[21-22]与牡丹中已知组分推测白牡丹花中具有抗氧化成分依次为6(没食子酸乙酯)、8(未知)、10(11α,12α-epoxy-3β,23-dihydroxy-30-norolean-20(29)-en-28,13β-olide)、14(未知)和15(未知)共5种成分,其中3种未知组分有待于今后通过分离纯化获得单体后进行结构解析。

表1 牡丹花样品的HPLC-Q-TOF-MS分析

表1(续)
化合物1在负离子模式下得到的分子量为331.055 4,推测为1-没食子酸酰葡萄糖或6-没食子酸酰葡萄糖[23-24]。化合物4在负离子模式下得到的分子量为609.111 8,推测为山奈酚-3,7-二-O-葡萄糖苷或山柰酚3-O-β-D-半乳糖(2→1)-β-D-葡萄糖苷[25-26]。化合物9和11在负离子模式下得到的分子量分别为447.064 3和447.064 6,推测可能为木犀草素-7-O-葡萄糖苷或山奈酚-3-O-β-D-吡喃葡萄糖苷[25,27],与参考文献[27]获得的色谱峰进行对照,确定化合物11为山柰酚-3-O-β-D-吡喃葡萄糖苷,因此判断化合物9为木犀草素-7-O-葡萄糖苷。化合物12在负离子模式下得到的分子量为577.118 2,推测该化合物为芹菜素-7-O-新橘皮糖苷或芹菜素-7-O-β-D-葡萄糖-4′-O-α-L-鼠李糖苷[27-28]。
对于同分异构体,由于几种化合物分子量相同,且没有参考文献报道,即使通过多级质谱也难以实现鉴定。后期可以考虑在获得单体后进行进一步分析,特别是通过核磁共振中HMBC、HSQC和1H-1H-COSY等二维核磁进行最终确认。
3 结论
本研究依据飞行时间质谱获得的精准分子量,共鉴定了15种成分并在线筛选出5种具有抗氧化活性的物质,参考现有文献,发现其中仅有没食子酸乙酯和11α,12α-epoxy-3β,23-dihydroxy-30-norolean-20(29)-en-28,13β-olide两种成分在牡丹成分研究中报道过,其他抗氧化组分均为首次发现,有待于后期结合分离技术和核磁等结构确证技术进一步鉴定。此外,鉴定的其他组分多为黄酮类化合物,理论上也具有清除DPPH的效果,通过该模型未能体现其在线清除DPPH的特性,该现象也有待于后期通过实验进一步深入探究。
