左心耳血管瘤临床及影像特征*
2022-10-18严高武邓建涛杨国庆
段 庆 严高武 李 艳 杨 玲 严 静 邓建涛 杨国庆 李 勇
1.川北医学院 (四川 南充 637000)
2.遂宁市中心医院放射影像科(四川 遂宁 629000)
3.遂宁市中心医院病理科(四川 遂宁 629000)
4.遂宁市中医院 (四川 遂宁 629000)
原发性心脏肿瘤非常少见,文献报道较少。心脏血管瘤(cardiac hemangioma,CH)是一种罕见的良性血管性病变,仅占原发性心脏肿瘤的5%~10%[1]。CH大多数发生于心室,以左心室多见。本文报道一例起源于左心耳的巨大海绵状血管瘤,现结合相关文献,总结CH的临床特征、影像学表现和鉴别诊断,以提高临床对CH的认识水平。
1 资料与方法
1.1 本中心病历资料女性,60岁,外伤后胸部CT检查偶然发现纵隔占位5+月入院。既往体健,患病以来无恶心、呕吐、心慌、气促等不适。查体和实验室检查无特殊,心脏彩超检查未见明显异常。胸部CT平扫+增强和血管三维重建:纵隔脏器区左侧可见一软组织肿块影(见图1),大小约7.0cm×8.5cm×6.0cm,其内密度不均(图1A),边缘光整,增强扫描动脉期其内见结节状、斑片状明显强化(图1B),静脉期和延迟期强化范围增加(图1C和图1D),病变紧邻左心房、左心室和肺动脉,与邻近结构分界清楚;另左心耳显示不清(图1E)。
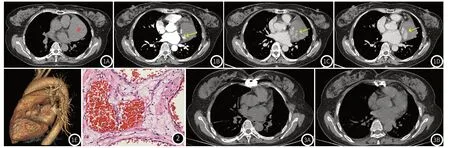
图1 女,60岁,CT平扫显示纵隔脏器区左侧软组织肿块(图1A,星),增强扫描动脉期(图1B)和静脉期(图1C和图1D)呈“渐进性”强化方式(黄箭),容积再现显示左心耳正常结构消失(图1E,红箭)。图2 女,60岁,左心耳海绵状血管瘤,海绵状血管型。管壁增厚并扩张的血管腔内镜下充满大量红细胞(HE,×200)。图3 左心耳血管瘤手术切除术后6+月,未见明显肿瘤复发征象
胸腔镜转开胸探查术中所见:(1)体外循环下见左心耳来源肿瘤,带蒂连于左心耳,蒂直径约1cm,紧邻左心房、心室和肺动脉,边缘光整,大小约6.5cm×9.0cm×7.0cm,与邻近结构分界清楚,剖开其密度不均;(2)心包肿胀,心包积液,术中腔镜监视下5mL注射器诊断性试穿刺,有血性液体,张力高。
术后病理检查:“左心耳肿瘤”为灰红结节样物一枚,大小5.5cm×4cm×3.5cm,表面光滑,包膜完整,切面灰白灰褐实性质中偏软,部分区域呈海绵状(见图2),考虑海绵状血管瘤,海绵状血管型。
患者术后恢复良好,手术切口Ⅰ/甲愈合,复查胸部CT、心脏彩超显示术区呈术后改变。术后6+月随诊未诉明显不适,复查胸部CT未见明显肿瘤复发征象(见图3)。
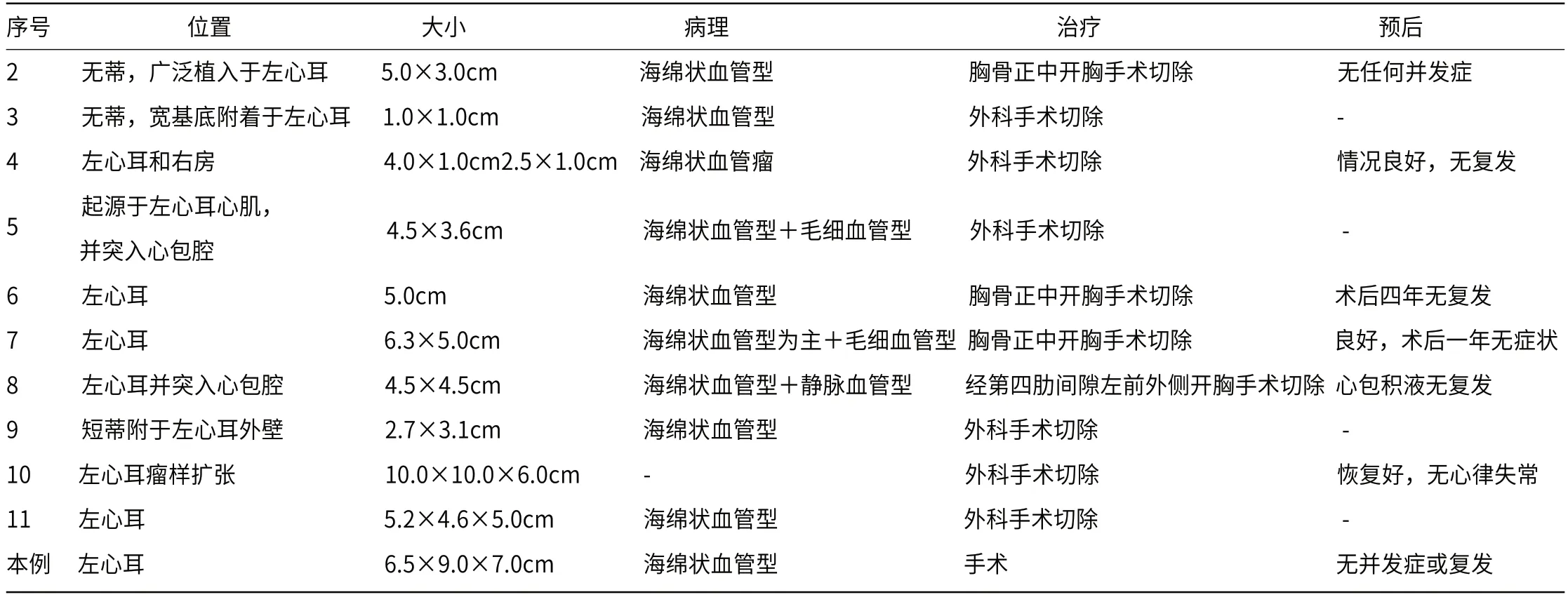
1.2 文献检索以“left atrial appendage”和“hemangioma”为关键词检索PubMed英文数据库并以“左心耳”和“血管瘤”为主题词检索中国知网、万方中文数据库,时间不限,筛选并整理相关文献。文献中所有病例均需经手术和病理检查证实,提取并总结患者临床资料,包括:发表时间、第一作者、例数、性别、年龄、临床表现、检查方法、病变特点等(见表1)。

表1 左心耳血管瘤临床特征汇总
2 结 果
本研究最终纳入10篇文献,其中6篇为英文,1篇为日文,3篇为中文,包含11例患者(女性9例,男性2例,平均年龄约为64岁)。
临床表现:4例有心悸或心率失常表现,3例有呼吸困难表现,2例无明显症状,1例表现为缺血性脑卒中,1例表现为高血压,1例表现为反复发作的心包积液,1例无明显临床表现但随着肿瘤增大出现劳力性呼吸困难。
检查方法:4例经超声心动图检出,4例经胸部X线平片发现,2例经胸部CT检查发现,1例于冠脉手术时发现。
病灶位置:11例患者均为左心耳的血管瘤,其中1例有蒂,1例为双病灶(左心耳和右心房)。
病灶大小:肿瘤大小在1.0~10.0cm范围内,最大直径集中在4.0~6.3cm范围内(7例,63.6%)。
病理分型:海绵状血管瘤为最常见类型(7例,63.6%),海绵状血管与毛细血管混合型2例(18.2%),1例为海绵状血管与静脉血管混合型,1例未报道具体分型。
治疗及预后:所有患者均行外科手术切除治疗,术后预后良好患者约占63.6%(7例),4例未报道其预后情况。
续表1
续表2
3 讨 论
3.1 概述CH是心脏的原发性良性肿瘤,与黏液瘤、乳头状弹性纤维瘤等常见的心脏良性肿瘤相比,血管瘤更为罕见。CH可发于心脏和心包的任何部位,主要位于心壁和左心室[12],新生儿血管瘤通常发生于右心房;发生于左心耳的血管瘤尤为罕见,国内外文献中仅有几例被报道。CH在组织学上可分为毛细血管型(大量更小的毛细血管组成,管腔内几乎没有红细胞)、海绵状血管型(薄壁扩张毛细血管,管腔内充满大量红细胞)以及动静脉畸形(由管壁增厚的发育不良的动脉、静脉血管和毛细血管组成)。大部分CH位于心肌内,但毛细血管瘤和海绵状血管瘤常附着于心肌壁但不浸润心肌。
3.2 发病年龄和性别CH可发生于任何年龄,文献报道就诊年龄常在40岁左右,且男性患者发病率较女性稍高[13-14];但本组病例中女性较多(9例,81.8%),平均就诊年龄约64岁。
3.3 临床表现随着血管瘤位置、大小、活动度、生长速度及浸润程度的不同,患者可表现为无明显临床症状到严重血流动力学不稳。大多数患者一般无明显临床症状,部分患者可表现为非典型胸痛、传导异常、冠状动脉供血不足、充血性心力衰竭、心包炎、心包积液、心包填塞以及血栓栓塞并发症[15-17]。本文从文献中收集的10例CH患者中仅1例无明显症状[5],另一患者开始无明显症状,但随着肿瘤增大而逐渐出现劳力性呼吸困难[7];本中心患者既往也无特殊,而在肋骨骨折后行常规胸部CT时偶然发现。此外,CH也可表现为卡 -梅利特综合征 (Kasabach-Merritt syndrome),其特点是多系统性血管瘤、血小板减少和消耗性凝血障碍[18]。
3.4 影像检查方法及表现超声心动图是诊断CH的首选影像学检查方法,它可以显示病灶的位置、大小并做出初步的定性诊断;但在显示肿瘤向腔外或纵隔侵犯方面,CT和MRI更具优势。本组病例中4例患者经超声心动图检出,4例患者于常规胸部X线片检查中发现异常,故超声心动图和胸部X片以其简便、快捷的特点在CH的首次检出中发挥着巨大的优势。
具有心外生长倾向的血管瘤常表现为心脏正常轮廓改变以及纵隔内异常肿块[19],CH于超声心动图常表现为高回声肿块或结节;CT检查常表现为不均匀的低密度病灶,肿瘤内可有更低密度的囊变区和小点片状高密度钙化影。CT增强扫描后肿块不均匀显著强化,海绵状血管瘤常表现为从边缘开始逐渐向中心填充的延迟强化特点(类似于肝脏海绵状血管瘤)。
在MRI上,由于血管瘤血流缓慢,肿瘤在T1WI表现为等信号、T2WI上表现为高信号,且随着回波时间的延长,信号强度增加,形成所谓“T2WI灯泡征”;MRI增强扫描表现同CT增强检查。
3.5 鉴别诊断CH不仅应与血栓、心包囊肿等心脏非肿瘤性病变进行鉴别,还应与黏液瘤、乳头状弹性纤维瘤、横纹肌肉瘤、脂肪瘤等心脏良性肿瘤性病变进行鉴别。
心脏血栓常发生房颤或二尖瓣疾病的基础上,以左心房最为常见。CT上表现为心腔内的低密度影,MRI上血栓信号与其所处期相有关。急性期血栓在T1WI和T2WI上均为高信号,亚急性期血栓在T1WI上为高信号、T2WI为低信号,慢性期血栓在T1WI和T2WI均为低信号,各期相血栓增强扫描后均不强化。心包囊肿通常位于右心膈角,表现为T1WI低信号、T2WI高信号的均一液体信号影,增强扫描无强化。
心脏黏液瘤是最常见的心脏良性肿瘤,约占50%。肿瘤一般位于左心房(75%)、右心房(23%)和左心室(2%),常有细小的蒂附着于房间隔的卵圆窝上。超声上表现为低或者高回声的可移动肿块,CT检查显示病灶密度多不均匀,可见高密度钙化区或(和)低密度囊变、坏死区。MRI示信号不均匀的肿块影,表现为等 T1、长T2信号;由于含铁血黄素沉积,T1WI上有时表现为低信号,增强后肿瘤不均匀轻度强化。
乳头状弹性纤维瘤是位于瓣膜游离缘(主动脉瓣最常见)的有细小的蒂、活动的瓣膜肿块,超声心动图上常呈中等信号,CT上通常不可见。MRI上呈等T1、T2信号,增强后明显强化。
心脏横纹肌肉瘤是儿童最常见的心脏肿瘤,约占儿童原发性良性心脏肿瘤的90%;肿瘤表现为心室壁的多发肿块(左室>右室),出血、钙化少见。超声心动图上表现为肌壁间或室间隔的强回声肿块,因肿块密度与周围正常心肌密度相似,故横纹肌瘤在CT上难以辨认。肿瘤在T1WI上表现为等或稍高信号,T2WI为高信号,增强后无明显强化。
纤维瘤是继横纹肌瘤和错构瘤之后第三大常见的儿童原发性心脏肿瘤[20],表现为起源于室间隔或左室游离壁的界限清楚的孤立性肿块,钙化常见,出血、坏死及囊变少见。超声心动图上显示为肌壁间均一回声的肿块,CT上以低密度影为主,伴有高密度钙化。T1WI上表现为等或高信号,T22WI为低信号,增强后表现为显著的均匀延迟强化。
脂肪瘤常起源于心内膜下、心外膜的脂肪或心肌本身,是边界清楚且具有完整包膜的均匀密度肿块。超声心动图上表现为心包周围间隙或心腔内的低回声肿块,CT上呈均匀的脂肪密度。MRI上为均匀的短T1、长T2信号,压脂序列呈低信号,增强扫描无强化。
错构瘤主要发源于主动脉根部,通常为位于心包的带蒂肿瘤,由内、中、外三个胚层组成。由于错构瘤含有脂肪、骨骼和牙齿等多种成分,故其在影像学表现为混杂回声(密度或信号),增强后不均匀强化。
CH具有转变为血管肉瘤的潜在风险,后者为心脏恶性肿瘤,具有侵袭性,故一旦发现CH均应判断其是否有侵袭性,并且应该与常见的心脏恶性肿瘤进行鉴别(表2)。
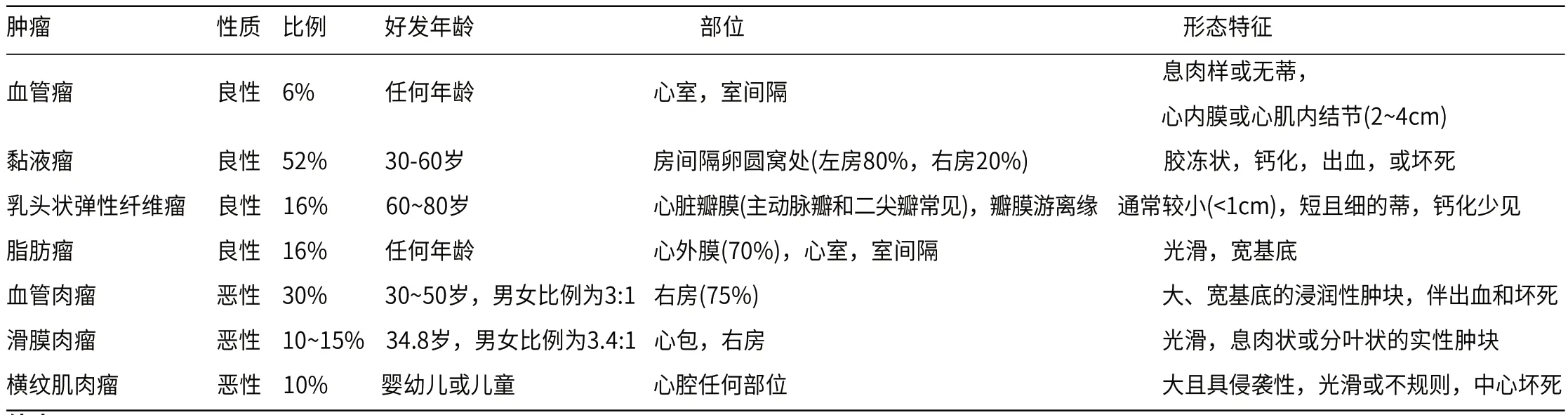
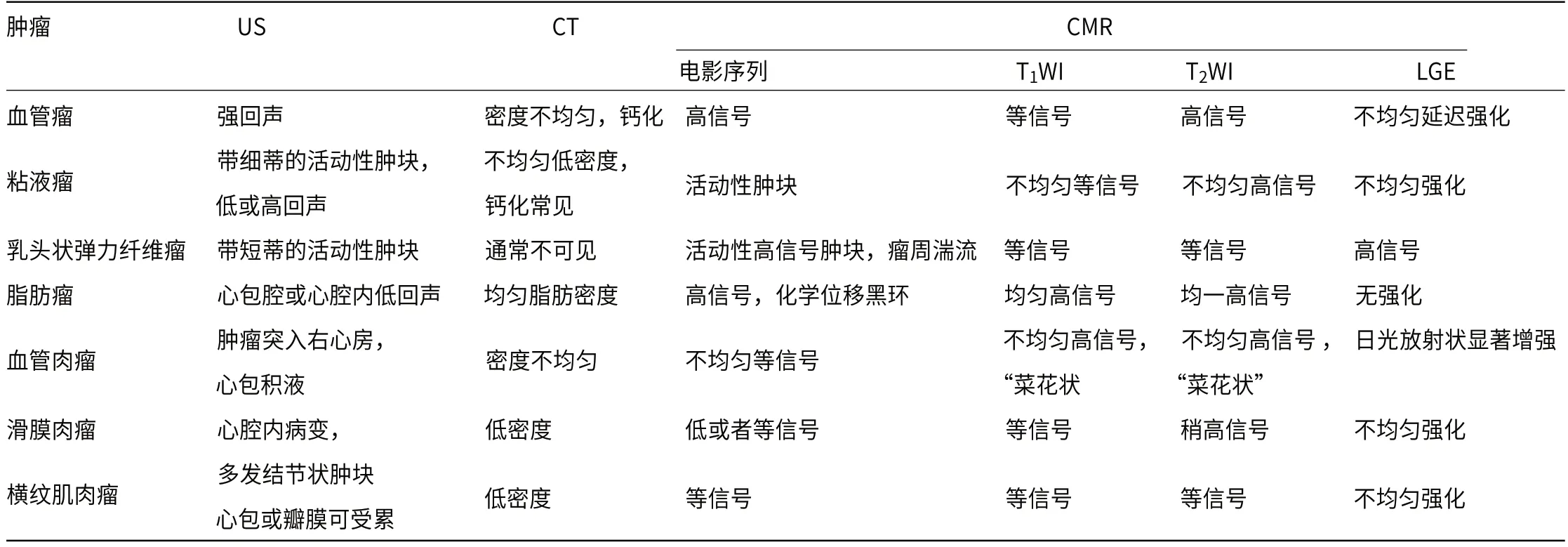
表2 血管瘤和常见心脏良恶性肿瘤临床及影像特征汇总
总的来说,CH的诊断需要密切结合临床和病理特点,影像学检查可以明确肿瘤的位置、大小以及与周围邻近组织结构的关系,最终确诊仍需依靠手术和组织病理学检查。
3.6 治疗CH虽为良性肿瘤,但因其具有转变为血管肉瘤的风险,且无症状的CH也可能突然引起危及生命的并发症,故一旦发现应尽早手术。手术一方面可以明确诊断,另一方面可降低CH破裂或发生肺栓塞的风险[21]。对于边界清楚的血管瘤,不论肿瘤大小都应尽可能行根治性手术切除,患者术后一般恢复良好;而不能完全切除的、巨大的、广泛的CH则具有复发的潜在风险,其预后往往不良。所有的CH患者术后均应进行定期地随访,通过影像学检查手段了解是否有新发或复发病灶[22]。
