两种分光光度法测定样品中铁含量的比较
——以化学实验技术技能大赛为例*
2022-10-12陈德霞李勇辉张渝秀
陈德霞,李勇辉,黎 亚,张渝秀,王 姝
(宜宾职业技术学院新材料与化工能源学院,四川 宜宾 64400)
化学实验技术是利用现代化学技术对各类天然或合成材料进行物理常数与化学性质测定、定性与定量分析、制备与合成的专门技术技能。依据《2021年全国职业院校技能大赛赛项规程 GZ-2021026 化学实验技术赛项》[1],化学实验技术赛项由三个模块组成,涉及物质的定性分析、定量分析、制备和质量控制。其中,B模块:样品中铁含量的测定,参考标准GB/T 3049—2006[2]、GB/T 6150.16—2009[3]、YS/T 281.1—2011[4],采用1,10-菲啰啉分光光度法或磺基水杨酸分光光度法测定试样中的铁含量,即基于特定pH条件下,不同价态的铁离子可以与特定显色剂(1,10-菲啰啉或磺基水杨酸)生成有色配合物,有色配合物在最大吸收波长处测量的吸光度符合朗伯—比尔定律(Lambert-Beer)。
依据化学实验技术赛项规程、样题、过程性考核评分表,参照相关检测标准,建立了两种分光光度法测定样品中铁含量的方法。两种检测方法的一致性评价主要有配对t检验、简单相关性分析、比对及偏倚评估和Bland-Altman法等方法[5-8],但相对复杂,且有一定的局限性,因此,本文拟依据化学实验技术赛项结果性考核评分表,通过标准曲线的相关性、精密度、准确度、F检验、t检验对两种方法进行一致性评价。
1 实验部分
1.1 实验原理
1.1.1 1,10-菲啰啉分光光度法测定铁含量的原理
依据GB/T 3049—2006[2]、HJ/T 345—2007[9],用盐酸羟胺或抗坏血酸把试液中Fe3+还原成Fe2+,在pH值为2~9时,Fe2+与1,10-菲啰啉生成稳定的橙红色络合物,在分光光度计最大吸收波长处(510 nm)测定其吸光度。
1.1.2 磺基水杨酸分光光度法测定铁含量的原理
依据GB/T 6150.16—2009[3]、YS/T 281.1—2011[4]、GB∕T 6730.7—2016[10],在pH值为8.5~11时,Fe3+与磺基水杨酸生成稳定的黄色络合物,在分光光度计最大吸收波长处(420 nm)测定其吸光度。
1.2 实验材料
1.2.1 铁标准溶液
国家标准样品(GSB 04-1726-2004)标准值:1000 μg/mL(国家有色金属及电子材料分析测试中心)。
1.2.2 铁使用溶液
移取样品铁标准溶液(1000 μg/mL)4.00 mL 至 100 mL 容量瓶中,加水定容至刻度线,混匀,即是 40 μg/mL 的铁使用溶液。
1.2.3 化学试剂
抗坏血酸、冰乙酸、三水乙酸钠、1,10-菲啰啉、磺基水杨酸、盐酸羟胺、氨水、氯化铵、硫酸铁(III)铵十二水合物、硫酸、过氧化氢等化学试剂(均为分析纯,成都市科隆化学品有限公司生产)。
1.2.4 溶液
1)抗坏血酸溶液(100 g/L);2)乙酸—乙酸钠缓冲溶液(pH≈4.5,依据GB/T 603—2002配制);3)1,10-菲啰啉溶液(1 g/L);4)盐酸溶液(180 g/L,依据GB/T 3049—2006配制);5)氨水溶液(1+1);6)过氧化氢(1+9);7)磺基水杨酸溶液(250 g/L);8)盐酸羟胺溶液(50 g/L);9)氨-氯化铵缓冲溶液甲(pH≈10,依据GB/T 603-2002配制);10)硫酸溶液(质量分数为25%);11)铁试样溶液(800.0 μg/mL,参照GB/T 602—2002配制,称取 6.9076 g 硫酸铁铵,溶于水,加 10 mL 硫酸溶液(质量分数为25%),移至 1000 mL 容量瓶中,用去离子水(RO)稀释至刻度,摇匀)。
1.3 仪器设备
1)电子天平(FA2004A,上海精天电子仪器有限公司);2)紫外-可见分光光度计(UV-1800PC-DS2,上海美普达仪器有限公司)。
1.4 绘制标准曲线
1.4.1 1,10-菲啰啉分光光度法标准曲线
1)配制铁标准系列溶液:用 10.00 mL 分度吸量管准确移取不同体积的铁使用溶液(标准曲线绘制专用)至一组 100 mL 容量瓶中(不少于 7 个),配制不同浓度的铁标准系列溶液;
2)溶液显色:上述铁标准系列溶液采用下述方式处理,如有必要,先用盐酸溶液(180 g/L)将上述标准系列溶液调至pH=2;加入 2 mL 抗坏血酸溶液(100 g/L),摇匀;然后加 20 mL 乙酸—乙酸钠缓冲溶液(pH≈4.5)和 10 mL 1,10-菲啰啉溶液(1 g/L);用去离子水(RO)稀释至刻度,摇匀;放置不少于 15 min。
3)绘制标准曲线:在最大吸收波长(约 510 nm)处,以不加铁标准溶液的一份为参比,测定铁标准系列溶液的吸光度。以质量浓度为横坐标,以相应的吸光度为纵坐标绘制标准曲线,参数如表1所示。
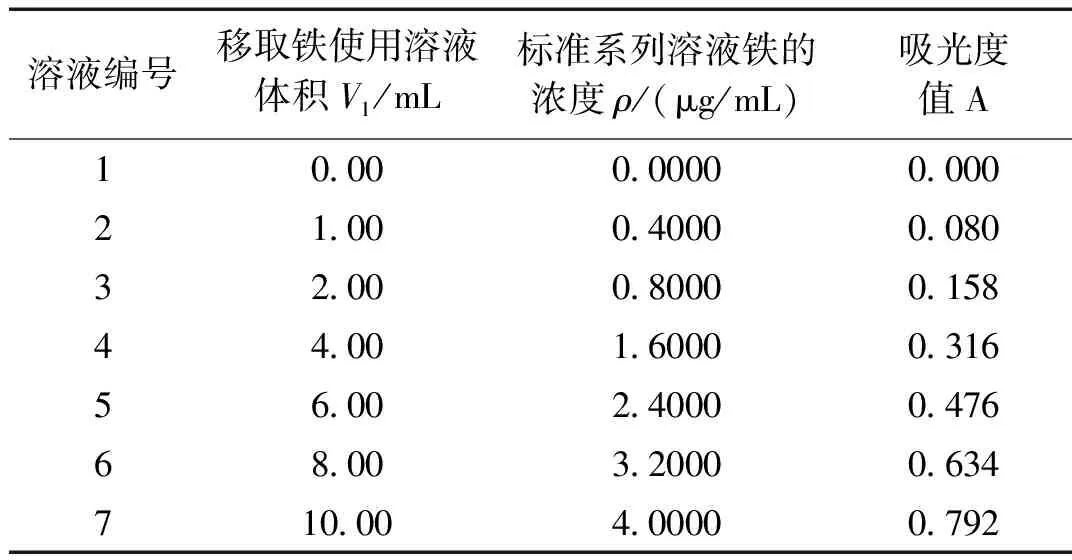
表1 绘制标准曲线(1,10-菲啰啉分光光度法)
4)拟合方程
拟合方程:ρ=5.049527A-0.000234;相关系数:R=0.99999797。
1.4.2 磺基水杨酸标准曲线
1)配制铁标准系列溶液:用 10.00 mL 分度吸量管准确移取不同体积的铁使用溶液(标准曲线绘制专用)至一组 50 mL 容量瓶中(不少于 7 个),配制不同浓度的铁标准系列溶液;
2)溶液显色:上述铁标准系列溶液采用下述方式处理。如有必要,先加3滴过氧化氢(1+9),用氨水溶液(1+1)将上述标准系列溶液调至pH=9~10;加入 5 mL 磺基水杨酸溶液(250 g/L)、2 mL 盐酸羟胺溶液(50 g/L),然后加入 10 mL 氨—氯化铵缓冲溶液甲(pH≈10);用去离子水(RO)稀释至刻度,摇匀;放置不少于 10 min。
3)绘制标准曲线:在最大吸收波长(约 420 nm)处,以不加铁标准溶液的一份为参比,测定铁标准系列溶液的吸光度。以质量浓度为横坐标,以相应的吸光度为纵坐标绘制标准曲线,参数如表2所示。
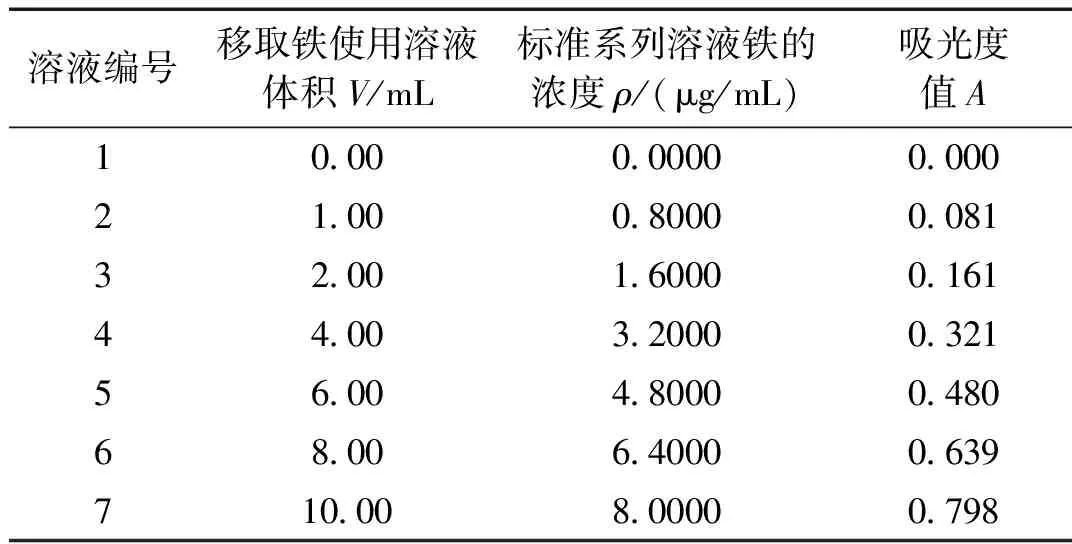
表2 绘制标准曲线(磺基水杨酸分光光度法)
4)拟合方程
拟合方程:ρ=10.031404A-0.011126;相关系数:R=0.99999743。
最后进入学生独立读写阶段(Independent Construction),用补充材料Text C让学生独立进行学习,至此学生在教师的一步步引导下,以学生为主导,最后能独立地阅读和写作。在KWL+理论和教与学循环理论的指导下,真正把阅读和写作有机地结合起来,实现了输入和输出的转化,提高了学生的学习兴趣,增强了阅读和写作能力。
1.5 试样中铁含量的测定
1.5.1 测定方法
1)确定未知铁试样溶液的稀释倍数,分别采用两种分光光度法测定样品中铁含量,按照绘制工作曲线时的溶液显色和测定方法,在最大吸收波长处进行吸光度测定。平行测定 3 次。
1,10-菲啰啉分光光度法:准确移取 5.00 mL 未知铁试样溶液于 100 mL 容量瓶中,配制成约 40 μg/mL 铁待测溶液(稀释20倍);准确移取 5.00 mL 铁待测溶液于 100 mL 容量瓶中(第二次稀释20倍,共稀释400倍),加入 2 mL 抗坏血酸溶液(100 g/L),摇匀;然后加 20 mL 乙酸—乙酸钠缓冲溶液(pH≈4.5)和 10 mL 1,10-菲啰啉溶液(1 g/L);用去离子水(RO)稀释至刻度,摇匀;放置不少于 15 min。在最大吸收波长处进行吸光度测定。平行测定6次。
磺基水杨酸分光光度法:准确移取 5.00 mL 未知铁试样溶液于 100 mL 容量瓶中,配制成约 40 μg/mL 铁待测溶液(稀释20倍);准确移取 5.00 mL 铁待测溶液于 50 mL 容量瓶中(第二次稀释10倍,共稀释200倍),加入 5 mL 磺基水杨酸溶液(250 g/L)、2 mL 盐酸羟胺溶液(50 g/L),然后加入 10 mL 氨-氯化铵缓冲溶液甲(pH≈10);用去离子水(RO)稀释至刻度,摇匀;放置不少于 10 min。在最大吸收波长处进行吸光度测定。平行测定 6 次。
2)由测得吸光度从标准曲线计算待测溶液中铁的浓度,根据未知铁试样溶液的稀释倍数,求出未知铁试样溶液中铁含量。
1.5.2 计算公式
以质量浓度ρ(Fe)计,数值以mg/L表示。取6次测定结果的算术平均值作为最终结果,结果保留4位有效数字。
ρ(Fe)=ρx×n
式中:ρ(Fe)为试样中铁的质量浓度,μg/mL;ρx为从标准曲线计算的待测溶液中铁质量浓度,μg/mL;n为试样溶液的稀释倍数。
2 结果与分析
2.1 标准曲线的相关性
两种方法的标准曲线相关性如表3所示。

表3 两种方法的标准曲线相关性
依据化学实验技术赛项结果性考核评分表,两种方法的标准曲线相关性均满足考核要求(相关系数R≥0.999995),检测方法可行。
2.2 检测结果分析
分别采用两种方法测定未知铁试样溶液中的铁含量,平行测定6次,结果如表4所示。
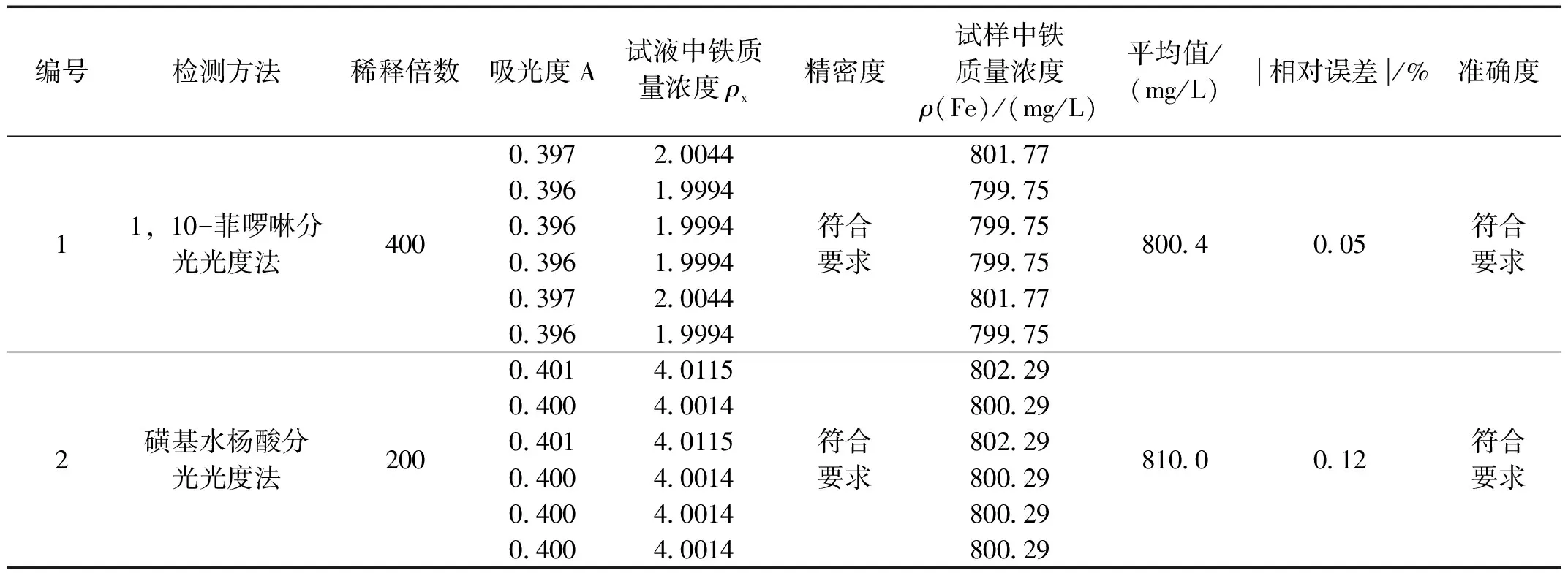
表4 两种方法的检测结果
依据化学实验技术赛项结果性考核评分表,两种方法的精密度、准确度均满足考核要求(未知液吸光度值的极差=0.001;|相对误差|≤0.5%),检测结果有效。
2.3 一致性评价
对上述检测结果进行F检验、t检验,结果如表5所示:

表5 两种方法检测结果的F检验、t检验结果
若采用显著性水平α=0.05的F双侧检验,查F分布表得F0.975(5,5)=0.140,F0.025(5,5)=7.15,因此,F0.975(5,5) 若采用显著性水平α=0.05的t单侧检验,查t分布表得t0.025(12)=2.179,因此|t| 1)对比两种方法的实验原理发现,1,10-菲啰啉分光光度法需要用盐酸羟胺或抗坏血酸等还原剂把试液中Fe3+还原成Fe2+,再进行显色反应;而磺基水杨酸分光光度法直接测定Fe3+,从反应的角度,磺基水杨酸分光光度法不受还原剂及氧化还原反应进程的影响。 2)对比两种方法的拟合方程发现,与1,10-菲啰啉分光光度法相比,溶液中铁含量相同时,磺基水杨酸分光光度法的吸光度值A偏小,即吸光系数偏小,这与反应生成的络合物及其最大吸收波长等因素有关。 1)依据化学实验技术赛项规程、样题、过程性考核评分表,参照相关检测标准,建立了两种分光光度法测定样品中铁含量的方法,两种方法的标准曲线相关系数R≥0.999995,满足检测要求,检测方法可行。 2)两种方法测定待测液吸光度值的极差=0.001,|相对误差|≤0.5%,精密度与准确度均达到化学实验技术赛项结果性考核要求,检测结果有效。 3)经F检验、t检验,两种方法的方差与平均值无显著性差异,检测结果是一致的。 4)与1,10-菲啰啉分光光度法相比,溶液中铁含量相同时,磺基水杨酸分光光度法的吸光度值A偏小,即吸光系数偏小,这与反应生成的络合物及其最大吸收波长等因素有关。2.4 差异性分析
3 结论
