外周血T淋巴细胞亚群流式检测方法的优化及验证
2022-10-11李新王园园侯婉毅李思佳江魁赵云霞
李新,王园园,侯婉毅,李思佳,江魁,赵云霞
华兰基因工程有限公司,河南新乡453003
流式细胞术(flow cytometry,FCM)是指利用流式细胞仪对液流中的细胞或生物颗粒逐个进行多参数快速分析的技术[1],已成为血液病研究和诊断的重要生物技术之一。尽管流式检测外周血淋巴细胞表面标志已有基本的实验步骤(加入荧光抗体→裂解红细胞→洗细胞→重悬后上机检测),但实验中仍可能存在多种因素影响结果的准确性[2],如抗体滴定[3]、红细胞裂解[4]、多聚甲醛固定[5]等,因此对影响因素进行优化可以提高分析结果的准确性。目前已有对B淋巴细胞亚群、单核细胞的流式检测方法进行优化的报道[6-7],但鲜见对T淋巴细胞流式检测方法进行优化的报道。T淋巴细胞膜上的主要抗原标志是CD3,按功能T细胞可分为辅助性T细胞(CD3+CD4+)和细胞毒性T细胞(CD3+CD8+)两个亚群。大量研究认为,优化流式检测外周血T淋巴细胞亚群的方法对临床前药物免疫毒性的评价[8]、患者免疫功能及疾病的诊断[9-11]均有重要意义。本研究从样本体积、抗体滴定、红细胞裂解条件对外周血T淋巴细胞亚群流式检测方法进行了优化,并验证了优化方法的精密度和样品稳定性,旨在完善实验方法,提高流式检测外周血样本结果的准确性,以期指导临床前评价中的流式相关检测,以及为某些血液病的临床诊断方法学研究提供一定理论依据。
1 材料与方法
1.1 实验动物
选取6只健康清洁级雄性美国国立卫生研究院(National Institutes of Health,NIH)小鼠,体质量16~18 g,均购自华兰生物疫苗股份有限公司,许可证号:SCXK(豫)2020-0003,质量合格证:410966211100075351。实验小鼠饲养于华兰基因工程有限公司动物中心屏障动物实验室,饲养环境:12 h光照/12 h黑暗,相对湿度40%~70%,温度22~25℃。实验过程符合动物福利3R指导原则,已通过动物关怀及使用委员会批准,批准号:ERHLGE-2021-P010。
1.2 主要试剂和仪器
磷酸盐缓冲液(phosphate buffer saline,PBS)购自美国Gibco公司;肝素钠和牛血清白蛋白(bovine serum albumin,BSA)购自索莱宝公司;抗体FITC rat anti-mouse CD3(货号:11-0032-82,克隆号:17A2,0.5 mg·mL-1)、APC rat anti-mouse CD4(货号:17-0041-82,克隆号:GK1.5,0.2 mg·mL-1)、PE rat anti-mouse CD8a(货号:12-0081-82,克隆号:53-6.7,0.2 mg·mL-1)和红细胞裂解液均购自美国eBioscience公司;死活染料7-氨基放线菌素(7-amino-actinomycin D,7-AAD)购自美国BD公司。离心机购自美国Eppendorf公司;细胞计数仪购自德国ROCHE公司;流式细胞仪C6购自美国BD公司。
1.3 预处理方法
小鼠眼眶静脉丛采集外周血,按50∶1的比例加入1%肝素钠溶液制备成抗凝血。于2 mL离心管中加入肝素钠抗凝血,再加入1% BSA-PBS稀释的荧光抗体进行染色,轻轻混匀,室温避光孵育30 min,加入红细胞裂解液裂解红细胞后,用PBS终止裂解反应,500 g·min-1离心5 min,弃上清,加入300 μL PBS重悬细胞沉淀,上机检测前加入7-AAD,孵育10 min。
1.4 方法优化
1.4.1 样本体积6只小鼠分别取50、100 μL抗凝血,裂解红细胞后用300 μL PBS重悬细胞沉淀,进行细胞计数。
1.4.2 荧光抗体 采用6只小鼠的抗凝血混合后,对抗体FITC rat anti-mouse CD3、APC rat anti-mouse CD4和PE rat anti-mouse CD8a分别进行了6个浓度的滴定:FITC rat anti-mouse CD3的终浓度分别为1.25、2.50、5.00、10.00、20.00、40.00 μg·mL-1,APC rat anti-mouse CD4的终浓度分别为0.625、1.250、2.500、5.000、10.000、20.000 μg·mL-1,PE rat anti-mouse CD8a的终浓度分别为1.25、2.50、5.00、10.00、20.00、40.00 μg·mL-1。每个浓度设3个重复,选择各抗体信噪比[signal/noise,S/N,阳性荧光强度中值与阴性荧光强度中值(median fluorescence intensity,MFI)的比值]较大的一组作为该抗体滴定的最佳工作浓度。
1.4.3 红细胞裂解条件 根据红细胞裂解液的使用说明书,筛选了5个裂解条件:①裂解1次,裂解时间为5 min;②裂解1次,裂解时间为8 min;③裂解1次,裂解时间为10 min;④裂解2次,每次裂解时间为5 min;⑤裂解2次,每次裂解时间为8 min。通过比较前向散射光(forward scatter,FSC,与细胞大小相关)和侧向散射光(side scatter,SSC,与细胞颗粒度相关)散点图中淋巴细胞门内的细胞占比情况、碎片杂质信号及白细胞亚群的基本形态,确定适宜的裂红条件。
1.5 方法学验证
1.5.1 精密度验证 通过检测批内差异和批间差异进行精密度验证。批内差异:将1只小鼠血样分成6份(编号分别为1、2、3、4、5、6)进行检测。实验合格标准:6份样品3个指标(CD3+细胞/淋巴细胞、CD3+CD4+细胞/淋巴细胞、CD3+CD8+细胞/淋巴细胞)的变异系数(coefficient of variation,CV)均≤15%。批间差异:将1只小鼠连续3 d(第1天、第2天、第3天)同一时间进行采样检测,设重复孔。实验合格标准:3次检测3个指标的CV值均≤15%。
1.5.2 样本稳定性验证 将5只小鼠的抗凝血混合后分为立即检测血样、4℃放置24 h血样和室温放置24 h血样共3份,每份5个样品。将4℃放置24 h、常温放置24 h血样染色处理的检测结果分别与采样后立即检测结果进行t检验差异分析。另外,将立即检测后的样品(即染色处理后样品)继续于4℃放置24 h后复测,将结果与立即检测结果进行t检验差异分析。
1.6 数据处理
流式图采用FlowJo V10软件分析,数据用GraphPad Prism 8.0.1统计学软件进行处理,结果用平均值±标准差(±s)表示。采用Student’st-检验计算组间显著性差异,以P<0.05为差异有统计学意义。
2 结果与分析
2.1 样本体积的确定
50 μL血样中裂红后细胞浓度为1.20×107cells·mL-1,活 细 胞1.19×107cells·mL-1,活 率99.0%;100 μL血样中裂红后细胞浓度为2.05×107cells·mL-1,活细胞浓度2.02×107cells·mL-1,活率98.3%(表1)。因流式检测要求细胞浓度范围为5×105~1×108cells·mL-1。依据实验动物福利3R中减少原则,以及生物制品临床前评价中可能需要对相同动物进行不同时间点的多次采血,以上研究表明50 μL抗凝血中的细胞浓度符合流式细胞仪上机要求,采用50 μL抗凝血进行后续试验。
表1 不同体积血样中的细胞浓度(±s,n=6)Table 1 Cell concentrations in blood samples of different volumes(±s,n=6)

表1 不同体积血样中的细胞浓度(±s,n=6)Table 1 Cell concentrations in blood samples of different volumes(±s,n=6)
样本体积/μL 50 100细胞浓度/(×106 cells·mL-1)12.03±1.49 20.53±1.36活细胞浓度/(×106 cells·mL-1)11.91±1.47 20.18±1.33细胞活率/%99.0±0.14 98.3±0.25
2.2 不同抗体的滴定结果分析
抗体滴定结果见图1,FITC rat anti-mouse CD3抗体随着滴定浓度的增加S/N值无明显变化;APC rat anti-mouse CD4和PE rat anti-mouse CD8a抗体S/N值随着滴定浓度的增加呈先增加后降低的趋势。经t检验差异分析表明,6个滴定浓度的FITC rat anti-mouse CD3抗体的S/N均无显著差异(P>0.05),为达到节约抗体的目的,选择FITC rat anti-mouse CD3的最佳滴定浓度为1.25 μg·mL-1;1.25 μg·mL-1APC rat anti-mouse CD4抗体的S/N显著高于0.625 μg·mL-1(P<0.05),但与2.50 μg·mL-1的S/N差异不显著(P>0.05),故APC rat anti-mouse CD4的最佳滴定浓度为1.25 μg·mL-1;5.00 μg·mL-1PE rat anti-mouse CD8a抗体的S/N显著高于1.25 μg·mL-1和2.50 μg·mL-1(P<0.05),但与10 μg·mL-1的S/N差异不显著(P>0.05),故PE rat anti-mouse CD8a的最佳抗体滴定浓度为5.00 μg·mL-1。而说明书中FITC rat anti-mouse CD3、APC rat anti-mouse CD4和PE rat anti-mouse CD8a的建议浓度分别为2.50 μg·mL-1、1.25 μg·mL-1和2.50 μg·mL-1。以上结果表明在进行抗体染色前需要根据具体的实验目的和样本对抗体进行滴定,确定抗体的最佳工作浓度。
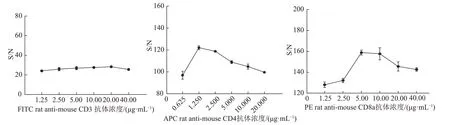
图1 FITC rat anti-mouse CD3、APC rat anti-mouse CD4、PE rat anti-mouse CD8a抗体不同浓度S/N值变化趋势Fig.1 Trend of S/N value of FITC rat anti-mouse CD3,APC rat anti-mouse CD4 and PE rat anti-mouse CD8a antibodies at different concentrations
2.3 红细胞裂解条件的确定
由图2可知,裂解2次的样品在FSCvs.SSC图中P2门内的淋巴细胞占比较高,且门前面的杂质碎片信号较少,白细胞亚群维持基本形态,整体裂红效果稍优于1次裂解效果;其中裂解2次、每次5 min和裂解2次、每次8 min效果相当,故选择裂解2次、每次5 min作为适宜的裂红条件。
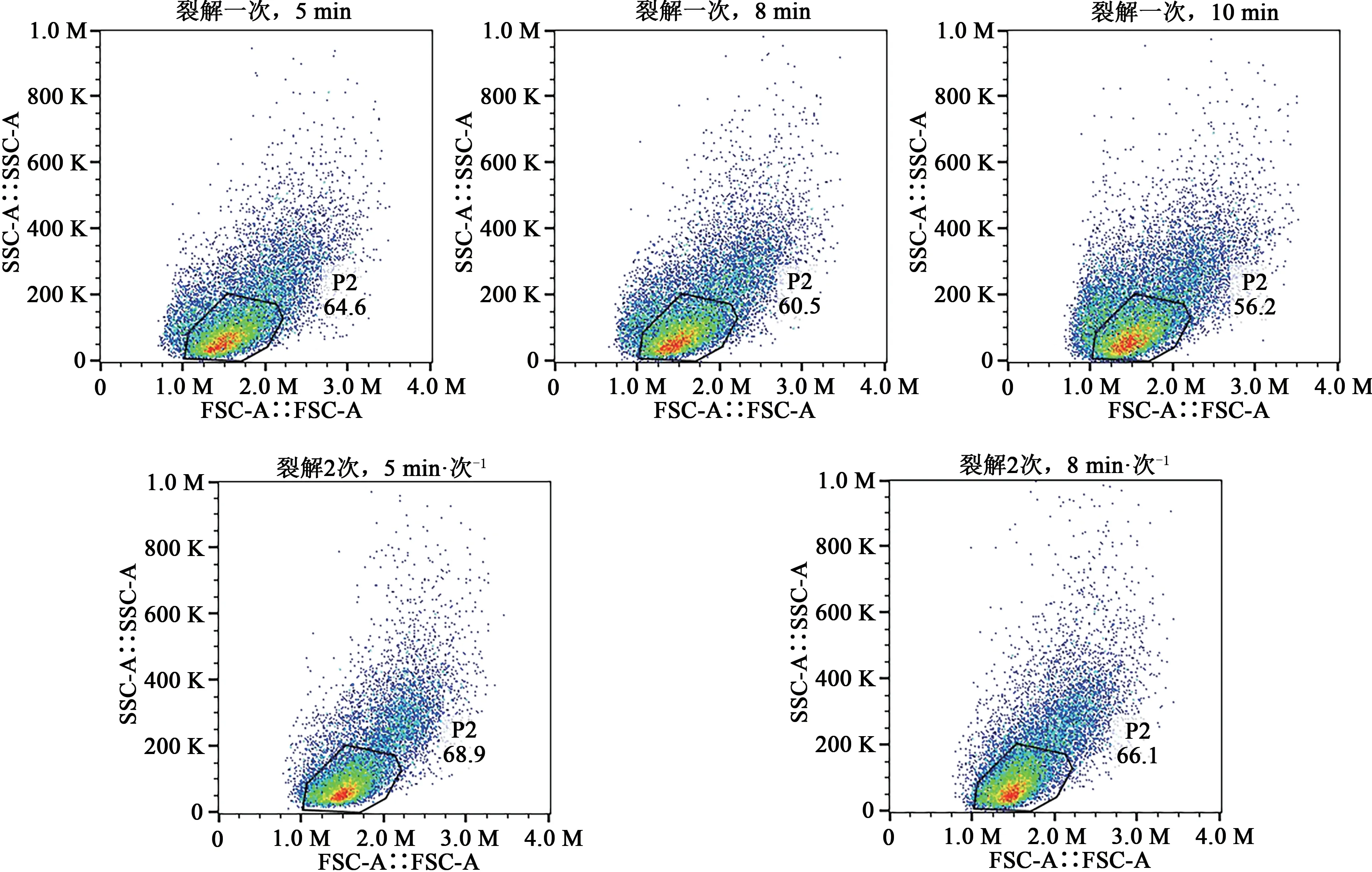
图2 不同裂解条件下的FSC vs.SSC图Fig.2 FSC vs.SSC diagram in different lysis conditions
2.4 样本精密度分析
由表2可知,6份样品3个指标批内差异的CV<15%。由表3可知,3 d连续检测3个指标的批间差异CV<15%。以上研究表明,优化后实验方法的精密度符合规定的合格标准。
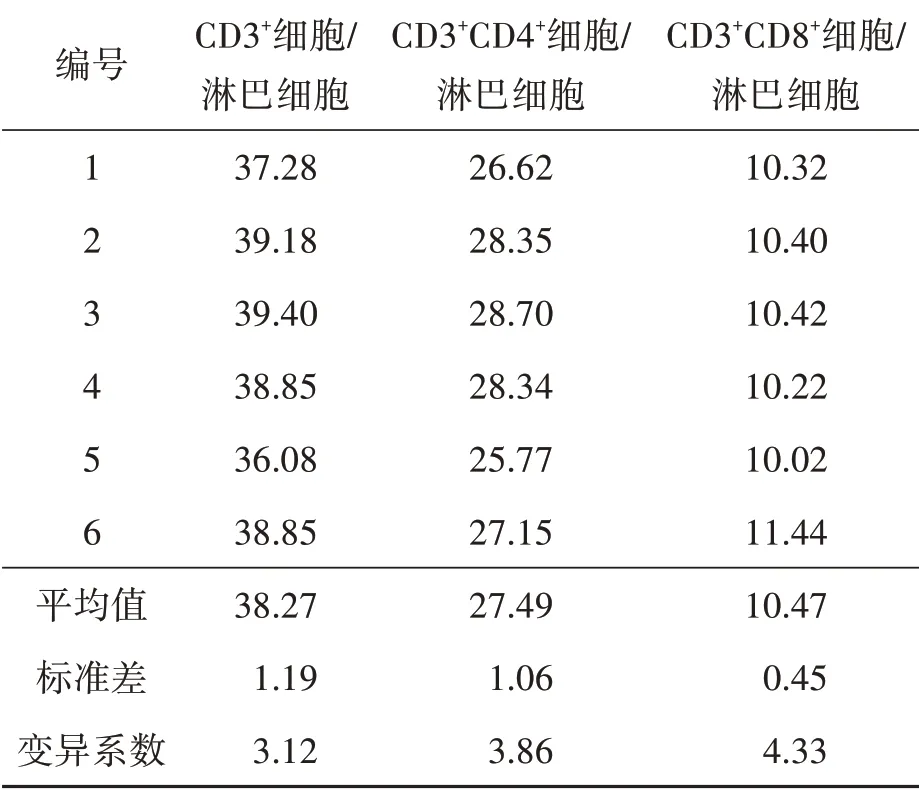
表2 批内差异结果Table 2 The results of intra-batch difference %
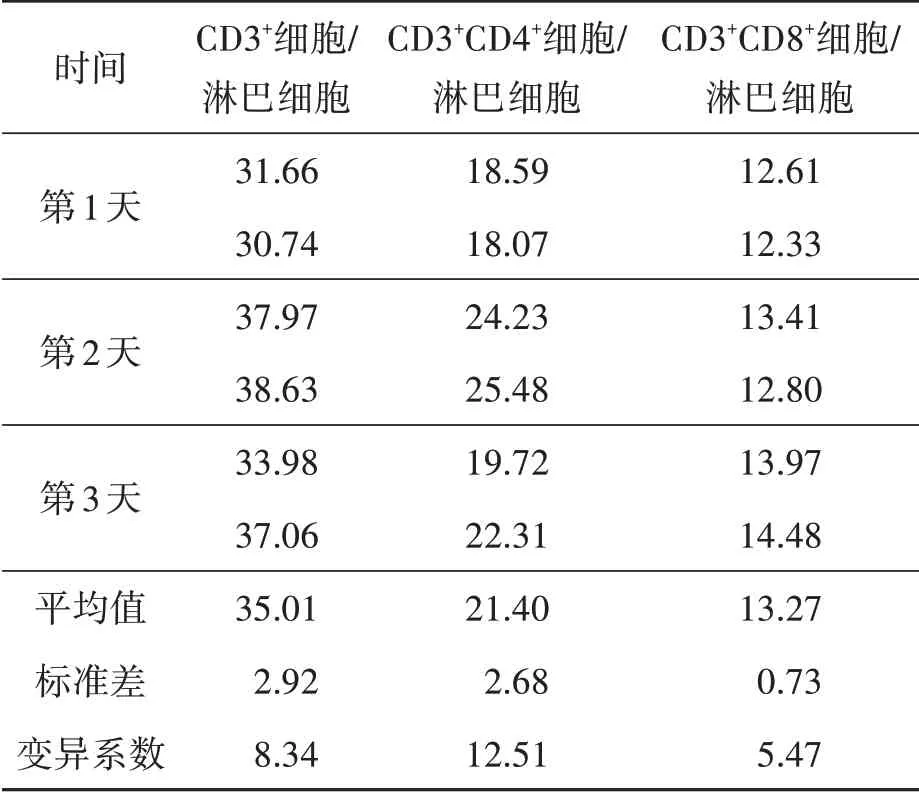
表3 批间差异结果Table 3 The results of inter-batch difference %
2.5 样本稳定性结果分析
经t检验差异分析表明,CD3+细胞/淋巴细胞、CD3+CD4+细胞/淋巴细胞和CD3+CD8+细胞/淋巴细胞3个指标在不同的放置条件下的差异性相似,即无论是4℃放置24 h还是室温放置24 h后血样染色处理的检测结果与采样后立即检测的结果差异均有统计学意义(P<0.05);染色处理后样本于4℃放置24 h复检结果与立即检测结果差异无统计学意义(P>0.05),见图3。以上结果表明采集后的血样在染色处理后立即上机检测和染色处理后于4℃放置24 h内检测,3个指标的变化不明显,即如果血样不能立即检测,应染色处理后放于4℃,24 h内进行检测,结果可靠。
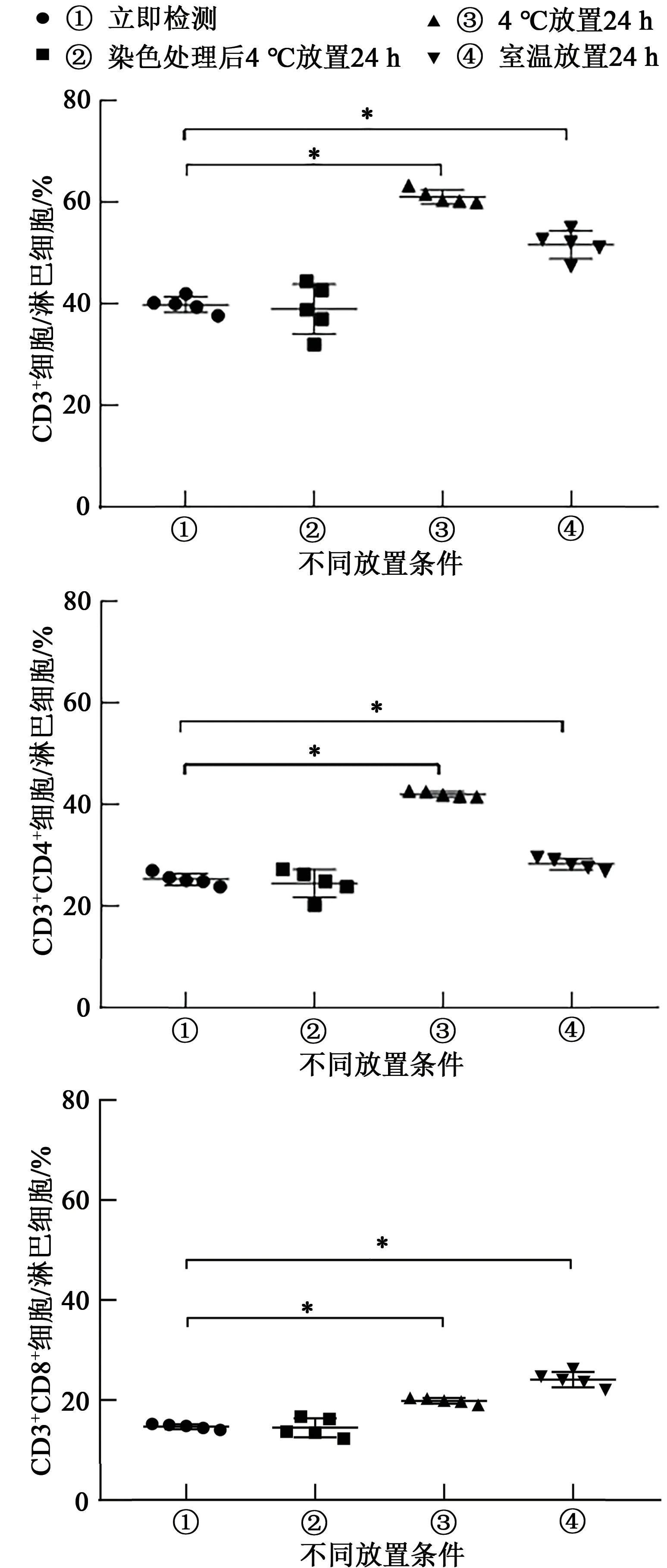
图3 血样在不同放置条件下检测CD3+细胞/淋巴细胞、CD3+CD4+细胞/淋巴细胞和CD3+CD8+细胞/淋巴细胞的结果Fig.3 The results of CD3+/lymphocytes,CD3+CD4+/lymphocytes and CD3+CD8+/lymphocytesof blood samples tested under different placement conditions
3 讨论
研究表明,微量全血可以解决临床上特殊病患抽血困难、血标本不足等难题[12]。本研究中样品体积优化后为50 μL,与相关报道中血样体积一致,对临床检测方法有借鉴意义,且在临床前检测中也更符合实验动物伦理福利中的减少原则。近两年抗肿瘤抗体药物研究较多,其中药效评价中需要构建免疫系统人源化小鼠模型[13],用流式检测外周血T淋巴细胞占比时,50 μL血液可以降低对操作人员的要求和对重度免疫缺陷小鼠的应激反应。
流式抗体滴定可以很好地消除非特异性抗体结合[14],一方面能够提高实验结果的精确性,另一方面可以节约实验成本,但由公司出售或由学术团体描述的近50%抗体不能直接使用推荐用量[15];而且,抗体存在批次间差异,即使是货号相同,批号不同的抗体,也会有8.8%的抗体CV值超过20%[16]。对于小鼠髓系细胞表面分子CD11b,说明书推荐的抗体浓度与滴定的最佳抗体浓度并不一致[3]。本研究通过用3个不同浓度荧光抗体滴定50 μL抗凝血,选择信噪比较大的浓度作为滴定的最佳工作浓度,结果表明,APC rat anti-mouse CD4抗体最优工作浓度与说明书推荐的一致,为1.25 μg·mL-1;FITC rat anti-mouse CD3抗体最优工作浓度是1.25 μg·mL-1,而说明书推荐浓度是2.50 μg·mL-1;PE rat anti-mouse CD8a抗体的最优工作浓 度为5 μg·mL-1,而 说明书推荐 浓度是2.5 μg·mL-1[17]。提示流式检测的相关实验人员,在使用抗体前需要根据具体的实验目的和样本对抗体进行滴定,以区分抗原阴性细胞和抗原阳性细胞,从而提高检测结果的准确性。
流式检测全血样品去除红细胞的方式一般分为红细胞裂解法和密度梯度离心分离法,而密度梯度离心法需要血量较大且会造成潜在的细胞丢失[12]。本研究中使用红细胞裂解液,从裂解时间(5、8、10 min)和裂解次数(1次和2次)上进行了对比,结果发现,裂解2次的样品淋巴细胞门前面的杂质碎片信号比较少,白细胞亚群能够维持基本形态,效果稍优于1次裂红效果,裂解2次、每次5 min和裂解2次、每次8 min效果相当,因此选择裂解2次、每次5 min作为本研究的裂红条件。市面上有多种红细胞裂解液,研究人员需要摸索适合实验需求的裂解条件,充分裂解红细胞可以准确提高淋巴细胞的比例。
方法学验证对于检测结果的准确性和可重复性至关重要,目前流式细胞术的方法学验证多应用于临床检测[18]。本研究的批内精密度即通常采用的重复性,由变异系数量化,国际血液标准化委员会对临床样本分析内重复性的共识建议为CV<10%[19]。本研究虽然是临床前样本,但研究中3个指标(CD3+细胞/淋巴细胞、CD3+CD4+细胞/淋巴细胞、CD3+CD8+细胞/淋巴细胞)的批内CV值分别为3.12%、3.86%和4.33%,均小于10%,表明优化后方法的重复性良好,为制定该类实验方法的标准操作手册提供了可能。
2011年发布的《流式细胞术检测外周血淋巴细胞亚群指南》[20]指出,临床血液样品采集后应立即检测,不能立即检测的标本应保存于室温(18~25℃)环境中;有文献[21]报道,在4℃条件下血细胞参数的稳定性优于室温;也有报道表明,临床抗凝全血无论放置在4℃还是在室温下,48 h内的检测结果都是可靠的[22]。为应对无法及时上机检测的突发情况,很多科研人员和临床检测从业者选择用多聚甲醛固定样品,在确定样品稳定性的一段时间内上机检测[5,23]。但由于甲醛交联蛋白的增加,使蛋白苯环结构上的抗原决定簇发生改变,可能降低抗原的敏感性[24]。本研究中未使用多聚甲醛进行固定,样本稳定性结果表明,血样在采集染色处理后立即检测或者染色处理后于4℃放置24 h内检测稳定性变化不明显,差异不显著,表明应用本研究所优化的方法,即使血样处理后不能立即上机,也不需要用多聚甲醛固定,置于4℃可以保持24 h内检测结果可靠,且简化了试验步骤,节约了试验时间。
综上所述,本研究对流式检测外周血T淋巴细胞亚群的方法进行了系统性优化并对优化的方法进行了初步验证,方法的重复性良好,不用固定样本稳定性也可以保持24 h,且研究中的优化指标均是影响流式检测外周血样本准确性的重要因素,不仅可以为多参数流式更准确深入地研究血液细胞的功能提供思路,也可以为流式细胞术分析临床血液淋巴细胞免疫表型的方法学研究提供参考依据。
