十味参蛇洗剂微生物限度检查方法的建立及验证
2022-10-11潘磊肖丽丽
潘磊,肖丽丽
1.江西中医药大学,江西 南昌 330004;2.江西省皮肤病专科医院,江西省皮肤病临床医学研究中心,国家皮肤与免疫疾病临床医学研究中心,江西省皮肤病研究所,南昌大学附属皮肤病医院,江西 南昌 330001
十味参蛇洗剂为江西省皮肤病专科医院的医院外用制剂,处方由苦参、蛇床子、地肤子、黄柏、金银花、连翘、百部、乌梢蛇、蜂房、千里光等十味药材组成。具有清热除湿,祛风止痒,解毒杀虫的作用。其中处方中大部分药材中含有抑菌成分[1-8],如君药苦参中的苦参总碱、苦参碱、氧化苦参碱、槐果碱等成分对金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌及白色念珠菌均具有一定程度的抑制效果[1]。此外中药制剂处方中的饮片大多来源于植物及动物等,极易受到微生物的污染,是中药制剂微生物污染的重要来源之一。本文根据《中国药典》2015 版四部通则[9]中关于微生物检查的规定和方法,对十味参蛇洗剂的微生物限度检查方法进行研究,并对建立的方法进行了验证,确保该医院制剂的微生物限度检查方法符合规定,能有效地反映该制剂中所含微生物的真实情况,确保用药安全。
1 仪器与材料
1.1 仪器设备
BT125D 电子天平,赛多利斯科学仪器(北京)有限公司;LMQ.C-50E 立式灭菌器,山东新华医疗器械股份有限公司;ZW-2008 智能集菌仪,琪摩(上海)电子科技有限公司;SJ-CJ-1D 超净工作台,苏州苏洁净化设备有限公司;BHC-1300 ⅡA2生物安全柜,阿尔泰实验设备有限公司;PYXDHS-55-40 细菌培养箱,上海跃进医疗器械一厂;MJ-250BSH-Ⅱ霉菌培养箱,上海新苗医疗器械制造有限公司。
1.2 菌种
金黄色葡萄球菌[CMCC(B)26003],批号:9a2-2;枯草芽孢杆菌[CMCC(B)63501],批号:2a27-2;白色念珠菌[CMCC(F)98001],批号:2a21-2;铜绿假单胞菌[CMCC(B)10104],批号:2a28-2;黑曲霉[CMCC(F)98003],批号:0A1004;以上菌种皆购自中国食品药品检定研究院。各试验菌株均为第三代工作菌。
1.3 培养基与稀释液
沙氏葡萄糖琼脂培养基(批号:20190808);胰酪大豆胨琼脂培养基(批号:20190907);甘露醇氯化钠琼脂培养基(批号:20190322);溴化十六烷基三甲铵琼脂培养基(批号:20190228);以上培养基均由北京奥博星生物技术有限责任公司生产。胰酪大豆胨液体培养基(批号:190708,上海博微生物科技有限公司);0.9%无菌氯化钠溶液(自制,氯化钠,批号:190911,西陇科学股份有限公司)。
1.4 供试品
十味参蛇洗剂(批号:200901、200902、200903,规格:每1 mL 相当于饮片0.425 g),均由江西省皮肤病专科医院提供。
2 实验方法
2.1 试验用菌液的制备
根据2015 版《中国药典》四部通则1105及1006 要求,将各试验菌制成菌悬液,浓度在50~100 cfu/mL 左右。
2.2 供试品的制备
十味参蛇洗剂为水溶性液体制剂,按规定可使用原液作为供试品。另取10 mL 供试品,用稀释液(0.9%无菌氯化钠溶液)稀释制成1∶10 供试液;
2.3 微生物限度检查方法研究
2.3.1 预实验 根据2015 版《中国药典》四部1105要求,选择对培养环境要求较高的枯草芽孢杆菌进行需氧菌检查,同时选择生长曲线较快进入稳定期的白色念珠菌[10]进行霉菌和酵母菌计数检查,进行预实验。预实验结果见表1。
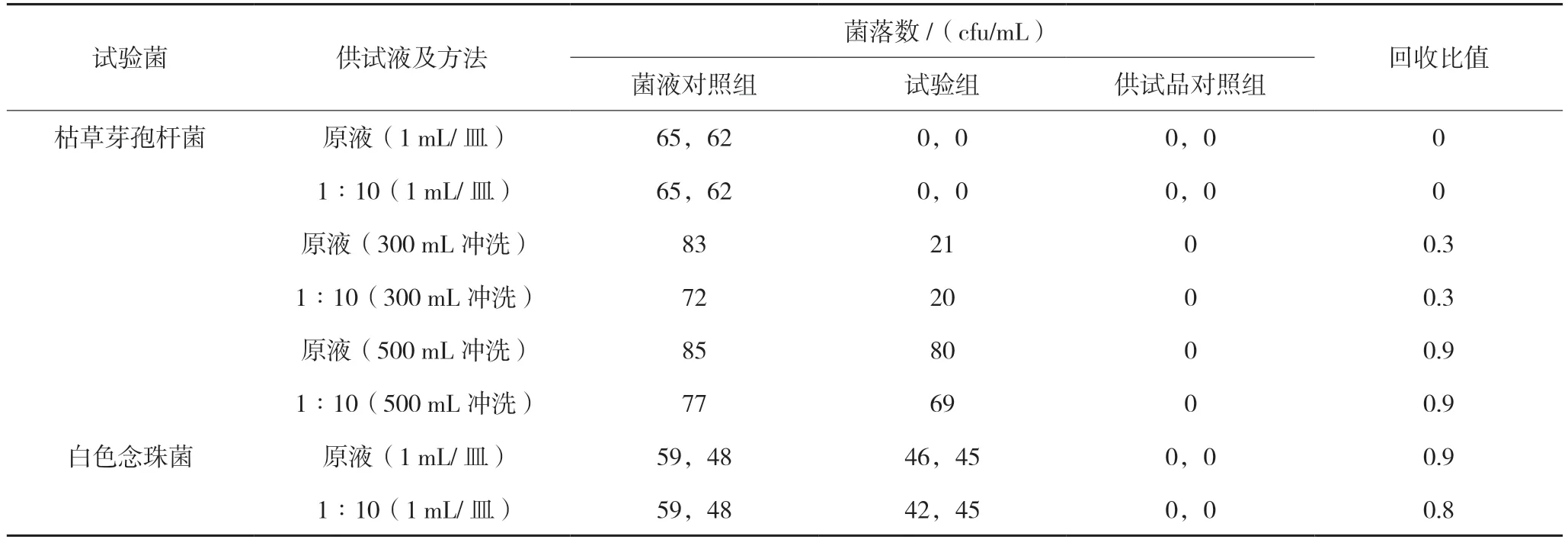
表1 预实验结果
预实验结果显示采用平皿法时十味参蛇洗剂会抑制枯草芽孢杆菌的生长,而对白色念珠菌抑制效果不明显。当以薄膜过滤法(原液、1∶10 供试液)检查需氧菌总数,冲洗量为300 mL 时,枯草芽孢杆菌的回收比值均为0.3,不在规定的范围内。冲洗量为500 mL 时,原液和1∶10 供试液回收比值均为0.9,所以进行需氧菌总数检查时采用薄膜过滤法(原液、1∶10 供试液,500 mL 冲洗,每次100 mL);进行霉菌及酵母菌总数检查时采用平皿法(原液、1∶10 供试液)。
2.3.2 需氧菌总数计数试验 分别取供试品原液及1∶10 供试液各1 mL,按照薄膜过滤法,用500 mL稀释液(0.9%无菌氯化钠溶液)进行冲洗,将100 cfu 左右的试验菌加入最后进行冲洗的稀释液中,待水分滤干后,取出滤膜,立即贴于胰酪大豆胨琼脂培养基平板上,在30 ℃~35 ℃进行1 d~3 d 的培养,每日进行观察。以稀释液替代菌液,按相同方法制备供试品对照组样品。另用稀释液替代供试液,按相同方法制备菌液对照样品。重复3 次上述试验。具体结果如表2 所示。表2 结果表明使用薄膜过滤法(原液、1∶10供试液,500 mL 冲洗,每次100 mL)进行需氧菌总数计数检测,所有试验菌的回收率都在药典要求的0.5~2.0 的范围内。
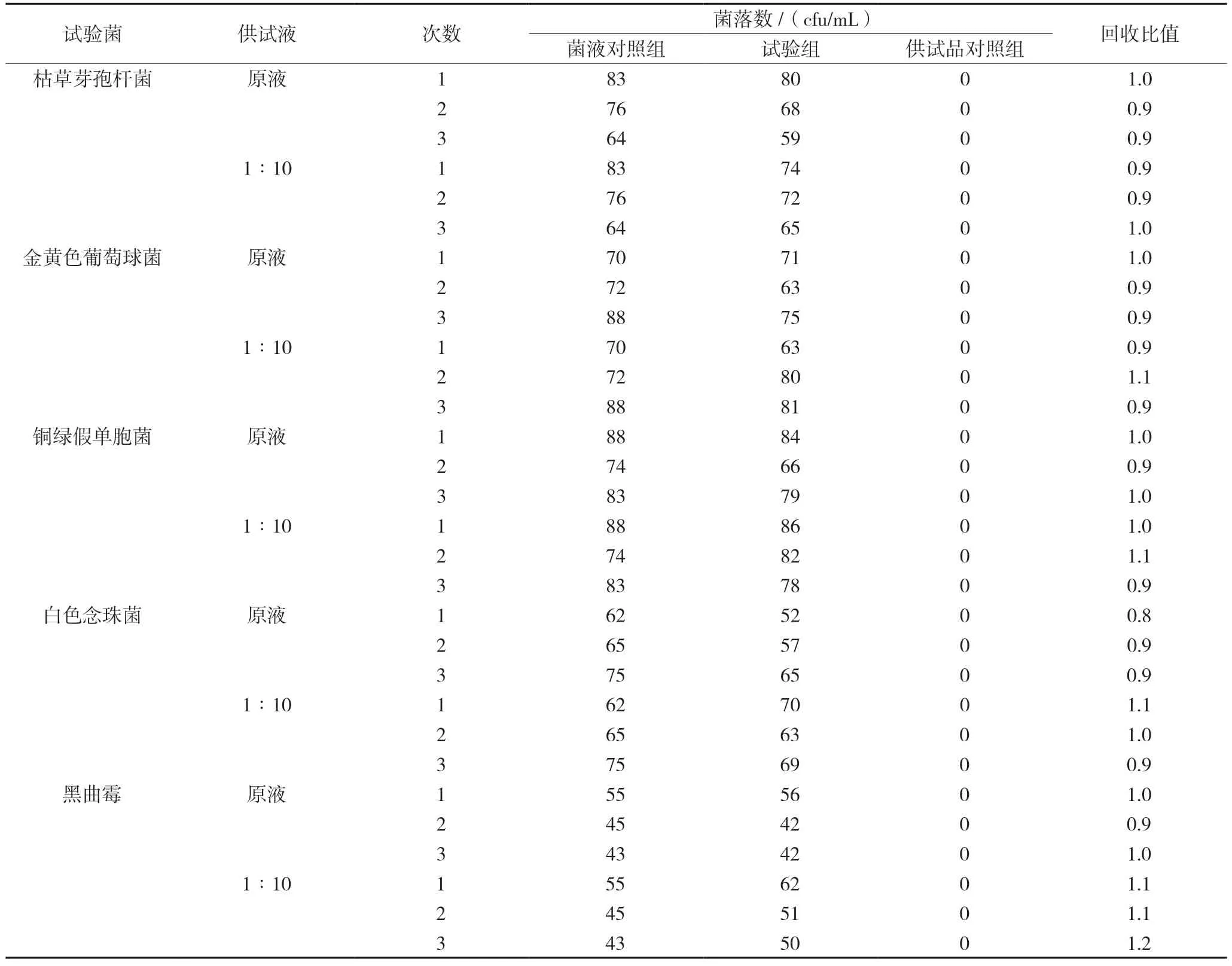
表2 需氧菌总数计数试验结果(n=3)
2.3.3 霉菌和酵母菌总数计数 分别取供试品原液及1∶10 供试液各9.9 mL,加入0.1 mL 适宜浓度的试验菌,使得每1 mL 供试液中试验菌含量不超过100 cfu,混匀。将1 mL 供试液注入平皿中,然后立即将适量的沙氏葡萄糖琼脂培养基倒入平皿;在20 ℃~25 ℃培养箱中进行1 d~5 d 的培养,每日进行观察。以稀释液替代菌液,按相同方法制备供试品对照组样品。另以稀释液替代供试液,按同样方法制备菌液对照组样品。重复3 次上述试验。结果如表3 所示。
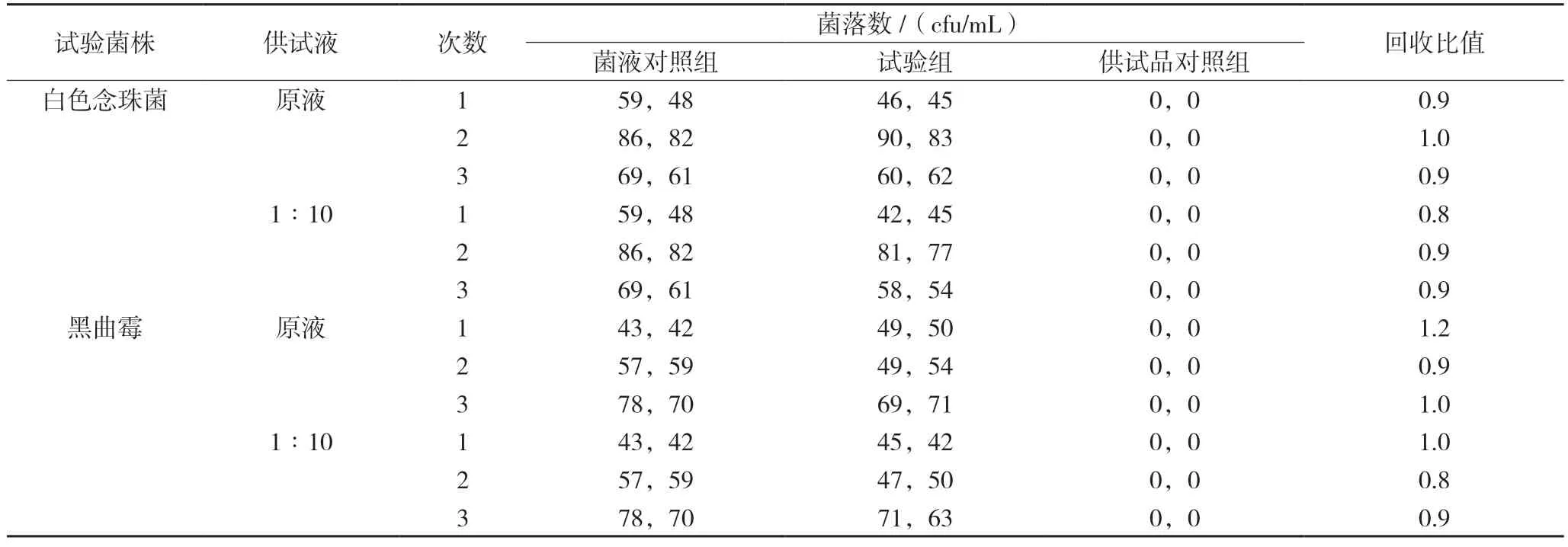
表3 霉菌和酵母菌总数计数试验结果(n=3)
表3 结果显示白色念珠菌和黑曲霉的菌数回收比值均在药典规定范围内,所以可以使用平皿法进行霉菌和酵母菌总数计数检查。
2.3.4 控制菌检查 十味参蛇洗剂为皮肤给药制剂,根据《中国药典》2015 版四部中规定以铜绿假单胞菌及金黄色葡萄球菌作为试验菌进行控制菌检查的研究。
按照药典规定的金黄色葡萄球菌检查方法操作,制备供试品样品,按要求进行培养观察。同时以稀释液替代供试液,按相同的方法操作,制备阴性对照样品,以消除稀释液及培养基的干扰。观察其菌落的生长情况。试验结果见表4。
按照药典规定的铜绿假单胞菌检查方法操作,制备供试品样品,并按要求进行培养观察。同时以稀释液替代供试液,按相同的方法操作,制备阴性对照样品,以消除稀释液及培养基的干扰。观察其菌落的生长情况。试验结果见表5。
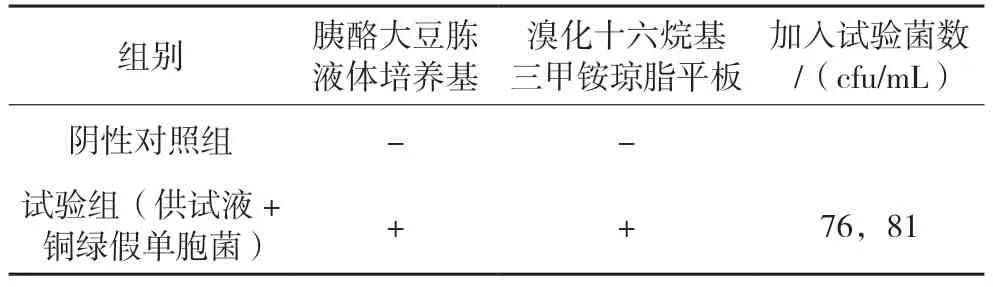
表5 铜绿假单胞菌检查结果
根据表4、5 的结果可以看出,十味参蛇洗剂对金黄色葡萄球菌以及铜绿假单胞菌的抑菌效果不显著,控制菌检查可采用常规方法进行。
2.4 三批样品的微生物限度检查
为验证所建的微生物限度检查方法的是否适用,对三个不同批次的十味参蛇洗剂进行微生物限度检查,结果显示建立的微生物限度检查方法适用于十味参蛇洗剂。结果见表6。
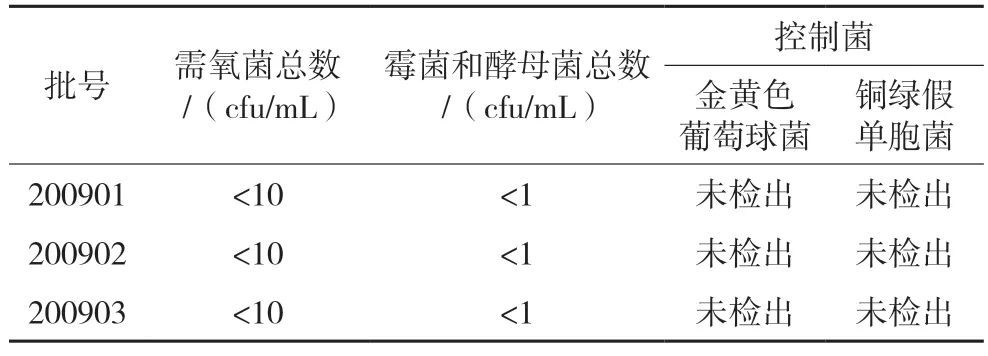
表6 三批样品微生物限度检查结果
3 讨论
供试品原液及1∶10 供试液采用薄膜过滤法检测需氧菌计数总数时,菌数回收比值均在规定范围内,但由于十味参蛇洗剂中有轻摇易散的沉淀,供试品原液过滤时,速度缓慢,且在薄膜上保留颜色较深,在观察菌落生长情况时存在一定的干扰,故在最终确定十味参蛇洗剂需氧菌计数总数检测方法中选用1∶10 供试液采用薄膜过滤法进行检测。使用平皿法(原液)进行霉菌和酵母菌总数进行检测,控制菌检查方法为常规法。此外本研究建立的微生物限度检查方法同样适用于2020 版《中国药典》的相关规定[11]。
