辛烯基琥珀酸芋头淀粉酯的制备工艺优化及理化性质分析
2022-10-11孙梦雯莫晓峰王亚娟
孙梦雯,莫晓峰,陈 樱,王亚娟, ,仇 丹,
(1.宁波工程学院材料与化学工程学院,浙江宁波 315211;2.浙江海洋大学食品与药学学院,浙江舟山 316022)
淀粉是食品中主要的能量供应物质,也是极其重要的工业原料。天然淀粉往往通过改性来获得一系列用于各种用途的功能特性,如溶解性、耐热性、乳化性等。自从Caldwell 等首次申请淀粉与二羧酸酸酐反应的专利以来,国内外的学者就开始了辛烯基琥珀酸淀粉酯(OSS)的相关研究。OSS 因具有更高的粘度、更好的糊状透明度、冻融稳定性和优异的乳化性能,已广泛被应用于肉制品、饮料、制药和微胶囊等领域。
芋头是一类具有保健价值的根茎类食物,主要产于热带亚热带地区,被认为是世界上第五大根作物。芋头中淀粉含量丰富,约占干基重的70%~80%;芋头淀粉颗粒小,粒径只有1~5 μm,淀粉粒径越小,经辛烯基琥珀酸酐(OSA)酯化后的乳化性越强,稳定油滴的能力也更强。另外,芋头淀粉中直链淀粉含量低,膨胀性强,因此被广泛应用在食品和制药工业。然而,芋头产地是影响其中淀粉性能的因素之一。奉化芋头为国家地理标志产品,长期以来备受瞩目,项目组之前的研究表明,奉化芋头淀粉的颗粒较其他品种及产地的小,大部分介于0.5~2 μm,且其中快消化淀粉质量分数较高,可达71.1%,而同为浙江产地的温岭芋头快消化淀粉的质量分数仅为64.8%。
目前关于芋头淀粉的研究多集中在其提取、理化性质等方面,而其OSA 酯化工艺的研究相对较少。由于奉化芋头淀粉中较低的直链淀粉含量、极小的粒径及微观结构有别于常规芋头淀粉,因此其辛烯基琥珀酸酯的反应工艺及理化性质有待进一步深入研究。此外,现有关于辛烯基琥珀酸芋头淀粉酯(OSTS)的研究,均以滴定法测定取代度(degree of substitution,DS),而该方法忽略了淀粉酯中游离的辛烯基琥珀酸的含量,从而降低了结果的准确性。
奉化芋头作为当地的一种丰富的经济作物,研究奉化芋头淀粉的辛烯基琥珀酸酯化工艺,有利于促进其在食品、医药等领域的应用。因此,本研究以奉化芋头为原料,采用水磨碱提法提取其中的淀粉,以OSA 为酯化剂制备辛烯基琥珀酸芋头淀粉酯(OSTS),使用高效液相法为检测手段,以芋头淀粉酯的DS 为响应值,通过单因素实验确定所选因素的影响规律,然后采用响应面法优化最佳酯化工艺。最后,对比了奉化芋头淀粉及其酯化产物的部分理化性质。
1 材料与方法
1.1 材料与仪器
奉化芋头 宁波当地菜市场;辛烯基琥珀酸酐(OSA) 上海麦克林生化科技有限公司;二甲亚砜DMSO 色谱纯,霍尼韦尔有限公司;乙腈 色谱纯,天津赛孚瑞科技有限公司;三氟乙酸 色谱纯,南京国晨化工有限公司;其他化学试剂 均为分析纯。
Agilent 1260 高效液相色谱仪、ZORBAX-SBC(5 μm,4.6×150 mm)色谱柱 安捷伦科技有限公司;D8 AdvanceX 射线衍射仪 德国Bruker;S4800扫描电镜 日本日立公司;OAC 15 水接触角测试仪德国Dataphysics 仪器有限公司。
1.2 实验方法
1.2.1 芋头淀粉(TS)提取工艺实验方法 参考Jiang等并稍作修改。具体操作如下:芋头洗净去皮切块,置于烧杯中,于4 ℃冰箱中用2.5 g/L 的氢氧化钠溶液浸泡12 h。使用搅拌机打浆,依次过筛3 次(网筛为70、270、400 目),收集滤液静置沉淀后,于3000 r/min 下离心10 min。去除液体及沉淀上层黄色的蛋白质,加入蒸馏水,搅拌形成悬浊液,再次于3000 r/min 下离心10 min,重复此步骤到上层无黄色蛋白层为止,用0.1 mol/L HCl 调至中性,再重复离心步骤3 次。将沉淀放入40 ℃烘箱中烘烤48 h,烘干后用研钵磨成粉,过70 目筛,装袋备用。
1.2.2 辛烯基琥珀酸芋头淀粉酯(OSTS)制备工艺实验方法 参考Bai 等并做适量修改。称取4.0 g芋头淀粉于四口烧瓶中,加适量的水配制成一定浓度的淀粉乳液,搅拌10 min 后用3% NaOH 溶液调节淀粉乳pH 至一定值,继续搅拌20 min,使用滴液漏斗将淀粉干基质量3%的辛烯基琥珀酸酐(OSA)(使用5 倍的无水乙醇稀释)逐滴滴加到淀粉乳中,特定温度下反应一定时间,期间使用自动电位滴定仪检测反应pH,使之维持在特定值,而后使用0.1 mol/L 盐酸调节pH 至6.0。将混合物过滤,使用去离子水及无水乙醇,各洗涤3 次,然后冻干得到OSTS。
1.2.3 单因素实验 参照徐琼等关于马铃薯淀粉酯化的条件,以取代度DS 为响应值,依次考察淀粉乳浓度、反应pH、反应温度及反应时间对DS 的影响。固定淀粉乳浓度35%、pH8.5、反应温度35 ℃、时间3 h 中的三个因素水平值,对第四个因素进行单因素实验。实验因素条件为反应温度20、30、40、50 ℃,反应时间1、2、3、4 h,淀粉乳浓度30%、35%、40%、45%,反应pH 为7.5、8.0、8.5、9.0。
1.2.4 响应面试验优化 在单因素实验的基础上明确芋头淀粉的最佳提取因素范围,采用Box-Behnken试验设计原理设计响应面,其因素与水平见表1。

表1 Box-Behnken 试验因素水平设计Table 1 Factors and levels of Box-Behnken
1.2.5 高效液相色谱法测定OSTS 的取代度 使用本课题组之前的高效液相方法测定。液相色谱参数:Agilent1260 高效液相色谱(HPLC),色谱柱为ZORBAX-SB-C柱;流动相:乙腈和水(0.1% 三氟乙酸(TFA))的混合物(45:55,v/v);检测波长为200 nm;流速1 mL/min;检测温度为30 ℃;进样量20 μL。
总OS 含量测定:取0.5000 g OSTS(干重),加入20 mL 4 mol/L 氢氧化钠,搅拌过夜,取4 mL 碱液到50 mL 容量瓶中,加入20 mL 1 mol/L 盐酸,用乙醇定容,过滤后用HPLC 检测。
游离OS 含量测定:取0.2500 g OSTS 样品(干重),加入10 mL 甲醇,磁力搅拌1 h,然后4000 r/min离心10 min,取上清液1 mL 于取样瓶,与1 mL 水(预先调到pH3)混合,过滤后进行HPLC 分析。
游离OS(%OS),总OS(%OS),取代OS(%OS),计算公式如下:

式中:W和W分别是游离的OSA 和总的OSA 的质量,代入标准曲线Y=0.0009x-0.3848计算(其中Y 为OSA 含量,μg;x 为峰面积);W 为检测的OS 淀粉的质量;210 和162 分别是OSA 和葡萄糖单元的分子量;1000 和12500 分别是稀释倍数。
1.2.6 X-射线衍射分析(XRD) 取适量样品平铺于样品盘的凹槽中,将样品表面平整使其与样品盘外表面相平,而后将样品盘置于仪器中,测试波长为1.5 Å的单色Cu-Ka 射线,测试条件为管压50 kV、管流27 mA,扫描区域为5°~60°。
1.2.7 扫描电镜分析(SEM) 芋头淀粉酯化前后的颗粒形态使用场发射扫描电子显微镜进行观测:取微量淀粉粉末样品,使用导电胶将其均匀分散于载物台上,洗耳球吹去未粘牢的样品。该样品台置于离子溅射喷镀仪中镀金,处理好后的样品放入扫描电镜样品室观察并拍照。
1.2.8 接触角的测定测试方法 参照Chi 等,并做适量修改。称取0.05 g 样品加入5 mL 二甲亚砜DMSO,75 ℃水浴中搅拌使之完全溶解。然后滴管滴到玻片上,在80 ℃烘箱中干燥2 h 后,测接触角。
1.3 数据处理
实验所得数据均为三次实验的平均值±标准差。使用软件Design-Expert(Version 10.0.5,State-Ease Inc.,Minneapolis,Minnesota,USA)对数据进行方差分析。
2 结果与分析
2.1 单因素实验结果
2.1.1 温度对OSTS 取代度的影响 酯化反应温度对OSTS 的取代度影响见图1。由图1 可看出,温度从20 到40 ℃,DS 逐渐增加,温度上升到50 ℃时DS 下降。主要原因是酯化反应为吸热反应,温度较低时,不利于酯化反应的发生,随着温度的升高,OSA 在溶液中的扩散增强,其与淀粉分子的接触及反应效率均会提高,但温度过高时,OSA 易发生水解,不利于反应的进行。因此反应温度优选40 ℃。

图1 温度对OSTS 取代度的影响Fig.1 Effect of the temperature on the degree of substitution of OSTS
2.1.2 时间对OSTS 取代度的影响 酯化反应时间对OSTS 的取代度影响见图2。图2 结果显示,随着反应时间延长,DS 也呈先增大后减小的趋势,这是因为OSA 在水相体系中除了发生酯化反应外,也会发生自身水解反应。3 h 后,可能是OSA 被消耗掉,因此不再发生酯化反应。在Lan 等关于美人蕉淀粉的OSA 酯化研究中也观察到类似的结果。
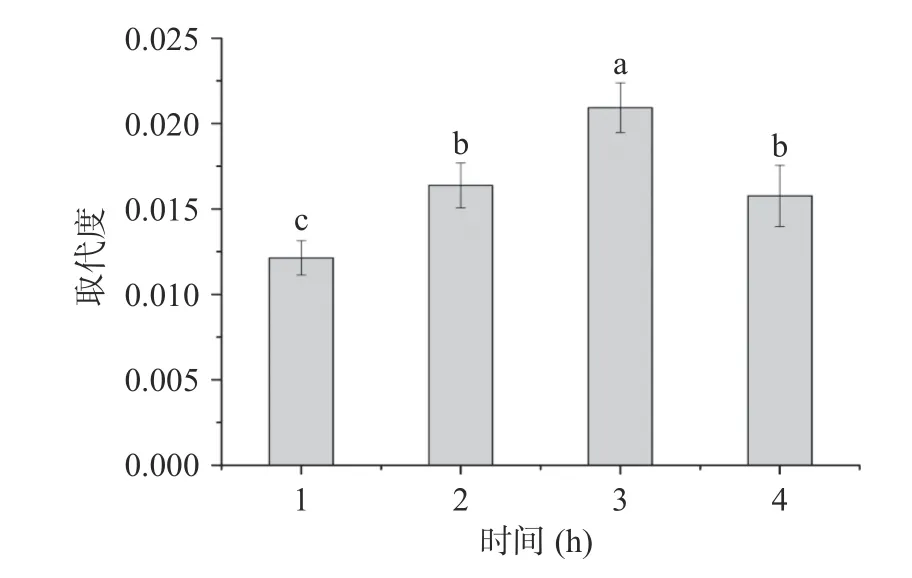
图2 时间对OSTS 取代度的影响Fig.2 Effect of the time on the degree of substitution of OSTS
2.1.3 淀粉乳浓度对OSTS 取代度的影响 图3 为不同淀粉乳浓度时制备的OSTS 中的取代度,由图3可知,随着淀粉浓度的增加,DS 呈现先增大后减小的趋势。这是由于淀粉浓度的增加提高了反应体系中OSA 与淀粉颗粒接触及反应的概率,使酯化反应朝着有利的方向进行。当TS 浓度高于40%时,淀粉浓度的增加使得溶液粘度高,限制了淀粉的非晶态区与OSA 的接触。
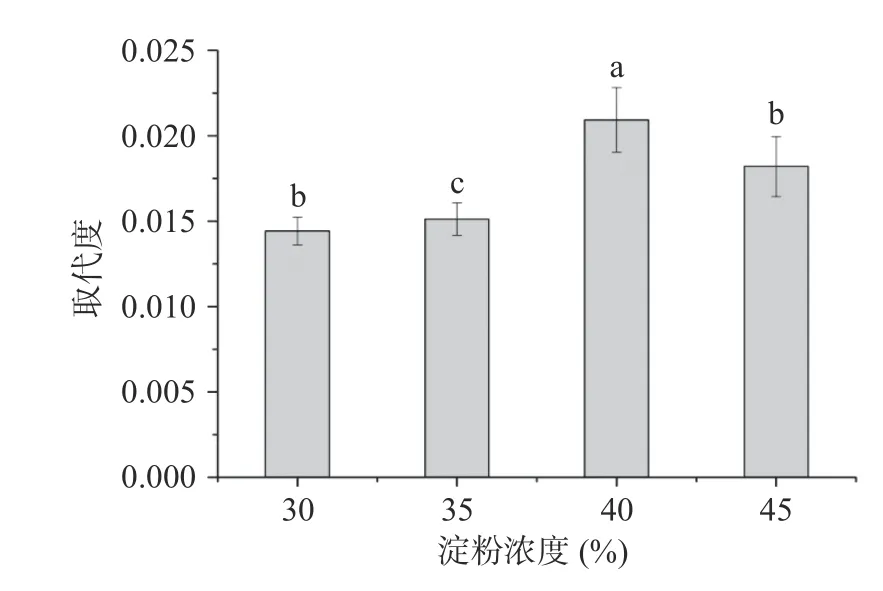
图3 淀粉乳浓度对OSTS 取代度的影响Fig.3 Effect of the starch concentration on the degree of substitution of OSTS
2.1.4 pH 对OSTS 取代度的影响 由图4 可知,随着pH 的增大,取代度也先增大后减小,当溶液pH为8.0 时,DS 达到最大值,当pH 进一步增加到8.5时,DS 下降,说明高pH 对酯化反应有一定的不利影响。此外,淀粉与OSA 的酯化反应是可逆亲核取代反应,pH 大于8 时,OSA 偏向水解趋势,当pH 小于8 时,溶液的碱性不能有效激活淀粉中羟基的反应活性,即不能形成亲核基团,取代度较低。

图4 反应pH 对OSTS 取代度的影响Fig.4 Effect of pH value on the degree of substitution of OSTS
2.2 响应面试验结果
在单因素实验结果的基础上,选择pH(A)、时间(B)、温度(C)和淀粉浓度(D)四个因素为自变量,相应OSTS 的DS 为响应值(Y),采用响应面方法探究芋头淀粉在不同条件下的取代度,试验方案及结果见表2。
根据表2 中的结果,采用Design-Expert 10.0 分析软件对实验数据进行多元线性回归,得到取代度(Y)与pH(A)、时间(B)、温度(C)和淀粉浓度(D)之间的二次多元回归方程为:

表2 Box-Behnken 试验设计结果Table 2 Design and results of Box-Behnken

通过软件对上述结果进行方差分析,结果见表3。
决定系数R表示方程的拟合性,R越接近1,表明该方程拟合的越好。由表3 可知,R=0.9871,说明该模型可以解释98.71%的实验数据,即影响DS 的因素98.71%来自淀粉浓度、pH、反应时间和反应温度这四个因素。模型的=76.24,<0.0001,极显著,说明模型良好可用。经过方差分析,四个因素对DS 的影响的主次顺序是:D>A>C>B,即淀粉乳浓度的影响最大,其次是反应的pH,再次为反应时间,其中反应温度对取代度的影响不明显。

表3 回归模型的方差分析Table 3 Variance analysis of regression model
利用Design-Expert 10.0 软件进行工艺参数的优化组合,得到芋头淀粉酯化的最佳工艺条件为:反应pH8.26、反应时间2.51 h、温度40.97 ℃、淀粉乳浓度38.68%,此时OSTS 的取代度为0.02072。为了验证模型的有效性,考虑到实际情况将最佳提取条件定为:反应pH8.5、反应时间2.5 h、温度41℃、淀粉乳浓度40%,在此工艺下,OSTS 的DS 为0.02069,此时的取代效率为68.97%,而Yu 等使用莱阳芋头淀粉做OSA 酯化时,当OSA 用量为3%时,其DS 为0.018,相应的取代效率为60%,低于采用本实验所确定的最优条件制备的产物。本实验所得DS与预测值的相对误差为0.14%,两者相比无显著差异,说明该模型合理。
2.3 淀粉酯化前后性质
2.3.1 XRD 分析 图5 为芋头淀粉酯化前后的XRD图,其中数字表示样品的相对结晶度。从图5 可以看出,奉化芋头淀粉的晶型为典型的A 型结晶,即其单峰出现在衍射角2为15°和24°左右,双峰出现在17°~19°左右。而样品OSTS 的衍射峰位并未发生明显偏移,即证明酯化并没有改变芋头淀粉的晶型,与Song 等关于大米、藜麦淀粉的酯化结果相似,即淀粉颗粒的酯化不会改变其原有的晶型。Liu 等研究发现淀粉颗粒有层状结构,即生长环,表层向内为结晶区-非结晶区-结晶区-非晶区交替存在。而在酯化反应时,少量的OSA 可渗透到结晶区,因此导致经酯化后淀粉结晶度的降低,如本实验中芋头淀粉的相对结晶度为19.04%,酯化后降至15.20%。这与Bajaj 等的结果相似,其研究发现高DS 的OSA 酯化芸豆淀粉相对结晶度从38.3%降为18.74%,原因是OSA 反应过程破坏了淀粉的晶体结构。

图5 芋头淀粉及其酯化淀粉XRD 图Fig.5 XRD patterns of TS and OSTS
2.3.2 微观形貌分析 芋头淀粉酯化前后的扫描电镜图见图6,A 为原芋头淀粉,B 为酯化芋头淀粉。比较该图可发现,芋头淀粉的粒径较小(0.5~4 μm),存在团簇现象,颗粒较光滑但向内凹。酯化后的OSTS 仍有团聚体,向内凹程度更明显,颗粒表面粗糙程度增加。这与Yu 等研究相似,即酯化过程中NaOH 对淀粉颗粒表面有一定的腐蚀作用。在酯化反应过程中,OSA 与淀粉颗粒接触,主要与非结晶区反应,使OSA 分布在每一层的非结晶区、通道、颗粒中心空腔中。

图6 芋头淀粉酯化前后不同放大倍率的电镜图Fig.6 SEM images of TS and OSTS with different magnification
2.3.3 接触角分析 接触角θ 可以体现样品的亲水程度,θ 越大代表颗粒疏水性越好。图7 列出了芋头淀粉酯化前后的水接触角,由图可发现TS 为86.2°,与Shao 等测的82°相近;而OSTS 的接触角为120.9°,这与Yu 等的结论相符,芋头淀粉经OSA酯化后其水接触角由25.4°增加到70.1°。的具体值相差较大的原因是测试方法的不同,Yu 等均是直接将淀粉压片,淀粉的结构相对完整,测定的是其表面的疏水性,而本实验中是先将淀粉溶于DMSO中后干燥成膜,在溶解的过程中淀粉的链状分子结构会舒展开,原本在其内部的疏水性基团更多的暴露出来,使得其水接触角更大,但是酯化前后变化趋势相似,即随着OSA 与淀粉反应的发生,淀粉分子中部分羟基被取代,疏水性增强,接触角变大。

图7 芋头淀粉及其酯化淀粉接触角Fig.7 Contact angle of TS and OSTS
3 结论
本实验采用响应面法优化了辛烯基琥珀酸酐酯化芋头淀粉的工艺参数,具体为:淀粉浓度40%,反应温度41℃,反应时间2.5 h,pH8.5,在此条件下酯化得到的实际取代度为0.02069,样品取代效率为68.97%;X 射线衍射及扫描电镜结果表明:芋头淀粉经OSA 酯化后,相对结晶度会降低,但晶型及颗粒表面不会受到明显影响;OSA 酯化后的芋头淀粉疏水性增加。结合芋头淀粉粒径较小的特点,其有望用作Pickering 乳化剂,在食品乳化剂、增稠剂、生物医药和缓释包装等方面具有广阔的应用潜力。
