经皮内镜腰椎间盘切除术治疗经保守治疗无效的腰椎间盘突出症的临床效果
2022-09-29赵锦胜曹汉岐杨寒石
赵锦胜,曹汉岐,杨寒石
(淮安市第二人民医院 骨科,江苏 淮安 223001)
腰椎间盘突出症(lumbar disc herniation,LDH)是临床上较为常见的一种退行性疾病,多发生于老年患者中,该病多由退变和纤维环撕裂等导致,几乎不会因为外力导致[1]。随着我国老龄化加剧,超过5.00%的中老年患者会出现腰腿疼痛,而这些症状好发的疾病就是腰椎间盘突出症[2],临床上一般行保守治疗,但治疗效果不佳,反复治疗后仍要进行手术,以改善患者生活质量。传统的腰椎间盘突出手术由于创口大,术中失血量较多,费用较高,已不被临床所接受[3]。近年来,随着骨科微创领域的发展,经皮内镜腰椎间盘切除术(percutaneous endosopic lumbar discectomy,PELD)在临床中广泛应用,且取得了不错的效果。本研究选择保守治疗无效的LDH 患者,对患者采用PELD治疗,疗效满意。现报道如下:
1 资料与方法
1.1 一般资料
选取2017年3月-2020年12月本院收治的60 例经保守治疗无效的LDH 患者作为研究对象,回顾性分析患者的临床资料。其中,男34 例,女26 例,年龄18~65 岁,平均(39.6±6.2)岁;突出节段:L3/420例,L4/528例,L5/S112例;随访时间12~18个月,平均(14.5±2.0)个月。本研究经医院伦理委员会审核并批准通过。
纳入标准:①临床表现为下肢放射性疼痛,伴或不伴腰痛;②经保守治疗3 个月以上,症状无缓解者;③经腰椎影像学证实为LDH,且具有与影像学一致的临床症状者;④治疗前知情同意,且具有高依从性。排除标准:①LDH 不同进展阶段者;②合并骨化、黄韧带增生等其他腰椎疾病者;③病变节段极度狭窄者;④有其他系统疾病不适宜手术治疗者;⑤腰椎过伸过屈位X 线片提示存在腰椎节段性不稳者;⑥高度移位游离的椎间盘脱出者。
1.2 器械
椎间孔镜(生产厂家:德国SPINENDOS 公司),射频机(生产厂家:西安高通科技发展有限公司)。
1.3 方法
所有患者均采用PELD 术。患者取俯卧位,架空腹部,使用局部麻醉,麻醉位置在棘突中线旁。在“C”臂下将穿刺针引导至病变椎间盘中心,注入造影剂(9.0 mL欧乃派克+1.0 mL亚甲蓝),观察正侧位椎间盘形态和椎间盘纤维化是否伴有撕裂及撕裂程度。在病变椎间盘原穿刺点处做小切口,将三级扩张套管逐渐向病变椎间盘扩张,将内镜置于责任椎间盘内,进行冲洗(3 000.0 mL 生理盐水+庆大霉素32 万u+肾上腺素0.5 mL),摘除染色突出变性髓核组织,用生理盐水灌洗,稀释炎性致痛因子。术中对病变的椎间盘进行观察,使用造影技术观察病变的形态和性质等,同时,对患者椎间盘的状态进行评估,使用上一椎间盘作为对照,用MRI对病变椎间盘进行分析。术后2 d 根据患者情况,带腰围下床活动,活动时间控制在30 min内。术后1个月坐、站及走等非卧床姿势固定,均在30 min 内。术后使用消炎止疼、消肿及神经营养药物行对症处理,也可结合中医药、针灸理疗和磁热疗等进行辅助治疗,必要时给予微创手术处理。术后3 个月内避免剧烈运动及重体力劳动,术后6和12个月门诊随访复查。
1.4 评价指标
1.4.1 疼痛情况采用视觉模拟评分(visual analogue scale,VAS)评价疼痛情况,0 分为无疼痛,10分为剧烈疼痛。
1.4.2 恢复情况采用日本骨科学会(Japanese Orthopaedic Association)评分进行评价,JOA 评分涉及临床体征、主观症状、活动受限及膀胱功能等内容,分值为0~29 分,分值越低,代表功能障碍越严重。
1.4.3 改良Macnab 优良率优:患者能够正常生活,体征和症状均消失;良:症状和体征有所改善,可独立进行日常生活及工作;中:症状及体征稍微改善,不能独立进行日常工作及生活;差:症状及体征未得到改善,甚至加重,日常工作及生活完全不能自理。
1.4.4 复发及并发症情况并发症包括硬脊膜破损、神经根损伤、术后切口感染、腰背僵硬疼痛和左下肢麻木等。
1.5 统计学方法
应用SPSS 22.0 统计软件分析数据。计数资料以例(%)表示,采用四格表χ2检验;计量资料以均数±标准差(±s)表示,两两比较采用t检验,多组间比较采用方差分析。检验水准为α=0.05。
2 结果
2.1 手术前后VAS比较
患者术前VAS 为(5.41±2.72)分,术后6 个月VAS为(1.12±0.54)分,术后12个月VAS为(0.25±0.11) 分,3 个时间点比较,差异有统计学意义(F=4.12,P<0.05);经两两比较,术后6 和12 个月VAS 明显低于术前(t=4.27,t=4.31,均P<0.05),且术后12 个月VAS 低于术后6个月(t=4.06,P<0.05)。
2.2 手术前后JOA评分比较
患者术前JOA 评分为(8.20±7.32)分,术后6个月JOA评分为(20.72±2.24)分,术后12个月JOA评分为(28.45±3.10)分,3 个时间点比较,差异有统计学意义(F=8.74,P<0.05);经两两比较,术后6 和12 个月JOA 评分明显高于术前(t=5.89,t=7.45,均P<0.05);术后12 个月的JOA 评分高于术后6个月,差异有统计学意义(t=4.11,P<0.05)。
2.3 术后患者改良Macnab优良率比较
术后3个月,患者改良Macnab优良率为90.00%,术后12个月,患者改良Macnab优良率为93.34%,两者比较,差异无统计学意义(χ2=0.44,P>0.05)。见附表。
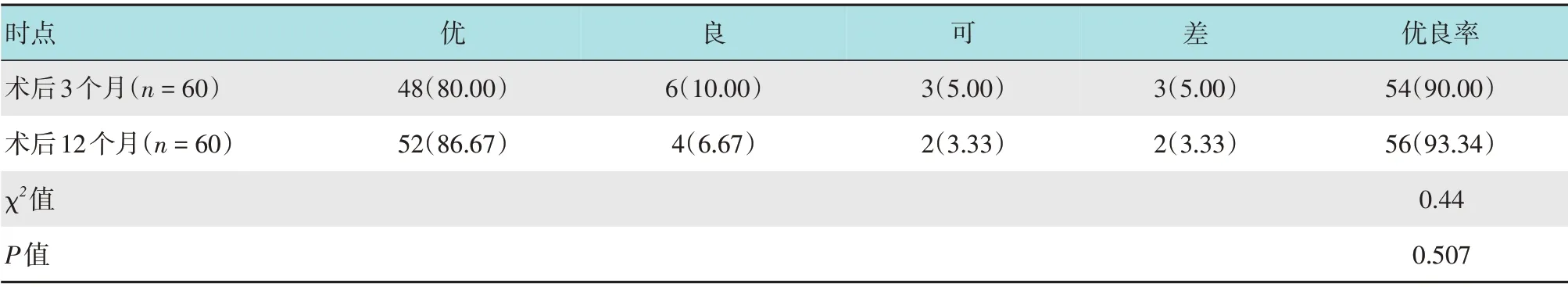
附表 术后患者改良Macnab优良率比较 例(%)Attached table Comparison of the excellent and good rate of modified Macnab in postoperative patients n(%)
2.4 术后复发及并发症发生率比较
所有患者均顺利完成手术,且无复发。术后6个月,有1 例发生切口感染,1 例发生腰背僵硬疼痛,并发症发生率为3.33%;术后12个月,有1例发生腰背疼痛,1例发生左下肢麻木,1例发生硬脊膜破裂,并发症发生率为5.00%,术后6和12个月的并发症发生率比较,差异无统计学意义(χ2=0.21,P>0.05)。
2.5 典型病例
患者男,55 岁,腰部疼痛2年,伴左下肢放射痛,再发加重半个月。查体:腰背部压痛,伴左下肢放射痛,左小腿外侧及足背感觉麻木,左趾长伸肌肌力减弱,左下肢直腿抬高试验20°阳性。术前MRI显示L5~S1椎间盘突出,压迫硬膜囊(图1);术前X线片显示高髂嵴,髂嵴连线超过L5椎弓根中线以上(图2);镜下可见突出的椎间盘被切除,神经根减压满意(图3)。
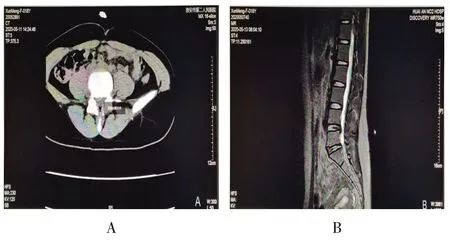
图1 术前MRI显示Fig.1 Preoperative MRI findings
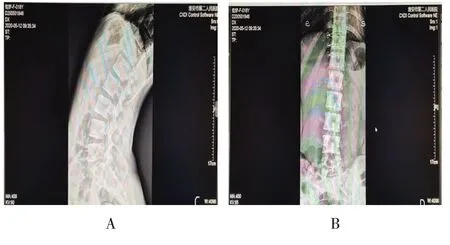
图2 术前X线显示Fig.2 Preoperative X-ray findings
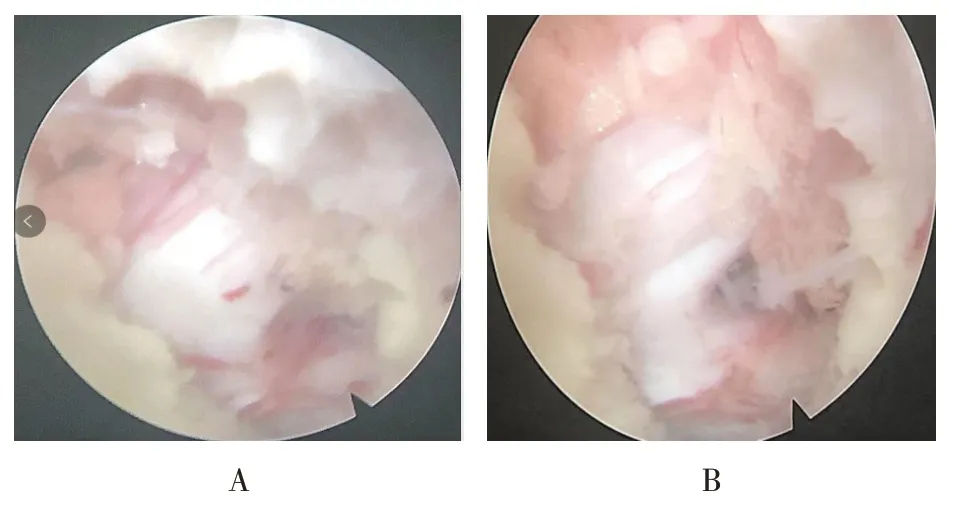
图3 经皮内镜显示Fig.3 Results of percutaneous endoscopy
3 讨论
3.1 LDH的治疗现状
LDH 是临床较为常见的一种退行性病变,大多数患者表现为腰腿疼痛、下肢麻木和酸胀等,LDH多发于老年人,与职业存在较大关系。有研究[4-5]表明,外伤史及背部受寒是疾病最为常见的诱因,L4/5、L5和S1是好发部位,也是腰椎间盘突出最易受累的节段,占所有发病患者的95.00%以上。影像学技术的发展,促进了临床治疗技术的进步,尤其是腰椎间盘摘除术,已广泛应用于临床,但选择手术治疗的患者较少,大多以理疗和药物治疗等为首选,当疾病进展,出现严重症状时,才会采取手术治疗[6]。开放探查减压+椎间融合内固定手术是治疗腰椎间盘突出的主要手段,治疗效果显著,但有手术出血量大、创伤大、切口易感染和异物排斥反应等缺点[7-8]。随着医学技术的发展,脊柱外科手术技术得到了较大发展,微创技术已成为外科领域的焦点,特别适用于脊柱外科疾病的治疗。
3.2 PELD的优缺点
3.2.1 PELD 的优点PELD是一种微创脊柱外科手术,适用于保守治疗无效的患者[9]。PELD 的优点在于:术中能够有效减少患者的出血量,并且能获得较为清晰的术中视野,能清楚地观察到患者的病变椎间盘,常规需进行局麻,术中能知晓患者的状态,及时了解患者的神经、血管损伤情况。PELD 在手术中采取局部麻醉的方式,能有效减少费用,避免全身麻醉带来的术后并发症,容易被患者所接受。PELD 能直接到达髓核突出的部位,且工作通道较小,不容易破坏周围椎旁肌群、软组织及其他重要骨质结构,真正达到了微创的效果[10-11]。通过影像学技术辅助PELD,能在直视下对病变椎间盘组织直接进行病变摘除,对于椎管内较大的椎间盘突出物,可以通过技术手段去除,并且能在术中直接对硬膜囊、神经根进行减压观察,明确是否减压充分。因此,在临床上,PELD 技术更适用于包含型椎间盘突出、巨大和游离的椎间盘突出、伴有椎间孔狭窄的突出和极外侧型椎间盘突出。术中采用亚甲蓝,能够选择酸性髓核进行染色,方便镜下发现突出的病变髓核,并能在直视下切除病变的髓核及钙化的后纵韧带、纤维环等[12]。PELD 较传统手术具有诸多优势[13-14]:①出血量少,一般少于50 mL,有利于患者的术后恢复;②术后并发症发生率低,几乎不存在软组织粘连和切口感染等问题;③可避免血管和硬脊膜等重要器官受损,由于PELD是借助内镜实现直视处理,可保证解剖位置的安全性;④局部麻醉术后,患者自主活动并不会受限,费用较低,患者的治疗依从性高。本研究显示,患者术后VAS明显降低,而JOA评分明显升高,术后6和12个月的改良Macnab 优良率均较高,分别为90.00%和93.34%,术后随访,所有患者均无复发,并发症发生率较低,治疗效果较为显著。
3.2.2 PELD 的局限性准确地将工作套管置入突出的髓核区域是PELD成功的关键,但是对于移位较高的游离髓核,手术效果一般,往往会残留髓核,需进行二次手术[15]。在进行PELD 手术时,术中需充分暴露手术部位,以找出病变髓核,术后要对神经根进行松解,保证硬膜规律的波动[16]。
3.3 PELD术后发生并发症的主要原因
3.3.1 硬脊膜破裂游离型椎间盘突出、中央型椎间盘突出和复发性椎间盘突出在手术精密操作过程中,会出现硬脊膜破裂,与操作的精细程度密切相关,但仅有极少数患者会发生。
3.3.2 神经根压迫LDH 的发病机制多是由于神经根出现压迫,造成神经根血运障碍,炎性物质长期刺激,导致出现病变。病情长时间进展,迁延不愈,导致神经根发生变化,结构损伤。虽在手术时解除了压迫,但由于神经根的适应作用,不能马上解除症状,需要一定时间恢复。
3.3.3 神经根缺氧在手术中,要对硬膜囊和神经根进行多次牵拉,且多为可持续性操作,会对神经根造成进一步的损伤,加重神经根缺氧。
3.3.4 疼痛和麻木对于全身而言,腰部神经根没有束膜和神经外膜,无法阻挡有害物质,缺血后机体不能耐受,导致炎症和水肿等病理情况时常发生,使神经内压增高,氧气供应不足,出现缺氧,长时间后,会造成局部神经控制区域出现疼痛和麻木等症状。
3.3.5 腰椎不稳定髓核摘除能使椎体的承受应力发生改变,应力分布不均匀及增大后,会导致腰椎不稳定,应力过大会损伤腰椎,破坏了血液循环和神经通道,影响神经功能的恢复。
综上所述,PELD 作为一种微创脊柱外科手术方式,能明显改善VAS 和JOA 评分,改良Macnab 优良率较高,且术后并发症发生率较低,疗效显著,但同时要正视该术式的局限性。
