辩证思维方法在高中化学教学中的应用
——以原子是如何构成形形式式的物质教学为例
2022-09-29傅爱华
傅爱华
(上海市华东师范大学附属周浦中学 上海浦东 201318)
辩证思维方法又称辩证分析方法,包括归纳与演绎、分析与综合、抽象与具体、逻辑与历史相统一。人类思维的发展,一般是由形象到抽象思维,再由抽象思维到辩证思维,辩证思维方法是最高层次的科学方法。辩证思维方法和我们新课标中化学学科素养中的宏观辨识与微观探析、证据推理与模型认知有很多不谋而合的地方。化学就是从物质的宏观特征入手,对物质及其反应进行分类和表征,从物质的微观结构说明同类物质的共性和不同类型物质性质差异及其原因,解释同类的不同物质性质变化的规律。
瑞士心理学家皮亚杰建议教学时要用主动的方法,即要求学生去发现或重新建构讲学习的事,这并不表示把学生和器材摆在一起即可,老师要扮演组织和创造呈现有用的问题情境的角色。笔者以原子是如何构成形形式式物质这一单元为例,讲述如何利用辩证思维的方法进行高中化学教学,提高学习有效性,如何在高中化学教学中培养学生的辩证思维能力。
在初中时,学生学习了原子构成分子,分子组成物质的知识。进入高中后,还是有很多学生根深蒂固地认为所有的物质都是由分子组成的。所有物质都由分子构成的?都是原子构成分子,分子再构成物质?化学变化中的最小微粒“原子”是如何构成世界上形形式式的物质的?对于这部分内容,教师可以用辩证思维的方法进行单元教学设计,帮助学生了解微观世界,并在微观化学教学中提高学生归纳与演绎、分析与综合、抽象与具体的思维能力。
辩证思维方法的特点:以抽象思维方法作为反映客观现实的认识论基础。没有抽象思维,辩证思维根本就无法进行,而且辩证思维同样也要遵从抽象思维的规则,并使思维概念在辩证运动中与客观现实相符,以便能够达到预期目的。
一、归纳与演绎中形成的“化学键”
经过对原子结构的认识、氧化还原的学习,学生心中已经埋下了“求稳”意识,不管是宏观世界还是微观世界,反应的最终目的是趋于“稳定”,化学键的学习就是归纳和演绎如何让微观世界的原子“稳定”。教师通过利用宏观世界中学生能看到、感受到的实物,让学生意识到微粒之间作用力的存在,食盐固体、氯气、金属钠、水……,构成这些物质的微粒,分子、原子、离子并没有满天飞,这些物质就在我们身边,我们看得见、摸得着它们。那么,这些微粒之间是不是像砖块建成高楼大厦那样,有“石灰、水泥这样的粘合剂”把他们“牵扯”到一起呢?
教师通过提出问题、引导学生重新建构微粒求稳的过程,可以促成有效学习。原子之间应该是存在互相牵扯的这种作用力的,这种看不见摸不着的作用力称之为化学键。氯化钠固体、氯气、金属钠,都是真实存在的,只有构成物质的原子成为稳定结构,才能让我们看到的这些物质稳定存在。大家都知道原子最外层为8电子是稳定的,化学键这种作用力是如何让各原子结合,从而达到“八稳”的呢?
这种原子间的结合可能是你情我愿,也可能是合作共赢,抑或是共同富余的。
1.化学键之你情我愿篇——当钠原子遇上氯原子
画出钠和氯的原子结构示意图。从它们的结构中,看出它们并未达到我们之前了解到的“化学中的八稳”,钠原子很想失去一个电子达到“八稳”,氯原子很想得到一个电子达到“八稳”,两人一拍即合,你情我愿地结合到了一起。钠原子失去一个电子后形成带正离子,氯原子得到一个电子后形成带负离子,正负相吸,像两个恋人一样看对眼了,互相靠近,但是它们可能无限靠近吗?两个离子核外的电子不允许,就像相爱的恋人一样,若要长久,也得保留自我,有私人空间。钠离子和氯离子之间这种即吸引又不完全融合的恰到好处的作用力把它们牵扯到了一起,这就是我们化学键中的离子键。
你情我愿达到“八稳”状态,形象地演绎了离子键的成键过程。再稍加思考氯化镁,硫化钠的成键过程,学生很容易就归纳出活泼金属和活泼非金属元素原子之间通过得失电子形成离子,进而正负离子通过离子键结合形成物质。通过归纳和演绎,学生得出结论离子键怎么形成,什么样的元素原子之间容易形成离子键。
2.化学键之合作共赢篇——当氯原子遇上氯原子
画出两个氯原子的电子式。“我少了一个电子”“我也少了一个电子”“我们都没达到八‘稳’”“怎么办呢?”“让我们每人拿出一个电子放在中间共用,就像共同分享快乐一样共同拥有,合作共赢行吗?”“我们一起组成一个快乐的氯气分子”。非金属元素的原子均有获得电子的倾向,原子间可通过共用电子对使双方最外层电子达到稳定结构。这就是我们化学键中合作共赢的共价键。
“合作共赢”,即通过合作,双方都能有所收获。原子间的共用电子对也是如此。氢原子和氢原子组成的氢气分子、氯原子与氯原子组成的氯气分子,中间的共用电子对受到两边“原子核对电子的吸引力”相同,即两个原子的核电荷数相同,对电子的吸引力相同,共用电子没有发生偏移,氢气中氢显0价、氯气中氯显0价。但是氢原子与氯原子构成的氯化氢分子,中间的共用电子对受到两边的作用力不同,很明显氯原子的原子核对电子的吸引能力更强,所以这对共用电子对向氯原子那边偏移了,氯化氢中氯原子带部分负电荷显-1价,氢原子带部分正电荷显+1价。
通过氯原子和氯原子通过共价键结合形成氯气分子、氢原子与氢原子通过共价键结合形成氢气分子、氢原子与氯原子通过共价键结合形成氯化氢分子,演绎中又稍加变化,归纳出:①非金属与非金属元素原子之间容易形成共价键;② 形成的共价键(共用电子对),如果是不同元素原子之间形成的,那么共用电子对偏向核电荷数大的原子。结合“合作共赢”,既有利于学生对知识进行理解和记忆,又提高了学生的人文素养,也使学科之间很好地融合。
3.化学键之共同富余篇——当钠原子遇上钠原子
“人人平等,共同走向富裕”这是我们所希望达到的理想的生活状态,这种状态在金属中也实现了。再看一下钠原子的结构示意图,核外有三个电子层,最外层只有一个电子,钠原子很想失去一个电子成为钠离子而达到“八稳”,金属钠中的众多钠原子都是这样的,都“富余”了电子。失去了电子形成稳定结构、带正电荷的钠离子和“富余”的带负电荷的电子之间形成的这种作用力就是我们化学键中共同“富余”的金属键。
金属钠的形成演绎到其他金属单质的形成,学生通过所知道的金属都是电的良导体这一常识,归纳出金属及其合金都是由金属正离子和自由电子通过金属键结合形成的。教师在讲解时把我们国家要带领大家最终走向共同富裕的“裕”改成“余”,也彰显出中华文字的奥秘之处,通过学科间渗透,不断提高学生的人文素养及爱国情怀。
化学键中离子键、共价键、金属键,本身就是对原子如何趋于稳定方式的归纳与演绎。氯化钠演绎到活泼金属和活泼非金属元素原子之间;氯气演绎到氢气、氯化氢、非金属元素原子之间;金属钠演绎到其他金属单质以及合金,每一部分的讲述都是使用辩证思维方法中的归纳和演绎。通过归纳和演绎,学生自己得出了三种化学键的本质,得出什么的元素原子之间会形成什么样的化学键,理解并掌握了知识点。化学键的整体内容是通过归纳和演绎完成的,每一个化学键的学习中又蕴含着归纳和演绎的方法。这使学生体会到辩证方法中归纳和演绎的普遍性,相信在不断应用之后,这一方法一定会深入人心,使学生在其他学科的学习中、在生活中也注意不断进行归纳,思考复杂的知识点是否可以通过简单的内容演绎来帮助理解和掌握。
二、分析与综合——形形式式物质的构成
原子与原子之间通过不同的“求稳”方式,以及某种作用力结合,构建成了我们看得见、摸得着,稳定存在于我们身边的各种物质。四大晶体的微观构成正是将化学键的内容进行分析后进行综合。打破常规教学模式,让学生顺着原子以什么样的方式求稳后,通过作用力结合成物质的方向,讨论思考原子构成物质的不同方式。
学生非常容易通过原子通过得失电子达到稳定状态后,通过离子键结合形成物质,也就是离子晶体的构成方式:

原子和原子之间通过共用电子对达到稳定状态,即以共价键结合成分子,那么这些分子是堆在一起就可以构成物质了吗?有化学键作为基础,冰、蔗糖这类由分子构成的物质也并不是分子满天飞的,分子之间也肯定存在互相牵扯的作用力,即分子间作用力。分子晶体的构成方式也就呼之欲出了:

离子键、共价键都利用起来了,顺其自然金属键就进入我们的思考范围,归纳出金属晶体的构成方式:

分析化学键后,学生很容易得出离子晶体、分子晶体、金属晶体的构成方式,教师稍加指引,他们就能把这三种晶体综合起来。那么对于原子晶体的构成方式,如何让学生更形象地掌握起来呢,笔者尝试再次演绎:由CH4分子为基础,将分子中的氢原子换成碳原子,每个碳原子都要形成4根共价键,那么换上去的碳原子就需要继续以共价键和其他原子结合,如果结合的仍然是碳原子,在黑板上简单地画出模型后就能得到原子之间直接以共价键结合形成的无限延伸的空间立体结构——原子晶体金刚石。

物质的形成过程等于是把化学键的知识点掰碎了再进行分析综合。通过辩证方法的分析与综合,学生做到了知其然并知其所以然。我们学习其他的知识也是如此,通过分析和综合,不仅看到了圆圈内的内容,是不是还能伸出触角,探索一下圆圈外的世界。这便可以为学生的终身学习、终身发展埋下小小的种子。
三、抽象与具体——晶体性质上的差异
通过氯化钠、氯气、金属钠、金刚石宏观物质确实存在,用较为抽象的微观世界分析其中存在的作用力——化学键,现在又通过这些微观世界的微粒、抽象的作用力,回到宏观物质,宏微结合,学生自然而然发现构成微粒不同、作用力不同,那么组成的物质性质肯定也是不同的。笔者通过查阅资料给出典型晶体的熔点,让事实说话,让抽象的观念具体化。
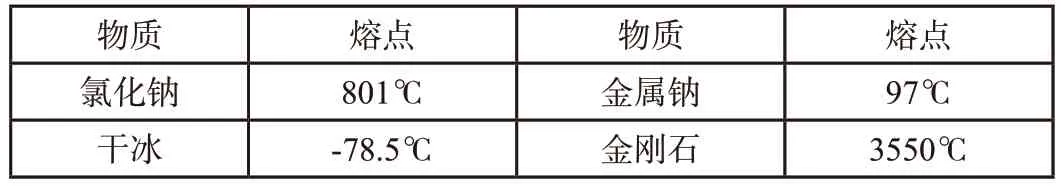
学生看到这几个高低不同的数字时,不仅看到了大小不同,也看到了这些晶体构成微粒,微粒间作用力的不同,还可以从数字归纳出通常共价键的键能大于离子键,共价键和离子键的键能比分子间作用力都要大得多。
从具体到抽象又从抽象到具体,这本身就是人类对于知识认识、规律认识过程的诠释。这部分单元的设计从宏观具体物质出发,研究抽象的、看不见、摸不着的化学键,又通过抽象的化学键组成具体的物质(四大晶体),从具体物质的性质(熔点)证实抽象微粒、化学键的不同。高中化学中氧化还原、化学反应速率、限度、弱电解质的电离、盐类水解等很多教学内容都可以使用辩证方法中抽象与具体这一方法[1]。
化学学科素养培养学生宏观辨识与微观探析水平中提到,能从物质的宏观特征入手对物质及其反应进行分类和表征,能联系物质的组成和结构解释宏观现象。结合辩证思维方法即演绎,分析与综合,抽象与具体,对原子是如何构成世界上形形式式的物质这部分教学内容进行了单元设计。归纳与演绎微粒之间存在不同类型的相互作用,认识离子键、共价键、金属键的本质;分析与综合微粒的种类及微粒之间的相互作用,构成了我们身边形形式式的物质;结合常见的离子晶体、分子晶体、金属晶体、原子晶体的实例,认识物质的构成微粒、微粒间相互作用与物质性质的关系,从具体到抽象,再从抽象到具体,宏微结合,实现教学目标。
现代心理学研究指出,学生对知识的学习是以一种“心理重演”的方式再现知识的探索和发现过程。这表明学生的学习过程和科学家的探索过程在本质上是一样的,都是一个发现问题、分析问题、解决问题的过程。反思我们的课堂,经常出现这样的现象:为了把知识完整地呈现,教师从自己的思维出发设计课程,把自己的思维路径和知识体系一股脑全部灌输给学生,学生虽然听课时明白了内容,但是缺少对知识的探寻过程,这样不求甚解学习知识很快会被遗忘。学生应该是充满探索和追求的,用辩证思维的方法进行这部分教学设计,就是要致力于让学生通过辩证的方法去发现或重新建构这些知识,提高学习效率,让学生从根本上理解,在理解的基础上进行记忆并应用。这样我们所教授的知识才能成为学生自己的知识,而不仅仅是印在课本上的文字[2]。
