医院医疗器械不良事件管理实践的分析与探讨
2022-09-28万里杨宁金剑
万里,杨宁,金剑
武汉市第一医院 设备处,湖北 武汉 430022
引言
医疗器械不良事件,是指获准上市的质量合格的医疗器械在正常使用情况下,发生导致或可能导致人体伤害的任何与医疗器械预期使用效果无关的有害事件[1]。随着医疗科技的不断发展,医疗器械种类繁多、来源广泛、更新迭代迅速,而所有的医疗器械受当时实验条件的限制或科技水平的制约、上市前的临床评价不足等因素的影响,都将可能导致医疗器械存在一定的缺陷,因而在临床应用过程中存在一定的风险。而现代医疗业务的开展,对医疗器械的应用又越来越广泛和依赖。因此,医疗器械在提高医疗技术及服务的同时,也随之出现了不少新的问题,医疗器械不良事件时有发生。
医院因其医疗器械数量多、品种全、用量大等特点,医疗器械不良事件发生的概率较高,是可疑医疗器械不良事件报告的主要来源。而保证报告的数量及其信息的完整性和有效性,才能更好地为上级监管部门提供准确的监测依据,以减少或者避免同类医疗器械不良事件的重复发生,保证用械安全,并促进医疗器械产业的健康发展。但在实际的监测工作中,依然存在着各种各样的问题[2-3]。本文结合某医院可疑医疗器械不良事件监测管理工作实践现状及相关报告数据,总结、分析并探讨医院可疑医疗器械不良事件监测工作中存在的问题及对策,以期提高医院的监测水平。
1 数据来源与方法
从某医院于2014—2021年在国家药品不良反应监测系统上报的可疑医疗器械不良事件报告中提取114例报告信息作为数据样本,并借助Excel筛选统计及图表功能,对样本数据从报告的整体、报告涉及的医疗器械类别和伤害程度、报告来源和报告数量、报告质量等方面,分别进行统计、分析和探讨,以得出相应结论或问题,并提出解决方案及对策。
2 医疗器械不良事件报告样本数据的统计、分析与探讨
2.1 报告的整体归纳统计与分析探讨
2.1.1 报告的整体归纳统计
114例报告中,涉及医疗设备63例(55.3%)、医用耗材51例(44.7%),所涉及的医疗器械类型、数量及不良事件主要表现如表1所示。
2.1.2 分析结论与探讨
从表1可以看出,可疑医疗器械不良事件的表现以多种形式存在。此外,不论医疗器械价值、用途或结构大小,医疗器械不良事件涉及了医疗器械的各个种类,也再次证明:任何医疗器械产品的设计和生产都具有一定的风险,被批准上市的医疗器械只是一个“风险可接受的产品”[4]。

表1 医疗器械不良事件报告样本的整体归纳统计表
2.2 医疗器械类别与伤害程度统计分析与探讨
2.2.1 医疗器械类别和伤害程度统计
根据国家医疗器械注册和分类管理方法[5-6],医疗器械根据风险程度不同,由低到高可分为Ⅰ、Ⅱ、Ⅲ类;而根据医疗器械是否需要除人体自身及重力以外的能源(如电能)来发挥其功能,又可以分为有源和无源器械。
医疗器械不良事件导致或可能导致的伤害,总体分为死亡、严重伤害(包含危及生命、导致或可能导致需内外科治疗才能避免机体功能结构永久损伤)和其他3大类。
2.2.1.1 器械类别统计
114例医疗器械不良事件报告所涉及的医疗器械中,按Ⅰ、Ⅱ、Ⅲ类管理类别和有源或无源类别来统计,各类器械数量及占比情况如图1所示。其中,Ⅰ类器械为5例,占比4.4%,全部为无源器械;Ⅱ类器械为51例,占比44.7%,其中有源器械34例、无源器械17例;Ⅲ类器械为58例,占比50.9%,其中有源器械25例,无源器械33例。
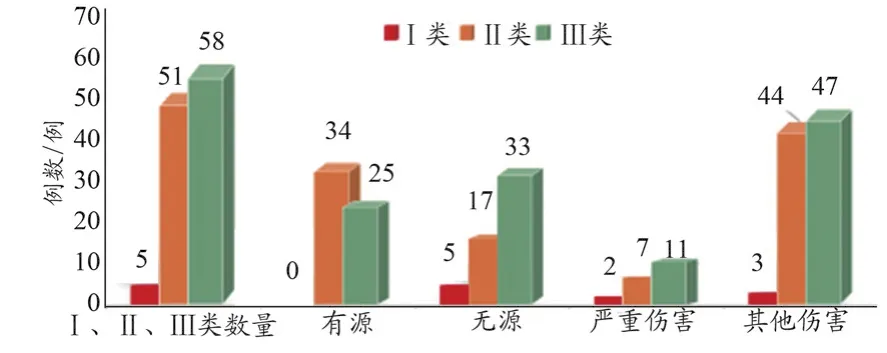
图1 医疗器械不良事件报告样本中器械类别和伤害程度统计
2.2.1.2 器械伤害程度统计
目前,该医院暂未发生死亡类医疗器械不良事件报告。图1报告样本中伤害程度统计数据显示,Ⅰ、Ⅱ、Ⅲ类医疗器械不良事件报告中,严重伤害报告数依次为2、7、11例,分别约占Ⅰ、Ⅱ、Ⅲ类器械报告数的40.0%、13.7%、19.0%。
2.2.2 分析结论与探讨
从图1可以看出:① 无论医疗器械属于Ⅰ、Ⅱ、Ⅲ类或有源/无源,都具有一定的使用风险,继而有发生不良事件的可能;② 不良事件医疗器械占比:Ⅲ类>Ⅱ类>Ⅰ类,这一实践结果与国家医疗器械风险程度划分和分类管理办法是完全相吻合的。医疗器械分类管理等级越高,发生不良事件概率越大[7];③ 无论医疗器械分类管理等级高低,均有导致严重伤害的可能,此点不容忽视。
以上结论,可充分提醒医务人员,各类医疗器械在日常使用和管理中,均需按不同类别医疗器械管理要求,采取对应措施进行管控,以减少不良事件发生,确保用械安全。
2.3 医疗器械不良事件报告来源、报告数量、报告质量统计分析与探讨
2.3.1 报告来源、报告数量、报告质量统计
2.3.1.1 报告来源统计
以往的研究表明,医生、护士、技师是医疗器械不良事件上报的主体[8]。从图2统计结果看出,医院可疑医疗器械不良事件报告主要来源于医生、护士、技师和临床工程师4个部分。数据显示,医疗器械不良事件护士和工程师上报数量最多,分别占比49.1%和42.1%,而医生和技师上报数量很少,分别仅占7.9%和0.9%,存在报告人类别占比严重不均的现象及问题。

图2 医疗器械不良事件报告来源数量及占比
2.3.1.2 报告数量统计
依据数据样本中2017—2021年度可疑医疗器械不良事件报告数量,并结合该院药品不良事件报告数量对比统计(图3),可以看出,该院存在着医疗器械不良事件报告数量整体偏少、远不如药品不良事件报告多的问题,这说明医院医疗器械不良事件监测工作的开展还有待加强。
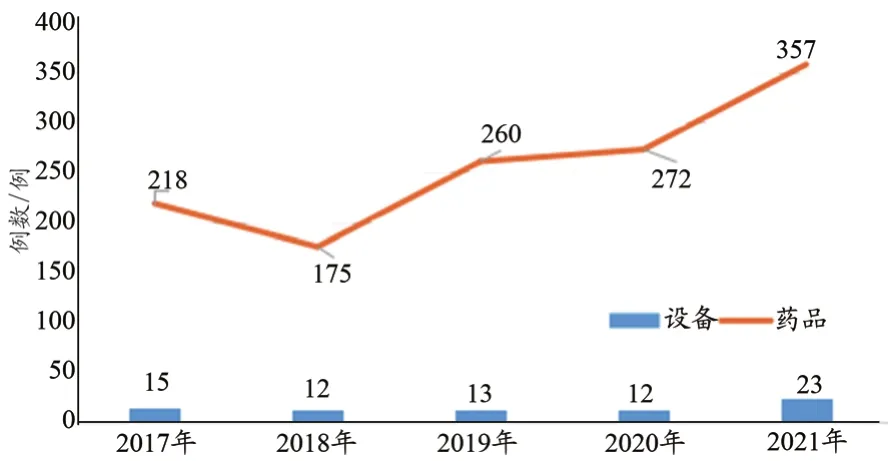
图3 2017—2021年医院医疗器械和药品不良事件报告数量
2.3.1.3 报告质量统计
在医疗器械不良事件的监测管理工作中,对不良事件信息的准确收集、填写和及时反馈有着重要意义和价值[9]。针对114例医疗器械不良事件报告中的关键信息缺失或误填情况进行统计,缺失或误填占比前5的信息如表2所示。

表2 医疗器械不良事件报告样本中报告信息缺失或误填排名前五的情况统计表[例,n(%)]
由表2数据显示,报告信息缺失最多的为“合并用药/械情况说明”,缺失占比高达96.5%;而排名第5位的报告信息“产品编号/批号”缺失率也达到了46.5%。此外,在日常工作中,实际收集到的可疑医疗器械不良事件报告中,还存在着很多关键信息简写、误写、漏写或对不良事件表现描述不清等问题,需监管人员不停往返于各临床科室之间,对事件情况及报告信息进行反复的核对、补充和修改,耗时耗力。这些都从侧面反映出,医院对可疑医疗器械不良事件的管理,存在着报告上报和接收体系不完善、报告关键信息缺失严重、报告质量整体偏低等多种问题。
2.3.2 问题及原因分析
针对可疑医疗器械不良事件报告人类别占比严重不均、报告数量偏少和报告质量偏低等问题,结合以上实践数据分析,并通过对医院各类医务人员的走访和了解,分析可能存在以下因素:
(1)临床医务人员对医疗器械不良事件辨别能力和上报意识不足。医院工程师人数较少但报告数量显示占比较高,是因为临床工程师对医疗器械的结构和原理有一定的专业认识,相对能更容易地判断出事件的发生原因,如由于器械自身老化、故障或使用不当,器械自身固有风险(如材质、设计缺陷)或未知的使用环境影响、联合用药/用械等因素导致不良事件;同时,工程师作为院内可疑医疗器械不良事件监管员,其具有一定的主动报告意识。而临床医务人员,对医疗器械的认识主要在于临床应用方面,当医疗器械不良事件发生时,其多数会认为该事件属于医疗事故范畴,而并非不良事件,当然也无法及时意识到需按不良事件处置流程进行上报。
(2)各类医务人员对医疗器械不良事件监测工作的了解和认识程度不够。虽然国家有关部门出台了医疗器械不良事件管理相关的法律法规,但临床医护技更多了解和关注的是药品和医疗不良事件,而对医疗器械不良事件认识不足、关注度不高[10]。从图2可以看出,护士报告数量占比最高,一方面主要是因为护士作为医院最大的群体,接触和使用医疗器械的种类和频次最高,遭遇不良事件概率最大;另一方面,当医疗器械使用出现异常情况后,大多会由护士第一时间联系临床工程师协助查看、处理,工程师对其上报不良事件也起到了一定的提醒和引导作用。
(3)对于医疗器械不良事件的上报存在心理顾虑。医疗器械不良事件的表现,相对来说没有药品不良反应和医疗事故那样直观,临床医务人员容易将医疗器械不良事件与医疗事故和医疗器械质量事故相混淆,从而有所顾虑,不敢或不愿主动上报[11-12]。
(4)临床科室上报时信息不全、实物没有及时保存下来或进行拍摄[13]、医务人员对可疑医疗器械不良事件报告的填写要求及规范认识不足,且因报告内容多,医务工作忙,不愿详细填写或因对器械结构缺少专业认识等,造成提交的不良事件报告存在信息存在不全、错漏或描述不清等多种问题。
2.3.3 解决方案及对策
针对上述问题,解决方案如下:
(1)从医院层面,结合医院自身实际情况,进一步加强《医院可疑医疗器械不良事件管理》制度建设,明确实施细则,落实责任主体,责任到科到人,全面推进监测工作[14]。
(2)全面做好可疑医疗器械不良事件监测的宣传工作。院内监管员需定期通过现场培训讲解或在院内OA、钉钉、监测微信群等多种办公平台,大力宣讲可疑医疗器械不良事件监测相关知识,提高医务人员的整体认识。
(3)院内可疑医疗器械不良事件监测主管部门,应加强对医务人员的正确引导。一方面,要加强培训,使医务人员明确医疗器械不良事件与医疗事故和医疗器械质量事故之间的区别与纠正其错误认识;另一方面,要定期主动收集整理并更新常见医疗器械及其不良事件表现的归纳统计表,并提供给医务人员对照、学习,有助于其对医疗器械不良事件进行识别和判定。
(4)利用电子信息化,结合医院电子病历系统,加强智能化管理。如在医院HIS的基础上,建设院内可疑医疗器械不良事件上报系统[15]。该系统可实现或优化以下功能:① 在报告系统首页或关键项处,加注填报说明和注意事项,由系统指导医务人员填写报告信息,避免院内监管员重复讲解;② 系统自动识别上报人信息(如姓名、科室、电话等),便于监管员与当事人及时联系、了解、核实并处置不良事件;③ 当可疑医疗器械不良事件关联患者时,填报人可在HIS直接点击并自动带入该患者相关信息(如姓名、年龄、病历号、既往病史、用药/械治疗情况等)到不良事件报告中,填写简便且可同时保证报告中患者相关信息的完整性;④ 通过系统锁定报告中必填项并加设提醒功能,避免报告中关键信息的漏填缺失;⑤ 在不良事件报告系统各关键信息处填写框架后,设置附件上传功能,可上传包含产品信息(如设备铭牌、器械包装信息等)或不良事件表现(如器械故障)的图片及事件相关文档附件,以利于对不良事件报告信息的补充,也便于院内监管员对报告信息的核对与修正,保证报告信息的准确性;⑥ 通过系统建立院内反馈机制及共享功能,可及时将事件的处置建议、报告的修改意见以及后续上级药监系统的审核评价情况等,通过系统反馈给填报人,或将事件信息定向共享或推送给相关科室,以提醒注意警戒。
(5)尝试开展院内多部门的联合管理,主动发现、提取可疑医疗器械不良事件信息。例如,当医院医疗、护理或药品不良事件监测系统收到报告,且报告内容及原因分析中涉及合并用械可能时,则系统将该报告信息自动触发和抄送给院内医疗器械不良事件监管部门,以提醒监管员主动核实和提取医疗器械风险信号。
(6)建立奖惩机制,促进上报。对发生医疗器械不良事件而刻意隐瞒不报,且造成不良后果的主要责任人,给予相应惩戒;而对如实并成功上报医疗器械不良事件的人员,可给予适当的现金奖励或在评优评先方面予以优先等,以提高医务人员上报医疗器械不良事件的积极性[16]。
3 讨论与总结
医疗器械相比于药品的不良事件监测工作起步晚、开展难、报告数量少,但可疑医疗器械不良事件监测工作是医疗器械管理过程中的重要一环,是一项长期且任重道远的工作;而医院作为该项工作中不可或缺的一部分,同时作为可疑医疗器械不良事件报告的主要来源,如何进一步提高自身能力,对监测工作进行更加积极有效的开展,是至关重要的[17-18]。本文通过对医院医疗器械不良事件监测实践情况的统计、总结、分析与探讨,目的在于提高医务人员对医疗器械不良事件风险的认识,加强医院监管力度,科学用械,安全用械,保障医患安全。同时,也希望未来能借助信息化手段,进一步改善和优化医院医疗器械不良事件监测管理的方法及流程,使监测工作更好地开展。
本文编辑 王晨晨
