中国化妆品原料管理回顾及展望
2022-09-27岑燕钊陈慧慧高倩铭
石 飞 岑燕钊 陈慧慧 高倩铭
完美(广东)日用品有限公司,广东中山,528400

2021年,《化妆品监督管理条例》正式实施,其配套相关文件陆续出台,是我国化妆品法规开启新征程的元年。新规对原料的管理,既延续了新原料审批、化妆品原料名单和禁限用物质管理制度,又针对行业的发展需求,结合风险管理的科学理念,开创了分类管理和监测期管理。
针对化妆品原料管理的3个主要特点,回顾化妆品原料监管的发展历程。
1 实行化妆品新原料审批制度
1989年,卫生部颁布《化妆品卫生监督条例》,我国化妆品监管开启卫生监管的时代。《化妆品卫生监督条例》对化妆品新原料给出明确定义,“化妆品新原料是指在国内首次使用于化妆品生产的天然或人工原料”,并指出“使用化妆品新原料生产化妆品,必须经国务院卫生行政部门批准”。
截至2008年8月29日,卫生部仅批准了6个化妆品新原料(表1),随后,进口化妆品、国产特殊用途化妆品和化妆品新原料的许可受理工作由卫生部转移至国家食品药品监督管理局负责。

表1 截至2008年8月29日卫生部批准的化妆品新原料
2008年9月1日起,国家食品药品监督管理局接管化妆品管理后,原料管理进入了一个新的阶段。2009年底,国家食品药品监督管理局发布《化妆品行政许可申报受理规定》,明确将化妆品新原料纳入行政许可审批范畴,并对申报资料的要求等做出了具体规定。法规实施后第一年有20个新原料申报,接下来几年中每年的新申报量约50个。新原料的申报审评工作进展并不顺畅,远远低于业界期待。审评中专家的态度比较保守,对细节要求过细过高,结果导致获批的凤毛麟角[1],截至2020年12月31日,也仅有8个新原料获批(表2)。

表2 国家食品药品监督管理局及国家药品监督管理局批准的化妆品新原料
另外,化妆品新原料获批后,所有化妆品企业均可使用。因此,研发投入高、获批困难、缺乏知识产权保护,致使原料生产企业和化妆品生产企业对新原料研发的积极性不高,从而在一定程度上限制了产品多样化,也使整个化妆品行业新原料发展基本处于停滞状态。
2021年1月1日《化妆品监督管理条例》正式实施,国家对风险程度较高的化妆品新原料实行注册管理,对其他化妆品新原料实行备案管理。自2021年5月1日条例附属文件《化妆品注册备案管理办法》落地以来,大大激发了化妆品原料生产企业及化妆品生产企业的原料研发热情,截至2022年6月14日,已有18个原料取得化妆品新原料备案凭证。
同时,新注册或备案的原料将设3年的监测期,不仅保证了新原料安全风险的持续监控,同时保护了创新企业的利益,鼓励其在研发的投入,一举两得。
2 实行化妆品原料名单制度
从1989年《化妆品卫生监督条例》开始,化妆品新原料是指在国内首次使用于化妆品生产的天然或人工原料。使用新原料前,必须通过监管部门的审批。但是,由于法规刚刚建立,还没有完善的数据库,企业仅熟悉自己所用原料,无法判断该原料在国内其他企业的使用情况,从而无法判断原料是否为新原料。
为解决无法判断新原料的困难,卫生部以截至2000年底批准的化妆品配方为基础,编制了《中国已使用化妆品成分名单》(2003年版),并于2003年4月发布。然而,该名单仅仅收录了卫生部审批的使用于特殊用途化妆品和进口化妆品的原料,共计3 265种,没有包括大量的国产非特殊用途化妆品原料,而此时国际上已使用原料多达1万多种,《中国已使用化妆品成分名单》(2003年版)仍然无法满足企业的实际诉求。
2007年和2010年,卫生部及国家食品药品监督管理局分别对美国化妆品盥洗用品及香水协会2004年和2008年《化妆品原料字典》所收录原料的国际化妆品原料名称(INCI名称)进行翻译,形成《国际化妆品原料标准中文名称目录(2007年版)》和《国际化妆品原料标准中文名称目录(2010年版)》。该两版目录分别收录了12 072种和15 649种原料,但是,该目录仅用于规范原料的标准中文名称和INCI名称,并不能作为判断新原料的依据。
2014年,国家食品药品监督管理总局在对已上市化妆品中曾使用化妆品原料进行整理和客观收录的基础上,形成了《已使用化妆品原料名称目录》,并于2015年进行了修订。2015年版《已使用化妆品原料名称目录》共收录8 783种已使用原料,为判断化妆品新原料提供了参考依据,为化妆品监管工作提供了可靠的技术支撑。
2015年版《已使用化妆品原料名称目录》的颁布,为产品、原料申报中判断是否为新原料提供了依据,对促进化妆品产业发展发挥了积极作用。但由于历史原因,其中的原料并未经过安全性评估。因此,为适应《化妆品监督管理条例》中对原料安全性的评估要求,国家药品监督管理局组织修订,并于2021年4月30日发布《已使用化妆品原料目录》(2021年版)。
2021年版《已使用化妆品原料目录》是对已获批准产品的配方使用原料情况进行数据整理,选取了2010年至2020年3月化妆品行政许可管理系统中已获批准的特殊用途化妆品和进口普通化妆品,通过信息化手段和人工审核整理,对产品配方所有使用过的原料情况进行梳理,分别按照淋洗类和驻留类明确不同原料的最高历史使用量,增补在《已使用化妆品原料目录》中,为化妆品安全风险评估工作提供技术支撑。
3 规定化妆品禁/限用物质
1987年5月28日,卫生部发布《化妆品卫生标准》GB 7916-1987,是中国化妆品首个综合规范性标准,其中涵盖化妆品中禁用物质清单、限用物质清单和准用物质清单(包括着色剂、染发剂、防腐剂、防晒剂清单)。1999年,卫生部颁布《化妆品卫生规范》,正式将上述清单纳入法规体系。此后,卫生部根据我国监管实际,同时参考全球主要国家/地区法规的变化,分别于2002年、2007年进行过两次修订,主要参考欧盟化妆品条例(The Cosmetic Directive 76/768/EEC)于2000年3月和2005年11月以前修订的内容。2007版《化妆品卫生规范》,禁用物质的数量由2002版的496个增加到1 386个,是中国化妆品行业发展新时期、新形势下与国际接轨的需要,为后续化妆品新监管时代的开启奠定了基础。
2008年,卫生部将化妆品卫生许可审批和卫生监督等职能移交国家食品药品监督管理局,2013年成立国家食品药品监督管理总局。此时化妆品行业快速发展,新原料、新技术不断地出现,为了满足行业的发展需求,国家食品药品监督管理总局组织对《化妆品卫生规范》进行了修订,于2015年发布了现行的《化妆品安全技术规范》。本次修订参考了欧盟及世界主要经济体的法规,也增加了我国特色的部分,如化妆品禁用植(动)物组分清单就是基于对中药及天然物质的广泛认知而提出的。此次规范修订也标志着我国化妆品技术法规与国际化妆品标准进一步接轨。《化妆品安全技术规范》的贯彻实施,意味着中国化妆品原料管理更加规范化、标准化和国际化,化妆品市场更加严格和正规,有利于化妆品行业的健康发展[2]。
历次化妆品禁限用物质修订情况见表3。
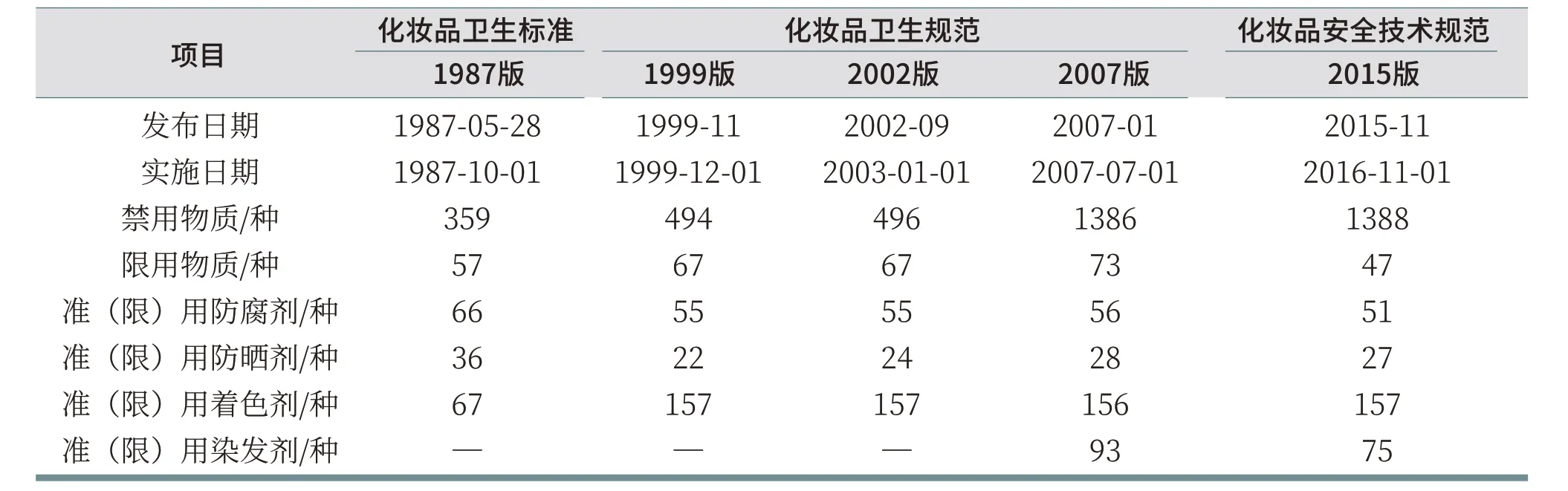
表3 化妆品禁/限用物质历年修订情况
纵观化妆品原料管理的历史,可以看到,化妆品原料的管理由简单到精细,由单一到灵活,但始终坚持原料安全的基本原则。
《化妆品监督管理条例》对化妆品原料管理制度的改革创新,充分体现了基于风险的科学管理理念,是推进简政放权、放管结合、优化服务、不断提高政府效能的具体举措。未来,化妆品原料的研发活力将被充分激发,从而促进我国化妆品产品的研发和创新,引导行业高质量发展。
