《成人肝移植受者免疫抑制方案:意大利工作小组的共识推荐》解读
2022-09-23章云涛吴萍萍沈世超张微梁廷波浙江大学医学院附属第一医院肝胆胰外科肝移植中心浙江杭州310003
章云涛,吴萍萍,沈世超,张微,梁廷波(浙江大学医学院附属第一医院肝胆胰外科,肝移植中心,浙江 杭州 310003)
随着实体器官移植技术的日趋精进和免疫抑制治疗方案的不断优化,各移植中心的移植受者数量不断增多,移植物存活率不断提高。但如何避免排斥反应和减少免疫抑制治疗相关并发症,仍然是移植医生面临的挑战。意大利专家根据不同的肝脏移植受者群体,对术后不同时期(0 ~3 个月及>3 个月)的免疫抑制剂方案进行了规范整理,并于2020 年9 月发表。我们在此解读该共识内容,希望可供国内从事移植相关工作的同行们参考。
长期使用钙调神经磷酸酶抑制剂(calcineurin inhibitor,CNI)会增加肝移植受者肾功能不全、代谢紊乱、神经毒性和新发恶性肿瘤的风险[1-3],约20%肝移植受者在移植后5 年内会出现慢性肾功能衰竭[4]。免疫抑制剂与代谢病关系密切,长期使用会加重或促进肝移植受者代谢性疾病 (糖尿病、高血压、血脂异常、肥胖、高尿酸血症)发生和发展。因此,减少或停用CNI 的策略是目前主流的方向[5]。mTOR 抑制剂(例如依维莫司、西罗莫司等)因其具有免疫抑制和抗增殖双重作用而备受关注。已有研究表明CNI 减量联合mTOR 抑制剂治疗可有效保护肝移植受者肾功能。为了进一步评估现有肝移植免疫抑制治疗方案及不同类型肝移植受者治疗方案的受益情况,意大利肝病和移植专家组成的科学委员会将肝脏移植受者划分为5 类:① 标准受者;② 危重症受者; ③ 具有特定病因的受者;④ 肝癌受者;⑤ 新发恶性肿瘤受者。他们为每类受者分别起草了免疫抑制方案并提交给临床专家评估形成共识,并通过临床实践对共识进行了修订和批准。
根据分类,成人ABO 兼容肝移植受者免疫抑制治疗方案见图1 ~图5。肝移植受者免疫抑制治疗方案的总原则见表1,有关注释如表2 所示。

表1 肝移植受者免疫抑制治疗方案综述

表2 肝移植受者免疫抑制治疗方案的注释

图1 标准受者的免疫抑制方案
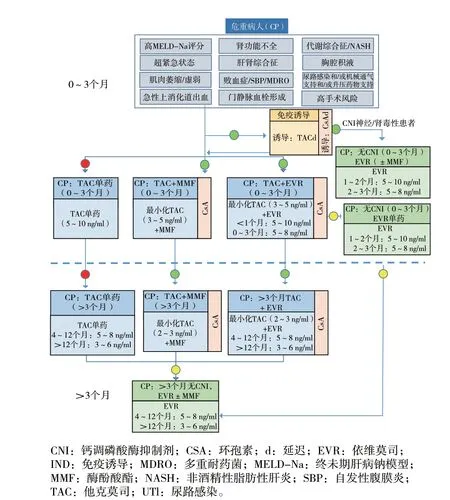
图2 危重受者的免疫抑制方案
3 具有特定病因学的肝移植受者
3.1 定义/描述: 伴或不伴肾脏受累的多囊性肝病、需要肝肾联合移植、自身免疫性肝病、神经内分泌肿瘤、转移性结直肠癌或胆管细胞癌等肿瘤移植适应证受者(图3)。

图3 针对特定病因受者的免疫抑制方案

图4 肝细胞癌患者的免疫抑制方案

图5 新发恶性肿瘤受者的免疫抑制方案
1 标准患者
1.1 定义/描述 :终末期肝病模型(model for endstage liver disease,MELD)评分<25 且无自身免疫性疾病、肝细胞肝癌(hepatocellular carcinoma,HCC)及肾功能不全等病史的低风险受者。
1.2 文献中相关支持证据:早期〔移植后(30±5) d〕或非常早期(移植后10 d)使用mTOR 抑制剂可以减少CNI 暴露,可将受者移植后1 年的估算肾小球滤 过 率(estimated glomerular filtration rate,eGFR)提高8 ~12 ml/(min·1.73m2)[6]。在H2304 研究及H2304 扩展研究中,移植后(30±5)d 随机分配肝移植受者到依维莫司加减量他克莫司组(实验组)与传统的他克莫司组,在移植术后12 个月、24 个月、36 个月实验组的eGFR 均优于对照组(P 值分别为P <0.001,P =0.002,P =0.005)[7-9]。在PROTECT 研究中,203 例肝移植受者在移植后4 周被随机分配到停用CNI 治疗并切换为依维莫司组或继续CNI 方案组,移植后12 个月eGFR 在依维莫司治疗组优于CNI 组(治疗差异为7.8 ml/min,P =0.021)[10],到35 个月,依维莫司依然优于实验组〔使用Cockcroft-Gault 公式计算的eGFR 差异为10.1 ml/min,P =0.082,使用Nankivell 公式计算的eGFR 差异为9.4 ml/(min·1.73 m2),P =0.053〕。依维莫司治疗组(将CNI 替换为依维莫司)与CNI治疗组(继续CNI 治疗),移植术后12 个月eGFR在依维莫司治疗组优于CNI 治疗组(治疗差异为7.8 ml/min,P =0.021)[10];至35 个月,依维莫司治疗组依然优于CNI 治疗组(Cockcroft-Gault公式计算的eGFR 差异为10.1 ml/min,P =0.082;Nankivell 公式eGFR 差异为9.4 ml/(min·1.73 m2),P =0.053)。另一项纳入78 例肝移植患者的研究显示在移植术后12 个月依维莫司治疗组(早期停用环孢素改依维莫司治疗)患者相比于环孢素持续治疗组患者肾功能显著改善〔平均eGFR值(MDRD 公式)分别为(87.6±26.1) ml/min 和(59.9±12.6) ml/min;P <0.001〕[11]。有随机研究和回顾性分析的证据表明CNI 的减量治疗策略宜尽早施行。如果将CNI 减量的治疗策略推迟到肾功能恶化发生〔eGFR <60 ml/(min·1.73 m2)〕时,肾功能的改善非常有限[12-14]。
1.3 推荐和专家意见摘要(图1):基础免疫抑制方案为CNI(他克莫司或环孢素),不推荐他克莫司单药治疗。早期CNI 减药后使用依维莫司或麦考酚酸衍生物是可行的,并可通过给予诱导剂(通常用巴利昔单抗)以进一步促进CNI 减量。建议采用不含类固醇的方案。
2 危重症受者
2.1 定义/描述:高终末期肝病模型联合血清钠评分(即MELD-Na >29 或者MELD-Na =25 ~29 伴有肾功能不全/透析或慢性脑病)、超紧急状态、急性上消化道出血、肾功能不全/透析、肝肾综合征、脓毒症,自发性细菌性腹膜炎、多药耐药菌的定植、门静脉血栓、代谢综合征或非酒精性脂肪性肝炎、胸水、尿路感染和/或机械通气支持和/或使用正性肌力药物、高手术风险及以肌少症为特征的体弱受者等。
2.2 文献相关支持证据:由于大多数临床研究纳入的都是低风险受者(如无肾功能损害),危重症受者的相关文献研究缺乏支持证据。
2.3 建议总结和专家意见(图2):建议对危重症受者进行诱导治疗(例如巴利昔单抗方案),CNI推迟到移植后3 ~5 d 使用。对于高MELD-Na(>29)的患者,应慎重考虑使用诱导治疗。与标准受者相比,CNI 应以更低剂量开始且不推荐CNI单药治疗。存在代谢异常和失代偿性糖尿病的受者可选择环孢素替代他克莫司。建议联合使用霉酚酸衍生物和依维莫司来进行CNI 减量。出现CNI 相关的神经或肾毒性症状的受者,可以考虑停用CNI。依维莫司适用于有肾功能不全风险或经eGFR 评估证实为肾功能不全的受者。有糖尿病或代谢性疾病的受者也会受益于依维莫司,因为mTOR 抑制剂除了具有肾脏保护特性外,还具有心血管保护作用。高脂血症、高三酸甘油酯血症在使用依维莫司前需要治疗。合并蛋白尿的受者需要进行肾功能检查并采取相应的对症治疗。
3.2 文献相关支持证据:内分泌肿瘤肝转移的受者可以进行肝移植,有研究发现移植后5 年总生存率为47%~97%,无瘤生存率为32%~87%[15-17],生存结果与HCC 受者肝移植相似[16]。术后肿瘤复发率仍然较高,建议维持低免疫抑制剂状态。对于结肠癌肝转移患者,肝移植效果需要通过临床试验和实践进行验证。挪威针对21 例无法切除的结直肠肝转移受者的研究表明,移植后5 年生存率为60%,优于单纯化疗组患者[18]。另一项无法切除的仅肝转移的结直肠癌受者肝移植研究中,移植后5 年总生存率达83%[19],充分说明患者选择标准的改进对获得最佳生存率有重要影响[20]。胆管细胞型肝癌是第二大常见的肝癌,预后很差。肿瘤大小 (>2 cm)和多发结节是肿瘤复发的危险因素[21]。接受新辅助放化疗后再行肝移植的一项临床研究结果发现有不错的临床效果[22]。当然,免疫抑制策略必须平衡肿瘤复发风险。也有实验和临床证据表明mTOR 抑制剂在胆管细胞型肝癌中具有抗增殖、抗肿瘤作用[23]。
3.3 建议和专家意见(图3):① 孤立的多囊肝(polycystic liver disease,PCLD)患者,由于手术复杂,免疫抑制剂使用可参考危重受者。患有常染色体多囊肝多囊肾和肾功能损害和/或接受肾脏替代治疗的受者可考虑同时或延迟联合肝肾移植。在这种情况下,免疫抑制治疗根据临床情况并经过仔细的多学科评估后,可将患者纳入标准组或者重症组。上述受者均应尽早实施CNI 减量联合依维莫司治疗,以避免进一步损害肾脏。② 对于肿瘤受者:应考虑早期使用mTOR 抑制剂,这也适用于移植后有新发恶性肿瘤风险的疾病,如酒精相关肝病。③ 自身免疫性肝病:应使用他克莫司和皮质类固醇治疗,并根据疗效和不良反应调整后者剂量,也可以添加依维莫司或霉酚酸酯。可以使用环孢素代替他克莫司,尤其是原发病复发接受二次移植的受者。
4 肝细胞癌受者
4.1 定义/描述:因HCC 接受肝移植的受者。
4.2 文献相关支持证据:mTOR 抑制剂可以减缓肝移植受者的HCC 复发和进展[24-26]。在对2491 例患者进行的多变量分析中,西罗莫司组肝癌肝移植受者术后生存率显著优于传统CNI 组(风险比=0.53,95% CI =0.31 ~0.92;P ≤0.05), 并 且其复发率也明显低于传统CNI 组[24-25](8%比13.8%;P <0.001)。尽管在525 例HCC 肝移植受者前瞻性随机3 期临床试验中,仅在符合米兰标准的患者(即低风险患者)中观察到mTOR 抑制剂的显著益处[27],并且mTOR 抑制剂对HCC 的复发和生存率的影响在移植后3 ~5 年是最明显的,但此后并未持续。来自美国移植受者登记库的资料表明,肝癌肝移植受者在肿瘤复发的生存率上均获益于以mTOR 为基础的免疫抑制剂治疗方案,并且在年龄<55 岁的受者中差异更明显[28]。将23 项关于肝移植受者肝癌生存和复发的研究进行系统回顾和荟萃分析发现:基于mTOR 信号途径的免疫抑制方案显著提高肝移植术后1 年和3 年的生存率(风险比分别为1.09 和1.1),减缓了复发风险(RR =0.67)[29]。
4.4 建议和专家意见(图4):建议所有HCC 肝癌肝移植患者实施CNI 减量的策略,并切换为以mTOR 抑制剂为基础的免疫抑制剂方案,以限制CNI 相关的肾脏毒性和CNI 暴露对癌症复发的影响。同时首选无类固醇免疫抑制方案。
5 新发恶性肿瘤
5.1 定义/描述:肝移植受者在移植后任何时候都可能发生新发恶性肿瘤,包括肝外实体瘤、非黑色素瘤皮肤癌和淋巴增生性疾病等。
5.2 文献相关支持证据:在心脏、肾脏和肝脏移植受者研究中发现,使用mTOR 抑制剂可降低实体器官移植后新发恶性肿瘤的发生率[30-31]。mTOR抑制剂可用作单一疗法或与低剂量CNI 联合使用,具体取决于个体风险因素(即移植后时间、移植适应证、移植年龄等)。
5.3 建议和专家意见(图5):所有具有新发恶性肿瘤高风险的肝移植受者(即人类疱疹病毒-8 型阳性、酒精性肝硬化、并发炎症性肠病、供器官来自有恶性肿瘤传播风险的捐献者、移植后EB 病毒DNA 阳性)均推荐使用基于mTOR 抑制剂的免疫抑制。
6 讨 论
此共识侧重于如何减少免疫抑制治疗带来的相关不良事件,而不聚焦治疗肝移植的急性排斥反应。对于肝移植急性排斥的管理和治疗,仍然建议参照国际肝移植协会免疫抑制剂共识指南[32]。
尽管肝移植在意大利和其他中心都快速开展,但不同移植中心使用的免疫抑制方案存在较大差异。意大利工作组开展此项目,旨在将成人ABO血型兼容的肝移植免疫抑制剂方案标准化,为移植医生提供指导。对移植受者的免疫抑制方案进行分层管理,体现了本共识的科学性和客观性。个体化免疫抑制方案的探索始终贯穿整个移植过程,只有准确充分地评估好不同移植受者及其每一个阶段的免疫状态、脏器功能、合并症等情况,才能制定出科学、合理、精准的个体化免疫抑制方案。这也是精准医疗最关键的核心[33-35]。现阶段仍存在许多有争议或未解决的问题,包括蛋白尿的管理、危重症受者的管理,mTOR 抑制剂在预防肝癌复发中的证据支持还非常有限,需要更深入的研究来佐证其预防肝癌复发的作用。
7 展 望
肝移植免疫抑制方案的选择应考虑多种临床变量[36-37],包括原发疾病、移植时患者状态、手术类型、术后早期事件以及与长期使用CNI 相关的预期并发症。目前的临床实践与证据支持移植后应尽早实施预防CNI 相关不良事件的策略。最有效的肾脏保护策略是通过早期使用依维莫司或霉酚酸酯(如果尚未应用依维莫司)来减少CNI 暴露。精准评估每一个移植受者及其不同阶段免疫状态,最大程度上科学合理制定个体化免疫抑制方案,是移植术后免疫抑制管理的精髓。同时,供器官短缺仍然是当今移植界面临的主要问题,探索并建立科学合理的边缘供器官移植术后的免疫抑制方案、异种移植免疫抑制方案,是移植专家们未来需要进一步研究的方向。
