呋喃唑酮代谢物人工抗原的制备与鉴定
2022-09-23吴海涛圣志存陈晓兰苏棪华柳青青
吴 萌, 吴海涛, 圣志存, 陈晓兰, 苏棪华, 柳青青
(江苏农牧科技职业学院,江苏泰州 225300)
呋喃唑酮(furazolidone),学名3-(5-硝基糠醛缩氨基)-2-唑烷酮,又名痢特灵,属于硝基呋喃类药物,具有广谱的抗菌作用;现代药理毒理试验研究表明,呋喃唑酮在机体内代谢周期短、易衰减,主要代谢物为3-氨基-2-唑酮(AOZ),分子结构式,结果见图1-A,AOZ可与机体内组织蛋白紧密结合,从而残留数周,对人体具有潜在的致癌、致突变作用。因此,我国相关法规明确规定严禁动物性食品中添加包括呋喃唑酮在内的硝基呋喃类药物。但在实际生产中,由于呋喃唑酮预防和治疗细菌性感染效果显著且价格低廉,所以仍存在非法使用的情况。因此,建立快速、简便的检测方法自然尤为重要。由于呋喃唑酮衰减原因,研究者们大多以AOZ作为标志物检测呋喃唑酮是否非法使用。
目前,检测呋喃唑酮代谢物AOZ残留常用的方法为液相色谱-串联质谱法(LC-MS/MS),具有检测灵敏度高、结果准确性好等优点,但存在前样处理复杂、检测时间长、成本昂贵等问题,尤其不适合大批量样品的快速筛查。免疫分析法因灵敏度高、特异性强、简便、样品高通量及成本低等优点也成为检测呋喃唑酮代谢物的一种重要手段,其建立的关键是获得免疫学特性优良的抗体,而抗体获得的前提条件为制备待测物的免疫原。
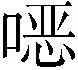

1 材料与方法
1.1 试验动物
试验于2020年12月于江苏农牧科技职业学院生物制药技术实验室完成。SPF级BALB/c小鼠(6周龄,雌性),购自扬州大学比较医学中心。
1.2 试剂及仪器设备
2-NP-AOZ:纯度≥99.9%,坛墨质检科技股份有限公司;弗氏完全佐剂、弗氏不完全佐剂、牛血清白蛋白(BSA):纯度≥98%;鸡卵清白蛋白(OVA):纯度≥98%,默克集团(Merck);BCA蛋白定量试剂盒、明胶封闭缓冲液、ELISA显色液与终止液、HRP-羊抗小鼠二抗:生工生物工程(上海)股份有限公司;1×PBS(pH值7.2~7.4)缓冲液、1×PBST缓冲液(pH值7.2~7.4):北京索宝来科技有限公司;乙腈、亚硝酸钠:均为AR,阿拉丁试剂(上海)有限公司。
DK-S11数显水浴锅,上海浦东荣丰科学仪器有限公司;4800 Plus MALDI-TOF/TOF质谱仪,AB SCIEX 公司;3500BR全自动凝胶成像分析系统,上海天能科技有限公司;VE180垂直电泳仪,上海天能科技有限公司。
1.3 方法
1.3.1 完全抗原的合成 采用重氮法合成呋喃唑酮代谢物AOZ的完全抗原,包括免疫原2-NP-AOZ-BSA和包被原2-NP-AOZ-OVA。准确称取AOZ衍生物(2-NP-AOZ)5 mg,溶解于500 μL乙腈中,加入2 mL浓度为1 mol/L的盐酸,搅拌,再加入2 mg锌粉,振荡混匀;水浴中加热 20 min,取上清冷却至4 ℃,获得2-NP-AOZ还原液。1 mol/L盐酸调节还原液pH值至1.0~2.0,加入2 mol/L亚硝酸钠溶液,至淀粉碘化钾试纸检验呈灰蓝色。将上述混合液逐滴加至1 mL含50 mg的0.01 mol/L BSA且pH值为7.4的PBS溶液中,搅拌,调节pH值至8.5,避光条件下振荡1 h,放置在4 ℃冰箱过夜。PBS透析4 h,5 000 r/min离心10 min,收集上清,即为免疫原2-NP-AOZ-BSA。包被原2-NP-AOZ-OVA的制备方法同上,以OVA代替BSA。
1.3.2 完全抗原浓度的测定 采用BCA试剂盒法测定人工抗原的浓度。将试剂盒中BSA标准品溶液(5 mg/mL)以PBS稀释成0.000、0.025、0.050、0.100、0.200、0.300、0.400、0.500 mg/mL,分别取稀释好的BSA标准品和待测人工抗原各20 μL置于96孔板中,加入200 μL/孔 BCA工作液,混匀;37 ℃ 水浴保温30 min。冷却至室温后,在酶标仪中测定各孔的值。以标准组各管平均值为纵坐标,对应的蛋白质浓度为横坐标,绘制标准曲线,计算待测人工抗原的浓度。
1.3.3 紫外扫描光谱鉴定合成的完全抗原 将2-NP-AOZ-BSA 和2-NP-AOZ-OVA稀释至0.5 mg/mL,以BSA、OVA、2-NP-AOZ标准品溶液作为对照,在200~400 nm范围内对上述溶液进行紫外光谱扫描,记录图谱,根据人工抗原与2-NP-AOZ标准品和载体蛋白BSA(OVA)吸收峰的变化判断偶联效果。
1.3.4 SDS-PAGE鉴定合成的完全抗原 将待测品BSA、OVA、2-NP-AOZ-BSA与2-NP-AOZ-OVA均配制为0.5 mg/mL溶液,分别与5×SDS Loading Buffer按照5 ∶1体积比混合,煮沸 10 min。取煮沸后待测样各20 μL加入上样孔,经10%分离胶分离;电泳结束后以考马斯亮蓝染色液染色1 h后,脱色,至蛋白条带清晰无杂色。根据条带位置即蛋白泳动速度判断偶联是否成功。
1.3.5 MALDI-TOF-MS鉴定合成的完全抗原 将2-NP-AOZ-BSA和2-NP-AOZ-OVA稀释至1 mg/mL,经脱盐处理后分别与基质溶液混合,BSA和OVA溶液作为对照。点靶,置于质谱仪内进行激光扫描,获取离子质谱图,根据样品相对分子量判断是否偶联成功并计算偶联比。偶联比=(-)/,其中:表示相对分子质量。
1.3.6 动物免疫 选6只6周龄雌性SPF级BALB/c小鼠,4只以2-NP-AOZ-BSA为免疫原免疫;1只为空白对照,以PBS为免疫原免疫;1只为阴性对照,相同的条件下饲养。首次免疫时加入等量的弗氏完全佐剂混合,以50 μg/只多点皮下注射。第2、第3、第4次免疫时用等量的弗氏不完全佐剂代替弗氏完全佐剂与免疫原混匀;第5次免疫时不添加7 d后采血,37 ℃放置2 h后置于4 ℃过夜,3 000 r/min 离心10 min,收集上清,-20 ℃保存。
1.3.7 免疫血清效价的测定 采用间接ELISA测定血清效价。将包被原2-NP-AOZ-OVA稀释至2.5 μg/mL,以100 μL/孔包被于96孔ELISA板上,37 ℃孵育2 h;PBST洗板,3次后加入 250 μL/孔 1%明胶封闭液,37 ℃孵育2 h;PBST洗板,3次后加入倍比稀释的多抗血清100 μL/孔,并设置阴性、空白对照,37 ℃孵育2 h;PBST洗板,3次后加入稀释好的羊抗鼠酶标二抗100 μL/孔,37 ℃ 孵育1.5 h;PBST洗板后,加入100 μL/孔 TMB显色液,避光反应10 min后加入终止液,50 μL/孔。酶标仪上选定空白对照后,测定值,待测孔为,阴性对照为,当≥02且≥2.1 时,判定为阳性。
1.3.8 免疫血清敏感性的测定 采用间接竞争ELISA测定AOZ免疫血清的敏感性。将2-NP-AOZ-OVA包被至ELISA板上,加入50 μL/孔不同质量浓度的2-NP-AOZ标准品(1 000.000、500.000、250.000、125.000、62.500、31.250、15.625、7.813、3.906、1.953、0.000 ng/mL)和 50 μL/孔为1.0对应稀释倍数的多抗血清;最后一孔只添加50 μL的PBS,设置为空白对照。其他步骤见“1.3.7”节。以(代表不同质量浓度 2-NP-AOZ标准品孔的,代表2-NP-AOZ标准品质量浓度为0时的)为纵坐标,以2-NP-AOZ标准品质量浓度对数为横坐标绘制抑制曲线,计算AOZ多抗的半数抑制浓度IC,并通过IC判断抗体的敏感性。
2 结果与分析
2.1 完全抗原浓度的测定
由图2可知,线性回归方程式为=0912 4+0110 4,=0.996 1,计算人工抗原2-NP-AOZ-BSA浓度为4.9 mg/mL,2-NP-AOZ-OVA浓度为5.2 mg/mL。
2.2 完全抗原的紫外光谱扫描测定
由图3-A可知,BSA在279 nm左右有最大吸收峰,2-NP-AOZ-BSA的特征性吸收峰相比BSA有一定程度的偏移,且与2-NP-AOZ的紫外光谱图和趋势不同,初步判断2-NP-AOZ与BSA偶联成功。
由图3-B可知,2-NP-AOZ-OVA的紫光吸收曲线较OVA与2-NP-AOZ均发生明显变化,初步判断2-NP-AOZ与OVA偶联成功。

2.3 完全抗原的SDS-PAGE鉴定
由图4可知,相同条件下2-NP-AOZ-BSA的迁移速率小于BSA,2-NP-AOZ-OVA的迁移速率小于OVA,均出现了明显的拖尾现象。说明2-NP-AOZ-BSA分子量明显大于BSA,2-NP-AOZ-OVA分子量明显大于OVA,推测BSA、OVA均成功偶联了部分2-NP-AOZ,可初步判定免疫原与包被原合成成功。

2.4 完全抗原的MALDI-TOF-MS分析
由图5可知,人工抗原2-NP-AOZ-BSA与 2-NP-AOZ-OVA相对分子量较载体蛋白相对分子量明显增大,与SDS-PAGE显示人工抗原比载体蛋白泳动速度慢的结果一致,表明偶联成功。由图5-A可知,2-NP-AOZ-BSA的相对分子量为67 892.54,BSA的相对分子量为66 228.92;由图 5-B 可知,2-NP-AOZ-OVA的相对分子量为 45 383.69,OVA的相对分子量为 44 484.31,根据 2-NP-AOZ相对分子量大小,得出2-NP-AOZ与BSA的偶联比为7.1 ∶1,2-NP-AOZ与OVA的偶联比为3.8 ∶1。

2.5 免疫血清效价的测定
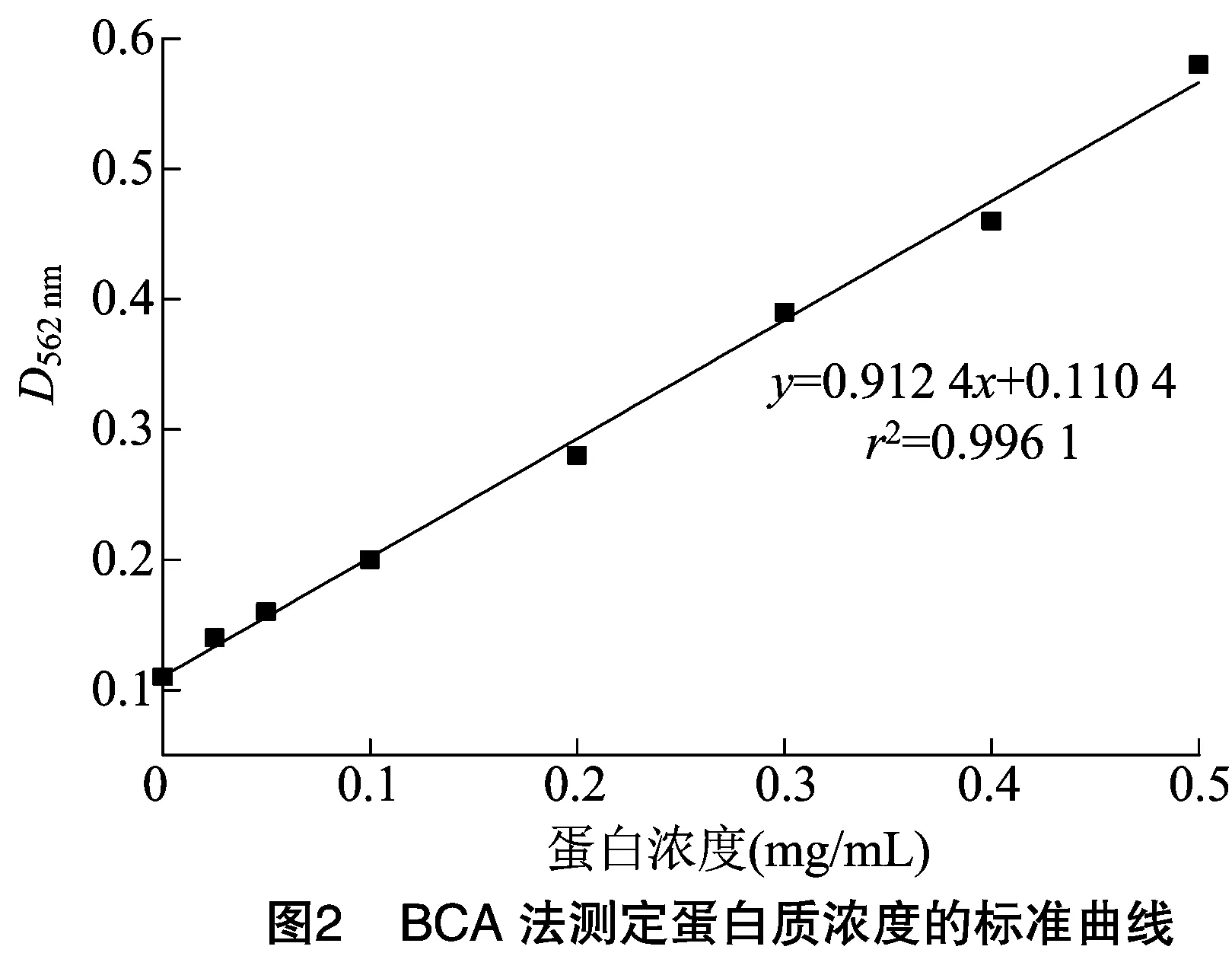
由表1、表2可知,4只以2-NP-AOZ-BSA为免疫原进行免疫的小鼠经3次免疫后血清效价均达1 ∶16 000及以上;经5次免疫后血清效价均达 1 ∶32 000 及以上。以2-NP-AOZ-OVA为包被原检测小鼠血清,避免了血清中针对载体蛋白的抗原-抗体特异性反应,表明以合成的免疫原免疫小鼠后产生了针对2-NP-AOZ的抗体,且随着免疫次数增加,人工抗原免疫效果增强。

表1 3次免疫后小鼠血清效价测定结果
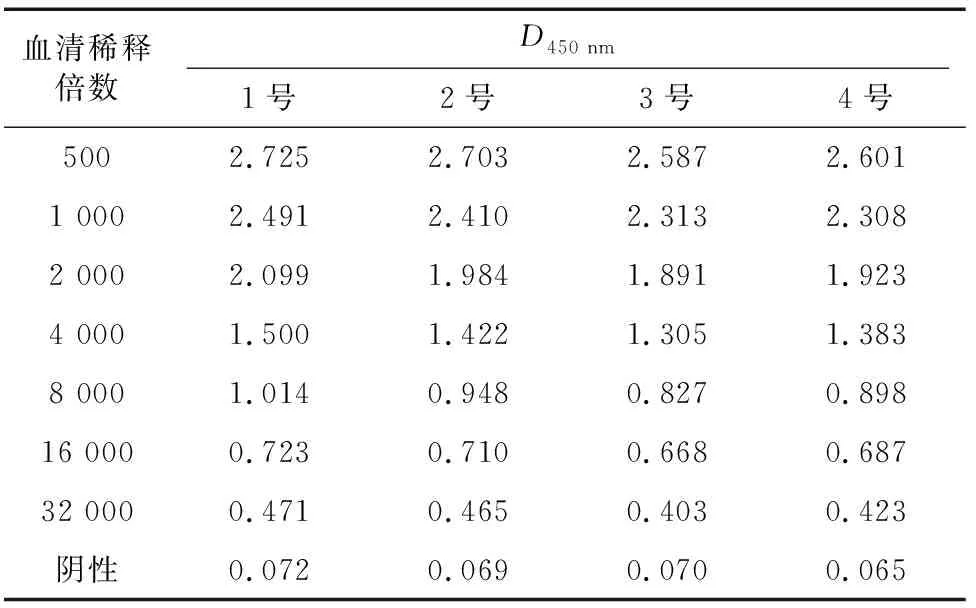
表2 5次免疫后小鼠血清效价测定结果
2.6 免疫血清敏感性的测定
以1号小鼠免疫血清为例,通过间接竞争ELISA测定免疫血清的敏感性。由图6可知,2-NP-AOZ对小鼠免疫血清有抑制作用,其线性回归方程式为=-0254+0890 3,为0.986 5,IC为34.43 ng/mL。免疫血清敏感性鉴定结果说明,2-NP-AOZ与载体蛋白成功偶联,合成了免疫原性良好的人工抗原,该抗原能有效刺激机体产生特异性免疫应答,可产生敏感性较好的抗2-NP-AOZ的血清。
3 讨论
免疫学认为相对分子量小于1 000 u的分子仅具备反应原性,无免疫原性。呋喃唑酮代谢物(AOZ)分子量为102,为典型小分子物质,因此不能刺激机体产生免疫应答,必须与大分子物质如蛋白质载体偶联,形成完全抗原后才具有免疫原性。本研究前期曾尝试以AOZ直接连接载体蛋白BSA来生产制备抗体,但效果不理想,这与李敏等的结果一致;原因可能是AOZ分子量太小,直接偶联载体蛋白会被蛋白质分子包裹,不能形成有效的抗原表位,导致产生的抗体免疫学特性较差,通常以AOZ衍生物(即在AOZ上连接1个间隔臂)代替AOZ合成人工抗原。相关研究表明,免疫效果与间隔臂有关,间隔臂长度为3~6个碳为宜;除此之外,具有苯环的半抗原分子制备抗体的成功率为30%,而不含苯环则成功率仅为9%。温丹华等选择AOZ衍生物CP-AOZ合成人工抗原,制备抗体,建立免疫学检测方法,与前人研究常用的AOZ衍生物不同,本研究选择了同样具有苯环的AOZ衍生物2-NP-AOZ合成人工抗原,原因是后期建立AOZ免疫学检测方法时需要将检测样品衍生化,常得到的衍生化产物为2-NP-AOZ,且市面上有2-NP-AOZ的标准品而无CP-AOZ的标准品。

小分子与蛋白质是否偶联成功可用多种方法鉴定,如紫外吸收光谱法、红外吸收光谱法、SDS-PAGE、核磁共振氢谱、质谱等。由于2-NP-AOZ中含有可还原硝基,本研究采用重氮法分别与BSA和OVA偶联获得免疫原和反应原;先通过SDS-PAGE判定偶联效果,结果显示,偶联物的泳动速度小于载体蛋白的泳动速度,初步证明偶联成功。然后通过MALDI-TOF-MS分析分子偶联物和载体蛋白的分子量差别,判断偶联成功。Erlange研究发现,偶联率3~25 ∶1比较合适;但也有学者认为半抗原与载体蛋白的偶联比对诱导抗体产生无决定性影响。本研究采用MALDI-TOF-MS分析法根据相对分子量差异计算偶联比,简单快速且结果准确,得出 2-NP-AOZ与BSA偶联比为 7.1 ∶1,与OVA偶联比为3.8 ∶1,均在适宜范围内。
半抗原与载体蛋白反应合成的人工抗原,虽然从其分子结果已经证明偶联成功,但合成的免疫抗原是否具有免疫原性,最终必须通过免疫学试验来检验。本研究以2-NP-AOZ-BSA为免疫原免疫小鼠,3次免疫后血清效价均达1 ∶16 000及以上,5次免疫后血清效价均达1 ∶32 000及以上,说明人工合成的抗原能有效刺激机体产生免疫反应,具有良好的免疫原性,且免疫次数增多,免疫效果增强。
4 结论
本研究以AOZ的衍生物2-NP-AOZ分别偶联BSA和OVA,制备免疫原2-NP-AOZ-BSA和包被原2-NP-AOZ-OVA,经紫外光谱扫描、SDS-PAGE、MALDI-TOF-MS分析初步判断偶联成功,偶联率分别为7.1 ∶1和3.8 ∶1。将免疫原以50 μg/只免疫小鼠,3次和5次免疫后小鼠血清效价达1 ∶16 000及以上和1 ∶32 000及以上,合成的人工抗原具有良好的免疫原性。本研究完成了AOZ人工抗原的合成,为AOZ单克隆抗体的制备和免疫学检测方法的建立奠定了基础。
