心脏外科术后肺部并发症发生风险的列线图预测模型构建
2022-09-22朱鑫灜
张 静 李 娟 朱鑫灜 袁 超
心脏瓣膜疾病是临床上常见的心脏疾病,通常采取心脏瓣膜置换手术[1-2]。目前,多数心脏瓣膜置换术依赖于体外循环,但体外循坏易导致血细胞破坏、炎性细胞因子释放及全身多脏器缺血性再灌注损伤,是引发肺部并发症的危险因素[3]。采取有效的临床措施保护患者心肺功能,可明显降低术后肺部并发症的发生。尽管临床已研究影响心脏外科手术患者术后发生肺部并发症的危险因素[4],但尚不能精准预测肺部并发症的发生风险。列线图是一种图形描述,可呈现回归模型并简化风险评估,反应每个患者发生不良事件的概率,以识别手术患者术后肺部并发症发生风险[5-6]。因此,本研究旨在通过构建个体化预测心脏外科术后患者肺部并发症发生的列线图模型,以早期辅助临床对心脏外科手术患者术后发生肺部并发症风险进行评估。现报道如下。
1 资料与方法
1.1 一般资料 选取2016年1月至2021年3月郑州市第七人民医院收治的择期进行心脏瓣膜手术的患者517例为研究对象,其中男性280例,女性237例;年龄31~74岁,平均(50.79±11.62)岁。纳入标准:①患有心脏疾病,且具有体外循环心脏手术治疗的适应症;②接受体外循环下心脏瓣膜置换术;③进行手术前肝功能正常。排除标准:①先天性心脏病者;②恶性肿瘤者;③妊娠期、哺乳期患者;④术前行气管插管患者。本研究对象行二尖瓣置换术403例,二尖瓣+主动脉瓣置换术86例,三尖瓣置换术28例。本研究经医学伦理委员会批准(批准文件号:2016-002)。
肺部并发症的诊断:肺部并发症定义为围术期肺炎或呼吸功能衰竭。肺炎依据相关性肺炎诊断标准[7]:痰培养阳性需用抗生素治疗﹐或胸部X线诊断肺炎;呼吸功能衰竭[8]:患者术后无创呼吸支持持续48 h以上或再次气管插管呼吸机>48 h。将所有患者根据术后是否发生肺部并发症,分为肺部并发症组(n=88)和无肺部并发症组(n=429)。肺部并发症组男性53例,女性35例,年龄31~74岁,平均(63.42±10.05)岁;无肺部并发症组男性227例,女性202例,年龄31~74岁,平均(48.26±10.74)岁。两组患者年龄、性别比较,差异无统计学意义(P>0.05)。
1.2 观察指标 收集所有研究对象的年龄、性别、糖尿病史、术前体质量指数、吸烟史、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)史、术后2 h清蛋白水平、术后2 h白细胞计数水平、术前NYHA心功能分级、术中体外循环时间、主动脉阻断时间、术后机械通气时间、应用血管活性药物情况、心脏换瓣手术类型(二尖瓣置换手术、二尖瓣+主动脉瓣置换术、三尖瓣置换术)等临床资料。比较肺部并发症组和无肺部并发症组以上指标差异,分析独立风险因素。
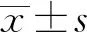
2 结果
2.1 两组患者术后发生肺部并发症风险的单因素分析 本研究517例心脏外科术后患者肺部并发症发生88例,发生率为17.02%(88/517)。两组患者性别、糖尿病比例、体质量指数、NYHA心功能分级、应用血管活性药物的比例心脏换瓣手术类型比较差异均无统计学意义(P>0.05);肺部并发症组年龄、吸烟史比例、COPD比例、术后清蛋白<35 g/L比例、术后清蛋白水平、术后白细胞计数≥10×109/L比例、术后白细胞计数水平、术中体外循环时间、主动脉阻断时间、术后机械通气时间明显高于无肺部并发症组患者,差异有统计学意义(P<0.05)。见表1。
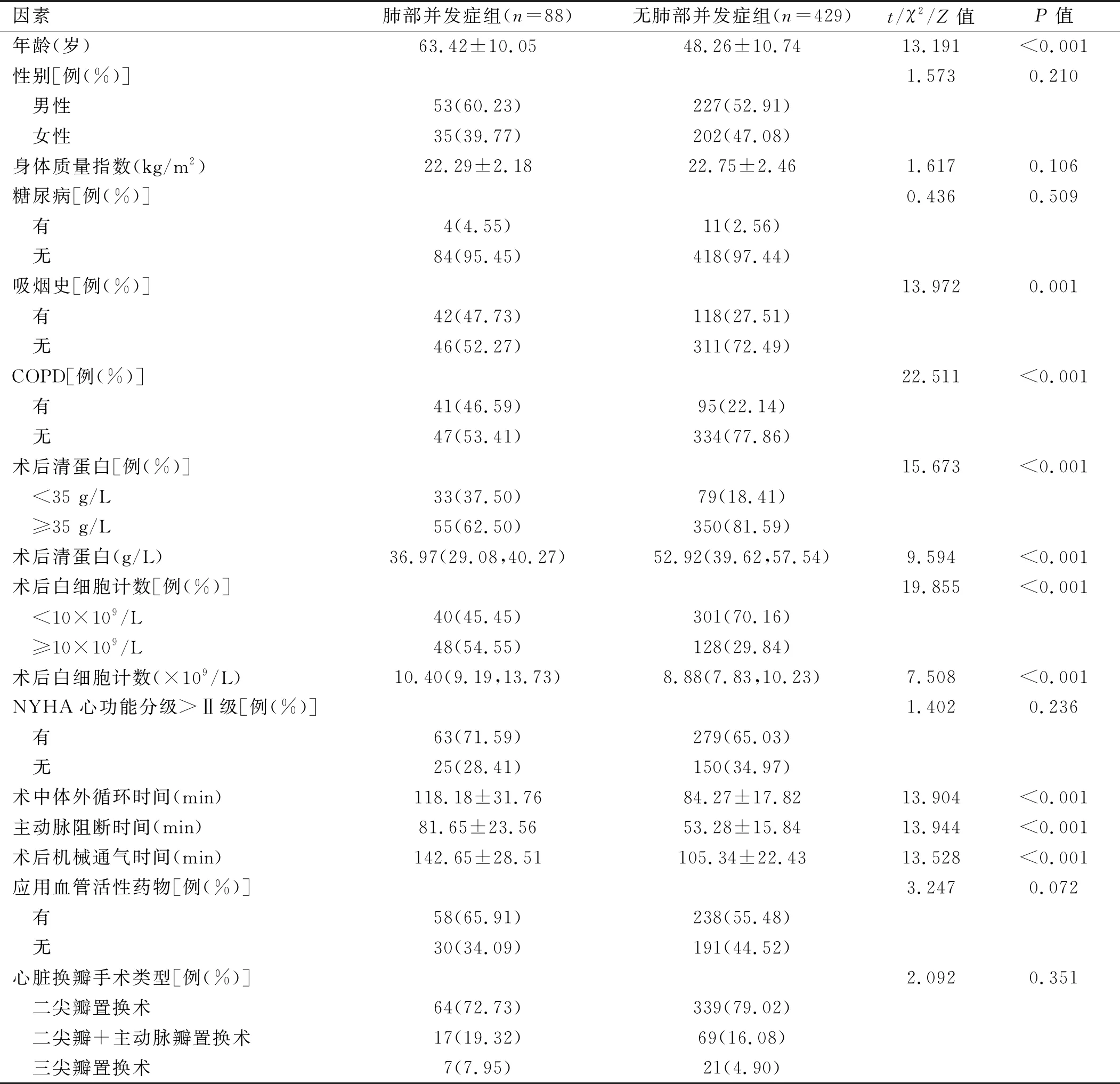
表1 两组患者术后发生肺部并发症风险的单因素分析
2.2 心脏外科手术患者术后发生肺部并发症的多因素logistic回归分析 将心脏外科术后患者是否有肺部并发症发生作为因变量(无肺部并发症=0,肺部并发症=1),将有统计学意义的单因素(年龄、吸烟史、COPD、术后清蛋白、术后白细胞计数、术中体外循环时间、主动脉阻断时间、术后机械通气时间)作为自变量进行分析,变量赋值方式见表2。多因素logistic回归分析结果显示,年龄(OR=1.163,95%CI:1.114~1.214)、术后清蛋白<35 g/L(OR=3.009,95%CI:1.339~6.763)、主动脉阻断时间(OR=1.065,95%CI:1.037~1.093)、术后机械通气时间(OR=1.052,95%CI:1.032~1.072)是影响心脏外科手术患者术后发生肺部并发症的危险因素(P<0.05)。见表3。

表2 变量赋值方式
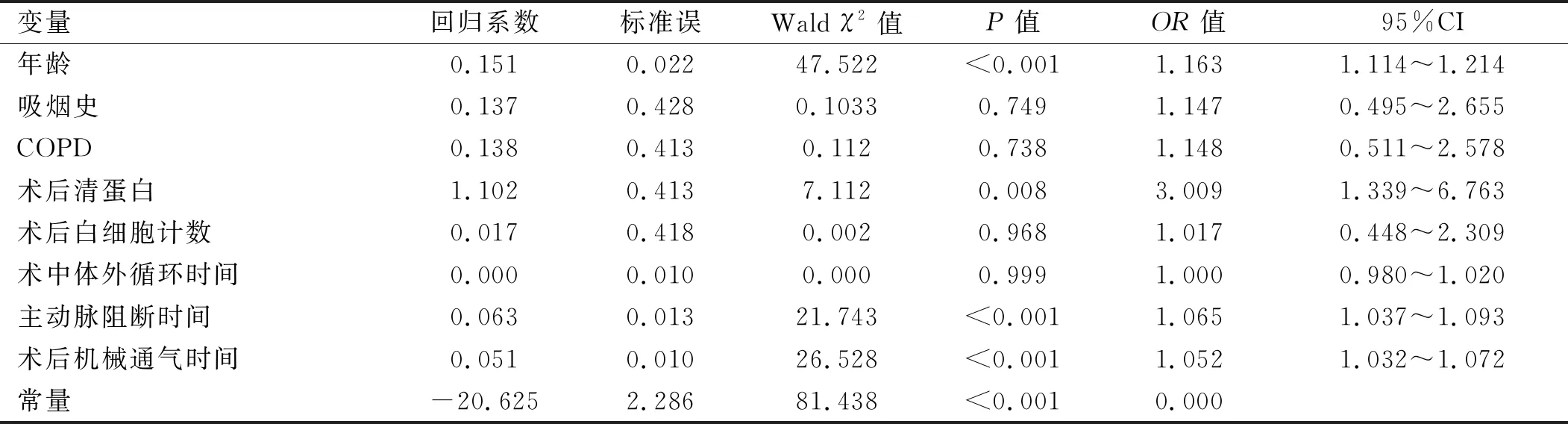
表3 心脏外科手术患者术后发生肺部并发症风险的多因素logistic回归分析
2.3 预测心脏外科手术患者术后发生肺部并发症的列线图模型建立 使用R软件构建心脏外科手术患者术后发生肺部并发症的列线图预测模型(见图1),各因素对心脏外科手术患者术后发生肺部并发症的影响程度以分值形式呈现,年龄每增加5岁,评分增加7.7分,术后清蛋白<35 g/L为11分,主动脉阻断时间每增加10 min,评分增加6.22分,术后机械通气时间每增加10 min,评分增加5.17分。假如1名患者年龄50岁(30.80分),术后清蛋白<35 g/L(11分),主动脉阻断时间80 min(37.32分),术后机械通气时间130 min(36.19分),即患者总分为115.31分,于总分值坐标115.31分处做垂线,对应的预测概率约为30%,则该心脏外科手术患者术后发生肺部并发症的预测值为30%。
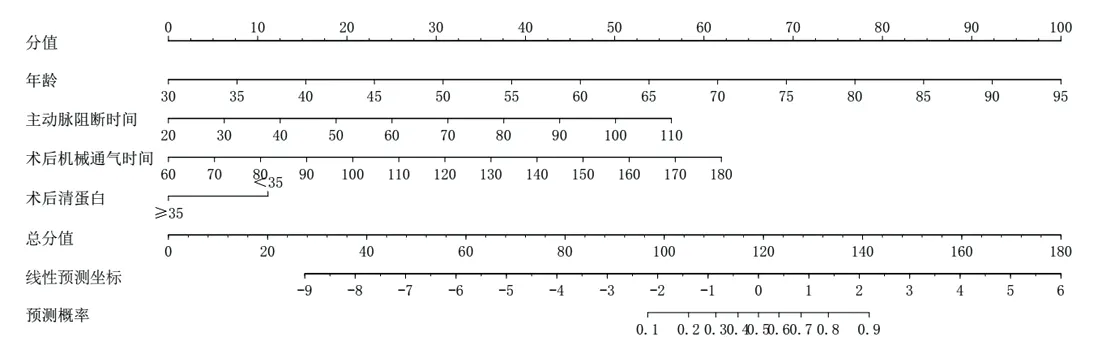
图1 预测心脏外科手术患者术后发生肺部并发症的列线图
2.4 预测心脏外科手术患者术后发生肺部并发症的列线图模型的验证 列线图模型预测心脏外科手术患者术后发生肺部并发症的列线图模型的校准曲线(见图2),预测值与实际值基本一致,且Hosmer-Lemeshow拟合优度检验χ2=9.443,P=0.336,一致性较好。ROC曲线下面积为0.942(95%CI:0.915~0.969),区分度较优。见图3。
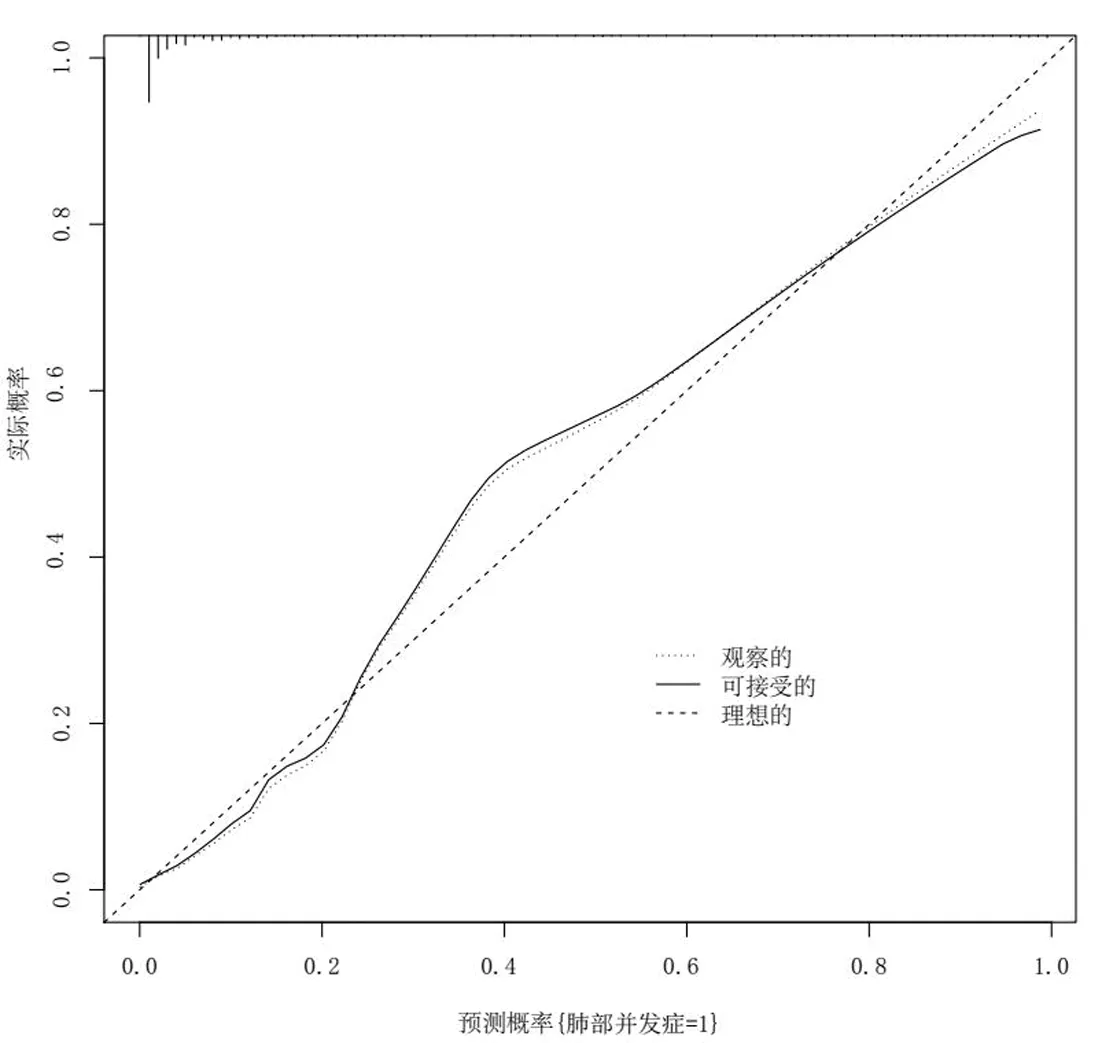
图2 预测心脏外科手术患者术后发生肺部并发症的校准曲线
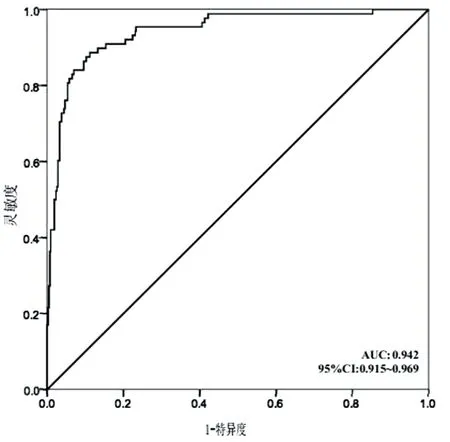
图3 预测心脏外科手术患者术后发生肺部并发症的ROC曲线
3 讨论
研究表明,心脏瓣膜置换术后肺部并发症的发生率大约为5%~28%[9]。本研究517例心脏外科术后患者肺部并发症发生发生率为17.02%。肺部并发症是体外循环的常见术后并发症,高龄、术前合并基础疾病、吸烟、肺部基础疾病、心功能状况、术中气道插管及术后机械通气等均易导致术后肺部并发症发生[10-12]。
多因素logistic回归分析显示年龄、术后清蛋白<35 g/L、主动脉阻断时间、术后机械通气时间是影响心脏外科手术患者术后发生肺部并发症的危险因素。本研究基于以上4项危险因素,构建预测心脏外科手术患者术后发生肺部并发症的列线图模型,有利于有效评估心脏外科手术患者术后发生肺部并发症情况并进行个体化预防。
本研究显示,患者年龄每增加5岁,列线图评分增加7.7分。高龄患者一般合并多种疾病,机体生理功能、心肺储备功能、免疫功能及肝肾代偿能力均发生减退,耐受创伤能力也发生下降;另外高龄患者术后康复时间也较年轻人长,病情容易反复,均会影响术后肺部并发症的发生[13]。老年人合并基础疾病例如糖尿病,血糖控制较差会增加患者术后肺炎的感染风险,而合并COPD会影响患者呼吸功能,加重患者肺部疾病[14-15]。本研究显示,主动脉阻断时间每增加10 min,对心脏外科术后患者肺部并发症贡献6.22分的影响权重。随着患者体外循环心脏手术延长,其体内主动脉被阻断的时间也会有所延长,进而导致体内各种器官功能均受到影响,甚至会加重器官损伤。本研究显示,术后机械通气时间每增加10 min,对心脏外科术后患者肺部并发症贡献5.17分的影响权重。心脏手术患者术后需要行机械通气,维持呼吸和循环功能的稳定性,但机械通气时间延长会增加血细胞的损伤,阻塞毛细血管,进一步加重肺功能损伤[16]。另外,气管插管会造成气道损伤及气管屏障损伤,致病菌易在损伤部位繁殖,减少机械通气时间可降低外科心脏手术后肺部并发症发生率。本研究显示,术后清蛋白<35 g/L对心脏外科术后患者肺部并发症贡献11分的影响权重。人体清蛋白可维持机体胶体渗透压和维持细胞的完整性,减少血浆的外渗;清蛋白水平降低表示基础疾病较为严重程度。另外清蛋白具有抗氧化的功能,可清除机体中活性氧[17]。心脏外科手术患者发生低清蛋白血症可能会影响肺组织的修复,加重胸腔积液并进一步损害肺功能,同时还可导致机体免疫功能下降,增加机体发生二次感染的风险[18]。列线图模型预测心脏外科手术患者术后发生肺部并发症的列线图模型的校准曲线预测值与实际值基本一致,且Hosmer-Lemeshow拟合优度检验χ2=9.443,P=0.336,一致性较好。ROC曲线下面积为0.942(95%CI:0.915~0.969),区分度较好。
综上所述,本研究基于年龄、术后清蛋白、主动脉阻断时间、术后机械通气时间4项危险因素构建的列线图模型,一致性、区分度及临床适用性较好,为临床制定针对性的个体化防治提供指导。
