HPLC-ICP-MS法测定贝类中烷基汞的不确定度分析
2022-09-08陈国
陈国
(宁波市农业科学研究院,浙江 宁波 315101)
环境中汞存在形态主要包括金属汞、无机化合态汞和有机化合态汞,有机化合态汞以有机汞(烷基汞)和有机络合汞形态普遍存在,其中烷基汞主要包括甲基汞和乙基汞,甲基汞是公认的“全球性环境污染物”,具有神经毒性,被世界卫生组织确认为2B致癌物。工业废水排放是水体汞污染的主要来源,无机汞在微生物的作用下可转化为甲基汞,水生生物摄入甲基汞,富集在体内,通过食物链逐级富集,进入鱼类和贝类体内,从而危害人类健康。本文采用液相色谱(HPLC)和电感耦合等离子体质谱仪(ICP-MS)联用技术,分析贝类中甲基汞和乙基汞含量,并对测量结果的不确定度进行了评价。
1 材料与方法
1.1 材料
1.1.1 主要仪器与装置
350D型电感耦合等离子质谱仪(美国PE公司),联用2695液相色谱仪(WATERS),Quiuti X124型电子天平(德国Sartorius公司)。
1.1.2 试剂及配制
氯化甲基汞、氯化乙基汞混标(Dr EHRENSTORFER),HCl(UPS级,苏州精锐化学股份有限公司),浓氨水(GR,国药集团化学试剂有限公司),L-半胱氨酸(99%,阿拉丁),甲醇(HPLC,TEDIA),试验用水为超纯水。
提取溶液。称取0.076 8 g L-半胱氨酸,用水溶解,缓慢加入41.66 mL盐酸,用水定容至100 mL。
50%氨水溶液。准确量取50 mL氨水,缓慢倒入50 mL水中,混匀。
0.8% L-半胱氨酸溶液。准确称取0.8 g L-半胱氨酸,用水稀释定容至100 mL。
流动相。称取0.771 g乙酸铵和0.768 5 g L-半胱氨酸,用900 mL水溶解,加入50 mL甲醇,用50%氨水溶液调节pH至7.0,加水稀释定容至1 000 mL。
1.2 方法
1.2.1 样品测定
准确称取1.000 g样品,置于50 mL的离心管中,加入10 mL提取溶液。振荡混匀,在室温下超声提取2 h,每30 min振摇1次,于4 ℃下以8 000 r·min-1转速离心15 min,准确移取2 mL上清液至10 mL容量瓶中,缓慢加入50%氨水溶液4.5 mL,用水定容至10 mL刻度,再转移至50 mL离心管中,于4 ℃下以8 000 r·min-1转速离心10 min,取上清液过0.45 μm滤膜,上机待测。
1.2.2 标准溶液配制
取1 mL的1 000 mg·L-1混标溶液定容至10 mL,获得混标储备液,再吸取0.5 mL储备液,用水定容至100 mL,获得标准使用液。分别移取标准使用液0、0.1、0.2、0.5、1.0、2.0、5.0 mL于50 mL塑料容量瓶中,分别加入2.0 mL 0.8% L-半胱氨酸溶液,用水定容至刻度,得到甲基汞(乙基汞)的浓度分别为0、1.0、2.0、5.0、10.0、20.0、50.0 μg·L-1的混标工作液。
1.3 仪器条件
HPLC条件。色谱柱为C18 54.6 μm×250 mm。等度洗脱流动相为10 mmol·L-1乙酸铵+0.076 8% L-半胱氨酸+5%甲醇,流速为2.0 mL·min-1,进样体积为100 μL。
ICP-MS条件。RF入射功率1 600 W,等离子体气体流速18 L·min-1,辅助气流速1.2 L·min-1,雾化气流量1.0 L·min-1,检测质量数m/z=202(Hg),standard模式:RPa=0,RPq=0.25。
1.4 数学模型
根据测定方法,建立样品中甲基汞(乙基汞)残留的数学模型:
式中,X为样品中甲基汞(乙基汞)的含量,C为回归方程拟合得到的样品溶液甲基汞(乙基汞)的质量浓度,V为定容体积,m为样品的质量。
2 结果与分析
综合试验过程分析,不确定度主要来源有样品称量引入的不确定度、使用参考物质及标准溶液配制引入的不确定度、样品提取过程引入的不确定度、标准曲线引入的不确定度和测量重复性引入的不确定度。
2.1 样品称量引入的不确定度
采用精度为0.000 1 g的电子天平,称量过程简化为m=m1-m2。
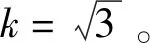
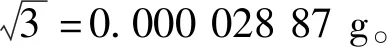
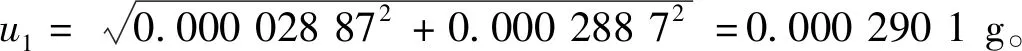
称量过程m2引入的合成不确定度:u2=0.000 290 1 g。
称取1.000 g,相对不确定度Urel1=0.000 580 8 g/1.000 g=0.000 580 8。
2.2 标准溶液引入的不确定度
标准溶液采用氯化甲基汞和氯化乙基汞混标,浓度均为1 000 mg·L-1(以汞计),查标准溶液证书获得包含因子C=2,不确定度为30 mg·L-1。标准溶液相对不确定度为Urel2=30/1 000÷2=0.015。
2.3 标准溶液配制过程引入的不确定度
标准溶液配制过程中引入的不确定度,期间用到100~1 000 mL移液器8次,10 mL容量瓶1次,50 mL容量瓶6次,100 mL容量瓶1次。
1)定容过程采用100~1 000 μL移液器,查相关检定证书,扩展不确定度u=3.5 μL,包含因子k=2,测量重复性0.4%。
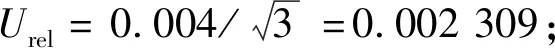
2)定容过程采用10 mL容量瓶,USP级,20 ℃误差为±0.02 mL,服从正态分布,半宽0.02 mL。
同理推断50、100 mL容量瓶引起的相对不确定度,结果如下表1所示。标准溶液配制过程中相对不确定度合成:
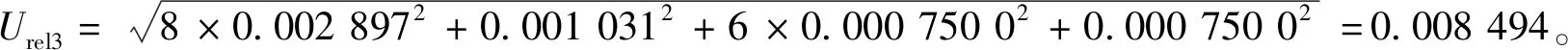
2.4 样品提取过程中引入的不确定度
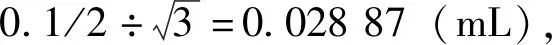

表1 定容过程引起的相对不确定度
2.5 甲基汞(乙基汞)标准曲线引入的不确定度分析
采用6个浓度水平的混合标准溶液,过原点建立线性回归方程,以标准溶液浓度Ci为横坐标,以测定获得的信号值甲基汞Ai(乙基汞Bi)为纵坐标,绘制标准曲线。具体测试数据见表2。

表2 系列标准溶液浓度对应信号值

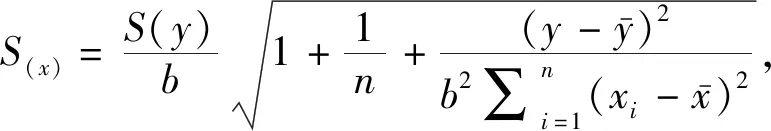
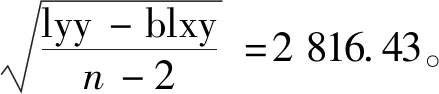
2.6 测量重复性引入的不确定度分析

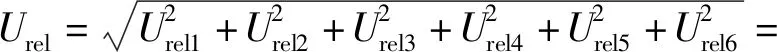
通过上述影响因子引入不确定度的定量分析,对比发现:标准曲线引入的不确定度是最高的,其次是参考物质引入的不确定度,再次是重复性测量引入的不确定度,相比于前三者,称量与定容所用量具引起的系统性误差对测量结果的影响相对较小,因为试验过程采用了合适的且精度相对较高的试验量具。测量仪器的稳定性和灵敏度对标准曲线的绘制有直接影响,也说明测量仪器的稳定性和灵敏度、参考物质的准确性以及人员分析中带来的偶然误差对测量结果产生关键性影响。因此,选择稳定性好、精度高的测量仪器,以及高纯度的参考物质,可有效提高试验结果的准确性。
3 小结
试验采用HPLC-ICP-MS测定了贝类中甲基汞和乙基汞,并对测量结果进行不确定度评价。结果显示,在检测过程仪器的灵敏度和稳定性、参考物质准确性以及人员分析过程偶然误差,对测量结果不确定度产生了重要影响。在日常检测中,要使用经过计量溯源的标准器皿对标准溶液和样品进行稀释和定容,以减少试验过程中产生的不确定度;选择稳定性好、精度高的测量仪器,高纯度的参考物质,可有效提高试验结果的准确性。总之,需要减少各测量不确定度分量的影响,来提高试验结果的准确度。
