基于卷积神经网络的房颤患者导管消融术后复发预测
2022-09-07徐亮陶倩钟菁肖晶晶
徐亮,陶倩,钟菁,肖晶晶
1.陆军军医大学第二附属医院医学工程科,重庆 400037;2.陆军军医大学第二附属医院心内科,重庆 400037
前言
心房颤动(房颤)是临床上最常见的心律失常[1],其主要临床特征包括心律紊乱、心功能受损和心房附壁血栓形成[2],在我国的发病率约为0.7%~1.0%[3]。该疾病危害性较大,极易诱发心悸、胸闷、呼吸困难、眩晕等不适症状,增加心力衰竭、心肌梗死和卒中的风险,有较高的致残率以及病死率[4]。随着人口老龄化和生活方式的改变,房颤发病率呈急剧上升趋势,其增长速度超过了心肌梗死和心力衰竭等疾病,已经成为影响居民健康水平、阻碍社会经济发展的重大公共卫生问题[5]。值得注意的是,抗心律失常药物通过维持窦性心律[6]、抗凝药物通过降低栓塞风险[7]可降低死亡率,但药物本身的副作用及配伍不当可能增加疾病预后不良风险[8]。近年来,导管消融进行节律控制能够改善房颤患者的生活质量,以及房颤合并心衰患者的心功能[9-10],但文献报道射频消融术后的整体复发事件高达25%~50%[11]。因此,为提高房颤治疗的预后效果,临床上亟须针对导管消融后并发症进行可靠预测[12],从而为临床医护人员提供更精准的决策支持。
近年来,随着人工智能及机器学习等技术的快速发展,大数据驱动下的深度学习体现了其强大的特征表达能力,各类深度学习算法被广泛运用于医疗健康领域。特别是针对不同检查数据的跨模态智能分析技术,通过分析多模态数据中各个模态的数据相关性和互补性,达到对数据高层特征的深层次理解,提高预测精准度,自动识别潜在危险因素。Nguyen 等[13]利用卷积神经网络(Convolutional Neural Net, CNN)成功捕获电子病历数据中的多模态特征信息,并实现了对患者因心血管疾病再入院的风险预测。Liang 等[14]对首次接受射频消融术治疗的肝细胞性肝癌患者利用机器学习算法对多种特征进行处理、筛选并进行训练,最后得到准确度为82%的术后复发预测模型。Preuer 等[15]提 出 了DeepSnergy 模型,成功预测了新的药物组合在癌症细胞系上的协同作用值。陈希等[16]进一步利用CNN对基因特征降维,探索了抗癌药物与细胞系的潜在关系,实现了有效药物组合的快速准确定位。因此,本文将基于深度学习的跨模态智能分析技术运用到心脏射频消融术后风险预警中,通过融合患者病史特征信息(例如性别、年龄、身高、体质量、既往史等),影像检查信息(例如超声、心电图等),生化检查信息(例如血常规、尿常规、肾功等),对术后风险及并发症进行预测。
1 资料与方法
1.1 一般资料
本文选取了2018年01月~2020年12月于陆军军医大学第二附属医院进行射频消融手术治疗的121名房颤患者信息,其中出现房颤复发的50 名患者作为试验组,没有出现房颤复发的71 名患者作为对照组。收集的信息包括患者的病史特征信息、影像检查信息和生化检查信息,不包含任何跟患者身份有关的资料信息。两组的年龄、性别、身体质量指数(BMI)、血压等信息均列入可能影响预测的因素而予以完整保存。
1.2 纳入及排除标准
1.2.1 纳入标准(1)房颤患者的诊断和分类标准参考《2020版ESC/EACTS心房颤动诊断与管理指南》[2];(2)症状性阵发性房颤,抗心律失常药物治疗失败且推荐等级为I和Ⅱa 适应症的患者;(3)具有资质的临床医师采用单纯的导管消融房颤(包括冷冻消融)手术方法;(4)患者年龄>18岁且≤79岁;(5)研究对象的信息选择全部获得陆军军医大学第二附属医院伦理委员会批准。
1.2.2 排除标准(1)患者适应症的推荐等级为Ⅱb 类(证据不够充分或普遍共识治疗和操作没有益处)和Ⅲ类(证据和普遍共识认为治疗和操作没有益处,甚至在部分情况下有害);(2)利用其他消除房颤的手术方法、多次消融手术或合并了其他的心脏手术;(3)缺乏足够的随访时间和随访资料;(4)缺少已知的关键性临床资料;(5)没有列入特征因素进行观察的其他伴随疾病患者;(6)术前已经具有可以临床诊断的并发症且观察程度改变;(7)术者操作规范明显错误和患者依从性差。
完整入组流程图如图1所示。
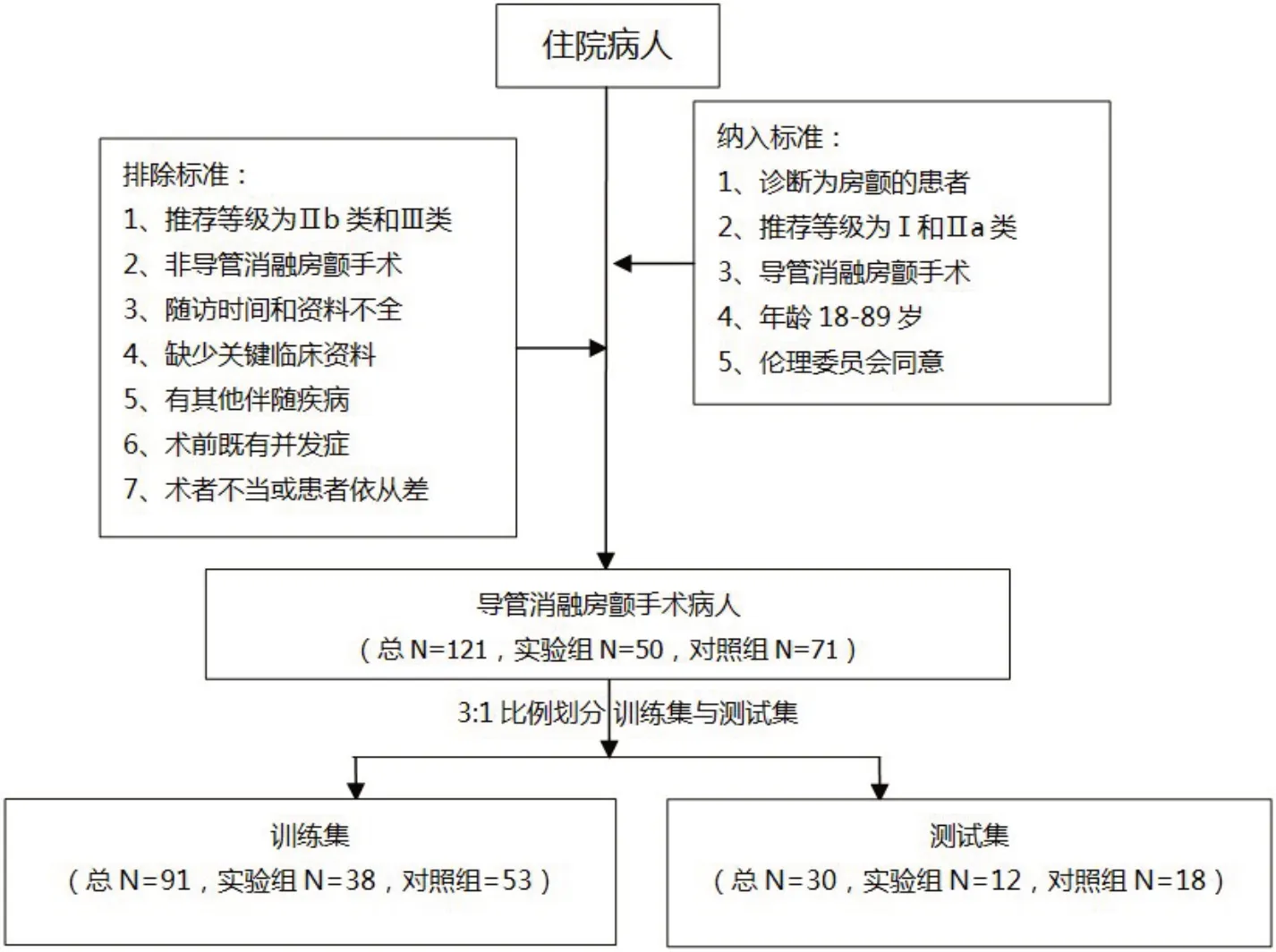
图1 入组流程图Figure 1 Enrollment flowchart
1.3 方法
将收集到的全部数据经过纳入和排除的标准筛查后,再经过清洗、标准化、数字化、代码化等预处理,成为完全结构化的数据集。将数据集根据复发的发生与否分为有复发的试验组和无复发的对照组,然后按比例随机均衡设置训练集和测试集。
1.3.1 统计学方法 对病史资料和影像学检查资料采用SPSS 26.0 软件进行统计学分析,符合正态分布的计量资料采用均数±标准差表示,采用独立样本t检验;计数资料用例数(%)表示,采用χ2检验;等级分组资料采用秩平均数表示,采用非参数Mann-WhitneyU检验。根据P值对所有因素进行降序排序,选择了P值最小的前10 个因素,也就是显著性差异最大的10个因素。
1.3.2 深度学习模型 笔者主要采用了结合统计学选出的病史资料和影像学检查中的10个因素以及生化检查指标,结合深度神经网络对房颤复发进行预测。使用Pytorch 深度学习库完成了模型构建,主要构建了3个模型,第一个模型Mulmodel 1主要采用了两层神经网络及一层全连接层,第二个模型Mulmodel 2与第三个Mulmodel 3 模型主要采用了一层神经网络及一层全连接层,但是采用了不同的参数,具体的技术路线如图2所示。
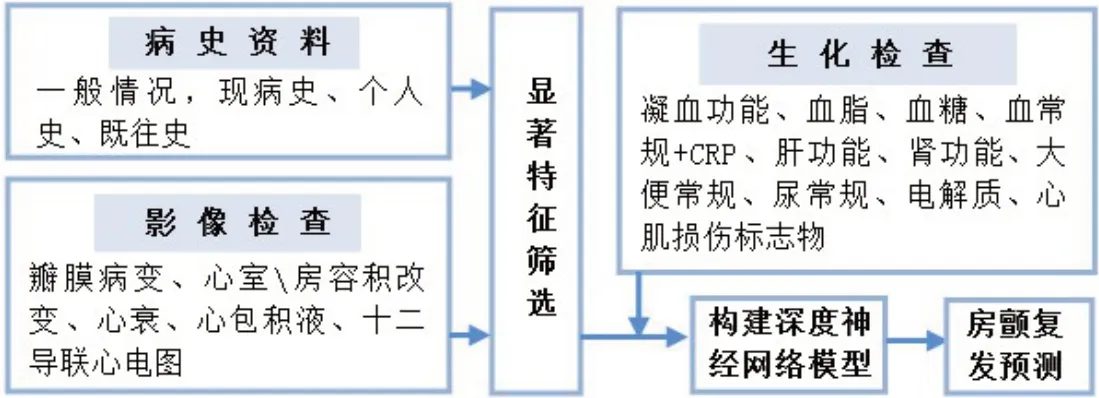
图2 技术路线图Figure 2 Technology roadmap
在训练过程中,采用的batch 大小为16,Loss 函数采用的是交叉熵公式,并用Adam 进行模型优化,学习率设定为0.001。交叉熵公式见式(1):
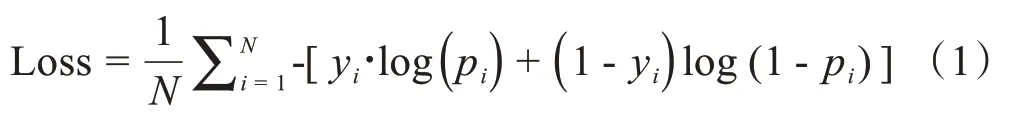
其中,yi表示样本i的标签,在本试验中标签1 代表房颤复发,标签0 代表未复发。pi表示样本预测为复发的概率。
2 结果
2.1 病史资料特征
统计结果将病史资料收集的重点放在与房颤发生相关的危险因素上,既往史还特别收录了长期服用药物的情况。训练集里的91例房颤患者的病史资料特征统计结果如表1所示,而特别收录的既往用药信息统计情况如表2 所示。从统计结果我们可以看出病史资料特征中P值最小的为脑卒中(P=0.136),而且所有病史资料特征因素的P值均>0.05,无统计学差异。
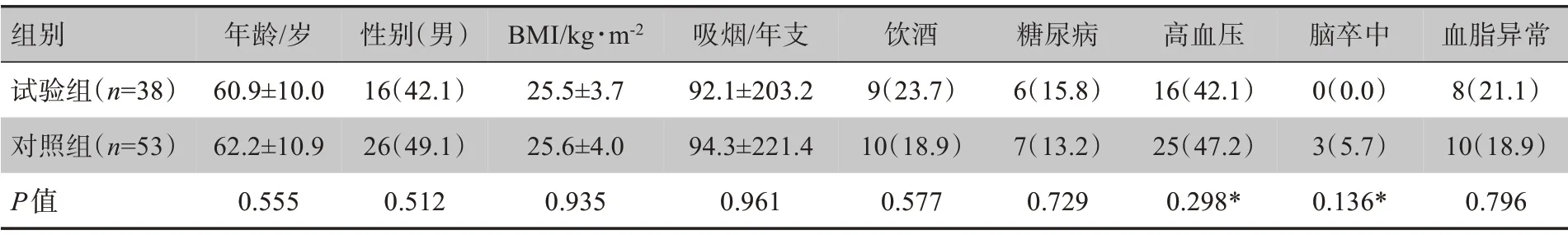
表1 病史资料特征信息统计[例(%)]Table 1 Statisticsof medical history data[cases(%)]
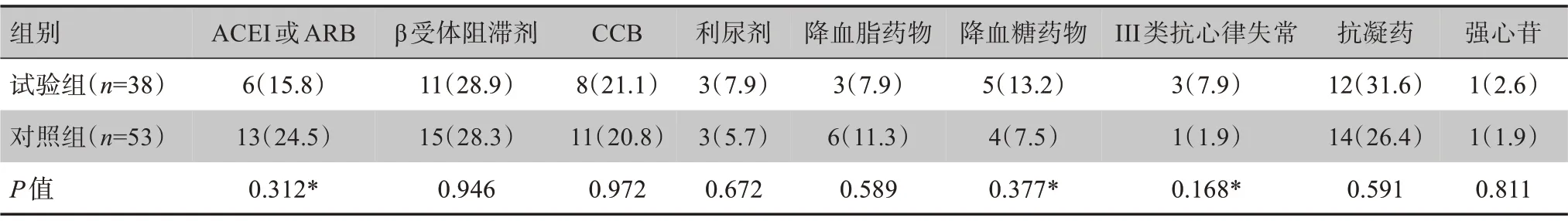
表2 既往用药信息统计[例(%)]Table 2 Statistics of medication history[cases(%)]
2.2 影像检查结果
射频消融术前常规检查包括心脏超声和12 导联心电图,通过具有专业资格的医师进行人工判读,这两项检查包含较多特征指标。笔者重点比较了严重改变心脏结构、心室节律和速率的指标(表3)。从结果可以发现心包积液是差异最大指标(P<0.01)。
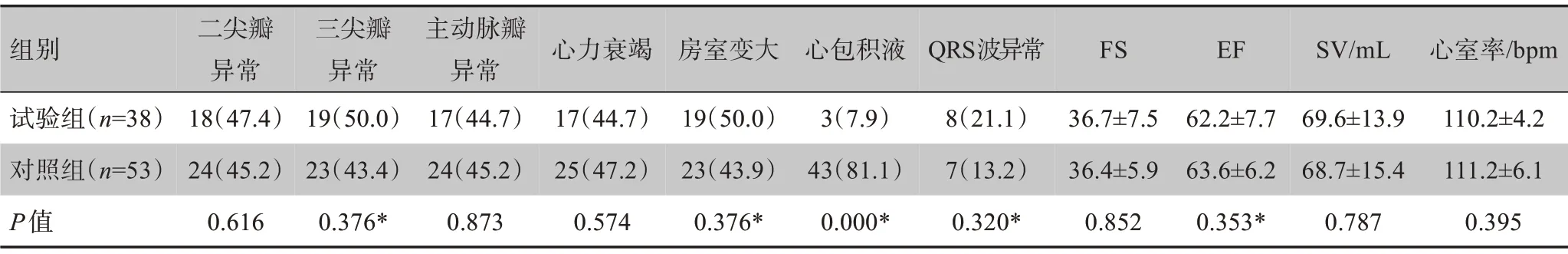
表3 影像检查特征信息统计[例(%)]Table 3 Statistics of imaging features[cases(%)]
根据P值进行排序,笔者采用了P值最小的10个因素代入到模型中对房颤复发进行预测,包括有心包积液、脑卒中、Ⅲ类抗心律失常药、房室变大、高血压、ACEI 或ARB 药物、QRS 波形态异常、三尖瓣异常、射血分数(EF)和降血糖药物。
2.3 生化检查预测结果
首先,笔者采用了血常规、尿常规、C 反应蛋白、凝血功能、血脂、血糖、肝功能、肾功能、电解质、心肌损伤标记物等共60 个特征进行预测,从表4 中可以看出MulModel 3 有最高的精度0.700(95%CI:0.536~0.864),MulModel 1 有最高的敏感度0.667(95%CI:0.391~0.862),MulModel 3 有 最高的 特异 性0.944(95%CI:0.742~0.990)。整体来看,MulModel 3 具有较高的精度和特异性,但是在敏感度上欠佳,相对MulModel 1 预测能力比较均衡缺乏特殊的预测优势,MulModel 2 的检出敏感性太差。值得注意的是,CNN 的模型并不是越复杂获得的结果就越好。在图3中看出,虽然复杂的模型可以快速收敛(MulModel 1),但是其容易过拟合导致其在测试集上的效果不佳,如表4所示。相反,简单的模型反而能获得更好的泛化能力。
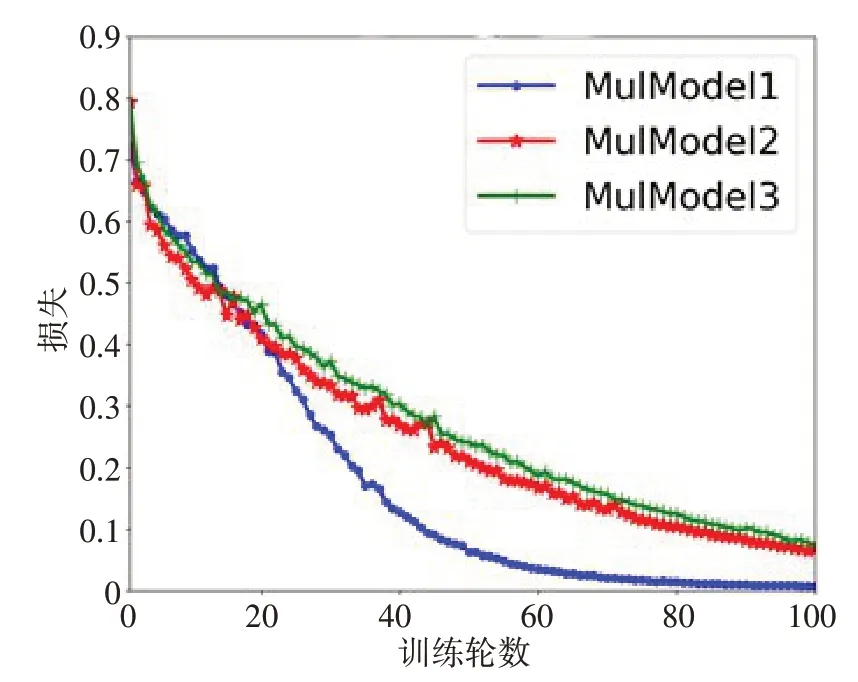
图3 基于生化检查的训练损失曲线Figure 3 Loss curves based on biochemical examination
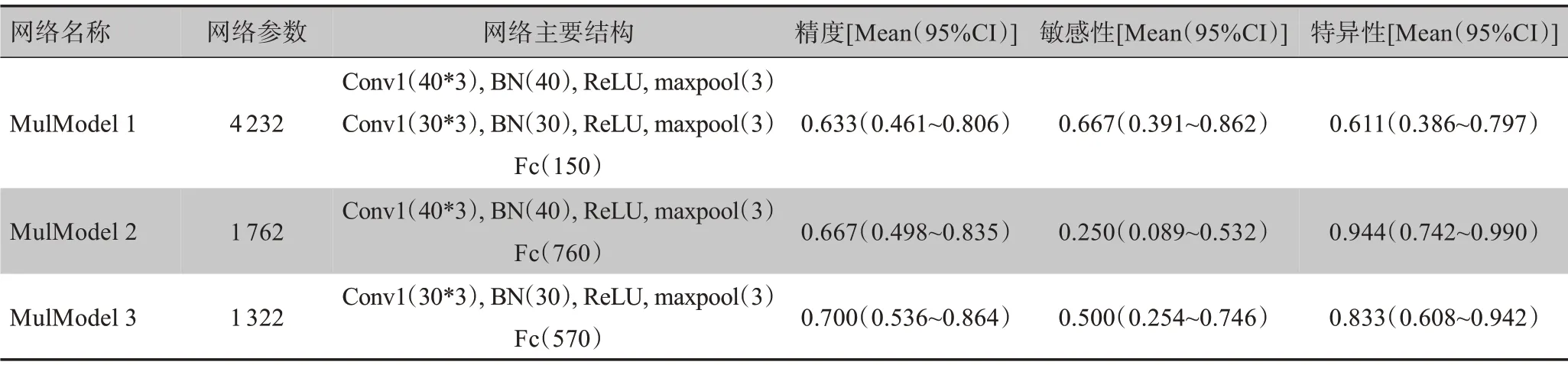
表4 不同模型的预测结果(基于生化检测结果)Table 4 Prediction performances of different models(based on biochemical examination)
2.4 多因素融合预测结果
笔者将通过统计学筛选出来的10 个特征与60个血气生化的检验指标相结合(共70个特征)代入到模型中。从表5的试验结果可以看出,预测房颤复发的能力有显著的提升,MulModel 3 的精度高达0.800(0.657~0.943),虽然离理想的模型尚有一定差距,但是已经可以对临床预测起到重要辅助作用。MulMode 1 和MulModel 3 的特异性均为1.000(0.824~1.000),融合后的MulModel 1 敏感性降低到0.250(0.089~0.532)。图4 所展示的loss 曲线更加平滑,拟合学习情况良好。MulModel 3 是综合预测最具有价值的模型。
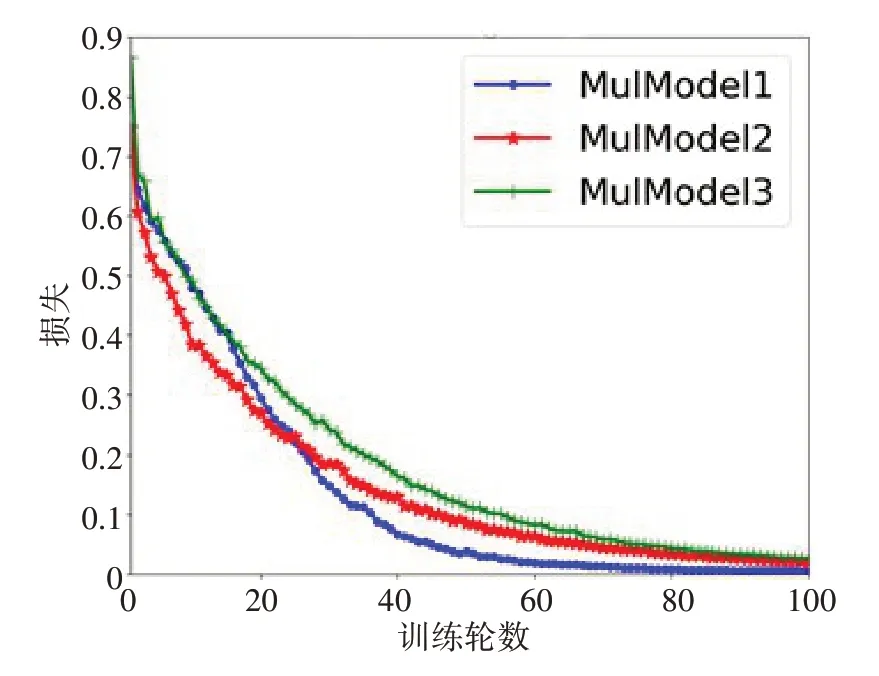
图4 基于全因素的训练loss曲线Figure 4 Loss curves based on all-factor training
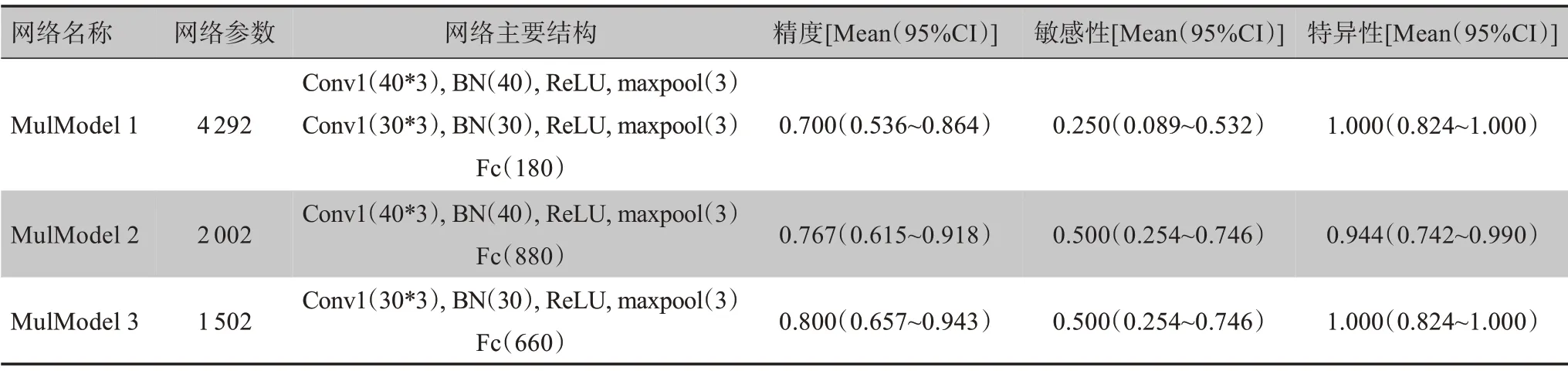
表5 不同模型的预测结果(基于全因素检测结果)Table 5 Prediction performances of different models(based on all-factor examination)
3 讨论
导管消融术后前3个月为空白期,这个期间的复发可以不认定为房颤导管消融手术复发,因为早期的复发可能在使用药物后消失或自行消失。晚期复发指术后3 个月~1年复发;远期复发是术后1年以上出现复发[2]。目前在临床上预测导管消融术后晚期和远期复发还处于研究阶段,晚期复发率为25%~40%[17],发生率与术前的房颤类型及复发筛查手段有关,远期复发率为11%~29%[18],临床诊断为持续性房颤是导管消融手术后房颤复发的主要危险因素,其他危险因素包括年龄、左心房大小、糖尿病、瓣膜性心脏病、左心功能不全、高血压栓塞积分等[18-19]。房颤复发主要表现为房速,占导管消融术后所有心律失常的50%[17]。房颤的复发原因主要包括肺静脉传导恢复、非肺静脉触发灶和心房基质未有效消融[20]。
房颤的导管消融术治疗综合复杂的主客观因素,本文在资料收集时充分考虑到手术医生技术在内的主观因素造成的影响,例如选择具有相同资质和水平的医生治疗的患者纳入研究,以抵消主观因素造成的影响。在表1 中可以看到的P值都无统计学意义,有些因素是经过广泛研究证实的预测因素,造成这种结果的原因可能是病例数量的不足,也可能是因为术前筛查已经将高危复发和不适宜手术的患者排除而造成选择性偏倚。表2既往药物使用中,服用了某项药物的患者房颤复发率有较明显的差异,这并不能证实这项药物本身对房颤复发率有影响,而可能是因为患者患有的疾病本身对复发率造成的影响,例如有证据表明Ⅲ类抗心律失常药物在术前和术后的使用具有有效的治疗和预防作用[21],但是在表2 中房颤复发的试验组有更高的抗心律失常药使用比例,本文把药物治疗相关资料也纳入到了全因素分析中来平衡这种差异。在表3 可以发现心房心室的结构改变以及瓣膜疾病也是重要的房颤复发影响因素,具有相当高的一致性。
在深度学习过程中,特征向量过多通常会涉及降维问题,并不是所有的特征都能对最终的结果产生有益作用。因此本文采取了统计学相结合的方法提前去除一些干扰,保留较强关联的特征。病历资料、超声和心电图部分因为涉及到人为主观的记录、标识和收集,在客观性上弱于纯仪器分析的生化检查资料,因此我们选择先将前者做一轮统计学的筛查。利用统计学筛选出来的特征与传统数字特征相结合,利用深度学习建立预测模型,实现了不同模态数据融合分析。本文使用的卷积神经网络不是单一固定的方式,而是通过不同的算法进行组合得到的,笔者利用的特征在一开始缺乏统计学差异,但是所选的模型可以对细微的差别进行互补和增强,通过学习优化细微差异获得准确的算法模型,获得较好的预后判断能力。值得注意的是,传统模型中尽量将网络建深建宽,但在样本量有限的情况下,选择合适大小的参数模型可以有效避免预测模型的过拟合问题,提高小样本训练模型的泛化能力。
病历资料、生化检查、心脏超声和心电图的检查主要对患者的术前状态做静态的记录,而术后复发的真实原因需要术后生理变化的动态追踪。我们建立的模型旨在创建一种数学方法,把多因素进行科学的融合评价患者个体状态,最大可能预测有适应症患者术后复发的可能,用以辅助临床医生进行术前评估。临床应用过程中,病历资料采集方法、仪器设备、术者临床技能、术后护理和治疗经过都会影响参数的变化,因此各研究机构根据自身的数据进行模型校正,从而进一步提高模型的准确性。
