三维CT支气管血管重建技术在胸腔镜肺段切除术治疗早期肺癌中的应用
2022-09-07代祖建林铿强黄明翔王世忠叶建刚许德新潘闪
代祖建,林铿强,黄明翔,王世忠,叶建刚,许德新,潘闪
福建省福州肺科医院胸外科,福建福州 350008
前言
近年来肺癌发病率与致死率呈现逐年升高趋势,在各种恶性肿瘤中居首位[1]。在肺癌病变早期筛查工作逐步推进下,更多早期肺癌患者得以被发现,手术切除为其首选疗法[2]。以往报道指出,中晚期肺癌患者术后5年生存率低至5%,而早期肺癌患者术后5年生存率则高达80%~90%[3]。当前,肺叶切除联合纵隔淋巴结清扫依然为非小细胞肺癌临床治疗标准术式。以往研究表明,相较于肺叶切除术,肺段切除术治疗早期肺癌(病灶直径≤2 cm)能够获得相似远期疗效,同时最大程度保留患者肺功能,降低术后并发症风险[4]。临床医师越来越重视胸腔镜肺段切除手术在早期肺癌中的应用。然而,肺段解剖结构十分复杂,具有较多变异支气管与微血管,因此如何更精准进行解剖性肺段切除为当前临床关注热点。现阶段,基于影像检查三维重建技术得到了有效发展,其工作原理是采用软件处理(包括提取及分割等)CT 断层图像,形成三维几何图形,同时以智能化软件系统构建三维模型。这种技术已经在整形外科、肝胆科以及骨科得到广泛应用[5-6]。理论上认为,胸腔镜肺段切除治疗中采用三维重建技术,能够提高手术精确度与安全性。本研究探索三维CT 支气管血管重建(3D-CTBA)在早期肺癌胸腔镜肺段切除术中的应用价值,希望为该技术的应用提供可靠依据。
1 资料与方法
1.1 一般资料
对福建省福州肺科医院2020年1月~2021年3月间60 例行胸腔镜肺段切除术+淋巴结清扫(或采样)早期非小细胞肺癌患者进行回顾性分析。纳入标准:(1)单发病灶;(2)根据影像学检查结果,高度怀疑为肺癌,磨玻璃成分占比≥50%,病灶直径≤2 cm,且经病理证实;(3)纵隔以及肺门处均无肿大(超过1 cm)淋巴结,且无远处转移;(4)具有肺段切除术适应证;(5)精神意识正常;(6)资料完整。排除标准:(1)中途改变术式;(2)合并凝血系统疾病或者自身免疫性疾病等;(3)合并严重脏器病变;(4)术中大出血,必须输血治疗;(5)术中发现病灶侵犯气管、大血管或者心脏、胸腔广泛粘连等。患者均签署知情同意书,本研究获得医院伦理委员会审批。其中30 例术前采用3D-CTBA 技术(三维重建组),30 例术前常规进行二维CT检查(CT组)。
1.2 方法
两组患者均接受胸腔镜肺段切除术,使用3 孔法,在患者第3~5 肋间作手术主操作孔,在肩胛下角线方位第7~9肋间作手术副操作孔,在腋中线处的第7/8肋间作观察孔;CT组与三维重建组分别按照二维CT图像与3D-CTBA图像实施手术。
CT 组:通过64 排128 层容积CT(购自美国GE)扫描患者全肺容积,予以平扫与增强扫描,注意由胸廓至膈肌平面进行扫描,采取高压注射器,从患者肘静脉团注一定造影剂,包括肺静/动脉期,接着扫描获得质量最佳图像。图像内容主要为肿瘤与肺动/静脉、邻近支气管及分支等的关系。术前规划:根据增强CT 图像,进一步明确肿瘤所处肺段,然后对切除范围进行规划,按照肿瘤位置及其邻近支气管与肺血管具体走形,进行肺段切除方式的选择。
三维重建组:在手术前同样采用CT 机予以平扫与增强扫描,接着导出增强扫描所得DICOM 文件,采取Mimics Medical 20.0软件完成三维重建过程,重建时间一般为30~60 min,对肿瘤位置进行标记,同时显示支气管与周围肺动静脉,进一步明确肿瘤靶肺段部位。术前规划:根据二维图像以及3D-CTBA 影像明确解剖结构类型、是否变异或者存在畸形。以肿瘤为中心,了解肿瘤肺段、肺亚段具体归属。结合肿瘤和肺段支气管结构、段间静脉以及亚段间静脉具体关系,进一步追根索源,确定肿瘤所处位置,直观并且准确地判断肿瘤肺段归属。然后以肿瘤为中心,往外大约延伸2 cm,从而明确安全切缘,合理规划切除范围,同时按照肿瘤位置及邻近支气管以及肺血管走形,确定应切除或者保留结构。基于3D 图像,遵循从浅入深原则确定切除顺序,采取合适手术入路方式,设计最佳操作顺序,尽量避免解剖并且分离处理需保留肺段,减少对各结构不必要的损伤,增加手术操作精确性,获得更好的手术效果。随访6个月,记录复发情况。
1.3 观察指标
收集患者性别、年龄、合并症、肿瘤直径、肿瘤深度(与脏层胸膜相隔最短距离)、肿瘤部位、病理诊断[原位腺癌(MIA)、非典型腺瘤样增生(AAH)、浸润性腺癌(IAC)、微浸润腺癌(MIA)等]及TNM 分期等基线资料;记录两组手术指标(出血量、手术时间、切缘宽度)、住院总费用、术后恢复情况(胸管留置时间、胸管引流量、住院时间)及并发症发生率。
1.4 统计学处理
采用SPSS22.0 软件进行数据处理,其中计数资料以频数与频率表示,使用χ2检验;计量资料经正态分布检验,以均数±标准差表示,使用t检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组基线资料比较
两组性别、年龄、糖尿病、高血压、肿瘤直径、肿瘤深度、肿瘤部位、病理诊断、TNM 分期比较无显著差异(P>0.05,表1)。
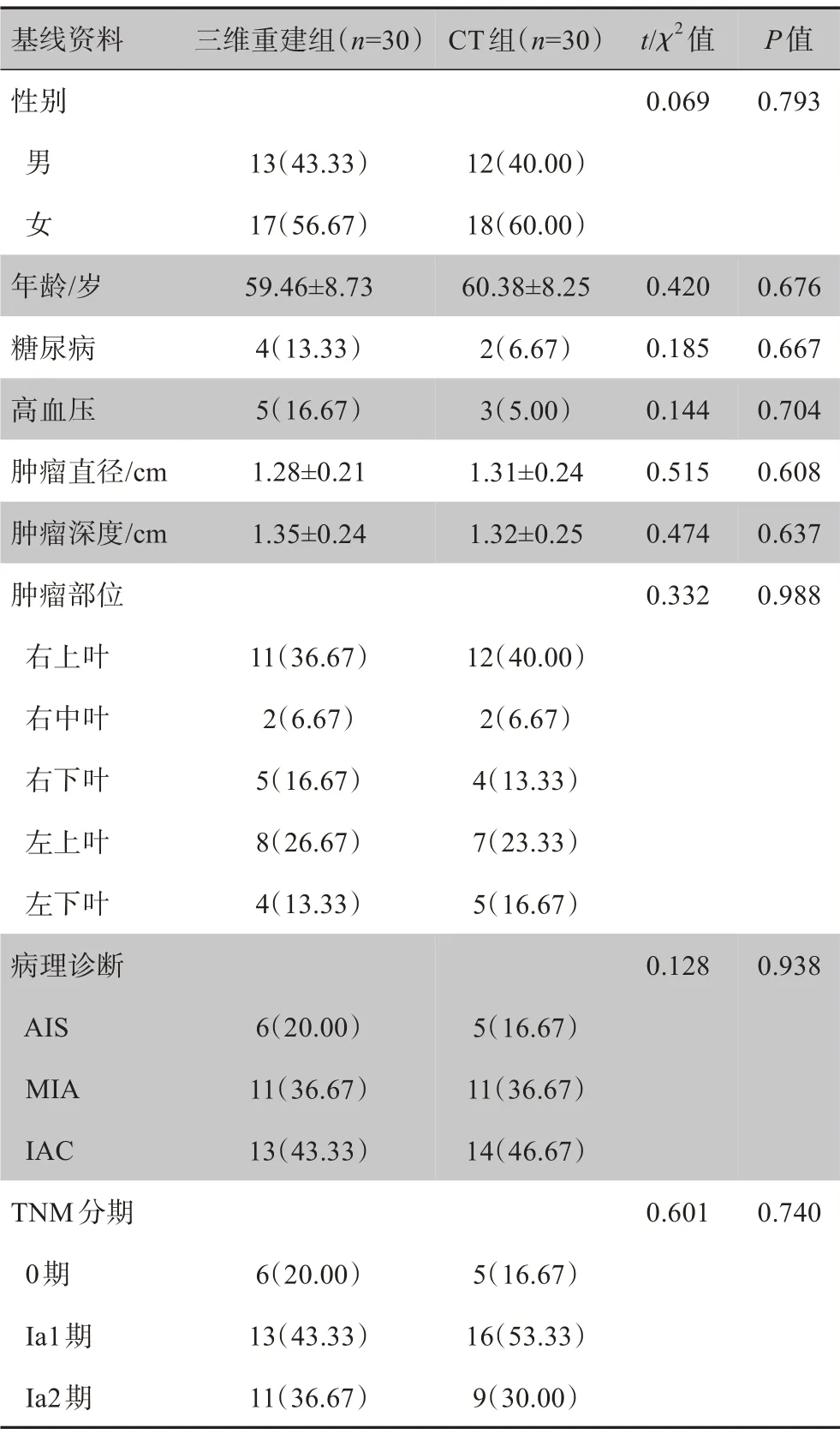
表1 两组基线资料比较[例(%)]Table 1 Comparison of baseline data between two groups[cases(%)]
2.2 两组手术指标比较
三维重建组术中出血量显著少于CT 组(P<0.05),手术时间显著短于CT组(P<0.05),切缘宽度显著大于CT组(P<0.05),见表2。
表2 两组手术指标比较(± s)Table 2 Comparison of operation indicators between two groups(Mean±SD)
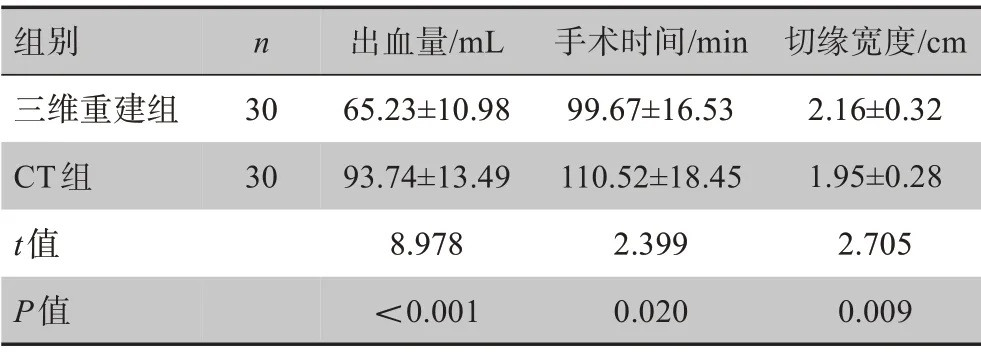
表2 两组手术指标比较(± s)Table 2 Comparison of operation indicators between two groups(Mean±SD)
组别三维重建组CT组t值P值n 30 30出血量/mL 65.23±10.98 93.74±13.49 8.978<0.001手术时间/min 99.67±16.53 110.52±18.45 2.399 0.020切缘宽度/cm 2.16±0.32 1.95±0.28 2.705 0.009
2.3 两组术后恢复情况与住院总费用比较
三维重建组术后胸管留置时间、住院时间显著短于CT组(P<0.05),胸管引流量、住院总费用显著少于CT组(P<0.05),见表3。
表3 两组术后恢复情况比较(± s)Table 3 Comparison of postoperative recovery between two groups(Mean±SD)

表3 两组术后恢复情况比较(± s)Table 3 Comparison of postoperative recovery between two groups(Mean±SD)
组别三维重建组CT组t值P值n 30 30胸管留置时间/d 2.74±0.36 3.81±0.58 8.585<0.001胸管引流量/mL 438.96±78.54 657.18±102.37 9.263<0.001住院时间/d 4.72±0.75 6.38±1.02 7.182<0.001住院总费用/万元3.72±0.52 4.16±0.75 2.641 0.011
2.4 两组并发症情况比较
三维重建组并发症总发生率显著低于CT 组(P<0.05,表4)。
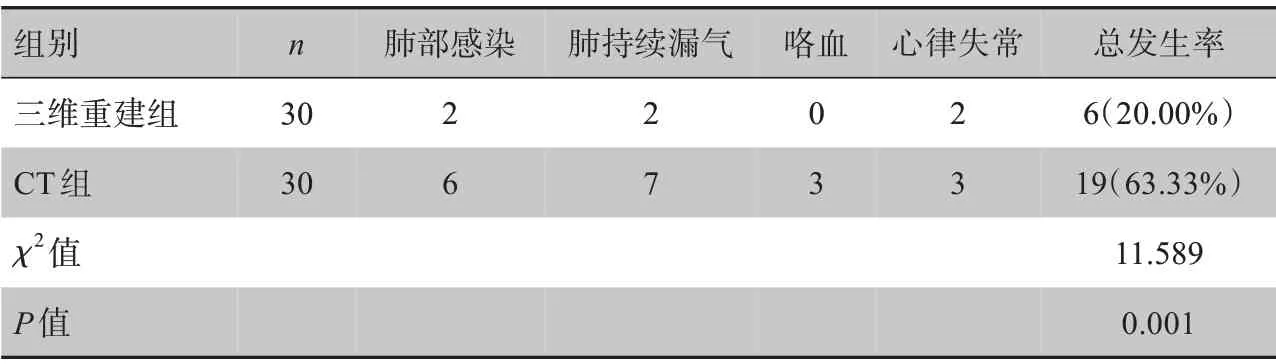
表4 两组并发症情况比较Table 4 Comparison of the incidence of complications between two groups
2.5 复发情况
随访6个月,经胸部CT检查,发现两组均无复发病例。
2.6 影像分析
早期非小细胞肺癌胸腔镜肺段切除术术前规划中二维CT与3D-CTBA分析图像见图1~图5。
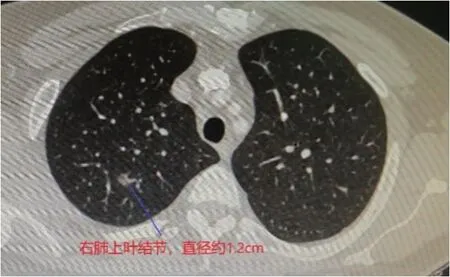
图1 二维CT图像显示肺结节位置Figure 1 Location of pulmonary nodules in two-dimensional CT image
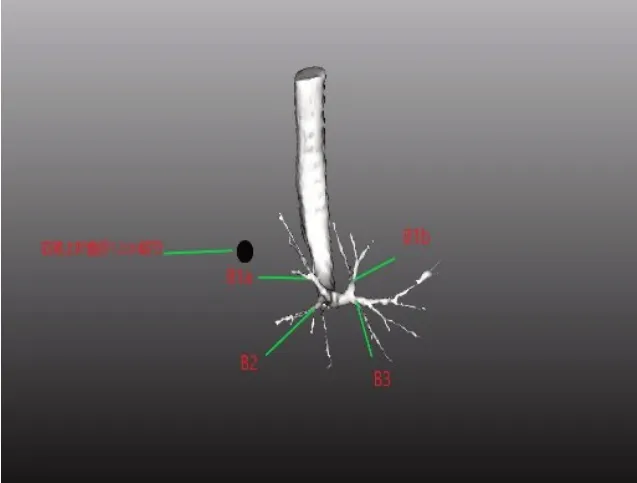
图2 3D-CTBA显示肺结节Figure 2 Pulmonary nodules in 3D-CTBA
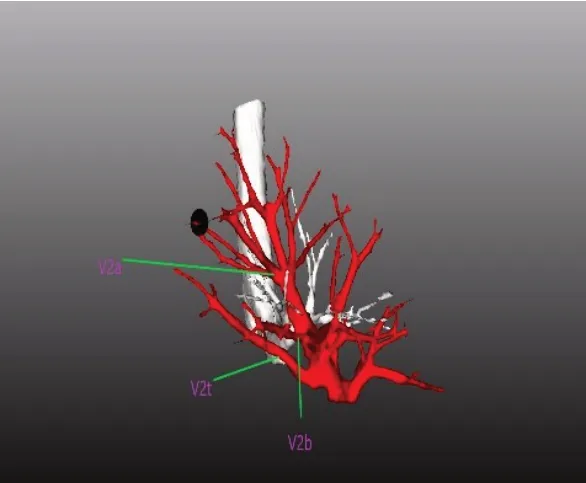
图3 3D-CTBA显示支气管Figure 3 Bronchi in 3D-CTBA
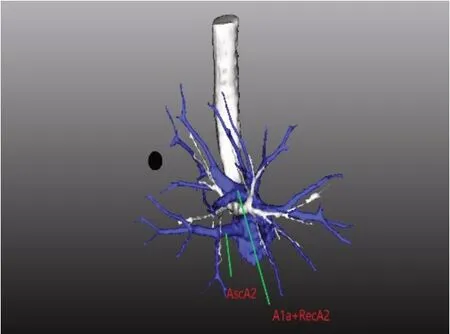
图4 3D-CTBA显示肺动静脉Figure 4 Pulmonary arteries and veins in 3D-CTBA
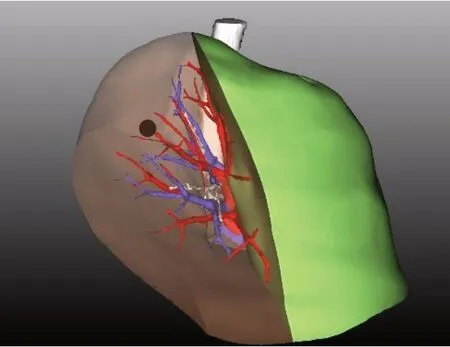
图5 3D-CTBA显示肺动静脉相对位置Figure 5 Relative position of pulmonary arteries and veins in 3D-CTBA
3 讨论
与肺叶切除相比,解剖性肺段切除过程中,由于肺段解剖结构比较偏向支气管以及血管远端,具有较多分支,并且肺动静脉与周围支气管结构关系复杂,存在较大个体差异,同时变异较多,以往传统手术方案一般是按照二维CT 图像计划的,但是常规二维薄层CT 无法精确定位病灶所属肺段、支气管与目标肺动静脉走行,因此手术容易产生误切、漏切以及多切等问题[7-8]。医学影像图3D 重建技术是当前多学科交叉的一个研究新领域,已经在诊断医学、模拟仿真、解剖教学、外科手术操作规划、放射治疗方案规划、整形手术规划等中得到应用[9-11]。临床认为,精准肺段切除必须熟悉肺部解剖结构,要求手术医师能够精确辨认所切肺段支气管以及动静脉属支,考虑到肺段解剖变异非常多,提高了切除难度,尤其是对于初学者而言,手术风险更大[12-13],3D 重建技术应运而生。当前,3D 重建技术与3D 打印技术于医院肺外科治疗中的应用仍然处于研究阶段,相关临床报道并不多。本研究中三维重建组术中出血量显著更少,手术时间显著更短,与刘宗昂等[14]研究观点相符。证实3D-CTBA 技术的应用能够减少手术损伤,提高手术安全性。分析原因,利用三维重建软件分析与构建影像学检查资料,有效还原3D图像,便于医生更直观了解肿瘤病灶、肺段血管以及支气管三者空间关系,同时还能够按照其走行情况协助肿瘤定位,制定精确手术规划[15];术中根据基于3D-CTBA技术制定的手术规划,能够快速找到最佳入路内各种解剖结构(如肺动静脉与相应肺段支气管等)具体解剖位置,为医师识别解剖结构提供了较为直观并且准确的导航,高效引导手术医师分离肺段支气管以及肺动静脉,减少对肺段支气管以及肺动静脉等造成的损伤,实现肺段精准切除。本研究中三维重建组切缘宽度显著大于CT 组,提示3D-CTBA 应用于胸腔镜肺段切除术,切缘优势明显。临床认为,切缘宽度不足为肺段切除术后出现局部复发情况的主要原因[16]。有研究指出对于直径不超过2 cm 的结节(主要是磨玻璃成分),手术中2 cm 切缘宽度能够有效降低术后局部复发风险[17]。故在手术前确定最小切除范围,可为意向性胸腔镜肺段切除手术治疗效果提供一定保障。有研究称以往传统方法仅根据二维CT 图像对手术最小切除范围进行辨认,往往具有较大难度[18]。利用3D-CTBA 中的软件对2 cm 安全切缘进行标记,结合肺血管、支气管结构和安全切缘之间的关系合理规划最小手术范围,能够提高手术操作准确性,确保切缘阴性。
以往研究表明,段间静脉属于肺段平面分界主要解剖标志,一般在相邻肺段之间,一旦判断失误,将引起咯血等并发症,情况严重时患者可能需接受二次手术治疗[19]。本研究发现三维重建组并发症总发生率显著低于CT 组,提示术前3D-CTBA 的应用能够降低患者术后并发症风险。主要由于肺段静脉变异相对较多并且复杂,利用二维CT 图像难以判断肺段间交界面,因此术中容易产生血管损伤或者误断,导致术后咯血等各种并发症风险增加[20];3DCTBA 能够于术前准确发现解剖变异,有利于医师术中准确辨别应该切除血管与相应支气管,避免段间静脉的误断,从而减少术后咯血,同时3D-CTBA的应用有利于保留有效肺组织,从而降低肺部感染或者肺持续漏气发生率[21]。此外,三维重建组心律失常并发症较少,可能与3D-CTBA 引导胸腔镜肺段切除术的实施,可减少脏器不必要损伤有关。本研究中三维重建组术后胸管留置时间、住院时间均显著更短,胸管引流量显著更少,表明术前3D-CTBA可缩短患者术后康复进程。可能由于术中3D-CTBA影像导航能够指导医师对于靶段支气管结构以及动静脉予以精细解剖,提高判别与处理准确性,有效减少手术对机体的创伤。本研究发现三维重建组住院总费用显著少于CT 组,提示3D-CTBA 的应用有利于减少患者医疗花费,一定程度上减轻其医疗负担。
综上所述,早期肺癌患者胸腔镜肺段切除术前进行3D-CTBA,有利于更安全地开展手术,确保手术切缘宽度足够,同时降低术后并发症风险,缩短患者康复进程,减少住院费用,具有重要应用价值。
