不同保存条件对化学发光微粒子免疫分析法监测环孢素血药浓度的影响Δ
2022-09-06张凌鹏陈井霞杨云云王学彬高丽红
张凌鹏,陈井霞,杨云云,李 丹,王学彬,高丽红,王 卓
(海军军医大学第一附属医院药剂科,上海200433)
环孢素为真菌源性的环状十一氨基酸多肽的免疫抑制剂,目前主要用于实体器官移植、造血干细胞移植和免疫性疾病[1]。环孢素治疗窗窄,药动学个体差异大,体内药物暴露量影响因素多,需定期对其进行治疗药物监测(TDM)[2]。临床常规监测全血环孢素谷浓度或峰浓度,评价环孢素的疗效和安全性,便于及时调整环孢素的用药方案[1-3]。
目前,新型冠状病毒奥密克戎在全球肆虐,社区、医院封控频繁,居家隔离成为常态[4]。使用环孢素治疗的患者免疫功能低下,新型冠状病毒感染风险较大,不能正常进行门诊随访和监测药物浓度,难以判断环孢素浓度是否在治疗窗内,治疗效果和安全性也无法评估[5]。因治疗的需要,封控小区居家患者及新型冠状病毒感染者定点医院隔离期间采集的环孢素标本,转运前消杀和运输耗时长,导致标本采集当日不能及时检测[6]。此外,在非新型冠状病毒肺炎疫情流行期间,诸多医疗机构TDM实验室接受本地或异地的快递标本,采集和送达当日均不能及时检测[2,6-7]。环孢素浓度检测试剂盒要求当日采集标本如不能及时处理,需在保存时限内完成检测。因此,亟需探究不同保存条件对环孢素浓度检测结果的影响。本研究通过探讨常温、冷藏和冷冻条件保存7 d后全血环孢素的稳定性,针对新型冠状病毒肺炎疫情居家隔离及非疫情期间异地不便门诊随访的患者,为其环孢素TDM样本的科学转运及保存提供依据,确保TDM结果的可靠性。
1 材料与方法
1.1 样本来源
收集2021年12月至2022年3月我院服用环孢素患者常规监测后的废弃标本80例次。采血管:EDTA抗凝管;样本量:1~2 mL;标本要求:不凝血;患者标本采样时间:再次服药前或服药2 h后;常规监测环孢素血药浓度作为初始对照值。
1.2 仪器
ARCHITECT i1000SR型全自动免疫分析仪(美国Abbott公司);XW-80A型旋涡混合器(上海琪特分析仪器有限公司);100/200/1 000 μL型移液枪(德国Eppendorf公司);Micro17型高速离心机(美国Thermo Electron Corporation公司);BCD-322型冰箱(德国Siemens公司)。
1.3 试剂
环孢素测定试剂盒(美国Abbott公司,批号为25039M800);标准曲线液(美国Abbott公司,批号为85K28921),全血质控品(美国Bio-rad公司,批号分别为21883、21891和21892)。
1.4 样本分装与保存
全血标本混匀后,每个标本用移液枪精密吸取200 μL至离心管中,平行分装3份,密封。分别室温(20~25 ℃)、冷藏(2~8 ℃)、冷冻(-35~-30 ℃)避光保存7 d。冷藏、冷冻保存的标本在测定前,均室温放置30 min以上,按照标本前处理标准步骤处理并检测。
1.5 环孢素分析方法
(1)环孢素血药浓度测定方法:采用化学发光微粒子免疫分析法(CMIA),测定标本保存前后环孢素浓度,试剂盒检测范围为0~1 500 ng/mL,检测限≤25.0 ng/mL[6,8-9]。(2)标本前处理操作步骤:①标本于旋涡混合器强力涡旋2~3 s,用移液枪精密吸取200 μL全血至离心管中;②移液枪精密吸取100 μL全血溶解剂加入离心管,用旋涡混合器强力涡旋5~10 s;③再移液枪精密吸取400 μL环孢素全血沉淀剂,立即盖上离心管,用旋涡混合器强力涡旋10~15 s至充分混匀;④用高速离心机10 000 r/min离心6 min(离心半径5.6 cm);⑤将上清液倒入移植预处理管中,用旋涡混合器涡旋5~10 s,上机检测。
1.6 统计学方法
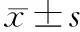
2 结果
2.1 基本资料
80例环孢素样本主要来自常规环孢素浓度监测后废弃标本,样本来源患者基本资料见表1。

表1 环孢素样本来源患者基本资料(n=80)Tab 1 General information of source patient of cyclosporine sample (n=80)
2.2 室内质量控制情况
TDM日常工作中做好室内质量控制对环孢素浓度检测至关重要[10]。本实验室采用质控图联合Westgard多规则法进行室内质量控制[11]。2021年11月至2022年3月,开展本研究期间,3个批号的在控质控品变异系数(CV)均<10%(见表2),实验当日室内质控实测值相对偏差均<10%(见表3)。以上合格的质控为本研究提供了保障。
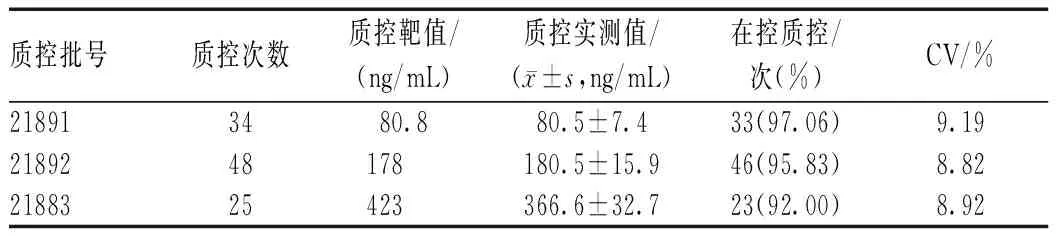
表2 2021年11月至2022年3月环孢素TDM室内质量控制情况Tab 2 Internal quality control of cyclosporine TDM from November 2021 to March 2022
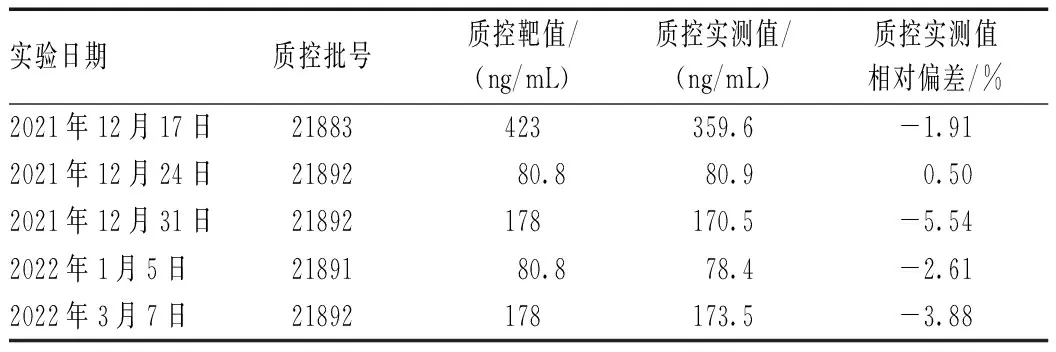
表3 实验日环孢素TDM室内质量控制情况Tab 3 Internal quality control of cyclosporine TDM on experimental day
2.3 不同条件保存7 d环孢素浓度变化
室温保存7 d,环孢素血药浓度降低者43例(占53.75%),浓度变化超过15%的有6例(占7.50%),差值为-1.4(-82.1,164.2) ng/mL,变化范围在-24.39%~27.25%;冷藏保存7 d,环孢素血药浓度降低者54例(占67.50%),浓度变化超过室温、冷冻保存7 d的环孢素浓度分别为(213.0±128.3)、(207.4±121.7) ng/mL,与采样当日测定的血药浓度[(212.0±123.5) ng/mL]相比,差异无统计学意义(P=0.792、P=0.188);冷藏保存7 d的环孢素浓度为(198.4±113.8) ng/mL,较采样当日测定浓度显著降低6.6%,差异有统计学意义(P=0.002),见表4。线性回归分析发现,尽管冷藏保存7 d较采样当日测定的环孢素浓度显著降低(P=0.002),但相关性好(R2=0.903 8),见图1。
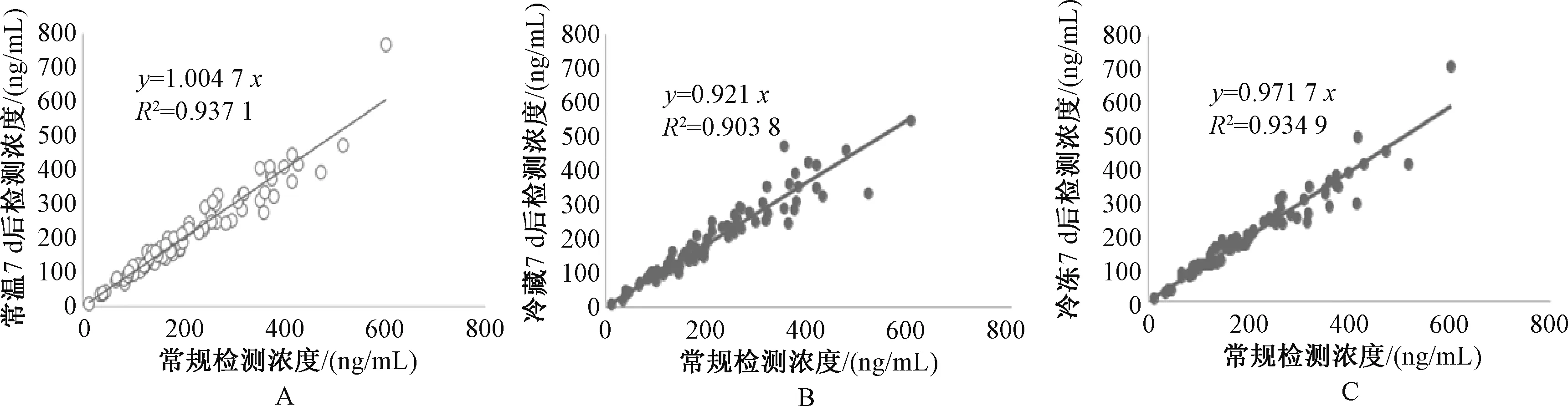
A.常温;B.冷藏;C.冷冻A. room temperature; B. refrigerated condition; C. frozen condition
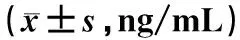
表4 不同条件保存7 d的环孢素血药浓度Tab 4 Blood concentration of cyclosporine under different preservation conditions for 7 days
15%的有22例(占27.50%),差值为-5.3(-184.3,118.4)ng/mL,变化范围在-43.90%~33.66%;冷冻保存7 d,环孢素血药浓度降低者47例(占58.75%),浓度变化超过15%的有11例(占13.75%),差值为-4.2(-123.4~102.5) ng/mL,变化范围在-33.77%~26.22%。
3 讨论
环孢素不仅被用于器官移植领域,还被用于自身免疫性疾病及不孕不育辅助生殖等[1]。相关指南、共识推荐,环孢素使用者必须定期进行TDM,优化环孢素用药方案,提高治疗效果和降低不良反应[1-3]。对于患者因各种困难(如新型冠状病毒肺炎疫情和异地居住)不能按计划进行门诊随访及监测环孢素浓度,在选择其他方式送检标本过程中,合适的标本保存条件对环孢素浓度检测结果至关重要[4-6]。
环孢素检测试剂盒说明书提示,EDTA-K2抗凝标本常温保存1 d,冷藏保存7 d,超过7 d需冷冻保存。按上述条件保存标本,环孢素浓度不会显著变化。
本研究结果发现,室温保存7 d与采样当日环孢素浓度的差异无统计学意义(P>0.05),与环孢素检测试剂盒说明书不一致。尽管冷藏保存7 d环孢素浓度相对于采样当日降低6.6%(P<0.05),但其与采样当日环孢素浓度线性相关性良好。环孢素检测试剂盒(CMIA法)总体精密度要求≤15%。因此,对冷藏保存7 d的环孢素标本进行TDM,为环孢素用药方案调整提供参考。另外,冷冻保存7 d与采样当日环孢素浓度的差异无统计学意义(P>0.05),标本溶血不影响稳定性研究结果,与环孢素检测试剂盒说明书一致,与文献报道一致[12]。
综上所述,针对新型冠状病毒肺炎疫情居家隔离及非疫情期间异地不便门诊随访的患者,本研究为其转运及保存环孢素TDM样本提供了科学依据。然而,本研究样本量少,具有一定的局限性,后续尚需进一步验证和探索。
