人工降解饱水木材制备方法与光谱研究
2022-09-05吴梦若秦振芳韩刘杨韩向娜
吴梦若, 秦振芳, 韩刘杨, 韩向娜
北京科技大学科技史与文化遗产研究院, 北京 100083
引 言
随着我国考古事业的蓬勃发展, 出土/出水考古木材的数量急速增加, 对木质文物保护质量提出了更多更高要求。 饱水木质文物的科学认知, 如木材解剖学、 物理性质和化学组分的分析, 以及保存状况评估, 糟朽程度量化表征等, 不仅利于认识考古木材本身, 阐明其降解劣化机制, 也对后续保护处理方法和保护材料的选择具有指导作用。 但不论是进行木质文物本体的科学认知还是保护治理方法研究, 测试表征均需要一定数量和规定体积的木材样品, 不可避免要对文物进行取样。 然而饱水木质文物是有限的文物资源, 本体往往具有重要的历史文化价值, 取样受到很大限制。 另外, 饱水木质文物出土状态差别较大, 糟朽程度不一, 降解程度不均匀, 在性质表征时会带来数据复杂、 离散性过大, 数据分析困难的问题。 如何在获得足够样本量和有效数据的同时尽量避免对文物产生损伤, 一直以来都很矛盾。 解决考古样品取样难的问题, 制备人工降解饱水木材样品是通用方法。
人工制备饱水木材的方法主要分为以下几类: 一是NaOH强碱浸渍的降解法; 二是利用细菌真菌侵蚀的微生物法; 三是利用生物酶降解的酶解法。 NaOH浸渍法是目前国际上研究较多的方法, 各研究者采用的浓度、 温度、 处理时间各异, 但都采用的是在常压下长时间浸渍的方法。 Kennedy等[1]利用1%稀NaOH溶液浸渍桦木压舌板7 d制备人工模拟饱水木材, 制得的样品降解程度较低, 最大含水量仅达到约177%。 Broda等[2]将现代健康橡木在50%NaOH溶液中浸泡56 d、 在90 ℃下加热12 h后清洗干燥, 制得模拟样品的纤维素、 半纤维素、 木质素均有明显降解, 质量损失达到30%。 对照实验尝试了真菌法, 将橡木样品暴露于白腐真菌下56 d, 降解后木材样品质量损失仅约为18%。 两种方法都没有达到仿真考古木材的目标。 Gelbrich等[3]利用考古木材和周围淤泥的原始菌种搭建细菌反应釜, 这种方法较好地还原了沉船饱水考古木材在海泥中的自然降解过程, 但反应比真菌法更加缓慢, 不具有实用价值。 Konnerth等[4]则利用来自黑曲霉的半纤维素酶溶液处理橡木样品, 真空浸渍后培养10 d, 使半纤维素被定向降解并从基质中去除, 制得饱水木材的力学性能有一定程度的降低。
基于前人研究与实验经验, 本研究对传统常温/加热常压下NaOH长期浸渍的方法进行参数与工艺上的创新与改进。 通过低浓度NaOH溶液真空浸渍和高温高压水热法联用, 极大地提高降解效率和木材内外均匀性。 对制得的人工降解饱水木材, 从物理性质、 力学性能等方面进行表征, 并通过红外和近红外光谱研究了样品的化学结构变化和降解机理。
1 实验部分
1.1 材料
黄松, 来自国家文物局考古研究中心。 根据标准GB1929—2009-T木材物理力学试材锯解及试样截取方法, 将健康木材制成尺寸为2 cm×2 cm×2 cm的样品。 氢氧化钠(分析纯), 购自国药集团化学试剂有限公司。
1.2 人工降解饱水木材制备方法
黄松样品置于温度(23±1) ℃、 湿度11.5%±1.5%的环境中至含水率达到平衡状态。 对照组在85 ℃热水中浸渍至饱水, 实验组采用以下2种方法进行制备: (1)NaOH常压浸渍法: 85 ℃、 20%(W/V)NaOH溶液浸渍; 共4组样品, 每组样本数量为10个, 浸渍时间分别为3, 5, 7和14 d; (2)水热联用法: 共三组样品, 每组样本数量为3个, 在高压水热釜中180 ℃下反应10 h, 三组样品配方如下: ①纯水-水热: 去离子水②NaOH-水热联用: 1%(W/V)NaOH溶液③NaOH-真空浸渍-水热联用: 1%(W/V)NaOH溶液真空浸渍。 以上所有样品处理后持续换水清洗至木材与水体均呈中性(pH 7)。 制得饱水木材干燥前后外观如图1所示, 木材颜色相较于对照组显著加深, 干燥后干缩开裂情况较严重。
1.3 物理性质测试
用JA2003型分析天平(上海舜宇恒平科学仪器有限公司), 测量样品反应前后气干质量M0和M1、 [气干环境温度(23±1) ℃, 湿度11.5%±1.5%]、 (103±2) ℃下烘箱绝干质量M0和处理后饱水状态质量M1; 采用排水法测量样品饱水体积V0。 基本密度(basic density, BD)根据式(1), 最大含水率(maximum water content, MWC)根据式(2), 质量损失(mass loss, ML)根据式(3)计算。
(1)
(2)
ML=(m0-m1)×100%
(3)
1.4 硬度测试
湿硬度采用LX-A型数显橡胶硬度计(测量范围0~100 HA、 分辨率0.5 HA; 压针行程0~2.5 mm、 压针端部压力0~44.5 N)。 各组每个样品三切面各取12个点测试, 选点覆盖早晚材区域, 同生长轮内取3个点。

图1 干燥前后人工降解饱水木材样品照片
1.5 傅里叶变换(FTIR)红外光谱分析
用NicoletTMiSTM5 傅里叶变换红外光谱仪(Thermo Scientific公司)进行红外光谱分析测试。 背景扫描次数16, 样品扫描次数16, 分辨率4.000, 采样增益1.0, 动镜速度0.474 7, 光阑100.00。 用OMNIC软件和Origin软件进行数据处理, 以1 373 cm-1处结晶纤维素C—H弯曲振动吸收峰为标准进行归一化处理。
1.6 近红外反射光谱分析
用TerraSpec4型矿物光谱仪(ASD公司)进行近红外反射光谱测试。 样品扫描次数25, 分辨率1 nm。 用ASD ViewSpec软件和Origin软件进行数据处理, 测得反射率(reflectivity,R)换算为log(1/R)再求一阶导数作图。
2 结果与讨论
2.1 物理力学性能
2.1.1 物理性能
物理性能(最大含水率和基本密度)是最常用的饱水木质文物保存状况的评估参数, 结合木材解剖结构、 化学结构表征, 可以综合判断木材的降解程度, 即木材在降解过程中发生的结构变化程度。 试验结果表明, 仅使用20%NaOH溶液浸渍的4组木材样品质量损失均高于20%, 基本密度与对照组相比有所降低、 最大含水率上升到250%~270%(表1), 和空白组对比上升非常有限, 与中高度降解饱水考古木材通常350%~800%, 甚至1 000%以上[5]的最大含水率相去甚远。 NaOH处理时间对降解程度影响并不明显, 该研究结果与波兰学者用50%高浓度碱处理56天后得到的结果相近[2], 由此推测, 传统NaOH常压浸渍法的降解作用有限, 各项指标远未达到饱水考古木材。 造成以上结果的原因可能是碱在木材中的渗透能力有限, 木材内部未与NaOH充分接触和反应, 也可能是因为NaOH反应后的木材残留物未能从木材基体中完全溶解脱除。
与NaOH常压浸渍法相比, 水热联用法3组样品降解程度显著提高。 纯水-水热处理10 h样品最大含水率达340.23%, 使用1%NaOH的两组联用法所得样品最大含水率则分别高达524.33%和575.87%, 达到了国际上一般认定的高度降解木材的最大含水率水平[5]。 高温高压下, 木材获得的能量更多, 分子间运动加剧, 木材结构变得松散, 比表面积增大, 利于碱液进入细胞内部发生反应, 同时加速了反应过程, 且反应产物更易溶出, 创造了更多的水结合位点和储水孔隙。 使用真空协助浸渍, 使碱液渗透到木材内部与细胞壁结构物质直接接触, 因此反应效率更高, 使木材细胞的降解程度更大。 纯水-水热组相较NaOH-水热联用法所得样品的质量损失和密度变化均较小, 说明木材的降解主要来自碱的化学降解作用; 但最大含水率仍高于传统NaOH常压浸渍法, 说明加压的水热处理对提高最大含水率有重要作用。
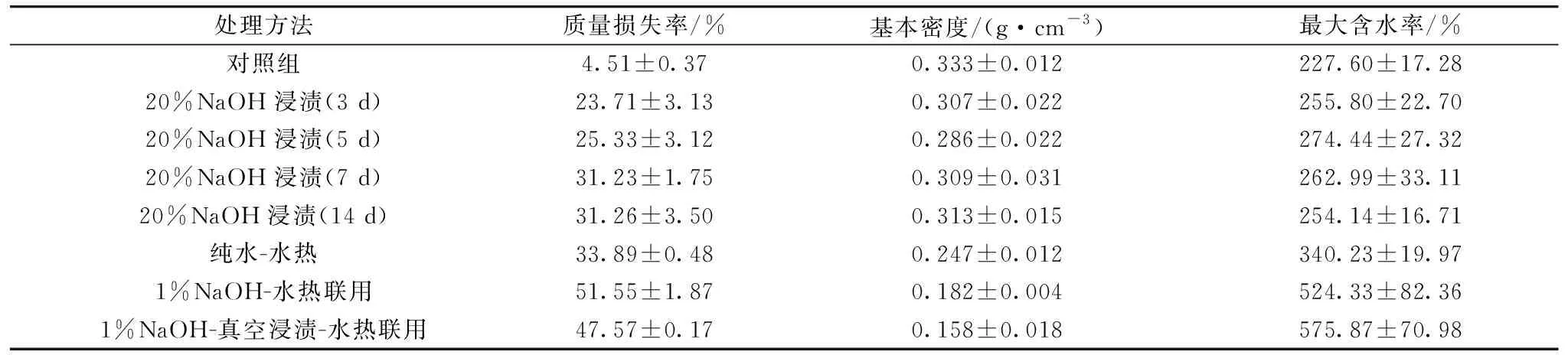
表1 人工降解饱水木材样品的质量损失、 基本密度、 最大含水率
2.1.2 力学性能
硬度是评价木材力学性能的重要指标, 本研究制得的模拟样品饱水状态下硬度数据与上述物理性质试验结果吻合较好, 具有一致的规律性(表2)。 各实验组样品相较于对照组, 硬度均有明显降低, 横切面硬度降低最多, 径、 弦两面硬度相近, 早晚材硬度无明显差异。 NaOH常压浸渍法样品的硬度降低程度随处理时间的延长未见明显变化, 但NaOH-水热联用法两组样品的处理效果较好, 其三切面湿硬度降低程度比传统碱法提高约一倍, 而纯水-水热法样品硬度降低不明显。 试验结果表明, NaOH-水热联用法能够更有效地降低人工降解饱水木材样品的力学性能, 结合物理性质数据, 此方法获得的模拟样品降解程度显著高于传统NaOH常压浸渍法和纯水-水热法。
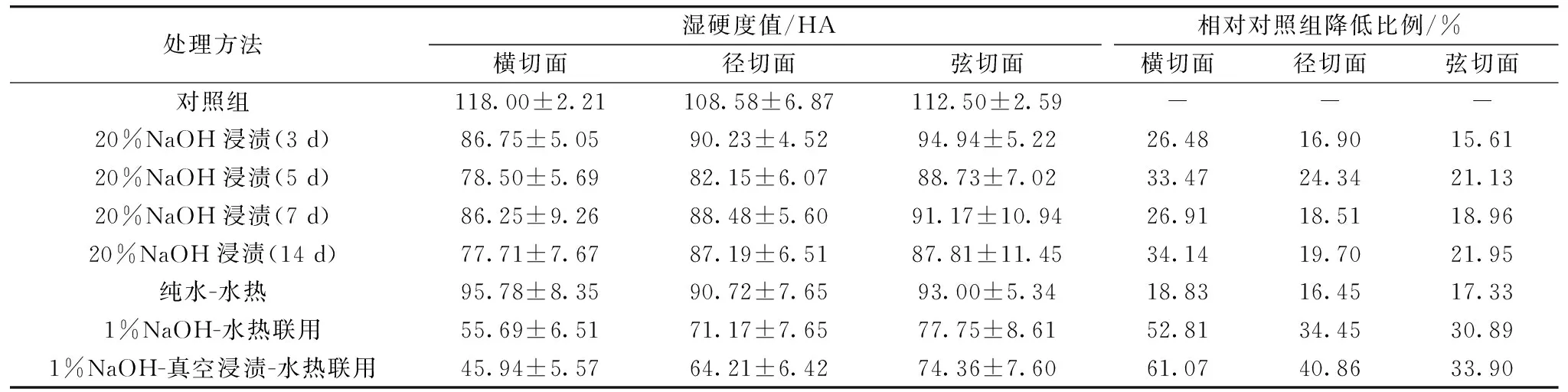
表2 人工降解饱水木材硬度值及降低比例
2.2 光谱特征
2.2.1 红外光谱
红外光谱分析结果表明, NaOH常压浸渍法制得样品在895和1 425 cm-1处与对照组高度重合, 意味着纤维素降解程度小[6], 纤维素结晶区无明显变化。 而水热联用法制得样品组中, 纯水-水热样品895和1 425 cm-1峰重合良好, 两组NaOH-水热联用样品1 425 cm-1处峰强度稍有降低且向1 419 cm-1偏移, 表明低碱浓度的联用法与一般NaOH常压浸渍法所得到的人工降解模拟样品的化学结构可能存在不同, 前者中纤维素结晶度可能受高温影响而降低, 同时配糖键可能因碱水解反应而部分断裂[7]。 另外, 两种方法的红外光谱均在1 337和1 207 cm-1处出现新峰, 可能与多糖的O—H平面内的形变和弯曲振动相关[6], 这说明虽然纤维素未发生明显降解, 但结晶区结构中的稳定氢键可能受到一定程度的破坏, 游离羟基含量略有增加。
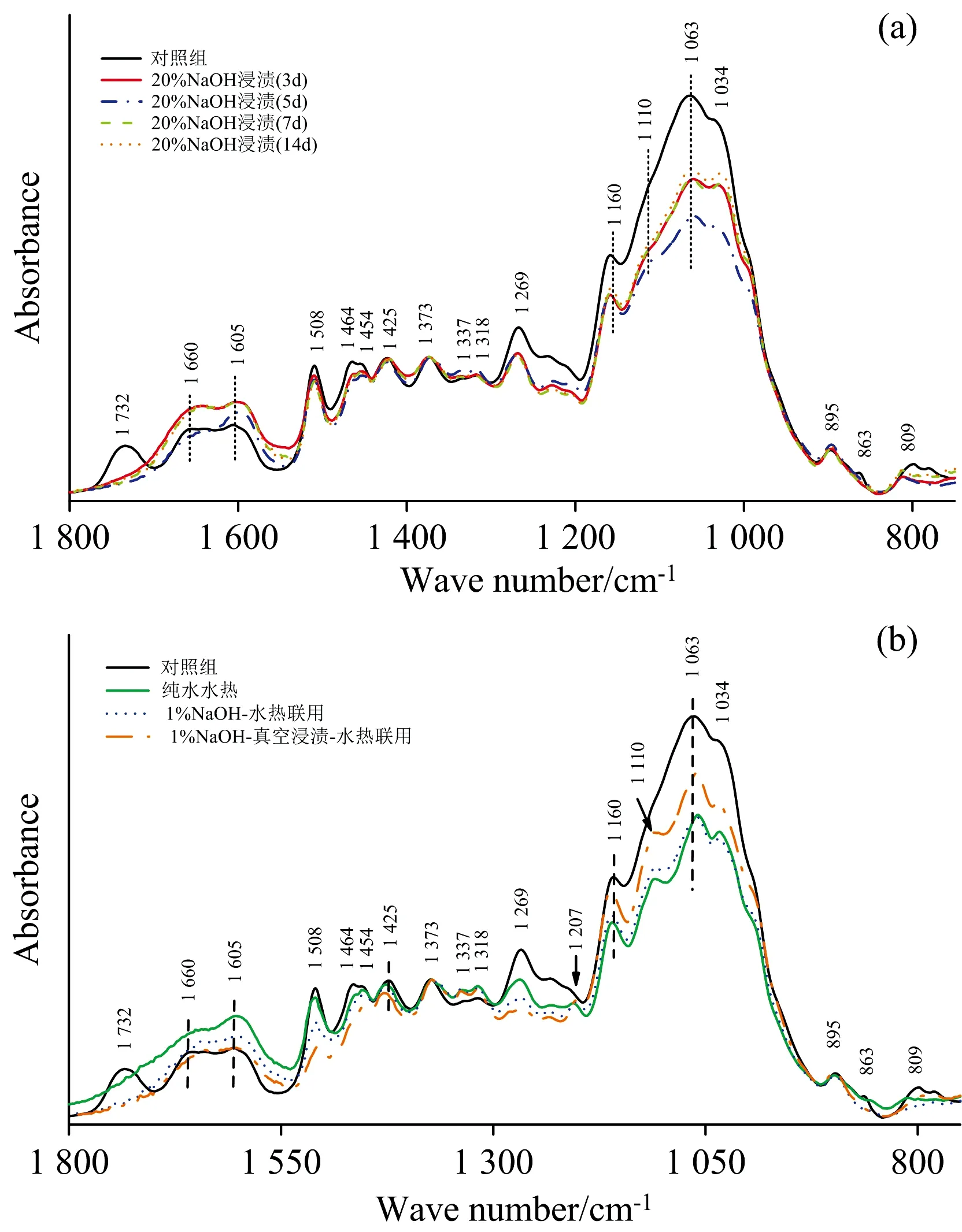
图2 人工降解饱水木材归一化FTIR红外光谱

NaOH常压浸渍法和水热联用法所得木材的红外光谱结果表明, 两种方法制得模拟饱水木材的多糖和木质素相对含量比例接近, 说明其在化学结构层面的降解模式相近, 均以多糖类的化学降解为主。 细胞壁结构物质降解主要是因为与NaOH发生反应, 半纤维素脱除最为明显, 随处理时间的延长、 降解程度升高, 造成木质素相对含量逐渐提高; 水热联用法制备的样品较NaOH常压浸渍法化学结构变化更大, 对碱稳定的纤维素也发生一定降解、 结晶区结构受高温破坏, 木质素降解程度更高, 可能由于水热法制备过程中高温高压条件使木材分子间运动加剧, 木材内部结构松散、 孔隙数量增加, 提高了木材细胞与碱的接触面积和反应速率, 造成木材三大素的较大程度降解。
2.2.2 近红外反射光谱
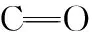
在制备的人工降解饱水木材近红外光谱的O—H一级倍频区内, 1 461 nm处归属于纤维素的峰形变宽, 表明纤维素结构发生一定变化[12]。 1 571 nm吸收峰与纤维素链间氢键相关, 1 544 nm则与结晶纤维素分子内部氢键相关, NaOH常压浸渍法样品在1 571 nm处吸收峰逐渐向1 554 nm偏移, 说明纤维素分子间氢键发生部分断裂, 但结晶区纤维素链降解程度较小[10, 13]; 水热联用法三组样品在1 544~1 581 nm间形成一个扁平峰, 峰强度降低, 表明纤维素结晶区分子内和分子链间氢键结构均发生断裂。 水和O—H合频吸收区内2 044 nm归属于木质素的吸收峰形变尖, NaOH浸渍5 d及以上样品、 水热联用法制备的三组样品2 061 nm附近出现与木质素相关的新峰, 可能与木质素相对含量提高有关[14]。 NIR分析结果和FTIR的结果类似, 印证了制备的人工模拟饱水木材的半纤维素和木质素发生较大程度降解, 纤维素的结晶结构遭到一定程度的破坏。
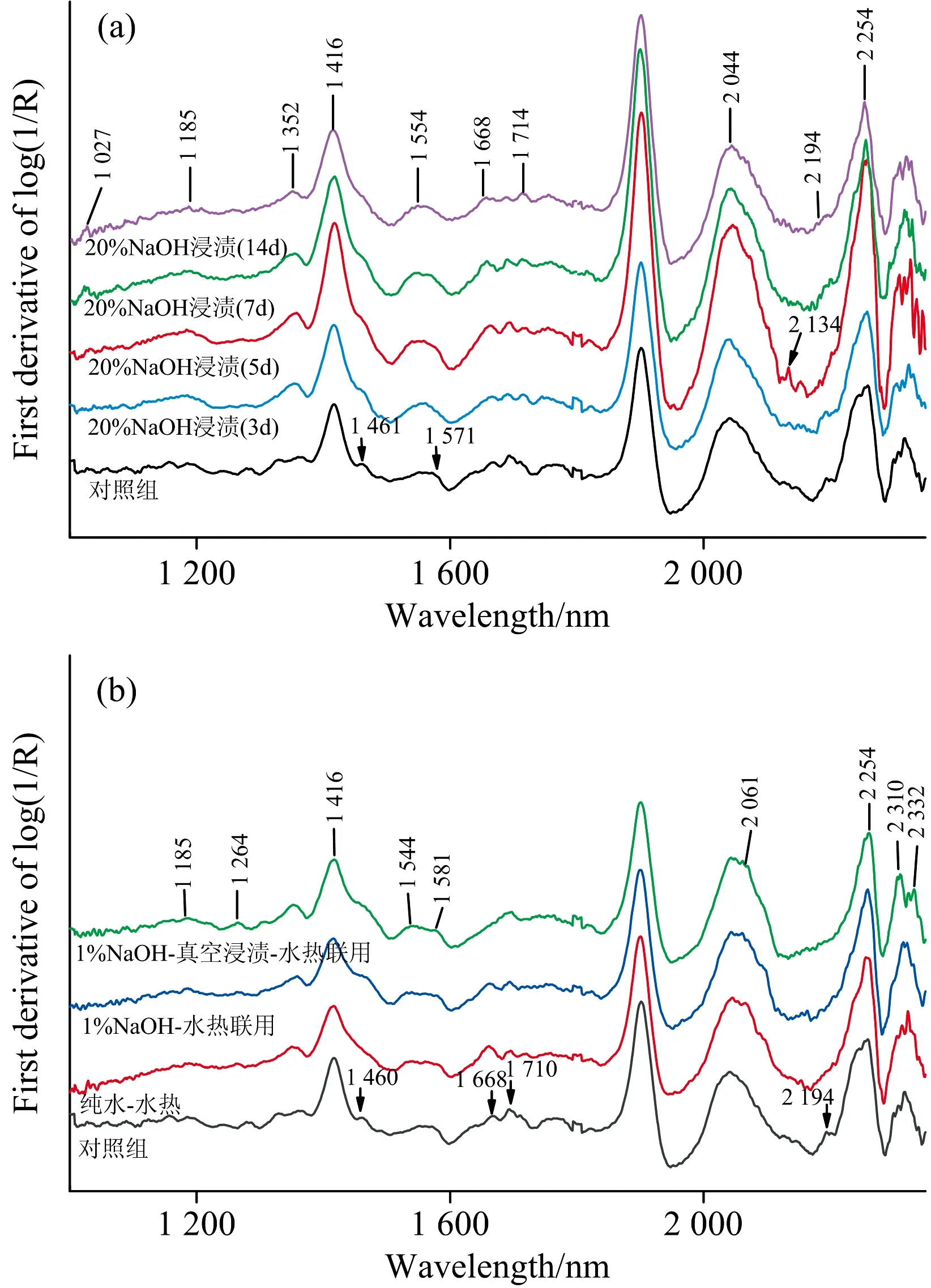
图3 人工降解饱水木材近红外反射光谱
3 结 论
在国际常用的NaOH常压浸渍法基础上, 创新地开发了一种NaOH-真空浸渍-水热联用方法, 将NaOH的浓度从50%降到了1%, 制备时间从数月减少到了10小时, 制备的人工降解饱水木材样品最大含水率可高达500%以上, 且能可控地制备低、 中、 高不同降解程度的样品, 物理性质和力学性能较为均一。 红外光谱和近红外光谱对制得木材细胞壁的主要成分化学结构表征结果显示, 真空浸渍-水热联用法的引入, 极大地提高了NaOH对半纤维素和木质素的降解效率, 对木质素的降解更显著, 纤维素分子及其结晶区结构也受到一定破坏, 其对细胞壁强度和形态结构的维持作用减弱, 使木材细胞壁结构发生变化, 导致木材中孔隙和水结合位点数大量增加, 因此在宏观上表现为含水率显著增大、 物理性质劣化和硬度显著降低。 本工作是对人工制备饱水木材的初步探索, 取得了一定的成效。 尚有不少问题需要继续研究, 如对模拟样品化学组分的定量分析, 根据具体木质文物案例的实际参数进行特定的仿真模拟等。 相信随着研究的细化和深入, 未来能够实现实验室快速、 大量、 可控制备不同降解程度、 且材性均一的模拟饱水木材, 对饱水木质文物的保护研究大有裨益。
