小儿感冒颗粒连翘苷的提取及含量测定研究*
2022-09-05胡秀虹张廷辉潘晓芸吴兰云
胡秀虹,张廷辉,潘晓芸,吴兰云
(1凯里学院大健康学院,贵州 凯里 556011;2黔东南州食品药品检验检测中心,贵州 凯里 556011)
小儿感冒颗粒为小儿感冒类非处方药药品,清热解表,主要用于风热感冒、发热重、恶寒轻、汗出而热不解、头痛鼻塞、咳嗽、口渴咽红等症状,其主要成分有连翘、广藿香、菊花、板蓝根、大青叶、薄荷等[1]。连翘来源于木犀科植物连翘的干燥果实[2],别名黄花条、连壳、青翘等,是早春优良观花灌木[3]。连翘株高约3 m,枝干丛生,小枝黄色,拱形下垂,中空,叶对生,单叶或3小叶,卵形或卵状椭圆形,缘具齿,花冠黄色,1~3朵生于叶腋;果卵球形、卵状椭圆形或长椭圆形,先端喙状渐尖,表面疏生皮孔,果梗长0.7~1.5 cm。连翘花期在3月至4月,果期在7月至9月,果实可以入药[4-5]。连翘性凉味苦,入心、肝、胆经,主要成分为连翘苷,每公斤连翘中连翘苷含量可以达到3%左右,连翘苷可药用,具有清热、解毒、散结排脓等功效[6-8]。临床上,连翘主要应用于治疗各种感染性疾病[9],常作为小儿感冒颗粒、双黄连口服液、双黄连粉针剂、清热解毒口服液、连草解热口服液、连翘解毒冲剂等中药制剂的主要原料[10-11]。
据《中国药典》记载,小儿感冒颗粒的处方工艺及质量标准的建立尚不完善,难以满足国家评价抽验的标准[12-13]。在最新版的2020年版《中国药典》里的小儿感冒颗粒的质量标准中,也还没有明确连翘有效成分的含量[13]。基于此,本文利用高效液相色谱法-单因素轮换法进行小儿感冒颗粒中连翘苷的提取工艺优化,同时随机抽取四个厂家的小儿感冒颗粒进行有效成分连翘苷的含量测定。本研究旨在为进一步完善该药品的质量标准提供参考。
1 材料与方法
1.1 材料
1.1.1 试药
小儿感冒颗粒(神奇制药),连翘苷对照品(批号:110821-201112纯度:96.8%),甲醇、乙腈,均为色谱醇,其他试剂均为分析醇,中性氧化铝、农夫山泉矿泉水。
1.1.2 仪器与设备
UItimate3000型高效液相色谱,津工仪器科技有限公司;AE240电子分析天平METTLER TOLEDO;KQ-500DA型数控超声波清洗仪,昆山市超声仪器有限公司;双列四5L(DK-98-Ⅱ)电热恒温水浴锅,南京伊诺达仪器设备有限公司;GM-0.33A隔膜真空泵,津藤实验设备有限公司。
1.2 方法
1.2.1 连翘苷对照品溶液的制备
称取连翘苷对照品12.22 mg,纯化水溶解并定容至20 mL,摇匀再量取1 mL,定容至25 mL,摇匀即得[14]。
1.2.2 供试品溶液的制备及工艺优化
取适量规格为6 g的小儿感冒颗粒研细混匀,称取一定量粉末2 g,置于100 mL具塞锥形瓶中,加入75%甲醇25 mL,精密称重,超声处理(功率500 W、频率40 kHz)15 min后,取出,放冷至室温后再次精密称重,用上述溶剂补足减失的重量,摇匀滤过,取滤液,过0.45 μm的微孔滤膜,即得供试品溶液[15]。
以提取溶剂、提取方式、纯化方式、提取时间、称样量为考察因素,以供试品溶液中连翘苷的含量为测定指标,进一步优化供试品溶液的制备工艺。各因素的设置条件如下:
提取溶剂:50%甲醇、75%甲醇和甲醇;
提取方式:80 ℃加热回流15 min、室温超声处理(500 W、40 kHz)15 min;
超声提取时间:15 min、30 min、45 min;
称样量:2 g、4 g、6 g。
1.2.3 连翘苷含量的测定及方法学考察
精密吸取上述连翘苷对照品溶液及供试品溶液通过高效液相色谱仪在特定色谱条件下进行连翘苷含量测定,以适量经0.45 μm微孔滤膜过滤的75%甲醇为空白溶液。色谱条件具体如下:色谱柱:Thermo SPZ-869(250×4.6 mm,5 μm);流动相:乙腈-水(25∶75)等度洗脱;检测波长:201 nm;柱温:25 ℃;流速:1.0 mL/min;进样量:10 μL。在此条件下,进一步确定其线性关系、精密度、稳定性、重现性及加样回收率。
1.2.4 不同厂家小儿感冒颗粒连翘苷的含量测定
随机抽取四个厂家(999、昆中药、神奇、小葵花)的小儿感冒颗粒,按1.2.2项下的操作方法制备供试品溶液,根据1.2.3项下的色谱条件依次测定其连翘苷含量[18]。
2 结果与分析
2.1 小儿感冒颗粒连翘苷的提取工艺研究
表1为提取溶剂的考察结果。由表1可知,75%甲醇处理的连翘苷提取含量最高,为0.1296 mg/g±0.0046 mg/g,用甲醇提取的连翘苷含量最低,为0.1086 mg/g±0.0086 mg/g,因此连翘苷提取的最佳溶剂为75%甲醇。

表1 提取溶剂的考察Tab.1 Investigation of extraction solvent
以75%甲醇为提取溶剂,考察提取方式对连翘苷提取含量的影响,结果见表2。由表2可知,超声提取法与加热回流提取法所得的连翘苷含量相差很小,考虑加热回流的提取方式较为麻烦且耗时较长,因此选择超声提取法作为连翘苷的提取方法。

表2 提取方式的考察Tab.2 Investigation of extraction method
采用超声提取法进行供试品溶液的制备,进一步分析提取时间对连翘苷提取含量的影响,结果见表3。由表3可知,随着超声时间的增加,连翘苷含量逐渐增大,但差值均在0.003 mg/g以内,从节约时间的角度考虑,故以超声时间15 min为最佳。

表3 提取时间的考察Tab.3 Investigation of extraction time
表4是小儿感冒颗粒称样量对连翘苷提取含量的影响结果。由表4可知,随着称样量的增加,样品中提取出的连翘苷含量依次减少,应该是提取溶剂所能溶解的连翘苷达到饱和,且干扰杂质增多所导致的,因此选择称样量为2 g。

表4 称样量的考察Tab.4 Investigation of sample weight
2.2 连翘苷含量测定的方法学考察
2.2.1 最佳波长的确定
图1是连翘苷对照品溶液在高效液相色谱仪上进行全波长扫描的结果。由图1可知,连翘苷对照品在201 nm处有最大吸收峰。据相关文献报道,连翘苷溶液在277 nm、278 nm处进行含量测定[14,16,18]。本研究经多次实验探索,最后确定在201 nm处进行连翘苷含量测定。

图1 连翘苷对照品紫外吸收曲线Fig.1 UV absorption curve of forsythin reference substance
2.2.2 线性关系的考察
取1.2.1项下的连翘苷对照品溶液,分别按照2 μL、4 μL、6 μL、8 μL、10 μL、12 μL的体积进样,测定峰面积,记录色谱图。以浓度(mg/g)为横坐标(x),以峰面积为纵坐标(y)计算回归方程[16],结果见图2。
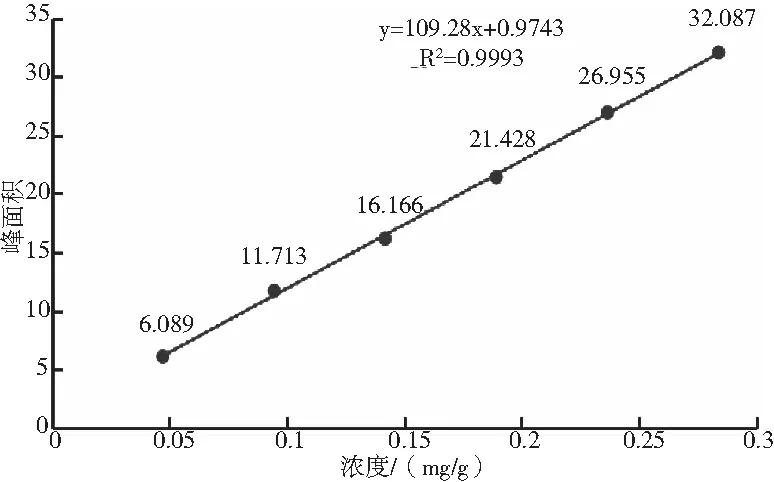
图2 连翘苷的线性回归曲线Fig.2 Linear regression curve of forsythin
由图2可知,在线性范围为0.0473~0.2839 mg/mL内,连翘苷的线性回归方程为Y=109.28x+0.9743,相关系数R2=0.9993,具有良好的线性关系。
2.2.3 精密度试验
取1.2.1项下的连翘苷对照品溶液,连续进样6次,进样量为10 μL,按照1.2.3项下的色谱条件测定连翘苷的峰面积,结果见表5。以峰面积计算RSD,计算公式如下。
由表5可知,6次进样的峰面积在32.81~33.97之间,RSD为1.39%,说明高效液相色谱仪的精密度良好。

表5 精密度试验结果Tab.5 Precision test results
2.2.4 稳定性试验
精密称取小儿感冒颗粒样品粉末1 g,按1.2.2项下的方法制备供试品溶液,按照1.2.3项下的操作,分别在0 h、2 h、4 h、6 h、8 h、10 h、12 h、24 h时进样,测定连翘苷的峰面积,以峰面积计算RSD,结果见表6。由表6可知,RSD为1.31%,由此说明供试品溶液24 h内稳定性良好。
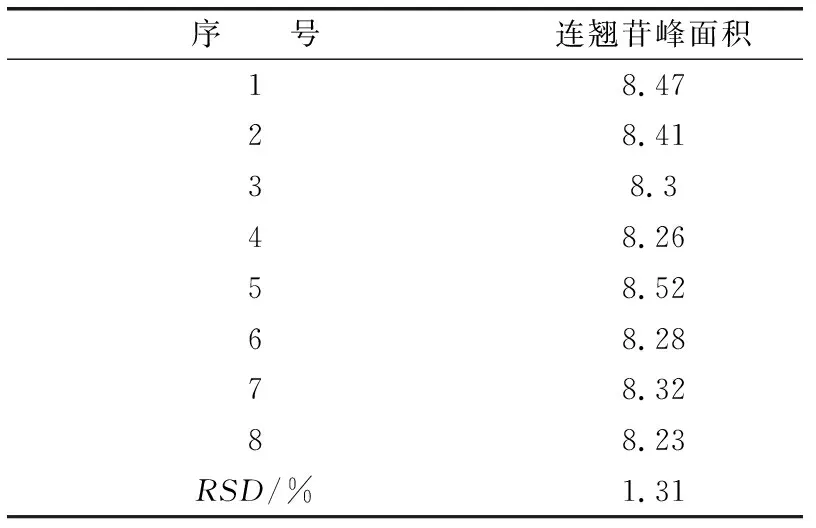
表6 稳定性试验结果Tab.6 Stability test results
2.2.5 重现性试验
精密称取小儿感冒颗粒样品粉末6份,按1.2.2项下的方法制备供试品溶液,按照1.2.3项下色谱条件测定连翘苷的峰面积,以峰面积计算RSD,结果见表7。由表7可知,连翘苷的峰面积在6.97~7.26之间,RSD为1.75%,表明该方法重现性良好。

表7 重现性试验结果Tab.7 Reproducibility test results
2.2.6 加样回收率试验
精密称取小儿感冒颗粒样品粉末1 g,共6份,按1.2.2项下的方法制备供试品溶液,分别精密加入浓度0.0237 mg/g的连翘苷对照品溶液0.5 mL,按照1.2.3项下方法测定连翘苷的含量并计算回收率[17],结果见表8。由表8可知,回收率在102.84~104.96之间,RSD为0.83%,说明该方法准确度良好。
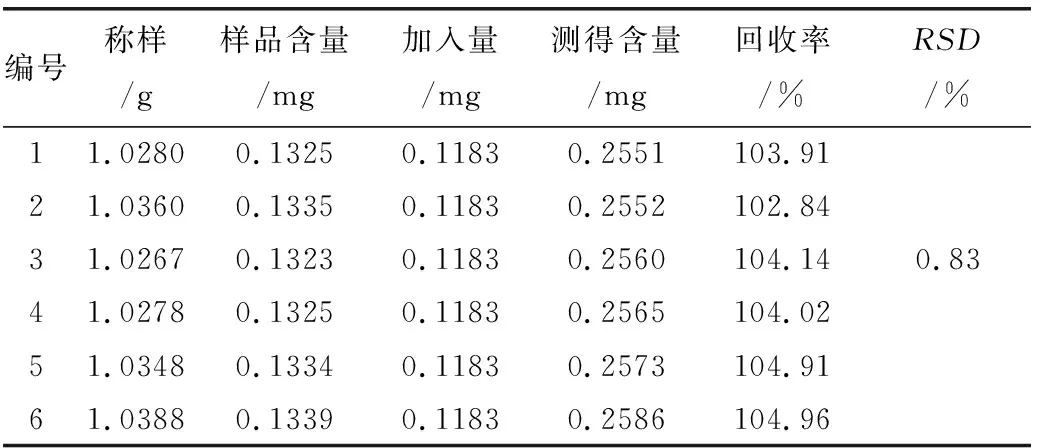
表8 加样回收试验结果Tab.8 Spiked recovery test results
2.2.7 阴性对照实验结果
以75%甲醇为空白对照溶液,进行阴性对照实验。图3为连翘苷对照品溶液、供试品溶液及空白对照溶液的高效液相色谱图。如图3所示,供试品的出峰位置与对照品的出峰位置差不多,都在接近6.5 min出峰,经确认是连翘苷的色谱峰,而空白溶液在相应位置没有出峰,因此确认阴性对照溶液无干扰。

图3 连翘苷高效液相色谱法测定的色谱图Fig.3 Chromatogram of forsythin determined by HPLC
2.3 不同厂家小儿感冒颗粒连翘苷含量测定
表9、图4是999、昆中药、神奇及小葵花四个厂家的小儿感冒颗粒连翘苷的含量测定结果。 由表9、图4所示,四个厂家的小儿感冒颗粒连翘苷含量存在一定的差异,其连翘苷含量分别为0.1505 mg/g、0.0931 mg/g、0.1302 mg/g和0.1435 mg/g,其中999小儿感冒颗粒连翘苷含量最高,昆中药最低。
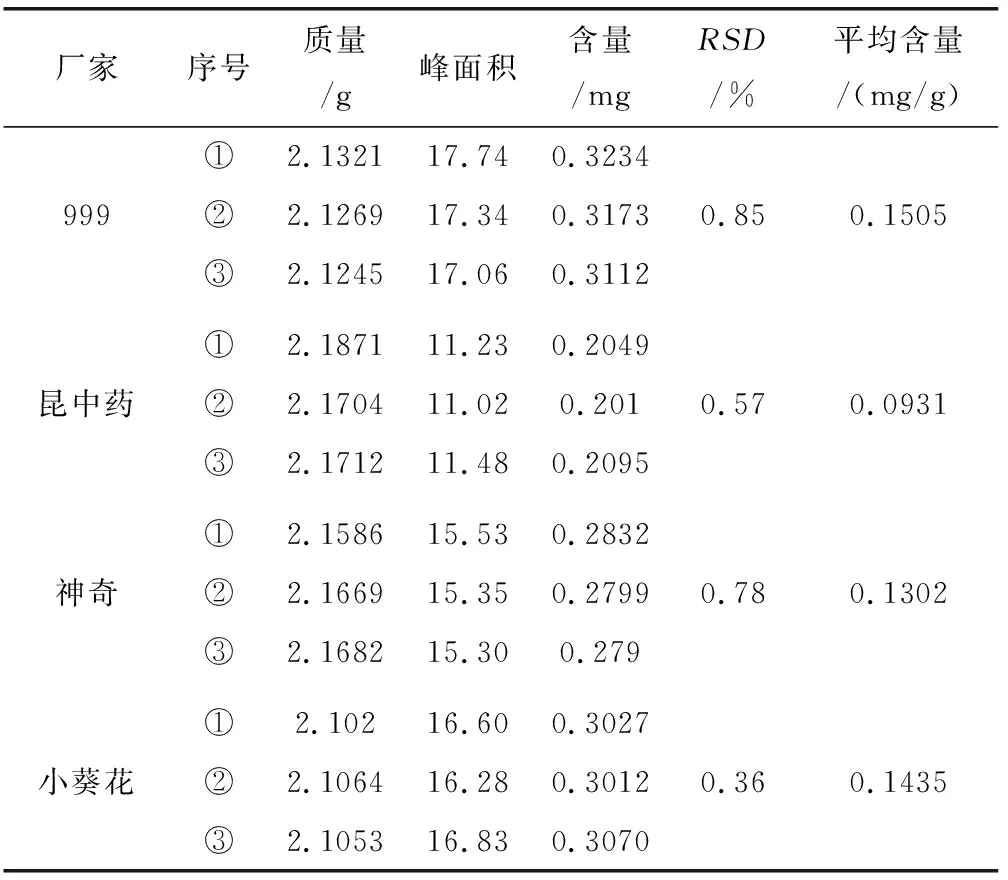
表9 不同厂家小儿感冒颗粒连翘苷含量测定结果Tab.9 Determination results of forsythin in Xiaoer Ganmao Granules from different manufacturers

图4 不同厂家小儿感冒颗粒连翘苷含量测定结果Fig.4 Determination results of forsythin in Xiaoer Ganmao Granules from different manufacturers
3 结论
本文采用单因素轮换法,考察了提取溶剂、提取方式、提取时间及称样量对小儿感冒颗粒连翘苷提取含量的影响,得出最佳工艺为:提取剂为75%甲醇,称样量为2 g,室温超声提取15 min。在最佳提取工艺条件下,进一步对高效液相色谱法进行了方法学考察,结果显示,在201nm波长处,0.0473~0.2839 mg/mL线性范围,连翘苷的线性回归方程为y=109.28x+0.9743,相关系数R2=0.9993,精密度(RSD=1.39%),稳定性(RSD=1.31%),重现性(RSD=1.75%)均良好。加样回收率为102.84~104.96,RSD为0.83%,准确度良好。
上述最佳条件下,对随机抽取的999、昆中药、神奇和小葵花四个厂家的小儿感冒颗粒进行连翘苷含量测定,得到999的连翘苷含量为0.1505 mg/g,昆中药的连翘苷含量为0.0931 mg/g,神奇的连翘苷含量为0.1302 mg/g,小葵花的连翘苷含量为0.1435 mg/g,其中999厂家的连翘苷含量最高,昆中药厂家的连翘苷含量最低。
