富氢半焦气化特性及气化反应动力学研究
2022-09-05徐春霞王学云
李 阳,徐春霞,王学云
(1.煤炭科学技术研究院有限公司 煤化工分院,北京 100013;2.煤炭资源高效开采与洁净利用国家重点实验室,北京 100013;3.国家能源煤炭高效利用与节能减排技术装备重点实验室,北京 100013)
0 引 言
固定床气化具有投资成本低、技术成熟可靠、产气中甲烷含量高的优点,目前已成为煤制清洁燃气的主要技术[1]。固定床气化过程中,气化炉炉体中的内料层自上而下分为干燥区、热解区、气化区及燃烧区,在富氢气氛下进行气化过程中的热解,故而研究加压富氢的热解规律、半焦气化特性及气化动力学等对了解气化炉的运行状况具有重要意义。
国内外学者已在富氢热解规律及煤的气化特性方面进行相应研究[2-5]。贺志宝[6]研究了在固定床中利用氢气及模拟煤气对热解产物与气相组成的影响,发现模拟煤气与氢气热解所得焦油近似且均高于氮气条件下的收率,同时氢气气氛下甲烷的收率增加幅度远高于氮气气氛下,说明在氢气气氛条件下快速热解十分有利于高甲烷收率。Xu 等[7]利用连续自由下落热解器研究了煤种、温度、氢气压力对产物收率的影响并建立热解过程中的碳质量平衡,结果发现,随着高温和氢气压力的升高则可通过半焦气化提高煤炭转化率,但须有足够的反应时间才可将高活性的炭转化为甲烷。李敏[8]通过 FTIR、Py-GC/MS 考察延长煤在 H2、CH4及2种混合气氛下的热解现象,发现随着2种不同气氛下的升温速率增大,氢气气氛下的热解失重率减小,氮气气氛下的热解失重率增加,而混合气氛可促进煤热解失重,并通过对比实际值与理论值活化能,验证甲烷与氢气混合气氛存在相互作用。同时对煤的气化特性[9-16]研究较多,而对热解半焦的气化性能研究甚少。
国内外学者也提出多种气化动力学模型[17-22],诸如均相反应模型[23]、缩核反应模型[24-25]、Johnson模型[26-28]、分布活化能模型(DEAM)[29]等。其中均相反应模型和缩核反应模型可用于描述时间和转化率的关系,且研究发现该2个模型能很好地描述温度低于973 K煤焦-水蒸气气化反应,但在描述较高温度的气化反应时存在较大偏差;Johnson模型可用于多种混合气为气化剂的煤焦气化反应研究。因煤焦气化反应是典型的气固多相反应,煤焦组成结构的不均匀性导致煤焦气化反应复杂,不同煤种、不同气化条件下的气化过程对应着不同的气化动力学参数,且目前尚无文献报道描述半焦的气化动力学参数模型。
笔者对富氢热解半焦开展常压及加压气化特性分析,考察不同因素对气化特性的影响规律,构建半焦气化反应动力学模型,探讨气化反应过程机理,期望为气化炉的设计和模拟计算提供基础数据。
1 实验材料和方法
1.1实验仪器
Cahn Ther Max500加压热重分析仪(卡尔斯鲁厄)、409 PG型热综合分析仪(德国耐驰)。
1.2 富氢气氛条件
采用氮气作为平衡气,分别配制氢气体积含量为15%、25%和35%的富氢混合气体,混合气体采用高压钢瓶储存。
1.3 实验研究内容
(1)富氢半焦常压气化特性。实验样品:0.5 MPa-600 ℃-25%H2富氢热解半焦;实验条件及步骤:采用409PG型热综合分析仪,将氮气流量调整至实验值,升温速率设定为10 ℃/min,样品温度到达设定值后,根据所需的CO2配比,通过流量计设定CO2流量,由氮气携带CO2进入反应室,与样品开始气化反应,记录反应时间和样品质量的变化。
(2)富氢半焦加压气化特性。实验样品:不同条件下制得的富氢热解半焦;实验条件及步骤:采用Cahn Ther Max500加压热重分析仪,先通氮气充分置换系统内空气,然后用惰性气体升压至设定压力,采用程序升温到达设定温度后,调整CO2的流量和氮气的流量至所需值,开始气化反应,记录反应时间和样品质量的变化。实验考察温度、富氢比、气化剂CO2含量等对气化特性的影响。
2 结果及讨论
2.1 富氢热解半焦常压气化性能规律研究
常压气化过程中,温度是影响气化性能的主要因素,因此研究温度对富氢热解半焦CO2气化性能的影响。采用0.5 MPa-600 ℃-25%H2富氢热解半焦与30%CO2在不同温度下(850 ℃、900 ℃、950 ℃、1 000 ℃、1 050 ℃)反应,得到碳转化率和反应时间关系如图1所示,反应速率和反应时间关系如图2所示。

图1 温度对富氢半焦碳转化率的影响Fig.1 Effect of temperature on conversion of hydrogen rich semi coke

图2 温度对富氢半焦反应速率的影响Fig.2 Effect of temperature on reaction rate of hydrogen rich semi coke
由图1可知:在常压、30%CO2浓度及同一反应时间下,温度越高则富氢半焦的碳转化率越高,且达到最大转化率的时间缩短。
由图2可知:在常压、30%CO2浓度下,富氢半焦与CO2的反应速率曲线在不同温度下均呈山峰状变化,且温度越高则反应速率的峰值越大,反应所需的时间越短。即温度提高有助于提高富氢半焦与CO2的气化反应性。
2.2 富氢热解半焦加压气化性能规律研究
加压气化过程中富氢比、气化剂CO2含量、气化温度是影响气化性能的主要因素,因此有必要开展各因素的影响研究实验。
2.2.1富氢比例对富氢热解半焦气化的影响
由实验总结可知温度在975 ℃时是半焦气化的最佳状态。为考察富氢比例对富氢热解半焦气化反应的影响,在1 MPa、975 ℃条件下分别考察了0.5 MPa-600 ℃-N2、0.5 MPa-600 ℃-15%H2、0.5 MPa-600 ℃-25%H2、0.5 MPa-600 ℃-35%H2制得富氢半焦的气化碳转化率和反应时间的关系,结果如图3所示。由图3可知:相同时间内富氢比例越大则半焦碳转化率越高,即提高富氢比例有助于提高富氢热解半焦的气化反应性。

图3 富氢比例对富氢半焦碳转化率的影响Fig.3 Effect of hydrogen rich ratio on conversion of hydrogen rich semi coke
2.2.2气化剂CO2含量对富氢热解半焦气化的影响
为考察气化剂中CO2含量对富氢热解半焦气化反应的影响,以0.5 MPa-600 ℃-25%H2为实验样品,在1 MPa、975 ℃条件下分别考察CO2含量为20%、30%、40%对富氢半焦的气化碳转化率和反应时间的关系。CO2含量对富氢半焦碳转化率的影响结果如图4所示。

图4 CO2含量对富氢半焦碳转化率的影响Fig.4 Effect of CO2 content on conversion of hydrogen rich semi coke
由图4可知:相同时间内气化剂中CO2含量越高则半焦碳转化率越高,即增加气化剂中CO2的含量有助于提高富氢热解半焦的气化反应性。
2.2.3气化温度对富氢热解半焦气化的影响
为考察气化温度对富氢热解半焦气化反应的影响,以1.0 MPa-600 ℃-25%H2为实验样品,在1 MPa,975 ℃下,分别考察了900 ℃、925 ℃、950 ℃、975 ℃下,富氢半焦的碳转化率和反应时间的关系,结果如图5所示。
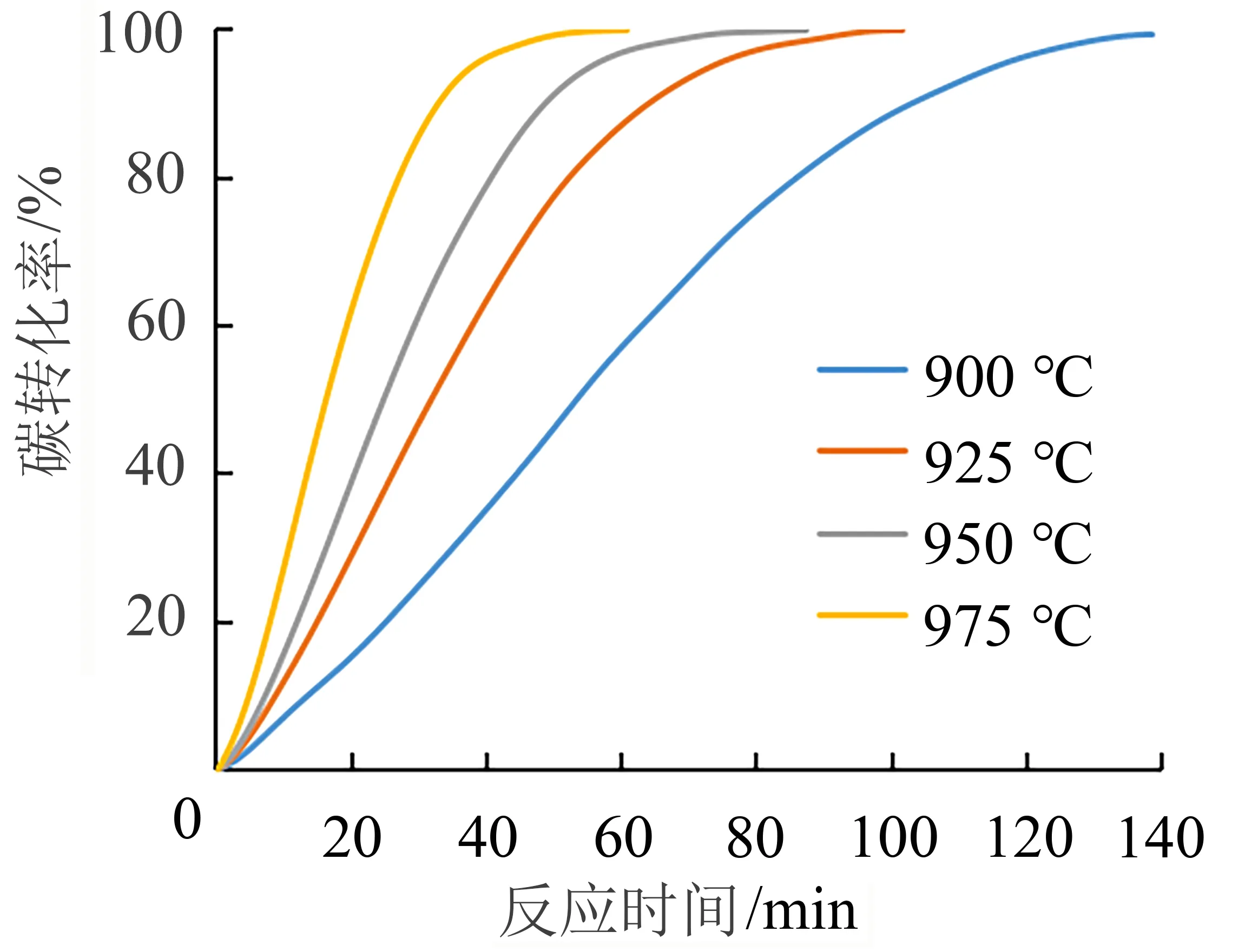
图5 温度对富氢半焦碳转化率的影响Fig.5 Effect of temperature on conversion of hydrogen rich semi coke
由图5可知:相同时间内气化温度越高则半焦的碳转化率越高,且半焦达到最大转化率的时间随温度升高而缩短。即在900 ℃~975 ℃温度段内,提高气化温度可显著提高富氢热解半焦的气化反应性。
2.3 气化反应动力学分析
2.3.1气化反应动力学模型建立
由于煤组成结构的不均一性,煤气化反应复杂,不同煤种、不同气化条件下的气化动力学参数不同。为建立定量描述煤气化过程的动力学模型,实验综合均相模型和缩核模型,在考虑部分物理参数意义及经验因素下,采用混合模型模拟反应动力学过程。其中,混合反应模型采用公式(1)表达:
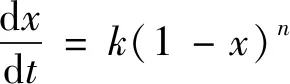
(1)
煤焦与水蒸气及CO2共气化反应速率方程详见式(2):

(2)
式中,P(H2O)为水蒸气分压,P(CO2)为CO2分压,纯水蒸气气化时,无Pm(CO2),纯CO2气化时无Pl(H2O)。
由于对于某一个具体的气化剂配比下的反应,水蒸气及CO2的流量都为定值,所以对于某一个具体的气化剂配比,P(H2O)及P(CO2)均为定值,上式可简化为公式(3):

(3)
式中,k为反应速率常数;n为反应总级数;x为固定碳转化率,%。
简化后的气化反应速率方程和混合反应模型相同。对式(3)两边取对数得式(4):
(4)
另外,在其他实验条件固定时,反应速率常数k仅是反应温度t的函数,并遵循阿伦尼乌斯(Arrhenius)方程,即:

(5)
式中,k0为频率因子,其单位与反应速率常数相同,决定于反应物系的本质;Ea为活化能,J/mol;R为通用气体常数(R=8.314 J/(mol·K))。
对式(5)两边取负对数得到公式(6):
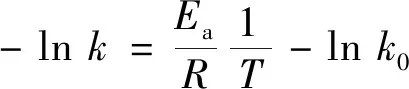
(6)

2.3.2富氢热解半焦常压气化动力学计算
利用混合反应模型对常压、1 123~1 323 K、30%CO2下25% H2半焦气化反应实验数据进行拟合,得到反应的阿伦尼乌斯如图6所示,动力学参数见表1。
由图6及表1可知:
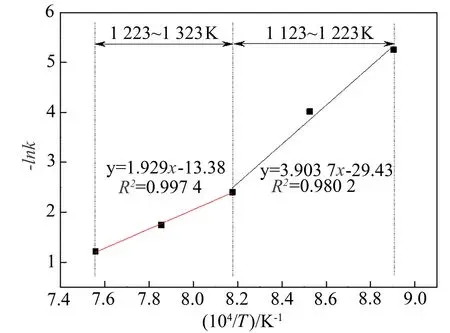
图6 常压下富氢半焦与30%CO2气化反应的ArrheniusFig.6 Arrhenius diagram of gasification reaction of hydrogen rich semi coke with 30% CO2 under atmospheric pressure

表1 常压下富氢半焦与30%CO2气化反应动力学参数Table 1 Kinetic parameters of gasification reaction between hydrogen rich semi coke and 30% CO2 under atmospheric pressure
(1)25%H2半焦与30%CO2的气化反应在不同的温度段具有不同的拟合线,说明25%H2半焦与30%CO2气化反应在不同的温度段的反应机理、活化能均不同。
(2)反应速率常数k均随温度升高而增加,当温度为1 123 K~1 223 K时,25%H2富氢半焦与CO2的反应总级数为0.585 0~0.709 7,活化能为324.55 kJ/mol;当温度为1 223 K~1 323 K时,25%H2半焦与CO2的反应总级数为0.709 7~0.749 0,活化能为160.38 kJ/mol。
(3)R2=0.99,即混合反应模型在不同气化温度段对实验数据的拟合度较高。
2.3.3富氢热解半焦加压气化动力学计算
利用混合反应模型对1.0 MPa、1 123 K~1 323 K及30%CO2条件下的25%H2半焦气化反应实验数据进行拟合,得到反应阿伦尼乌斯如图7所示。

图7 加压下富氢半焦与30%CO2气化反应的Arrhenius图Fig.7 Arrhenius diagram of gasification reaction of hydrogen rich semi coke with 30% CO2 under pressure
加压下富氢半焦与30%CO2气化反应动力学参数见表2。
由图7及表2可知:① 在1 MPa、1 173 K~1 248 K条件下,25%H2半焦与30%CO2气化反应的反应总级数为0.485 3~0.653 5,活化能为198.40 kJ/mol,且反应速率常数k随温度升高而增加;②R2=0.99,即混合反应模型对实验数据拟合度较高。

表2 加压下富氢半焦与30%CO2气化反应动力学参数Table 2 Kinetic parameters of gasification reaction betw-een hydrogen rich semi coke and 30% CO2 under pressure
3 结 论
(1)采用富氢热解半焦开展常压气化反应时,在常压、850 ℃~1 050 ℃下升高温度可提高富氢半焦与CO2的气化反应性,且随温度升高则反应速率的峰值越大,反应所需的时间越短。
(2)采用富氢热解半焦开展加压气化反应时,富氢比例、气化剂中CO2的含量及气化温度的提高均可显著提升富氢热解半焦的气化反应性。
(3)建立定量描述煤气化过程的混合反应模型并对富氢半焦开展常压及加压下的模拟研究,可发现以下结果:① 在常压及加压条件下,混合反应模型在不同温度段对实验数据的拟合度均较高,即模型可良好地模拟煤气化的反应过程;② 常压下在1 123 K~1 223 K的反应总级数为0.585 0~0.709 7,活化能为324.55 kJ/mol;在1 223 K~1 323 K的反应总级数为0.709 7~0.749 0,活化能为160.38 kJ/mol;③ 在1 MPa、1 173 K~1 248 K下,反应总级数为0.485 3~0.653 5,活化能为198.40 kJ/mol。
