乙酰水杨酸制备实验副产物分析
2022-09-03程绍玲张环解洪祥韩聪
程绍玲,张环,解洪祥,韩聪
天津科技大学理学院,天津 300457
乙酰水杨酸(ASA)又称为阿司匹林(Aspirin),与青霉素和安定并称为世界医药史上三大经典药物。阿司匹林具有消炎、镇痛、抗风湿等诸多功效,有神药之称。ASA的制备具有方法成熟、机理明确、合成和纯化路线清晰、操作训练多样等特点,成为高校有机化学实验经典项目之一,多数有机化学实验教材都包含ASA的制备[1-8]。教材中对ASA制备实验中副产物的描述基本一致,认为是水杨酸(SA)自身缩合的聚合物,分子结构见图1a。但笔者经反复实验,收集副产物,进行了相关检测,发现副产物中并没有水杨酸的聚合物,只有乙酰水杨酸酐,分子结构见图1b。本文对ASA制备实验副产物结构的重新确认,为有机化学实验教学提供参考,有利于培养学生大胆质疑敢于探索精神和教学质量的提高。
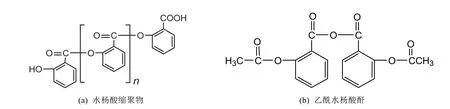
图1 副产物的结构式
1 实验部分
1.1 实验步骤
按文献[1]方法投料,2 g水杨酸加入5 mL乙酸酐,再滴入5滴浓硫酸,轻摇使水杨酸溶解。将反应瓶置于85-90 °C下,反应5-10 min。反应液转移至小烧杯,加入1.5 mL去离子水,静置10 min。加入30 mL去离子水,冰水冷却使析出完全,抽滤得粗产物。
粗产物加入25 mL饱和NaHCO3水溶液,搅拌至固体不再溶解,抽滤,收集副产物。滤液加入15 mL 4 mol·L−1盐酸酸化,冰水浴冷却,抽滤得ASA。
副产物反复用水洗涤,除去表面粘附的乙酰水杨酸钠盐,真空干燥备用。
1.2 产物表征
(1) 薄层色谱检测。
配制展开剂,取3 mL石油醚和1 mL乙酸乙酯,倒入展缸中,加入5滴乙醇,混匀。取少量粗产物、纯化后产物和副产物,用95%乙醇分别配成溶液,在GF254硅胶板上点样,展开。在紫外灯下观察样品斑点位置,做出标记。
(2) 红外光谱测定。
取干燥的副产物,使用Tensor 27傅立叶变换红外光谱仪(德国,布鲁克)测定红外光谱,溴化钾压片,扫描速度为4 cm−1·s−1。
(3) 核磁氢谱测定。
取干燥的副产物,用氘代氯仿为溶剂,使用AV Ⅲ 400 M核磁共振波谱仪(德国,布鲁克)测定核磁氢谱。
(4) 熔点测定。
取干燥的副产物,使用XT4A显微熔点仪(北京科仪电光仪器厂)测定熔点。测三次,取平均值。
2 结果讨论
2.1 副产物形态
按文献[1]方法,得到的副产物往往是粘稠状物,笔者深入分析了反应过程及后处理方法,经实验验证,发现粘稠状物是由于乙酸酐没有水解完全造成的。乙酸酐在常温下水解较慢[9-11],后处理用冰浴冷却,水解更慢,乙酸酐又不溶于水,内部溶有副产物和ASA,共同形成粘稠状物。笔者改进了文献[1]后处理方法如下:反应结束,趁热加入1.5 mL水来水解乙酸酐,当乙酸酐完全水解后再加入大量水进行沉淀,冰浴冷却充分沉淀后,抽滤得粗产物,向粗产物中加碱溶解,副产物呈细颗粒悬浮在溶液中,抽滤得浅肤色粉末状固体。收集副产物,进行成分与结构分析。
2.2 薄层色谱成分分析
粗产物、纯化后产物和副产物在硅胶板上展开,结果如图2所示。图中可见,粗产物中含有ASA和副产物,副产物只有一种物质,纯化后副产物被完全除去。ASA因含有羧基,薄层色谱斑点有拖尾现象。副产物色谱斑点没有拖尾现象,比移值大于ASA,说明副产物极性小于ASA,初步判断可能没有羧基。
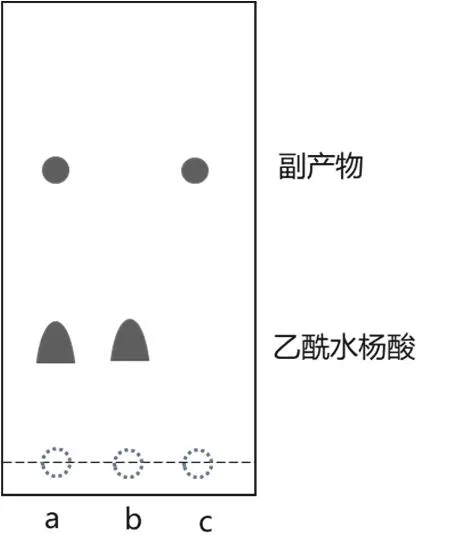
图2 薄层色谱分析图
2.3 红外光谱分析
ASA和副产物的红外光谱图见图3。图中可见,ASA在3300-2500 cm−1有明显的羧基强吸收峰,而副产物在此处只有一个弱的吸收峰,说明副产物没有羧基,与薄层色谱推断结果一致。副产物在3000 cm−1附近的吸收峰为C-H键伸缩振动吸收峰。在羰基吸收峰位置,副产物有3个强吸收峰,推断副产物可能是酸酐。
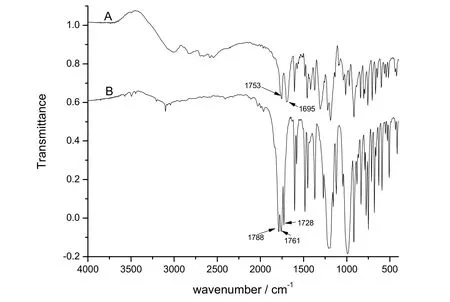
图3 乙酰水杨酸和副产物的红外光谱图
2.4 核磁氢谱分析
副产物的核磁氢谱见图4。化学位移δ为:2.304 (s, 3H),7.20 (d, 1H),7.36 (t, 1H),7.68 (t, 1H),8.08 (d, 1H)。根据核磁氢谱数据及反应体系分析,副产物为邻二取代苯,含有乙酰基。谱图中苯环氢与甲基氢个数比为4 : 3,说明副产物有ASA的结构单元,结合红外光谱分析,不含有羧基,再结合薄层色谱分析,副产物极性较弱,判断副产物可能是乙酰水杨酸酐。
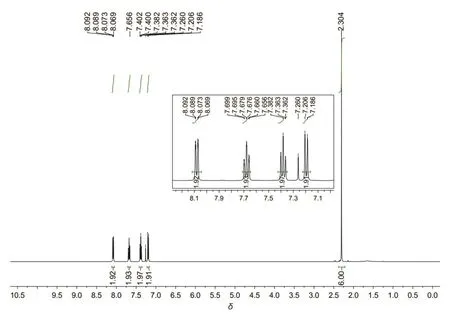
图4 副产物的核磁氢谱图
2.5 熔点分析
测定副产物熔点,三次平均值为83-84 °C。由日本Nishi 1966公开的专利可知[12],乙酰水杨酸酐的熔点为85 °C。Pathak等[13]2014年报导乙酰水杨酸酐熔点为80-85 °C。副产物熔点与文献报导乙酰水杨酸酐的熔点基本一致。结合红外与核磁数据,可以判断副产物正是乙酰水杨酸酐。
2.6 ASA制备实验中副产物形成分析
乙酸酐和水杨酸都含有羰基碳,在酸催化下,都可以被酸性氢活化,发生共振形成碳正离子,如图5所示。图中中间体B碳正离子受苯环共轭作用,活性大大下降,远小于中间体A的活性。水杨酸中酚羟基的亲核性很弱,特别是在酸性条件下,亲核性更弱,与活性很弱的中间体B很难发生反应。另外,从空间效应来看,中间体B的碳正离子处于苯苄位,位阻较大,亲核试剂水杨酸也有一个苯环,同样存在空间位阻问题,两个空间位阻都较大的反应物相遇,较难发生反应。因此,无论是电子效应还是空间效应,两个水杨酸分子都不利于缩合成酯,更不会继续反应生成聚合物。
图5中间体碳正离子A,因乙酰基的吸电子作用,增加了碳正离子的活性,尽管水杨酸中酚羟基亲核性弱,也能顺利发生取代反应,生成乙酰水杨酸。
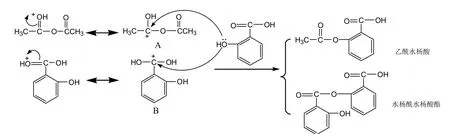
图5 反应机理
反应体系中,乙酸酐既做酰化试剂,又做溶剂,同时也是脱水剂。反应初期主要生成ASA,但随着水杨酸的不断消耗,ASA浓度不断增加,两个ASA分子在脱水剂乙酸酐的作用下,可能发生脱水反应形成乙酰水杨酸酐。特别是当反应达到终点,水杨酸反应完全后,再延长反应时间,乙酰水杨酸酐的量会明显增加。在相同的反应时间下,温度越高,ASA脱水成酐越容易,副产物越多。按文献[1]方法,85 °C下分别反应5、10和15 min,在加碱溶解后收集副产物并称重,结果见表1。实验中用FeCl3监测反应进程,发现5 min已检测不到水杨酸,说明已反应完全。表1可见,反应到达终点再延长反应时间,副产物的量明显增加。按文献[1]方法,反应温度设定在50、70和85 °C,反应时间15 min,同样方法收集副产物并称重,结果见表2。用FeCl3监测反应进程,15 min后,三个温度下的反应都检测不到水杨酸。表2显示,在乙酰水杨酸都能反应完全的情况下,相同反应时间,温度升高,副产物的量增加。用薄层色谱检测以上各反应在碱溶后得到的副产物,发现只有乙酰水杨酸酐一种成份。乙酰水杨酸酐由两个ASA缩合而成,消耗产物ASA,因此乙酰水杨酸酐的量增加会导致ASA产率降低。

表1 延长反应时间对副产物的影响

表2 反应温度对副产物的影响
关于ASA制备实验中的副产物,教材普遍认为是水杨酸的聚合物,文献报导中除生成水杨酸聚合物外,推测副产物还有水杨酰水杨酸酯和乙酰水杨酰水杨酸酯[14,15]。本文通过实验分析测试,副产物只有乙酰水杨酸酐。
3 结语
按文献[1]制备了ASA,收集了副产物,对副产物结构进行了分析鉴定。薄层色谱显示副产物极性较弱,不含有强极性基团;红外光谱显示副产物不含有羧基,可能有酸酐键;核磁氢谱显示副产物含有ASA的结构单元;熔点与乙酰水杨酸酐相同。确认副产物正是乙酸水杨酸酐,不含有教材及文献中提到的水杨酸聚合物。本文重新鉴定了ASA制备中副产物的结构,为该实验教学中知识传授的准确提供了科学依据,有利于教学质量的提高。
